初中化学方程式练习题.
- 格式:docx
- 大小:21.79 KB
- 文档页数:8

【化学】 化学方程式的计算练习题(含答案)经典一、中考化学方程式的计算1.碳酸氢钠用于焙制糕点,在270℃时分解:323222NaHCO Na C ΔO H O CO ++↑。
现取3NaHCO 16.8g ,在敞口容器中加热到质量不再改变为止,减少的质量为( ) A .4.4gB .6.2gC .8.8gD .10.6g【答案】B【解析】【分析】【详解】根据题意可知,在敞口容器中加热到质量不再改变为止,剩余物质为固体碳酸钠。
此题为固体的差量计算,设减少的质量为x 。
323222NaHCO Na CO +H O +CO 1681066216.8g x ↑△固体减少的质量16816.8g =62xx=6.2g2.铝被称为“年轻的金属”,工业上用电解氧化铝的方法制取金属铝。
反应的化学方程式为2Al 2O 3通电 4Al +3O 2↑。
请计算生成1.08t 金属铝,理论上需要氧化铝的质量是多少____?【答案】2.04t【解析】【分析】【详解】解:设生成1.08t 金属铝,理论上需要氧化铝的质量为x 2322Al O 4Al +3O 204108x 1.08t↑通电 204x =108 1.08tx=2.04t答:生成1.08t 金属铝,理论上需要氧化铝的质量为2.04t 。
3.我国科学家实现电催化高效分解硫化氢制氢技术,反应的化学方程式为H 2S 一定条件S ↓ +H 2 .请计算生产 3吨 H 2,理论上需要 H 2S 多少吨?【答案】51吨【解析】【分析】【详解】解:设理论上需要H 2S 的质量为x22S +H 342x3tH S ↓一定条件34x =23tx=51 t答:理论上需要H 2S 51吨。4.某工厂需要16kg 氧气作原料,若用电解水的方法制取这些氧气,消耗水的质量是_________?(要求写出计算过程)【答案】18kg【解析】【分析】【详解】设消耗水的质量为x2222H O2H +O 3632x 16kg↑↑通电 36x =3216kgx=18kg答:消耗水的质量是18kg 。


化学方程式的书写练习一、化合反应:1、碳在氧气中完全燃烧生成二氧化碳。
2、碳在氧气中不完全燃烧生成一氧化碳。
3、一氧化碳在氧气中点燃生成二氧化碳。
4、二氧化碳在灼热的碳中生成一氧化碳。
5、往水中通入二氧化碳,生成碳酸。
6、铁在氧气中点燃生成四氧化三铁。
7、磷在氧气中点燃生成五氧化二磷。
8、铜在空气中加热生成氧化铜。
9、硫在氧气中点燃生成二氧化硫。
10、氢气在空气中点燃生成水。
11、氢气在氯气中点燃生成氯化氢气体。
12、氧化钙加水生成氢氧化钙。
二、分解反应:13、在二氧化锰的催化作用下加热氯酸钾,生成氯化钾和氧气。
14、加热高锰酸钾,生成锰酸钾、二氧化锰和氧气。
15、电解水,生成氢气和氧气。
16、在二氧化锰的催化作用下分解双氧水,生成水和氧气。
17、加热碳酸,分解为二氧化碳和水。
18、碳酸钙高温生成氧化钙和二氧化碳。
19、碳酸氢钠加热生成碳酸钠和二氧化碳。
20、加热碱式碳酸铜,生成氧化铜、水和二氧化碳。
(一)生成二氧化碳气体。
21、碳酸钙和稀盐酸反应,生成氯化钙、水和二氧化碳。
22、碳酸钠和稀盐酸反应,生成氯化钠、水和二氧化碳。
(二)生成水25、氢氧化钙和二氧化碳反应,生成碳酸钙沉淀和水三、氧化还原反应:26、氢气还原氧化铜,加热,生成铜和水。
27、碳还原氧化铜,高温,生成铜和二氧化碳。
28、一氧化碳还原氧化铜,加热,生成铜和二氧化碳。
29、一氧化碳还原氧化铁,高温,生成铁和二氧化碳。
30、一氧化碳还原氧化铁,高温,生成铁和二氧化碳六、其他反应:31、甲烷在空气中点燃,生成二氧化碳和水。

初中化学方程式练习题1. 氢气和氧气反应生成水的化学方程式是什么?2H2 + O2 → 2H2O2. 用硫酸和钠反应生成氢气和钠硫酸的化学方程式是什么?Na + H2SO4 → NaHSO4 + H23. 氢气和氯气反应生成盐酸的化学方程式是什么?H2 + Cl2 → 2HCl4. 碳酸钙分解成氧气和二氧化碳的化学方程式是什么?CaCO3 → CaO + CO25. 氯化钠和硫酸反应生成氯化氢和硫酸钠的化学方程式是什么?NaCl + H2SO4 → HCl + NaHSO46. 氢氧化钠和盐酸反应生成氯化钠和水的化学方程式是什么?NaOH + HCl → NaCl + H2O7. 铁和硫反应生成硫化铁的化学方程式是什么?Fe + S → FeS8. 氧化铜和硫酸反应生成硫酸铜和水的化学方程式是什么?CuO + H2SO4 → CuSO4 + H2O9. 硝酸银和氯化钠反应生成氯化银和硝酸钠的化学方程式是什么?AgNO3 + NaCl → AgCl + NaNO310. 氢氧化铝和盐酸反应生成氯化铝和水的化学方程式是什么?Al(OH)3 + HCl → AlCl3 + H2O11. 氧化铁和氢气反应生成水和铁的化学方程式是什么?Fe2O3 + 3H2 → 2Fe + 3H2O12. 氯化铜和氨水反应生成氨合铜离子和氯化物的化学方程式是什么?CuCl2 + 4NH3 + 2H2O → [Cu(NH3)4(H2O)2]Cl213. 碳酸钠和盐酸反应生成氯化钠、水和二氧化碳的化学方程式是什么?Na2CO3 + 2HCl → 2NaCl + H2O + CO214. 氧化铁和硫酸反应生成硫酸铁和水的化学方程式是什么?Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O15. 氧化铜和氯化铵反应生成氯化铜和氨气的化学方程式是什么?CuO + 2NH4Cl → CuCl2 + 2NH3 + H2O16. 氯化钠和硫酸铜反应生成氯化铜和硫酸钠的化学方程式是什么?NaCl + CuSO4 → CuCl2 + Na2SO417. 氧化铜和硝酸反应生成硝酸铜和二氧化氮的化学方程式是什么?CuO + 2HNO3 → Cu(NO3)2 + NO2 + H2O18. 硫酸铜和氢氧化钠反应生成氢氧化铜和硫酸钠的化学方程式是什么?CuSO4 + 2NaOH → Cu(OH)2 + Na2SO419. 氧化铜和氢氧化铵反应生成氢氧化铜和氨气的化学方程式是什么?CuO + 2NH4OH → Cu(OH)2 + 2NH3 + H2O20. 氯化铁和硫酸铜反应生成硫酸铁和氯化铜的化学方程式是什么?FeCl3 + CuSO4 → Fe2(SO4)3 + CuCl221. 碳酸钙和硝酸反应生成硝酸钙、水和二氧化碳的化学方程式是什么?CaCO3 + 2HNO3 → Ca(NO3)2 + H2O + CO222. 氧化亚铁和氧气反应生成氧化铁的化学方程式是什么?4FeO + O2 → 2Fe2O323. 氢氧化钠和硫酸铜反应生成氢氧化铜和硫酸钠的化学方程式是什么?2NaOH + CuSO4 → Cu(OH)2 + Na2SO424. 碳酸钠和氢氧化铜反应生成氢氧化钠、水和二氧化碳的化学方程式是什么?Na2CO3 + Cu(OH)2 → 2NaOH + CuCO3 + H2O + CO225. 氯化铁和氢氧化铵反应生成氢氧化铁和氯化铵的化学方程式是什么?FeCl3 + 3NH4OH → Fe(OH)3 + 3NH4Cl26. 硫酸铜和氯化铵反应生成氯化铜和硫酸铵的化学方程式是什么?CuSO4 + 2NH4Cl → CuCl2 + (NH4)2SO427. 氧化铁和氢氧化铵反应生成氢氧化铁和氨气的化学方程式是什么?Fe2O3 + 6NH4OH → 2Fe(OH)3 + 6NH328. 氯化铁和硫酸钠反应生成硫酸铁和氯化钠的化学方程式是什么?FeCl3 + 3Na2SO4 → Fe2(SO4)3 + 6NaCl29. 碳酸钙和盐酸铵反应生成氯化铵、水和二氧化碳的化学方程式是什么?CaCO3 + 2NH4Cl → 2NH4Cl + H2O + CO230. 氢氧化铝和盐酸反应生成氯化铝和水的化学方程式是什么?Al(OH)3 + 3HCl → AlCl3 + 3H2O。
1.化学反应在防治环境污染中扮演了重要角色。
某工厂废气中的 SO2,可用以下方式处理:方式一:2SO2 +O2+2CaO=2CaSO4方式二:2SO2 +O2 +4NaOH= aNa 2SO4 +bH2O回答下列问题:(1) CaSO4中有两种元素的质量分数呈整数倍关系,这两种元素是硫元素和_______ (填元素符号)。
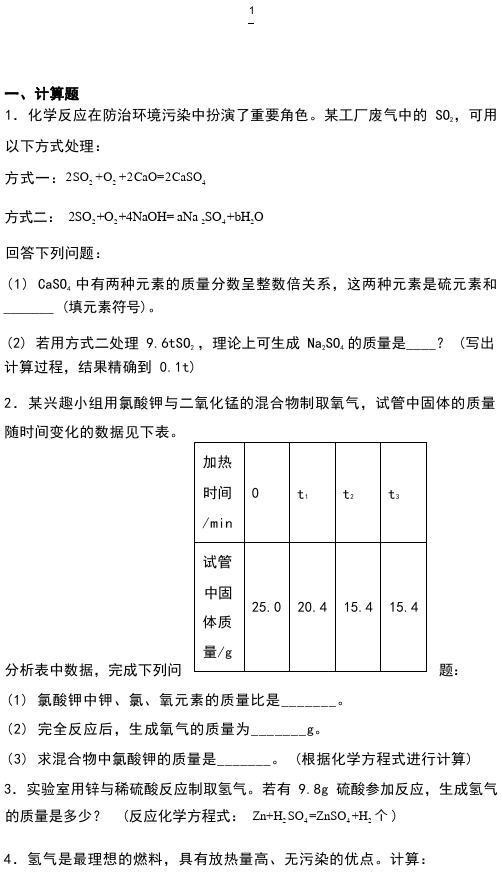
(2) 若用方式二处理 9.6tSO2 ,理论上可生成 Na2SO4的质量是____? (写出计算过程,结果精确到 0.1t)2.某兴趣小组用氯酸钾与二氧化锰的混合物制取氧气,试管中固体的质量随时间变化的数据见下表。
(1) 氯酸钾中钾、氯、氧元素的质量比是_______。
(2) 完全反应后,生成氧气的质量为_______g。
(3) 求混合物中氯酸钾的质量是_______。
(根据化学方程式进行计算) 3.实验室用锌与稀硫酸反应制取氢气。
若有 9.8g 硫酸参加反应,生成氢气的质量是多少? (反应化学方程式:Zn+H2 SO4=ZnSO4+H2个)4.氢气是最理想的燃料,具有放热量高、无污染的优点。
计算:分析表中数据,完成下列问题:(1) 10kg 氢气完全燃烧可生成水的质量是多少?(2) 消耗氧气的质量至少是多少?5.碳酸氢钠固体受热易分解生成一种盐和两种氧化物,反应的化学方程式为______;将 10g 碳酸钠和碳酸氢钠的混合物充分加热至固体的质量不再改变,冷却,称量剩余固体的质量为 6.9g,则原混合物中碳酸钠和碳酸氢钠的质量比为______。
6.实验室常用氯酸钾和二氧化锰的混合物制取氧气。
现有氯酸钾和二氧化锰的混合物 50g,完全反应后称量剩余物质的质量为 40.4g。
请计算:(1) 制得氧气的质量为__________。
(2) 混合物中氯酸钾的质量分数。
7.加热氯酸钾和二氧化锰固体混合物来制取氧气时,反应时间和剩余固体质量的关系如图所示。
计算:的质量是___________g。

初三化学化学方程式计算练习题一、选择题1、电解水得到的氢气和氧气的质量比是()A 2:1B 4:8C 1:8D 1:16答案:C解析:电解水的化学方程式为:2H₂O 通电 2H₂↑ + O₂↑,氢气和氧气的相对分子质量分别为 2 和 32。
生成氢气和氧气的物质的量之比为 2:1,质量之比为(2×2):(1×32)= 4:32 = 1:8。
2、在反应 2A + 3B = 2C + 4D 中,若 A、B、C、D 的质量比为8:12:11:9,则 A、B、C、D 的相对分子质量之比为()A 8:12:11:9B 16:36:22:36C 16:16:22:9D 2:3:2:4答案:B解析:设 A、B、C、D 的相对分子质量分别为 x、y、z、m。
因为 A、B、C、D 的质量比为 8:12:11:9,根据化学方程式中各物质的质量比等于相对分子质量乘以化学计量数之比,可得:(2x):(3y):(2z):(4m) = 8:12:11:92x : 3y = 8 : 12 ,解得 x : y = 16 : 362x : 2z = 8 : 11 ,解得 x : z = 16 : 222x : 4m = 8 : 9 ,解得 x : m = 16 : 36所以 A、B、C、D 的相对分子质量之比为 16:36:22:36,故选 B。
3、用氢气还原氧化铜,若还原 8 克氧化铜,需要氢气的质量是()A 02 克B 05 克C 1 克D 2 克答案:A解析:氢气还原氧化铜的化学方程式为:H₂+ CuO 加热 Cu +H₂O氧化铜的相对分子质量为 80,设需要氢气的质量为 xH₂+ CuO 加热 Cu + H₂O2 80x 8g2/80 = x/8g ,解得 x = 02g4、要制取 48 克氧气,至少需要分解多少克高锰酸钾?()A 474 克B 474 克C 948 克D 948 克答案:C解析:加热高锰酸钾制取氧气的化学方程式为:2KMnO₄加热K₂MnO₄+ MnO₂+ O₂↑高锰酸钾的相对分子质量为 158,氧气的相对分子质量为 32设需要分解高锰酸钾的质量为 x2KMnO₄加热 K₂MnO₄+ MnO₂+ O₂↑316 32x 48g316/32 = x/48g ,解得 x = 474g但需要注意的是,在实际实验中,高锰酸钾不能完全分解,所以至少需要 948 克高锰酸钾。

化学化学方程式的计算练习题20篇含解析一、中考化学方程式的计算1.在盛有24.3g 硫酸钠和氯化钠组成的固体混合物的烧杯中,加入100g 水使硫酸钠和氯化钠全部溶解。
向其中逐渐滴加溶质质量分数为20%的氯化钡溶液。
生成沉淀的总质量与所滴入氯化钡溶液的质量关系曲线如图Z7-6所示,请根据题意回答问题。
(1)过程中观察到的现象_____。
(2)滴加到B 点时,溶液中的溶质是_____(填化学式)。
(3)当滴加氯化钡溶液至图中A 点时,所得溶液中溶质的质量分数。
_____(结果保留一位小数)【答案】生成白色沉淀,溶液变浑浊; NaCl 和BaCl 2 10.6% 【解析】 【分析】 【详解】(1)硫酸钠和氯化钡生成硫酸钡沉淀和氯化钠,所以会看到有白色沉淀生成,故填:生成白色沉淀,溶液变浑浊;(2)硫酸钠和氯化钡生成硫酸钡沉淀和氯化钠,A 点表示恰好完全反应,此时溶质为氯化钠,B 点表示氯化钡过量,此时溶质为氯化钡和氯化钠,故填:NaCl 和BaCl 2; (3)当滴加氯化钡溶液至图中A 点时,所得溶液中溶质为氯化钠 设生成氯化钠质量为x 反应硫酸钠质量为y ,生成沉淀质量为z 。
2244BaCl Na SO BaSO 2NaCl208142233117104g 20%yzx208104g 20%208104g 20%208104g 20%===117x 142y 233z x=11.7gy=14.2g z=23.3g+=↓+⨯⨯⨯⨯,,,,反应后氯化钠质量为:11.7g+(24.3g-14.2g)=21.8g ,反应后溶液质量为:24.3g+100g+104g-23.3g=205g,反应后溶液质量分数为;21.8g100%10.6%205g⨯≈ 答:溶质质量分数为10.6%2.向盛有100g质量分数为8%的氧氧化钠溶液的烧杯中,逐滴加入193.8g硫酸铜溶液,二者恰好完全反应。
请计算:(化学方程式为 CuSO4+ 2NaOH = Cu(OH)2↓+ Na2SO4)(1)恰好完全反应时生成沉淀的质量__________。
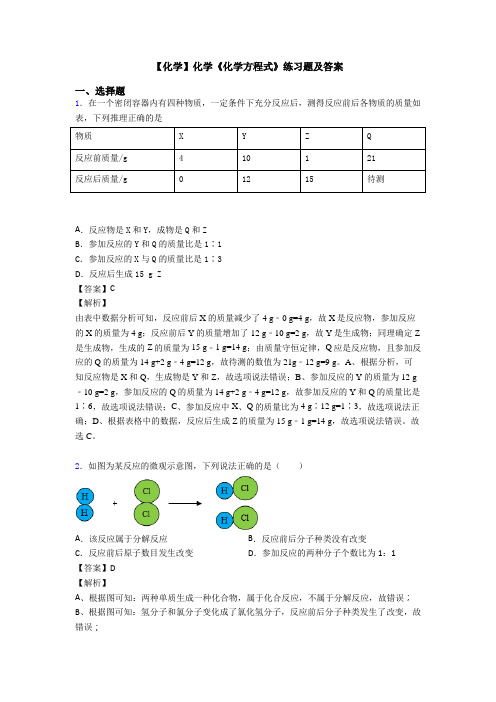
【化学】化学《化学方程式》练习题及答案一、选择题1.在一个密闭容器内有四种物质,一定条件下充分反应后,测得反应前后各物质的质量如表,下列推理正确的是物质X Y Z Q反应前质量/g410121反应后质量/g01215待测A.反应物是X和Y,成物是Q和ZB.参加反应的Y和Q的质量比是1∶1C.参加反应的X与Q的质量比是1∶3D.反应后生成15 g Z【答案】C【解析】由表中数据分析可知,反应前后X的质量减少了4 g﹣0 g=4 g,故X是反应物,参加反应的X的质量为4 g;反应前后Y的质量增加了12 g﹣10 g=2 g,故Y是生成物;同理确定Z 是生成物,生成的Z的质量为15 g﹣1 g=14 g;由质量守恒定律,Q应是反应物,且参加反应的Q的质量为14 g+2 g﹣4 g=12 g,故待测的数值为21g﹣12 g=9 g。
A、根据分析,可知反应物是X和Q,生成物是Y和Z,故选项说法错误;B、参加反应的Y的质量为12 g ﹣10 g=2 g,参加反应的Q的质量为14 g+2 g﹣4 g=12 g,故参加反应的Y和Q的质量比是1∶6,故选项说法错误;C、参加反应中X、Q的质量比为4 g∶12 g=1∶3,故选项说法正确;D、根据表格中的数据,反应后生成Z的质量为15 g﹣1 g=14 g,故选项说法错误。
故选C。
2.如图为某反应的微观示意图,下列说法正确的是()A.该反应属于分解反应B.反应前后分子种类没有改变C.反应前后原子数目发生改变D.参加反应的两种分子个数比为1:1【答案】D【解析】A、根据图可知:两种单质生成一种化合物,属于化合反应,不属于分解反应,故错误;B、根据图可知:氢分子和氯分子变化成了氯化氢分子,反应前后分子种类发生了改变,故错误;C 、由微粒的变化可知,反应前后原子数目没有发生改变,故错误;D 、由微粒的变化可知,参加反应的两种分子个数比为1:1,故正确。
点睛:化学反应的实质一般是指在化学变化中,分子分成原子,原子重新组合成新的分子(或直接聚集构成新物质)。

初三化学方程式练习题一、写出下列反应的化学方程式:1. 铁在氧气中燃烧生成四氧化三铁。
2. 氢气在氯气中燃烧生成氯化氢。
3. 碳酸钙受热分解生成氧化钙和二氧化碳。
4. 硫在氧气中燃烧生成二氧化硫。
5. 锌与稀硫酸反应生成硫酸锌和氢气。
二、配平下列化学方程式:1. 铜与稀硝酸反应生成硝酸铜、水和氮的氧化物。
2. 碳与水蒸气反应生成一氧化碳和氢气。
3. 钠与水反应生成氢氧化钠和氢气。
4. 氯酸钾在二氧化锰催化下加热分解生成氯化钾和氧气。
5. 过氧化氢在二氧化锰催化下分解生成水和氧气。
三、根据题目所给的反应物和生成物,写出相应的化学方程式:1. 氢氧化钠与盐酸反应生成氯化钠和水。
2. 铁与硫酸铜反应生成硫酸亚铁和铜。
3. 碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳。
4. 氧化铜与氢气反应生成铜和水。
5. 碳酸氢钠受热分解生成碳酸钠、水和二氧化碳。
四、写出下列物质的化学式:1. 氢氧化钙。
3. 硝酸银。
4. 碳酸氢铵。
5. 磷酸氢二钠。
五、根据题目所给的化学反应,判断下列说法是否正确:1. 镁在空气中燃烧生成氧化镁,反应的化学方程式为:Mg + O2 → MgO。
2. 二氧化碳与氢氧化钠反应生成碳酸钠和水,反应的化学方程式为:CO2 + 2NaOH → Na2CO3 + H2O。
3. 氧化铁与稀盐酸反应生成氯化铁和水,反应的化学方程式为:Fe2O3 + 6HCl → 2FeCl3 + 3H2O。
4. 锌与硫酸铜反应生成硫酸锌和铜,反应的化学方程式为:Zn + CuSO4 → ZnSO4 + Cu。
5. 碳酸钠与稀硫酸反应生成硫酸钠、水和二氧化碳,反应的化学方程式为:Na2CO3 + H2S O4 → Na2SO4 + H2O + CO2↑。
六、根据题目所给的反应物和生成物,写出相应的化学方程式,并配平:1. 铜与浓硝酸反应生成硝酸铜、水和二氧化氮。
2. 碳与氧气反应生成二氧化碳。
3. 钠与氯气反应生成氯化钠。

【化学】化学《化学方程式》练习题及答案一、选择题1.CH 4和某种氮的氧化物反应的化学方程式为CH 4+2口催化剂N 2+CO 2+2H 2O ,则框内物质的化学式是 A .NO B .NO 2C .N 2OD .N 2O 5【答案】B 【解析】试题分析:化学变化前后各种原子的个数不变,反应后有2N 、C 、4H 、4O ,而反应前有4H 、一个C 原子,反应前后差2N 、4O ,所以框内物质的化学式为NO 2,故选B 考点:质量守恒定律的应用2.将一定质量的氧化铜和氧化铁混合粉末与足量的CO 充分反应后,测得质量减少了4.0g 。
另取等质量的该粉末用适量的稀硫酸完全溶解后,再加入足量的氢氧化钠溶液,得到了20.5g 的沉淀。
则粉末中的氧化铜的质量分数为 A .20% B .40%C .50%D .80%【答案】C 【解析】 【分析】分别假设氧化铜和氧化铁的质量,进而结合化学方程式、关系式及对应的数据求解,进而求出粉末中氧化铜的质量分数。
【详解】设粉末中氧化铜的质量为x ,氧化铁的质量为y ,21CO +CuO Cu +CO 806416x m 高温固体质量减少116x xm ==80523223CO +Fe O 2Fe +3CO 16011248ym 高温固体质量减少248y 3ym ==16010氧化铜与稀硫酸反应生成硫酸铜和水,硫酸铜与氢氧化钠反应生成氢氧化铜沉淀和硫酸钠;氧化铁和稀硫酸反应生成硫酸铁和水,硫酸铁和氢氧化钠反应生成氢氧化铁沉淀和硫酸钠,根据元素守恒列关系式:423CuO ~CuSO ~Cu(OH)8098xm398x 49xm ==80402324334Fe O ~Fe (SO )~2Fe(OH)160214ym4214y 107ym ==16080结合题干,列出方程:x 3y+=4.051049x 107y+=20.54080解得x=8g ,y=8g则粉末中氧化铜的质量分数为:8g100%50%8g+8g⨯= ,故选C 。

化学方程式练习题(含答案)经典一、化学方程式选择题1.科学家采用“组分转化”技术,将 CO2和H2按一定比例混合,在一定条件下反应的化学方程式为2CO2 + 6H2= X + 4H2O中,X的化学式是A.CH4 B.C2H4 C.H2CO3 D.H2C2O4【答案】B【解析】化学反应前后各种原子个数相等,反应前有2C、4O、12H,反应后(X除外)有4O、8H,所以x中有有2C、4H,X的化学式为C2H4,故选B。
点睛:要顺利解答此题,必须熟练掌握质量守恒定律并会灵活应用,化学反应前后各种原子个数相等,根据反应前后原子个数的差量即可推断出X的化学式。
2.某反应前后分子变化的微观示意图如下(图中“●”和“○”分别代表不同元素的原子),下列说法不正确的是()A.该反应前后涉及到三种物质B.反应后分子种类没有改变C.反应后分子数增多D.该反应属于分解反应【答案】B【解析】【详解】由化学反应的微观示意图可知,各物质反应的微粒个数关系是:A、由图示可知,该反应前后涉及到三种物质,故A正确;B、由微粒的变化可知,反应后分子种类发生了改变,故B不正确;C、由微粒的变化可知,该反应后分子数增多,故C正确;D、该反应由一种物质生成了两种物质,属于分解反应,故D正确。
故选B。
【点睛】化学变化中分子的种类一定改变,数目可变可不变。
3.如图表示某个化学反应,据图分析判断,下列各项中,不正确的是A .该反应属于置换反应B .反应中乙、丙两物质质量比为2: 7C .图示中x 的数值为4D .反应前后氢元素的化合价发生了改变【答案】B 【解析】 【分析】由化学反应的微观模型图可知,该反应是在一定条件下氢气与四氯化硅(SiCl 4)反应生成了硅和氯化氢气体,反应的化学方程式为:42SiCl +2H Si+4HCl 一定条件,由方程式可知: 【详解】A 、该反应是一种单质和一种化合物反应生成了另一种单质和另一种化合物,属于置换反应,故A 正确;B 、反应中乙、丙两物质质量比就是氢气和硅的质量比为:(2×1×2):28=1:7,故B 不正确;C 、由方程式可知,图示中x 的数值为4,故C 正确;D 、由方程式可知,氢元素的化合价由0价变成了+1价,故D 正确。

化学化学方程式的计算练习题20篇及解析一、中考化学方程式的计算1.为测定某过氧化钠样品的纯度,将2g 该样品与足量水发生如下反应(杂质不参与反应) :22222Na O + 2H O=4NaOH+O ↑ 。
生成气体质量与时间的关系如图所示。
计算该样品中过氧化钠的质量分数。
____________【答案】78%【解析】【分析】=100%⨯过氧化钠的质量样品中过氧化钠的质量分数样品的质量【详解】 由生成气体质量与时间的关系图可知,完全反应生成的氧气的质量为0.32g 。
设样品中过氧化钠的质量为x22222Na O +2H O =4NaOH +O 15632x 0.32g↑15632=x 0.32gx=1.56g 该样品中过氧化钠的质量分数为1.56g 100%78%2g⨯= 答:该样品中过氧化钠的质量分数为78%。
2.为测定某石灰石矿中碳酸钙的含量,进行了如下实验:称取10g 石灰石样品,高温煅烧至质量不再改变,称得剩余固体质量为6.7g (假设杂质不参与反应)。
请计算: (1)反应生成的CO 2的质量______________。
(2)该石灰石样品中碳酸钙的质量分数____________。
【答案】3.3g 75%【解析】【分析】【详解】(1)由质量守恒定律,反应生成的CO 2的质量为10g-6.7g=3.3g ,故填:3.3;(2)解:设该石灰石样品中碳酸钙的质量为x3222CaCO +2HCl =CaCl +H O +CO 10044x3.3g 10044=x 3.3g↑x=7.5g该石灰石样品中碳酸钙的质量分数为7.5g 10g×100%=75% 答:该石灰石样品中碳酸钙的质量分数为75%。
3.某碳酸钠样品中混有少量氯化钠,根据下图所示信息,计算该样品中碳酸钠的质量分数(计算结果精确到0.1%)。
【答案】70.7%【解析】【分析】【详解】设该样品中碳酸钠的质量分数为x2323Na CO +CaCl =CaCO +2NaCl1061007.5gx 5.0g↓ 1067.5gx =100 5.0gx ≈70.7% 答:该样品中碳酸钠的质量分数为70.7%。
《化学方程式》练习题(含答案)一、单选题1. 实验室加热一定质量的高锰酸钾制氧气,各物理量随加热时间变化的图像正确的是( )A. B.C. D.2. 下列关于2C+O22CO的说法中,正确的是( )A. 表示碳加氧气等于一氧化碳B. 该反应中,分子、原子的种类均发生了改变C. 参加反应的碳与氧气的质量比为3:8D. 参加反应的氧气与生成的一氧化碳的分子个数比为1:23. 化学反应前后肯定没有发生变化的是( ) ①原子数目; ②分子数目; ③元素种类; ④物质种类; ⑤原子种类; ⑥物质的总质量A. ① ④ ⑥B. ① ③ ⑤ ⑥C. ① ② ⑥D. ② ③ ⑤4. 乙烷(C2H6)是重要的化工原料,与氯气反应前后分子种类变化的微观示意图如图。
下列说法正确的是( )A. 甲中碳、氢元素质量比为1:3B. 乙的相对分子质量为71C. 甲和丙的元素组成相同D. 生成丙与丁的分子个数比为1:15. 下列化学方程式书写正确的是( )A. Mg+O=点燃MgO2B. 4Fe+3O=点燃2Fe2O32C. 2KMnO4=K2MnO4+MnO2+O2↑D. CO2+Ca(OH)2=CaCO3↓+H2O6. 某化学反应的微观示意图如图所示,下列有关说法正确的是( )A. 该反应的两种反应物均为化合物B. 该反应前后没有发生变化的粒子只有氧原子和氢原子C. 该反应的化学方程式为4NH3+5O24NO+6H2OD. 该反应读成:氨气加氧气在一定条件下生成一氧化氮加水7. 一定质量的某化合物完全燃烧,需要3.2g氧气,生成4.4g二氧化碳和1.8g水。
下列判断错误的是( )A. 参加反应的该化合物的质量为3.0gB. 该化合物中一定含有碳、氢、氧三种元素C. 该化合物中碳、氢、氧的原子个数比为2:4:1D. 该化合物中碳元素的质量分数为40%8. 从2H2+O22H2O中获取的信息错误的是( )A. 在反应前后,元素的种类没有变化B. 在常温下氢气与氧气混合就可以发生反应C. 4g氢气与32g氧气完全反应,可以生成36g水D. 在反应前后,氢原子和氧原子的数目都没有改变9. 漂白粉可用于自来水的杀菌消毒,其有效成分是次氯酸钙[化学式为Ca(ClO)2]。

化学方程式的专项练习一、写出下列反应的化学方程式:1、镁在空气中燃烧:______________________ _____2、铁在氧气中燃烧:____________________ _______3、铜在空气中受热:______________ _____________4、铝在空气中燃烧:_________________ __________5、氢气中空气中燃烧:__________ _______________6、红磷在空气中燃烧:_______________ ___ ______7、硫粉在空气中燃烧:__________________ _______11、利用过氧化氢和二氧化锰的混合物制氧气:____________________________12、水在直流电的作用下分解:___________________________________________13、加热氯酸钾:_______________________________________________________14、加热高锰酸钾:____________________________________________________二、题型变化:1、3Cu+8HNO3 ==3Cu(NO3)2+2X↑+4 H2O,求X的化学式为。
2、R+3O2==2CO2+3H2O 求R的化学式为。
3、4K2Cr2O8==4K2CrO4+2R+3O2求R的化学式为。
4、a C3H6+b O2==c CO2+d H2O 找出a、b、c 之间的等量关系。
三、计算题:1、二氧化碳和氢氧化钠反应化学方程式为2NaOH+CO2=Na2CO3+H2O,将CO2通入NaOH溶液中,溶液的质量比原来增加了13.2g,求:(1)参加反应的CO2的质量(2)求生成物Na2CO3的质量2、氯酸钾与二氧化锰的混合物26.5g,放入试管中加热,完全反应后剩余物质为16.9g,求:(1)生成氧气多少克?(2)有多少克氯酸钾发生了反应?(3)剩余固体中的物质是什么?质量各多少克?3、将一定质量的氯酸钾和二氧化锰的混合物充分加热,待完全反应后,收集到标准状况下3.36L氧气(密度为1.429g/L),剩余固体物质为11.45g,求原混合物的总质量?4、8g铁丝在氧气中燃烧可得到四氧化三铁多少克?同时消耗氧气多少克?在标准状况下,这些氧气体积占体积多少升?(标准状况下氧气的密度1.43g/L)5、质量为3.25g的金属锌与足量的盐酸反应,在标准状况下能生成多少升氢气?如果锌含有2%不跟HCl反应生成的杂质,则制得多少升?(标准状况下氢气的密度为0.09g/L)6、在标准状况下氢气密度为0.09 g/L,问标准状况下:(1)10 L氢气的质量是多少?(2)1.8 g氢气的体积是多少?7、某学生称取12.25 g氯酸钾(KClO3)制氧气,他用少量高锰酸钾(KMnO4)代替二氧化锰(MnO2),待反应完毕后,制得氧气4.96g。

单质与氧气的反应:(化合反应)1)1. 镁在空气中燃烧:Mg + O2 ===2. 铁在氧气中燃烧:Fe + O2===2)3铜在空气中受热:Cu + O2 ===4. 铝在空气中燃烧:Al + O2 ===5. 氢气中空气中燃烧:H2 + O2===6. 红磷在空气中燃烧(研究空气组成的实验):P + O2 ===7. 硫粉在空气中燃烧:S + O2===碳在氧气中充分燃烧:C + O2 ===8.9. 碳在氧气中不充分燃烧:C + O2 ===(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:CO + O2 ===11. 甲烷在空气中燃烧:CH4 + O2 ===12. 酒精在空气中燃烧:C2H5OH + O2 ===(3)氧气的来源:13.玻义耳研究空气的成分实验HgO ===14.加热高锰酸钾:KMnO4=== (实验室制氧气原理1)15.过氧化氢在二氧化锰作催化剂条件下分解反应H2O2=== (实验室制氧气原理2)二、自然界中的水:16.水在直流电的作用下分解(研究水的组成实验):H2O ===17.生石灰溶于水:CaO + H2O ==18.二氧化碳可溶于水:H2O + CO2==三、质量守恒定律:19.镁在空气中燃烧:Mg + O2 ===20.铁和硫酸铜溶液反应:Fe + CuSO4 ===21.氢气还原氧化铜:H2 + CuO===22. 镁还原氧化铜:Mg + CuO ===四、碳和碳的氧化物:(1)碳的化学性质23. 碳在氧气中充分燃烧:C + O2 ===24.木炭还原氧化铜:C+ CuO ===25.焦炭还原氧化铁:C+ Fe2O3 ===(2)煤炉中发生的三个反应:(几个化合反应)26.煤炉的底层:C + O2 ===27.煤炉的中层:CO2 + C ===28.煤炉的上部蓝色火焰的产生:CO + O2 ===(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应(实验室制二氧化碳):CaCO3 + HCl ==30.碳酸不稳定而分解:H2CO3 ==31.二氧化碳可溶于水:H2O + CO2==32.高温煅烧石灰石(工业制二氧化碳):CaCO3 ===33.石灰水与二氧化碳反应(鉴别二氧化碳):Ca(OH)2 + CO2 ===(4)一氧化碳的性质:34.一氧化碳还原氧化铜:CO+ CuO ===35.一氧化碳的可燃性:CO + O2 ===其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理):Na2CO3 + HCl ==燃料及其利用:37.甲烷在空气中燃烧:CH4 + O2===38.酒精在空气中燃烧:C2H5OH + O2===39.氢气中空气中燃烧:H2 + O2 ===六、金属(1)金属与氧气反应:40.镁在空气中燃烧:Mg + O2 ==41.铁在氧气中燃烧:Fe + O2 ===42. 铜在空气中受热:Cu + O2 ===43. 铝在空气中形成氧化膜:Al + O2 ====(2)金属单质+ 酸---盐+ 氢气(置换反应)44. 锌和稀硫酸Zn + H2SO4 =45. 铁和稀硫酸Fe + H2SO4 =46. 镁和稀硫酸Mg + H2SO4 =47. 铝和稀硫酸Al + H2SO4 =48. 锌和稀盐酸Zn + HCl ==49.铁和稀盐酸Fe + HCl ==50. 镁和稀盐酸Mg+ HCl ==51.铝和稀盐酸Al + HCl ==(3)金属单质+ 盐(溶液)---- 新金属+ 新盐52. 铁和硫酸铜溶液反应:Fe + CuSO4 ==53.锌和硫酸铜溶液反应:Zn + CuSO4 ==54.铜和硝酸汞溶液反应:Cu + Hg(NO3)2 ==(3)金属铁的治炼原理:55.CO+ Fe2O3===七、酸、碱、盐1、酸的化学性质(1)酸+ 金属--盐+ 氢气(见上)(2)酸+ 金属氧化物--盐+ 水56. 氧化铁和稀盐酸反应:Fe2O3 + HCl ==57.氧化铁和稀硫酸反应:Fe2O3 + H2SO4 ==58.氧化铜和稀盐酸反应:CuO + HCl ==59. 氧化铜和稀硫酸反应:CuO + H2SO4 ==(3)酸+ 碱--- 盐+ 水(中和反应)60.盐酸和烧碱起反应:HCl + NaOH ==61. 盐酸和氢氧化钙反应:HCl + Ca(OH)2 ==62.氢氧化铝药物治疗胃酸过多:HCl + Al(OH)3 ==63. 硫酸和烧碱反应:H2SO4 + NaOH ==63.(4)酸+ 盐----另一种酸+ 另一种盐64.大理石与稀盐酸反应:CaCO3 + HCl ==64.65.碳酸钠与稀盐酸反应: Na2CO3 + HCl == 66.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl==67. 硫酸和氯化钡溶液反应:H2SO4 + BaCl2 ==2、碱的化学性质(1)碱+ 非金属氧化物---- 盐+ 水68.苛性钠暴露在空气中变质:NaOH + CO2 == 69.苛性钠吸收二氧化硫气体:NaOH + SO2 == 70.苛性钠吸收三氧化硫气体:NaOH + SO3 == 71.消石灰放在空气中变质:Ca(OH)2 + CO2 == 72.消石灰吸收二氧化硫:Ca(OH)2 + SO2 ==(2)碱+ 酸-- 盐+ 水(中和反应,方程式见上)(3)碱+ 盐--- 另一种碱+ 另一种盐73. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 ==3、盐的化学性质(1)盐(溶液)+ 金属单质--- 另一种金属+ 另一种盐74. 铁和硫酸铜溶液反应:Fe + CuSO4 ==4、(2)盐+ 酸---- 另一种酸+ 另一种盐75.碳酸钠与稀盐酸反应: Na2CO3 + HCl ==碳酸氢钠与稀盐酸反应:NaHCO3 + HCl==(3)盐+ 碱---- 另一种碱+ 另一种盐76. 氢氧化钙与碳酸:Ca(OH)2 + Na2CO3 ==(4)盐+ 盐--- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 == 78.硫酸钠和氯化钡:Na2SO4 + BaCl2 ==。

化学方程式的专项练习一、写出下列反应的化学方程式:1、镁在空气中燃烧:______________________ _____2、铁在氧气中燃烧:____________________ _______3、铜在空气中受热:______________ _____________4、铝在空气中燃烧生成氧化铝:______________ __________5、氢气中空气中燃烧:__________ _______________6、红磷在空气中燃烧:_______________ ___ ______7、碳在氧气中燃烧:__________________ _______11、利用过氧化氢和二氧化锰的混合物制氧气:____________________________12、水在直流电的作用下分解:___________________________________________13、加热氯酸钾:_______________________________________________________14、加热高锰酸钾:____________________________________________________二、配平下列化学方程式:(一) 最小公倍数法:1、Al + O2——Al2O32、Al + Fe3O4——Fe + Al2O33、Fe + O2——Fe3O44、Al + MnO2——Mn + Al2O35、N2+ H2——NH36、Al + H2SO4——Al2(SO4)3 + H2(二) 观察法:1、CO + Fe2O3 ——Fe + CO22、C + Fe2O3——Fe + CO23、CO + Fe3O4 ——Fe + CO24、C + Fe3O4——Fe + CO25、H2 + Fe2O3——Fe + H2O6、H2 + Fe3O4——Fe + H2O10、H2 + WO3——W + H2O 11、CO + O2 ——CO212、Fe + H2O——H2 + Fe3O413、Al(OH)3+ HCl ——AlCl3 + H2O(三) 奇数配偶法:1、FeS2 + O2 ——Fe2O3 + SO22、C2H2 + O2——CO2+ H2O3、C + Fe2O3——Fe + CO24、MnO2 + HCl——MnCl2 + Cl2 + H2O5、Cl2 + Ca(OH)2——CaCl2 + Ca(ClO)2 + H2O(四) 归一法:1、C2H2 + O2——CO2 + H2O2、C6H6 + O2——CO2 + H2O3、C22H46 + O2——CO2 + H2O4、NH3 + Cl2 ——NH4Cl + N25、As2O3+ Zn + HCl——AsH3+ ZnCl2+ H2O6、C X H Y+ O2——CO2+ H2O三、题型变化:1、3Cu+8HNO3 ==3Cu(NO3)2+2X↑+4 H2O,求X的化学式为。

化学方程式练习题(含答案)一、化学方程式选择题1.下图是甲转化为丙的微观过程。
下列说法不正确的是・・・O 氨原子尊氧原子 「 ■硫原子甲乙丙A .反应前后原子种类不变B .转化①中甲和O 反应的分子个数比为1:21C .转化②是化合反应D .丙中氢、硫、氧元素的质量比为1:16:32 【答案】B 【解析】 【分析】根据微观示意图可知甲物质是H 2S ,乙物质是SO 2,丙物质是H 2SO 4。
【详解】A 、根据质量守恒定律可知,化学反应前后原子的种类、数目和质量不变,不符合题 意;B 、转化①发生的化学方程式是2H 2S+3O 2鲁=2SO 2+2H 2O ,甲和O 2反应的分子个数 比为2: 3,符合题意;C 、转化②是二氧化硫和过氧化氢反应生成硫酸,是多种物质反应 生成一种物质,属于化合反应,不符合题意;D 、丙中氢、硫、氧元素的质量比 1x 2:32x1:16 x 4 = 1:16:32,不符合题意。
故选B 。
2 .某化学反应的微观示意图如图下所示,由该图示不能得出的的结论是()•氢原子00十七卢 0*十OO o 氧原子甲 乙丙 丁。
氟原子A .该反应属于置换反应B .氟气比氧气更活泼C .反应前后分子数目没有改变D .丙不是氧化物【答案】C【解析】 根据反应条件和图中信息知,A 、反应物是一种单质和一种化合物,生成物是另一种单质 和另一种化合物,该反应属于置换反应;B 、活泼的置换不活泼的,氟气能把氧气置换出 来,说明氟气比氧气更活泼;C 、根据质量守恒定律,反应前4个分子,反应后5个分子, 反应前后应分子数目已改变;D 、丙是氟化氢,不是氧化物。
故选C 。
点睛:对于金属来说,活泼的置换不活泼的;对于非金属单质来说,同样是活泼的置换不 活泼的。
a £完全燃烧)转化①3 .下图为某反应的部分微观示意图,其中不同的球代表不同元素的原子。
下列说法正确的 是( )A .该反应属于置换反应B .参加反应的两种分子个数比为1:1 C. 1个X 分子中含有3个原子 D. 1个X 分子中含有3种不同的原子 【答案】C 【解析】 【分析】由图可知,不同球代表不同元素的原子,两种化合物反应生成单质与化合物,由原子守恒 可知,X 中含1个大黑球和2个小白球,以此来解答。

初中化学方程式练习题一、书写化学方程式1. 碳在氧气中燃烧二氧化碳。
2. 氢气与氧气在点燃条件下反应水。
3. 铁在氧气中燃烧四氧化三铁。
4. 铜在空气中加热氧化铜。
5. 铝与氧气反应氧化铝。
二、配平化学方程式1. \( \text{H}_2 + \text{O}_2 \rightarrow\text{H}_2\text{O} \)2. \( \text{C} + \text{O}_2 \rightarrow \text{CO}_2 \)3. \( \text{Fe} + \text{O}_2 \rightarrow\text{Fe}_3\text{O}_4 \)4. \( \text{Cu} + \text{O}_2 \rightarrow \text{CuO} \)5. \( \text{Al} + \text{O}_2 \rightarrow\text{Al}_2\text{O}_3 \)三、判断化学方程式正误1. \( \text{2H}_2 + \text{O}_2 \rightarrow\text{2H}_2\text{O} \)()2. \( \text{C} + \text{O}_2 \rightarrow \text{CO} \)()3. \( \text{3Fe} + \text{2O}_2 \rightarrow\text{Fe}_3\text{O}_4 \)()4. \( \text{2Cu} + \text{O}_2 \rightarrow \text{2CuO} \)()5. \( \text{4Al} + \text{3O}_2 \rightarrow\text{2Al}_2\text{O}_3 \)()四、根据化学方程式计算1. 氢气与氧气反应水,计算4克氢气与足量氧气反应水的质量。
2. 碳在氧气中燃烧二氧化碳,计算12克碳与足量氧气反应二氧化碳的质量。
3. 铁在氧气中燃烧四氧化三铁,计算56克铁与足量氧气反应四氧化三铁的质量。

化学方程式的专项练习一、写出下列反应的化学方程式:1、镁在空气中燃烧:______________________ _____2、铁在氧气中燃烧:____________________ _______3、铜在空气中受热:______________ _____________4、铝在空气中燃烧:_________________ __________5、氢气中空气中燃烧:__________ _______________6、红磷在空气中燃烧:_______________ ___ ______7、硫粉在空气中燃烧:__________________ _______11、利用过氧化氢和二氧化锰的混合物制氧气:____________________________12、水在直流电的作用下分解:___________________________________________13、加热氯酸钾:_______________________________________________________14、加热高锰酸钾:____________________________________________________一、计算题:1、二氧化碳和氢氧化钠反应化学方程式为,将通入NaOH溶液中,溶液的质量比原来增加了13.2g,求:(1)参加反应的的质量(2)求生成物的质量2、氯酸钾与二氧化锰的混合物26.5g,放入试管中加热,完全反应后剩余物质为16.9g,求:(1)生成氧气多少克?其体积为多少升(密度是1.429g/L)(2)有多少克氯酸钾发生了反应?(3)剩余固体中的物质是什么?质量各多少克?3、8g铁丝在氧气中燃烧可得到四氧化三铁多少克?同时消耗氧气多少克?4、某学生称取12.25 g氯酸钾(KClO3)制氧气,他用少量高锰酸钾(KMnO4)代替二氧化锰(MnO2),待反应完毕后,制得氧气4.96g。
初中化学方程式练习题.化学方程式的专项练习一、写出下列反应的化学方程式:1、镁在空气中燃烧:______________________ _____2、铁在氧气中燃烧:____________________ _______3、铜在空气中受热:______________ _____________4、铝在空气中燃烧:_________________ __________5、氢气中空气中燃烧:__________ _______________6、红磷在空气中燃烧:_______________ ___ ______7、硫粉在空气中燃烧:__________________ _______11、利用过氧化氢和二氧化锰的混合物制氧气:____________________________12、水在直流电的作用下分解:___________________________________________13、加热氯酸钾:_______________________________________________________14、加热高锰酸钾:____________________________________________________二、配平下列化学方程式:(一) 最小公倍数法:1、Al + O2——Al2O32、Al + Fe3O4——Fe + Al2O33、Fe + O2——Fe3O44、Al + MnO2——Mn + Al2O35、N2+ H2——NH36、Al + H2SO4——Al2(SO4)3 + H2(二) 观察法:1、CO + Fe2O3 ——Fe + CO22、C + Fe2O3——Fe + CO23、CO + Fe3O4 ——Fe + CO24、C + Fe3O4——Fe + CO25、H2 + Fe2O3——Fe + H2O6、H2 + Fe3O4——Fe + H2O10、H2 + WO3——W + H2O 11、CO + O2 ——CO212、Fe + H2O——H2 + Fe3O413、Al(OH)3+ HCl ——AlCl3 + H2O(三) 奇数配偶法:1、FeS2 + O2 ——Fe2O3 + SO22、C2H2 + O2——CO2+ H2O3、C + Fe2O3——Fe + CO24、MnO2 + HCl——MnCl2 + Cl2 + H2O5、Cl2 + Ca(OH)2——CaCl2 + Ca(ClO)2 + H2O(四) 归一法:1、C2H2 + O2——CO2 + H2O2、C6H6 + O2——CO2 + H2O3、C22H46 + O2——CO2 + H2O4、NH3 + Cl2 ——NH4Cl + N25、As2O3+ Zn + HCl——AsH3+ ZnCl2+ H2O6、C X H Y+ O2——CO2+ H2O三、题型变化:1、3Cu+8HNO3 ==3Cu(NO3)2+2X↑+4 H2O,求X的化学式为。
2、R+3O2==2CO2+3H2O 求R的化学式为。
3、4K2Cr2O8==4K2CrO4+2R+3O2求R的化学式为。
4、a C3H6+b O2==c CO2+d H2O 找出a、b、c 之间的等量关系。
四、根据信息书写化学方程式练习:1、发射卫星的火箭用联氨(N2H4)作燃料,以四氧化二氮(N2O4)作氧化剂,燃烧尾气由氮气和水蒸气组成。
试写出反应的化学方程式。
2、用粮食作原料酿酒时,往往发现制得的酒发酸,这实际上是因为酒精(C2H5OH)在酶的作用下与空气中的氧气作用,生成了醋酸(CH3COOH)和水,请你写出该反应的化学方程式为。
3、工业上常用接触法制硫酸(H2SO4),所使用的原料是硫铁矿(主要含FeS)。
在高温下,将硫铁矿的粉末与氧气充分反应生成三氧化二铁和二氧化硫,再经过一系列转化可生成硫酸。
试写出硫铁矿与氧气反应的化学方程式,在这个反应中铁由+2价升到+3价,硫元素的化合价由。
4、壁画颜料中的铅白[Pb2(OH)2CO3]由于受到空气中硫化氢气体的作用而变成黑色硫化铅(PbS),影响画面的色泽。
当用双氧水处理时就可以使黑色的硫化铅氧化成白色硫酸铅和水,试写出双氧水处理硫化铅的化学方程式。
5、哥伦比亚号航天飞机曾用金属铝和高氯酸铵(NH4ClO4)的混合物作为固体燃料。
加热铝粉使其被氧气氧化,放出大量的热,促使混合物中的高氯酸铵受热分解,同时生成四种气体:两种气体是空气中的主要成分,一种气体是Cl2,还有一种气体是化合物(常温下是液态),因而产生巨大的推动力。
试写出其中涉及的化学方程式:⑴、铝粉被氧气氧化成三氧化二铝:;⑵、高氯酸铵受热分解:;6、在通常情况下,碳单质的化学性质稳定,但它在常温下可与一种叫高氯酸的物质发生反石墨,产物除水是液体外,其余都是气体,一种是有毒的氯气(Cl2),一种是无色无毒的化合物。
请写出此反应的化学方程式:。
7、砷化氢AsH3是一种很强的还原剂,在室温下它能在空气中自燃,其氧化产物是砒霜(As2O3),写出该反应的化学方程式:8、将黑色氧化铜粉末装入试管中加热,通入氨气(NH3)则生成红色的铜、水和一种气体单质,该反应的化学方程式:一、计算题:1、二氧化碳和氢氧化钠反应化学方程式为,将通入NaOH溶液中,溶液的质量比原来增加了13.2g,求:(1)参加反应的的质量(2)求生成物的质量2、氯酸钾与二氧化锰的混合物26.5g,放入试管中加热,完全反应后剩余物质为16.9g,求:(1)生成氧气多少克?其体积为多少升(密度是1.429g/L)(2)有多少克氯酸钾发生了反应?(3)剩余固体中的物质是什么?质量各多少克?4、将一定质量的氯酸钾和二氧化锰的混合物充分加热,待完全反应后,收集到标准状况下3.36L氧气(密度为1.429g/L),剩余固体物质为11.45g,求原混合物的总质量?5、8g铁丝在氧气中燃烧可得到四氧化三铁多少克?同时消耗氧气多少克?在标准状况下,这些氧气体积占体积多少升?(标准状况下氧气的密度1.43g/L)6、质量为3.25g的金属锌与足量的盐酸反应,在标准状况下能生成多少升氢气?如果锌含有2%不跟HCl反应生成的杂质,则制得多少升?(标准状况下氢气的密度为0.09g/L)7、在标准状况下氢气密度为0.09 g/L,问标准状况下:(1)10 L氢气的质量是多少?(2)1.8 g氢气的体积是多少?1、某学生称取12.25 g氯酸钾(KClO3)制氧气,他用少量高锰酸钾(KMnO4)代替二氧化锰(MnO2),待反应完毕后,制得氧气4.96g。
该学生加入了多少克高锰酸钾?2、甲醇( CH3OH )是一种有毒,有酒的气味的可燃性液体。
甲醇在氧气中不完全燃烧可发生如下反应:8CH3O H +nO2mCO2+2CO + 16H2 O。
若反应生成3.6g 水,请计算:( 1 )m值是;( 2 )参加反应的氧气质量是多少克?(写出规范计算步骤)3、实验室用加热分解氯酸钾的方法制取氧气,若制取9.6g氧气,试计算参加反应的氯酸钾的质量。
4、将KClO3和MnO2的混合物15.5克,加热完全反应后,剩余固体加水溶解,过滤,洗涤不溶物,洗涤液与滤液合并,得100克溶质质量分数为7.45%的溶液,求(1)产生O2的质量;(2)原混合物中MnO2的质量。
5、工业上用电解氯化镁的方法生产金属镁,反应的化学方程式为:MgCl2 直流电Mg + Cl2↑,若生产240 kg金属镁,理论上需电解氯化镁多少千克?6、高温下煅烧含杂质为5%的石灰石100吨,问可得到含杂质的生石灰多少吨?(高温煅烧时,杂质不分解)7、4g镁带在氧气中充分燃烧,生成物的质量比4g镁带重,增重了多少克?8、13g锌与足量的盐酸反应生成的氢气能与多少克氧气恰好完全反应生成水?这些氧气需要分解多少克氯酸钾才能制得?9、在反应2A + B = 3C + D中,A和B的相对分子质量之比为5﹕1,已知20克A与一定质量的B恰好反应,生成5克D,则在此反应中B和C的质量比为( )10、化学方程式aC2H2+bO2 = cH2O+dCO2则a、b、c、d等数之和为()11、在反应A+2B=C+2D中,9.8gA与8gB完全反应,生成14.2gC,则下列结论正确的是()A、生成D1.8gB、质量比为49∶40∶71∶18C、生成D7.2gD、相对分子质量比98∶80∶142∶3613、9g水在通电条件下可生成氢气的质量是()14、在2A+B == 2C反应中,已知A的相对分子质量为24,C 的相对分子质量为40,则B的相对分子质量为()15、在化学反应X + 2Y ==== Z中,3g X和足量Y充分反应后生成8g Z,则参加反应的Y的质量为()16、植物的光合反应可以用下式表示:,在该反应中,若植物吸收了54g和132g,那么在生成90g的同时,释放的氧气质量为()17、己知反应3A+2B 2C+D,A、B两物质完全反应时的质量比为3:4,若生成C和D共140g,则该反应消耗B的质量为18、对于化学方程式2H2+O2 =2H2O的意义叙述正确的是A.氢气加氧气点燃等于水B.两个氢气和一个氧气点燃生成两个水C.每4份质量的氢气和32份质量的氧气点燃生成36份质量的水D.32g氢气和4g氧气点燃生成36g水19、A、B、C三种物质各15 g,它们化合时只能生成30 g新物质D。
若增加10 g A,则反应停止后,原反应物中只余C。
根据上述条件推断下列说法中正确的是A.第一次反应停止后,B剩余9g B.第二次反应后,D的质量为55 gC.反应中A和B的质量比是3∶2 D.反应中A和C的质量比是5∶220、2A + 3B== C +3D 中A和C的相对分子质量比为3:38,D 的相对分子质量为2 。
已知一定量的A和B恰好完全反应,生成34.2gC 和0.6gD,则B的相对分子质量为21、A、B、C三种物质各15g,它们化合时只能生成30g新物质D.若增加10gA,则反应停止后,原反应物中只余C.根据上述条件推断下列说法中正确的是A.第一次反应停止后,B剩余9g B.第二次反应后,D的质量为50gC.反应中A和B的质量比是3:2 D.反应中A和C的质量比是5:322、等质量的氢气、碳、镁、铁分别在足量的氧气中充分燃烧,消耗氧气的质量最多的是23、在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表:请根据质量守恒定律判断x的值()24、在电解水的化学反应中,H2O、H2、O2的质量比为 ( )A.9:1:16B.9:1:8C.9:2:8D.10:1:925、在反应2A+5B=2C+4D中,C、D的相对分子质量之比为9:22,若2.6gA与B完全反应,生成8.8gD,则在此反应中B与D的质量比为()28、3克碳与10克氧气完全反应后,生成CO2的质量是()30、在反应A+2B====C+D中,5.6 g A与7.3 g B恰好完全反应生成12.7 g C,现要得到0.6 g D,则所需要A的质量为31、电解9 g水,得到氢气、氧气的质量分别是32、在反应3X+4Y=2Z中,已知X的相对分子质量是32,Z的相对分子质量是102,则Y的相对分子质量为()A.27B.70C.108D.17234、相同质量的下列物质在氧气中完全燃烧,消耗氧气最多的是[ ]A.H2B.P C.C D.S35、相同质量的下列物质全部分解后,放出氧气最多的是____;放出氧气最少的是____。