化学方程式练习题经典
- 格式:doc
- 大小:181.50 KB
- 文档页数:10

化学方程式练习一、写出下列反应的化学方程式:1、镁在空气中燃烧:______________________ _____2、铁在氧气中燃烧:____________________ _______3、铜在空气中受热:______________ _____________4、铝在空气中燃烧:_________________ __________5、红磷在空气中燃烧:_______________ ___ ______6、硫粉在空气中燃烧:__________________ _______7、利用过氧化氢和二氧化锰的混合物制氧气:____________________________8、水在直流电的作用下分解:___________________________________________二、配平下列化学方程式:(一)最小公倍数法:(找出两边同种原子的个数最多的原子,然后求最小公倍数,得原子个数。
)1、 Al + O2—— Al2O32、Al + Fe3O4—— Fe + Al2O33、 Fe + O2—— Fe3O44、Al + MnO2—— Mn + Al2O35、 N2 + H2—— NH36、Al + H2SO4—— Al2(SO4)3 + H2(二)观察法:(观察顺序:从复杂入手,推导其它)(具体观察顺序——O、C、Fe)1、 CO + Fe2O3 —— Fe + CO22、 C + Fe2O3—— Fe + CO23、 CO + Fe3O4 —— Fe + CO24、 C + Fe3O4—— Fe + CO25、 CO + FexOy —— Fe + CO26、 C + FexOy—— Fe + CO27、 H2 + Fe2O3—— Fe + H2O 8、H2 + Fe3O4—— Fe + H2O9、 H2 + Fe X O Y—— Fe + H2O 10、H2 + WO3—— W + H2O11、 CO + O2 —— CO2 12、Fe + H2O—— H2+ Fe3O413、 Al(OH)3+ HCl ——AlCl3 + H2O(三)奇数配偶法:(找出左右两边出现次数较多的元素,该元素的原子个数在两边为一基数一偶数)1、 FeS2 + O2 —— Fe2O3 + SO22、 C2H2 + O2——CO2+ H2O3、 C + Fe2O3—— Fe + CO24、 MnO2 + HCl—— MnCl2 + Cl2 + H2O5、 Cl2 + Ca(OH)2—— CaCl2 + Ca(ClO)2 + H2O(四)归一法:(找出化学式中原子数目最多的化学式,使其化学计量数为“1”,观察配平,若是分数再进行通分去掉分母,保证最后得到最简整数比)1、 C2H2 + O2——CO2 + H2O2、C6H6 + O2—— CO2 + H2O3、 C22H46 + O2——CO2 + H2O4、 NH3 + Cl2 —— NH4Cl + N25、 As2O3+ Zn + HCl——AsH3+ ZnCl2+ H2O6、C X H Y+ O2——CO2+ H2O三、题型变化:1、在X + 2O2===CO2 + 2H2O的反应中,根据质量守恒定律可判断出X的化学式为:A COB CH 4C CH 3OHD C 2H 42、 某纯净物X 在空气中完全燃烧,反应式为: X + 3 O 2=== 2CO 2 + 3 H 2O ,根据质量守恒定律可判断出X的化学式为:A C 2H 4BC 2H 4O C C 2H 6D C 2H 6O3、在4Cu + 10HNO 3 = 4Cu(NO 3)3 + X + 5H 2O 反应方程式中,X 的化学式为:A NOB NO 2C N 2OD N 2O 34、物质X 和B 2能发生下列反应:2X + B 2 = 2 AB 3,则X 的化学式是:A AB 2 B A 2B 2C AB 3D A 2B 35、 某化合物R 在空气燃烧后生成二氧化碳和水,下列关于R 化学式叙述正确的是:A R 一定含有碳,氢,氧三种元素B R 一定含有碳和氢元素,不含有氧元素C R 一定含有碳和氢元素,可能含有氧元素D R 不一定含有碳和氢元素,但一定不含有氧元素6、 某物质W 在氧气中充分燃烧后,生成了4.4克CO 2和3.6克的水,消耗的氧气为6.4克 ,则W 中所含有的元素判断正确的是:A . 一定含有C H 元素,不含O 元素 B. 一定含有 C H 元素,可能有O 元素C. 一定含有C H O 三种元素D. 条件不足,不能判断7、 对于质量守恒定律的解释不正确的是:A 化学反应前后,分子的数目不变B 化学反应前后,原子的种类不变。

【化学】 化学方程式的计算练习题(含答案)经典一、中考化学方程式的计算1.碳酸氢钠用于焙制糕点,在270℃时分解:323222NaHCO Na C ΔO H O CO ++↑。
现取3NaHCO 16.8g ,在敞口容器中加热到质量不再改变为止,减少的质量为( ) A .4.4gB .6.2gC .8.8gD .10.6g【答案】B【解析】【分析】【详解】根据题意可知,在敞口容器中加热到质量不再改变为止,剩余物质为固体碳酸钠。
此题为固体的差量计算,设减少的质量为x 。
323222NaHCO Na CO +H O +CO 1681066216.8g x ↑△固体减少的质量16816.8g =62xx=6.2g2.铝被称为“年轻的金属”,工业上用电解氧化铝的方法制取金属铝。
反应的化学方程式为2Al 2O 3通电 4Al +3O 2↑。
请计算生成1.08t 金属铝,理论上需要氧化铝的质量是多少____?【答案】2.04t【解析】【分析】【详解】解:设生成1.08t 金属铝,理论上需要氧化铝的质量为x 2322Al O 4Al +3O 204108x 1.08t↑通电 204x =108 1.08tx=2.04t答:生成1.08t 金属铝,理论上需要氧化铝的质量为2.04t 。
3.我国科学家实现电催化高效分解硫化氢制氢技术,反应的化学方程式为H 2S 一定条件S ↓ +H 2 .请计算生产 3吨 H 2,理论上需要 H 2S 多少吨?【答案】51吨【解析】【分析】【详解】解:设理论上需要H 2S 的质量为x22S +H 342x3tH S ↓一定条件34x =23tx=51 t答:理论上需要H 2S 51吨。4.某工厂需要16kg 氧气作原料,若用电解水的方法制取这些氧气,消耗水的质量是_________?(要求写出计算过程)【答案】18kg【解析】【分析】【详解】设消耗水的质量为x2222H O2H +O 3632x 16kg↑↑通电 36x =3216kgx=18kg答:消耗水的质量是18kg 。

化学方程式配平一化学方程式的基础知识:1化学方程式配平常用方法:最小公倍数法、奇数配偶法(先配奇数大):(1) P + O2 点燃P2O5 (2) C + O2点燃CO(3) Al + O2点燃Al2O3 (4)Fe + O2点燃Fe3O4(5) Mg + O2点燃MgO (6) H2O2MnO2 H2O + O2↑(7) H2O 通电H2↑+ O2↑(8) H2+ O2点燃H2O2观察法:先金属后原子团(1)CuSO4 +NaOH —Na2SO4 + Cu(OH)2(2)Mg + HCl —MgCl2+ H2↑(3)Fe2O3 + H2SO4Fe2(SO4)3+ H2O(4)Al + H2SO4 —Al2(SO4)3+ H2↑(5)Fe(OH)3 + H2SO4Fe2(SO4)3+ H2O(6)Al2(SO4)3 +NaOH —Na2SO4 + Al(OH)33配平下列的各个化学反应的方程式:(1)KMnO4—K2MnO4+ MnO2+ O2↑(2)Al + CuSO4 —Al2(SO4)3 + Cu(3)Zn + HCl —ZnCl2 + H2↑(4)Al2O3 + H2SO4Al2(SO4)3 + H2O(5)Fe2(SO4)3+NaOH —Na2SO4+ Fe(OH)3(6)Fe(OH)3+ H2SO4Fe2(SO4)3+ H2O(7)CH4+ O2点燃CO2 + H2O(8) C + CO2高温CO(9)NH3+ O2催化剂NO + H2O(10) CO + Fe2O3高温Fe + CO2二练习1 在X + 2O2===CO2 + 2H2O的反应中,根据质量守恒定律可判断出X的化学式为:A COB CH4C CH3OHD C2H42某纯净物X在空气中完全燃烧,反应式为:X + 3 O2=== 2CO2 + 3 H2O,根据质量守恒定律可判断出X的化学式为:A C2H4B C2H4OC C2H6D C2H6O3在4Cu + 10HNO3 = 4Cu(NO3)3 + X + 5H2O反应方程式中,X的化学式为:A NOB NO2C N2OD N2O34物质X和B2能发生下列反应:2X + B2 = 2 AB3,则X的化学式是:A AB2B A2B2C AB3D A2B35某化合物R在空气燃烧后生成二氧化碳和水,下列关于R化学式叙述正确的是:A R一定含有碳,氢,氧三种元素B R一定含有碳和氢元素,不含有氧元素C R一定含有碳和氢元素,可能含有氧元素D R不一定含有碳和氢元素,但一定不含有氧元素6某物质W在氧气中充分燃烧后,生成了4.4克CO2和3.6克的水,消耗的氧气为6.4克,则W中所含有的元素判断正确的是:A 一定含有C H元素,不含O元素B 一定含有C H 元素,可能有O元素C 一定含有C H O三种元素D 条件不足,不能判断7氢气与氧气反应生成水的反应过程中,氢气与氧气的质量之比是:A 1 :1B 2 :1C 2 :32D 4 :328对于质量守恒定律的解释不正确的是:A 化学反应前后,分子的数目不变B 化学反应前后,原子的种类不变。

第五单元:化学方程式一、写出下列反应的化学方程式并注明反应类型:(1—6题每题1分,其余每空2 分,共50分)1、碳的燃烧:2、硫的燃烧:3、磷的燃烧:4、铁的燃烧:5、镁的燃烧:6、铜在空气中加热:7、氢气的燃烧:8、用过氧化氢制氧气9、用氯酸钾制氧气10、用高锰酸钾制氧气11、电解水12、碳酸钙与盐酸的反应13、碳酸钠与盐酸的反应14、锌与盐酸(HCl)的反应15、锌与硫酸(H2SO4)的反应16、铁与硫酸铜的反应17、高温煅烧石灰石(CaCO3)18、氢气与氧化铜的反应19、氢气在氯气中燃烧20、硫酸铜与氢氧化钠的反应21、毒品大麻的化学式为C21H30O2,销毁大麻的方法是在空气中焚烧。
写出在空气中焚烧大麻生成二氧化碳和水的化学方程式。
22、黑火药是我国四大发明之一,古代生产黑火药是把木炭、硫粉、硝石(KNO3)按一定比例混合制成的,黑火药爆炸时产生硫化钾、氮气和二氧化碳。
试写出黑火药爆炸的化学方程式。
23、一些豆科植物能将空气中的氮气转化为能被植物吸收的含氮的化合物,其反应是氮气、碳和水在根瘤菌的催化作用下,生成氨气(NH3)和二氧化碳,试写出该反应的化学方程式。
24、过氧化钠(Na2O2)与二氧化碳反应生成碳酸钠和氧气,试写出该反应的化学方程式。
25、工业上用电解氯化镁来生产金属镁和氯气,试写出该反应的化学方程式。
二、化学方程式的计算:(每题5分,共20分)26、实验室用一定量的二氧化锰催化分解6.8g过氧化氢制取氧气,求可制得氧气的质量是多少?27、氯酸钾、二氧化锰的混合物26g,加热后完全反应,最后剩余物质的质量为16.4g。
求:(1)生成氧气的质量;(2)原混合物中二氧化锰的质量;(3)原混合物中氯酸钾的质量分数。
28、向8g不纯的氧化铜中通入足量的氢气,充分反应后测得剩余固体的质量为7.2g。
求参加反应氧化铜的质量。
29、小强同学前往当地的石灰石矿区进行调查,他取回了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测,采用了以下的办法:取用8g这种石灰石样品,把40g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的杂质不溶于水,不与盐酸反应)。

初中化学方程式练习题一、书写化学方程式1. 碳在氧气中燃烧二氧化碳。
2. 氢气与氧气在点燃条件下反应水。
3. 铁在氧气中燃烧四氧化三铁。
4. 铜在空气中加热氧化铜。
5. 铝与氧气反应氧化铝。
二、配平化学方程式1. \( \text{H}_2 + \text{O}_2 \rightarrow\text{H}_2\text{O} \)2. \( \text{C} + \text{O}_2 \rightarrow \text{CO}_2 \)3. \( \text{Fe} + \text{O}_2 \rightarrow\text{Fe}_3\text{O}_4 \)4. \( \text{Cu} + \text{O}_2 \rightarrow \text{CuO} \)5. \( \text{Al} + \text{O}_2 \rightarrow\text{Al}_2\text{O}_3 \)三、判断化学方程式正误1. \( \text{2H}_2 + \text{O}_2 \rightarrow\text{2H}_2\text{O} \)()2. \( \text{C} + \text{O}_2 \rightarrow \text{CO} \)()3. \( \text{3Fe} + \text{2O}_2 \rightarrow\text{Fe}_3\text{O}_4 \)()4. \( \text{2Cu} + \text{O}_2 \rightarrow \text{2CuO} \)()5. \( \text{4Al} + \text{3O}_2 \rightarrow\text{2Al}_2\text{O}_3 \)()四、根据化学方程式计算1. 氢气与氧气反应水,计算4克氢气与足量氧气反应水的质量。
2. 碳在氧气中燃烧二氧化碳,计算12克碳与足量氧气反应二氧化碳的质量。
3. 铁在氧气中燃烧四氧化三铁,计算56克铁与足量氧气反应四氧化三铁的质量。


化学方程式的书写练习一、化合反应:1、碳在氧气中完全燃烧生成二氧化碳。
2、碳在氧气中不完全燃烧生成一氧化碳。
3、一氧化碳在氧气中点燃生成二氧化碳。
4、二氧化碳在灼热的碳中生成一氧化碳。
5、往水中通入二氧化碳,生成碳酸。
6、铁在氧气中点燃生成四氧化三铁。
7、磷在氧气中点燃生成五氧化二磷。
8、铜在空气中加热生成氧化铜。
9、硫在氧气中点燃生成二氧化硫。
10、氢气在空气中点燃生成水。
11、氢气在氯气中点燃生成氯化氢气体。
12、氧化钙加水生成氢氧化钙。
二、分解反应:13、在二氧化锰的催化作用下加热氯酸钾,生成氯化钾和氧气。
14、加热高锰酸钾,生成锰酸钾、二氧化锰和氧气。
15、电解水,生成氢气和氧气。
16、在二氧化锰的催化作用下分解双氧水,生成水和氧气。
17、加热碳酸,分解为二氧化碳和水。
18、碳酸钙高温生成氧化钙和二氧化碳。
19、碳酸氢钠加热生成碳酸钠和二氧化碳。
20、加热碱式碳酸铜,生成氧化铜、水和二氧化碳。
(一)生成二氧化碳气体。
21、碳酸钙和稀盐酸反应,生成氯化钙、水和二氧化碳。
22、碳酸钠和稀盐酸反应,生成氯化钠、水和二氧化碳。
(二)生成水25、氢氧化钙和二氧化碳反应,生成碳酸钙沉淀和水三、氧化还原反应:26、氢气还原氧化铜,加热,生成铜和水。
27、碳还原氧化铜,高温,生成铜和二氧化碳。
28、一氧化碳还原氧化铜,加热,生成铜和二氧化碳。
29、一氧化碳还原氧化铁,高温,生成铁和二氧化碳。
30、一氧化碳还原氧化铁,高温,生成铁和二氧化碳六、其他反应:31、甲烷在空气中点燃,生成二氧化碳和水。
1.化学反应在防治环境污染中扮演了重要角色。
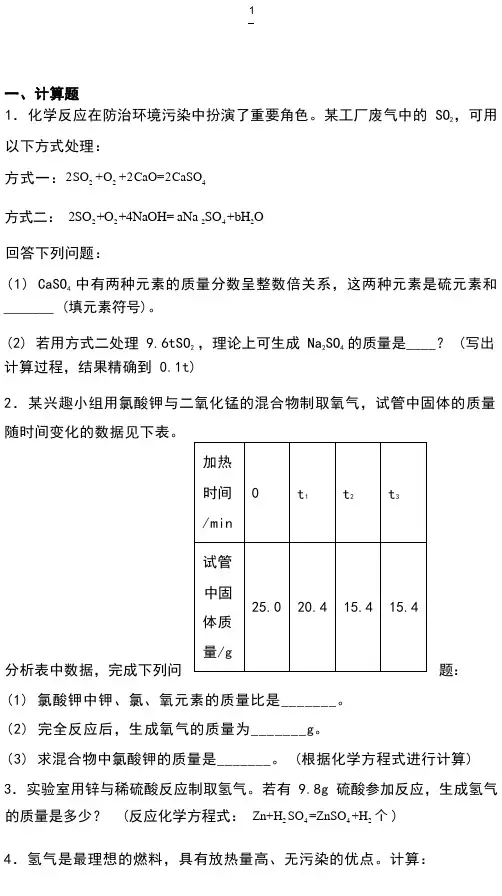
某工厂废气中的 SO2,可用以下方式处理:方式一:2SO2 +O2+2CaO=2CaSO4方式二:2SO2 +O2 +4NaOH= aNa 2SO4 +bH2O回答下列问题:(1) CaSO4中有两种元素的质量分数呈整数倍关系,这两种元素是硫元素和_______ (填元素符号)。
(2) 若用方式二处理 9.6tSO2 ,理论上可生成 Na2SO4的质量是____? (写出计算过程,结果精确到 0.1t)2.某兴趣小组用氯酸钾与二氧化锰的混合物制取氧气,试管中固体的质量随时间变化的数据见下表。
(1) 氯酸钾中钾、氯、氧元素的质量比是_______。
(2) 完全反应后,生成氧气的质量为_______g。
(3) 求混合物中氯酸钾的质量是_______。
(根据化学方程式进行计算) 3.实验室用锌与稀硫酸反应制取氢气。
若有 9.8g 硫酸参加反应,生成氢气的质量是多少? (反应化学方程式:Zn+H2 SO4=ZnSO4+H2个)4.氢气是最理想的燃料,具有放热量高、无污染的优点。
计算:分析表中数据,完成下列问题:(1) 10kg 氢气完全燃烧可生成水的质量是多少?(2) 消耗氧气的质量至少是多少?5.碳酸氢钠固体受热易分解生成一种盐和两种氧化物,反应的化学方程式为______;将 10g 碳酸钠和碳酸氢钠的混合物充分加热至固体的质量不再改变,冷却,称量剩余固体的质量为 6.9g,则原混合物中碳酸钠和碳酸氢钠的质量比为______。
6.实验室常用氯酸钾和二氧化锰的混合物制取氧气。
现有氯酸钾和二氧化锰的混合物 50g,完全反应后称量剩余物质的质量为 40.4g。
请计算:(1) 制得氧气的质量为__________。
(2) 混合物中氯酸钾的质量分数。
7.加热氯酸钾和二氧化锰固体混合物来制取氧气时,反应时间和剩余固体质量的关系如图所示。
计算:的质量是___________g。

化学方程式计算练习题1. 计算下列化学反应中,如果生成物中二氧化碳的质量为44g,那么需要多少质量的碳酸钙反应?CaCO3 → CaO + CO2↑2. 某化学反应中,甲烷和氧气反应生成二氧化碳和水,如果甲烷的质量为16g,计算生成的二氧化碳的质量。
CH4 + 2O2 → CO2 + 2H2O3. 铁与稀硫酸反应生成硫酸亚铁和氢气,若生成的氢气质量为2g,计算反应中消耗的铁的质量。
Fe + H2SO4 → FeSO4 + H2↑4. 铜与硝酸银溶液反应生成硝酸铜溶液和银,若生成的银质量为216g,计算反应中消耗的铜的质量。
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag5. 碳酸氢铵受热分解生成氨气、水和二氧化碳,若生成的二氧化碳质量为88g,计算反应中消耗的碳酸氢铵的质量。
NH4HCO3 → NH3↑ + H2O + CO2↑6. 硫酸铜与氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,若生成的氢氧化铜质量为98g,计算反应中消耗的硫酸铜的质量。
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO47. 锌与稀盐酸反应生成氯化锌和氢气,若生成的氢气质量为0.2g,计算反应中消耗的锌的质量。
Zn + 2HCl → ZnCl2 + H2↑8. 碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,若生成的二氧化碳质量为22g,计算反应中消耗的碳酸钠的质量。
Na2CO3 + 2HCl → 2NaCl + H2O + CO2↑9. 镁条在空气中燃烧生成氧化镁和氮气,若生成的氧化镁质量为60g,计算反应中消耗的镁的质量。
2Mg + O2 → 2MgO10. 硫酸和氢氧化钡反应生成硫酸钡沉淀和水,若生成的硫酸钡沉淀质量为233g,计算反应中消耗的硫酸的质量。
H2SO4 + Ba(OH)2 → BaSO4↓ + 2H2O。
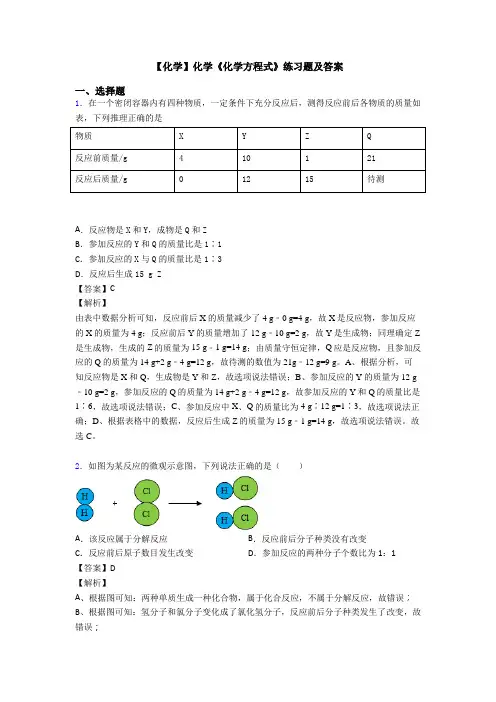
【化学】化学《化学方程式》练习题及答案一、选择题1.在一个密闭容器内有四种物质,一定条件下充分反应后,测得反应前后各物质的质量如表,下列推理正确的是物质X Y Z Q反应前质量/g410121反应后质量/g01215待测A.反应物是X和Y,成物是Q和ZB.参加反应的Y和Q的质量比是1∶1C.参加反应的X与Q的质量比是1∶3D.反应后生成15 g Z【答案】C【解析】由表中数据分析可知,反应前后X的质量减少了4 g﹣0 g=4 g,故X是反应物,参加反应的X的质量为4 g;反应前后Y的质量增加了12 g﹣10 g=2 g,故Y是生成物;同理确定Z 是生成物,生成的Z的质量为15 g﹣1 g=14 g;由质量守恒定律,Q应是反应物,且参加反应的Q的质量为14 g+2 g﹣4 g=12 g,故待测的数值为21g﹣12 g=9 g。
A、根据分析,可知反应物是X和Q,生成物是Y和Z,故选项说法错误;B、参加反应的Y的质量为12 g ﹣10 g=2 g,参加反应的Q的质量为14 g+2 g﹣4 g=12 g,故参加反应的Y和Q的质量比是1∶6,故选项说法错误;C、参加反应中X、Q的质量比为4 g∶12 g=1∶3,故选项说法正确;D、根据表格中的数据,反应后生成Z的质量为15 g﹣1 g=14 g,故选项说法错误。
故选C。
2.如图为某反应的微观示意图,下列说法正确的是()A.该反应属于分解反应B.反应前后分子种类没有改变C.反应前后原子数目发生改变D.参加反应的两种分子个数比为1:1【答案】D【解析】A、根据图可知:两种单质生成一种化合物,属于化合反应,不属于分解反应,故错误;B、根据图可知:氢分子和氯分子变化成了氯化氢分子,反应前后分子种类发生了改变,故错误;C 、由微粒的变化可知,反应前后原子数目没有发生改变,故错误;D 、由微粒的变化可知,参加反应的两种分子个数比为1:1,故正确。
点睛:化学反应的实质一般是指在化学变化中,分子分成原子,原子重新组合成新的分子(或直接聚集构成新物质)。
【化学】化学《化学方程式》练习题及答案一、选择题1.CH 4和某种氮的氧化物反应的化学方程式为CH 4+2口催化剂N 2+CO 2+2H 2O ,则框内物质的化学式是 A .NO B .NO 2C .N 2OD .N 2O 5【答案】B 【解析】试题分析:化学变化前后各种原子的个数不变,反应后有2N 、C 、4H 、4O ,而反应前有4H 、一个C 原子,反应前后差2N 、4O ,所以框内物质的化学式为NO 2,故选B 考点:质量守恒定律的应用2.将一定质量的氧化铜和氧化铁混合粉末与足量的CO 充分反应后,测得质量减少了4.0g 。
另取等质量的该粉末用适量的稀硫酸完全溶解后,再加入足量的氢氧化钠溶液,得到了20.5g 的沉淀。
则粉末中的氧化铜的质量分数为 A .20% B .40%C .50%D .80%【答案】C 【解析】 【分析】分别假设氧化铜和氧化铁的质量,进而结合化学方程式、关系式及对应的数据求解,进而求出粉末中氧化铜的质量分数。
【详解】设粉末中氧化铜的质量为x ,氧化铁的质量为y ,21CO +CuO Cu +CO 806416x m 高温固体质量减少116x xm ==80523223CO +Fe O 2Fe +3CO 16011248ym 高温固体质量减少248y 3ym ==16010氧化铜与稀硫酸反应生成硫酸铜和水,硫酸铜与氢氧化钠反应生成氢氧化铜沉淀和硫酸钠;氧化铁和稀硫酸反应生成硫酸铁和水,硫酸铁和氢氧化钠反应生成氢氧化铁沉淀和硫酸钠,根据元素守恒列关系式:423CuO ~CuSO ~Cu(OH)8098xm398x 49xm ==80402324334Fe O ~Fe (SO )~2Fe(OH)160214ym4214y 107ym ==16080结合题干,列出方程:x 3y+=4.051049x 107y+=20.54080解得x=8g ,y=8g则粉末中氧化铜的质量分数为:8g100%50%8g+8g⨯= ,故选C 。
化学方程式练习题(含答案)经典一、化学方程式选择题1.科学家采用“组分转化”技术,将 CO2和H2按一定比例混合,在一定条件下反应的化学方程式为2CO2 + 6H2= X + 4H2O中,X的化学式是A.CH4 B.C2H4 C.H2CO3 D.H2C2O4【答案】B【解析】化学反应前后各种原子个数相等,反应前有2C、4O、12H,反应后(X除外)有4O、8H,所以x中有有2C、4H,X的化学式为C2H4,故选B。
点睛:要顺利解答此题,必须熟练掌握质量守恒定律并会灵活应用,化学反应前后各种原子个数相等,根据反应前后原子个数的差量即可推断出X的化学式。
2.某反应前后分子变化的微观示意图如下(图中“●”和“○”分别代表不同元素的原子),下列说法不正确的是()A.该反应前后涉及到三种物质B.反应后分子种类没有改变C.反应后分子数增多D.该反应属于分解反应【答案】B【解析】【详解】由化学反应的微观示意图可知,各物质反应的微粒个数关系是:A、由图示可知,该反应前后涉及到三种物质,故A正确;B、由微粒的变化可知,反应后分子种类发生了改变,故B不正确;C、由微粒的变化可知,该反应后分子数增多,故C正确;D、该反应由一种物质生成了两种物质,属于分解反应,故D正确。
故选B。
【点睛】化学变化中分子的种类一定改变,数目可变可不变。
3.如图表示某个化学反应,据图分析判断,下列各项中,不正确的是A .该反应属于置换反应B .反应中乙、丙两物质质量比为2: 7C .图示中x 的数值为4D .反应前后氢元素的化合价发生了改变【答案】B 【解析】 【分析】由化学反应的微观模型图可知,该反应是在一定条件下氢气与四氯化硅(SiCl 4)反应生成了硅和氯化氢气体,反应的化学方程式为:42SiCl +2H Si+4HCl 一定条件,由方程式可知: 【详解】A 、该反应是一种单质和一种化合物反应生成了另一种单质和另一种化合物,属于置换反应,故A 正确;B 、反应中乙、丙两物质质量比就是氢气和硅的质量比为:(2×1×2):28=1:7,故B 不正确;C 、由方程式可知,图示中x 的数值为4,故C 正确;D 、由方程式可知,氢元素的化合价由0价变成了+1价,故D 正确。
《化学方程式》练习题(含答案)一、单选题1. 实验室加热一定质量的高锰酸钾制氧气,各物理量随加热时间变化的图像正确的是( )A. B.C. D.2. 下列关于2C+O22CO的说法中,正确的是( )A. 表示碳加氧气等于一氧化碳B. 该反应中,分子、原子的种类均发生了改变C. 参加反应的碳与氧气的质量比为3:8D. 参加反应的氧气与生成的一氧化碳的分子个数比为1:23. 化学反应前后肯定没有发生变化的是( ) ①原子数目; ②分子数目; ③元素种类; ④物质种类; ⑤原子种类; ⑥物质的总质量A. ① ④ ⑥B. ① ③ ⑤ ⑥C. ① ② ⑥D. ② ③ ⑤4. 乙烷(C2H6)是重要的化工原料,与氯气反应前后分子种类变化的微观示意图如图。
下列说法正确的是( )A. 甲中碳、氢元素质量比为1:3B. 乙的相对分子质量为71C. 甲和丙的元素组成相同D. 生成丙与丁的分子个数比为1:15. 下列化学方程式书写正确的是( )A. Mg+O=点燃MgO2B. 4Fe+3O=点燃2Fe2O32C. 2KMnO4=K2MnO4+MnO2+O2↑D. CO2+Ca(OH)2=CaCO3↓+H2O6. 某化学反应的微观示意图如图所示,下列有关说法正确的是( )A. 该反应的两种反应物均为化合物B. 该反应前后没有发生变化的粒子只有氧原子和氢原子C. 该反应的化学方程式为4NH3+5O24NO+6H2OD. 该反应读成:氨气加氧气在一定条件下生成一氧化氮加水7. 一定质量的某化合物完全燃烧,需要3.2g氧气,生成4.4g二氧化碳和1.8g水。
下列判断错误的是( )A. 参加反应的该化合物的质量为3.0gB. 该化合物中一定含有碳、氢、氧三种元素C. 该化合物中碳、氢、氧的原子个数比为2:4:1D. 该化合物中碳元素的质量分数为40%8. 从2H2+O22H2O中获取的信息错误的是( )A. 在反应前后,元素的种类没有变化B. 在常温下氢气与氧气混合就可以发生反应C. 4g氢气与32g氧气完全反应,可以生成36g水D. 在反应前后,氢原子和氧原子的数目都没有改变9. 漂白粉可用于自来水的杀菌消毒,其有效成分是次氯酸钙[化学式为Ca(ClO)2]。
化学方程式的专项练习一、写出下列反应的化学方程式:1、镁在空气中燃烧:______________________ _____2、铁在氧气中燃烧:____________________ _______3、铜在空气中受热:______________ _____________4、铝在空气中燃烧生成氧化铝:______________ __________5、氢气中空气中燃烧:__________ _______________6、红磷在空气中燃烧:_______________ ___ ______7、碳在氧气中燃烧:__________________ _______11、利用过氧化氢和二氧化锰的混合物制氧气:____________________________12、水在直流电的作用下分解:___________________________________________13、加热氯酸钾:_______________________________________________________14、加热高锰酸钾:____________________________________________________二、配平下列化学方程式:(一) 最小公倍数法:1、Al + O2——Al2O32、Al + Fe3O4——Fe + Al2O33、Fe + O2——Fe3O44、Al + MnO2——Mn + Al2O35、N2+ H2——NH36、Al + H2SO4——Al2(SO4)3 + H2(二) 观察法:1、CO + Fe2O3 ——Fe + CO22、C + Fe2O3——Fe + CO23、CO + Fe3O4 ——Fe + CO24、C + Fe3O4——Fe + CO25、H2 + Fe2O3——Fe + H2O6、H2 + Fe3O4——Fe + H2O10、H2 + WO3——W + H2O 11、CO + O2 ——CO212、Fe + H2O——H2 + Fe3O413、Al(OH)3+ HCl ——AlCl3 + H2O(三) 奇数配偶法:1、FeS2 + O2 ——Fe2O3 + SO22、C2H2 + O2——CO2+ H2O3、C + Fe2O3——Fe + CO24、MnO2 + HCl——MnCl2 + Cl2 + H2O5、Cl2 + Ca(OH)2——CaCl2 + Ca(ClO)2 + H2O(四) 归一法:1、C2H2 + O2——CO2 + H2O2、C6H6 + O2——CO2 + H2O3、C22H46 + O2——CO2 + H2O4、NH3 + Cl2 ——NH4Cl + N25、As2O3+ Zn + HCl——AsH3+ ZnCl2+ H2O6、C X H Y+ O2——CO2+ H2O三、题型变化:1、3Cu+8HNO3 ==3Cu(NO3)2+2X↑+4 H2O,求X的化学式为。