鲎试剂灵敏度
- 格式:ppt
- 大小:6.22 MB
- 文档页数:28


细菌内毒素试验(鲎试验)的全面解析一般细菌毒素可分为两类,一类为外毒素(Exotoxin);它是一种毒性蛋白质,是细菌在生长过程中分泌到菌体外的毒性物质。
产生外毒素的细菌主要是革兰氏阳性菌。
如白喉杆菌、破伤风杆菌、肉毒杆菌、金黄色葡萄球菌以及少数革兰氏阴性菌。
另一类为内毒素(Endotoxin),是革兰氏阴性菌的细胞壁的产物。
细菌在生活状态时不释放出来,只有当细菌死亡自溶或粘附在其它细胞时,才表现其毒性,内毒素的主要化学成分是脂多糖中的类脂A成分。
和热原的关系热原(pyrogen)系指能引起恒温动物体温异常升高的致热物质。
它包括细菌性热原、内源性高分子热原、内源性低分子热原及化学热原等。
热原是否就是内毒素?细菌内毒素是热原的一种,即细菌性热原。
细菌内毒素被认为是热原的本质,此事在学术上仍有争议,热原不仅是细菌内毒素。
但在药检的范畴,细菌内毒素是主要的热原物质,可以说无内毒素就无热原,控制内毒素就是控制热原。
热原反应:含有热原的注射剂注入人体可引起发热反应,使人体产生发冷、寒战、体温升高、出汗、恶心、呕吐等症状,有时体温可升至40℃,严重者甚至昏迷、虚脱,如不及时抢救,可危及生命。
来源和控制方法1、细菌内毒素的特性2、去除细菌内毒素的方法(1)吸附法此法是利用活性炭对热原的吸附作用达到去除作用的方法。
常用的吸附剂中,活性炭对热原的吸附作用最强,一般用量为总容量的0.1%-0.5% ,将溶液加热到70℃左右保温一定时间效果更好。
使用的活性炭应符合药典规定要求。
(2)蒸馏法此法是利用热原具有不挥发性而达到去除目的。
因此,凡适于蒸馏的药品均可用蒸馏法除去热原。
(3)热破坏法此法是利用热高温能破坏热原质达到去除目的。
因此,凡适用于高温处理的如热原检查试验中接触药液的容器,可用180℃干烤3小时,或250℃干烤30min以上。
(4)强酸强碱处理法此法利用强酸强碱能破坏热原而达到去除的目的。
(5)其他,也可以采用过滤等方法去除热原。

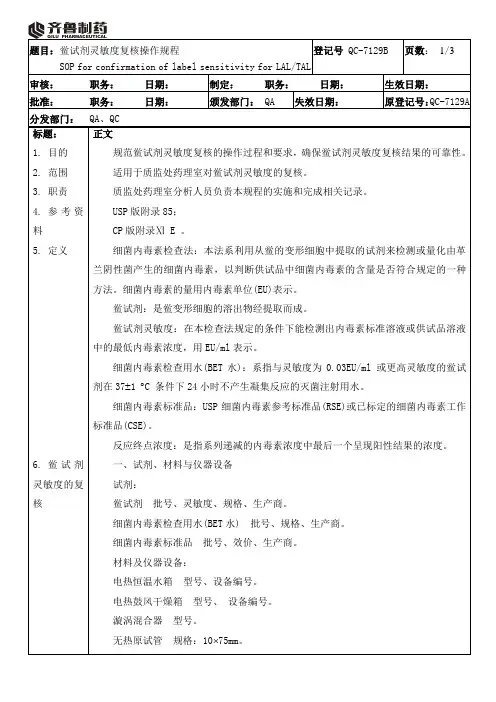
正文规范鲎试剂灵敏度复核的操作过程和要求,确保鲎试剂灵敏度复核结果的可靠性。
适用于质监处药理室对鲎试剂灵敏度的复核。
质监处药理室分析人员负责本规程的实施和完成相关记录。
USP版附录85;CP版附录Ⅺ E 。
细菌内毒素检查法:本法系利用从鲎的变形细胞中提取的试剂来检测或量化由革兰阴性菌产生的细菌内毒素,以判断供试品中细菌内毒素的含量是否符合规定的一种方法。
细菌内毒素的量用内毒素单位(EU)表示。
鲎试剂:是鲎变形细胞的溶出物经提取而成。
鲎试剂灵敏度:在本检查法规定的条件下能检测出内毒素标准溶液或供试品溶液中的最低内毒素浓度,用EU/ml表示。
细菌内毒素检查用水(BET水):系指与灵敏度为0.03EU/ml 或更高灵敏度的鲎试剂在37 1 C 条件下24小时不产生凝集反应的灭菌注射用水。
细菌内毒素标准品:USP细菌内毒素参考标准品(RSE)或已标定的细菌内毒素工作标准品(CSE)。
反应终点浓度:是指系列递减的内毒素浓度中最后一个呈现阳性结果的浓度。
一、试剂、材料与仪器设备试剂:鲎试剂批号、灵敏度、规格、生产商。
细菌内毒素检查用水(BET水) 批号、规格、生产商。
细菌内毒素标准品批号、效价、生产商。
材料及仪器设备:电热恒温水箱型号、设备编号。
电热鼓风干燥箱型号、设备编号。
漩涡混合器型号。
无热原试管规格:1075mm。
正文无热原玻璃瓶规格:25ml。
无热原玻璃吸管规格:1ml、2ml、5ml、10ml。
试管架、无热原封口膜、洗耳球、酒精棉球、砂轮片。
二、试验准备试验所用的容器、用具都必须经过处理,250C以上干烤至少1小时,以去除外源性内毒素。
试验操作过程应避免微生物的污染。
三、内毒素溶液配制细菌内毒素标准品系列溶液配制取RSE或CSE 1瓶,按照使用说明书加入规定量的细菌内毒素检查用水使溶,并用漩涡混合器间歇混匀30分钟,然后用细菌内毒素检查用水进一步稀释至2.0、、 0.5、 0.25四个浓度的内毒素标准溶液,每一步稀释应混匀至少30秒钟。
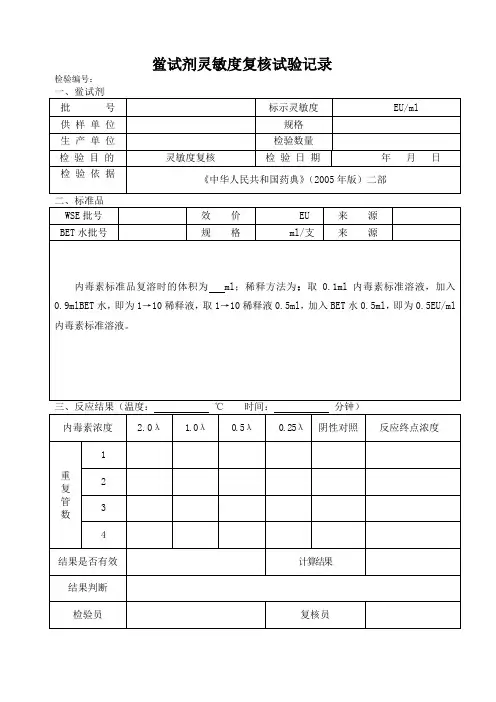
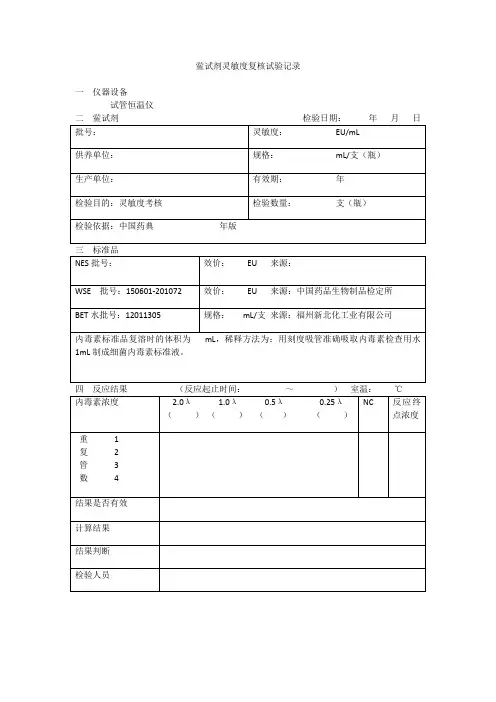

鲎试验检查细菌内毒素应注意的问题鲎试验检查细菌内毒素应注意的问题发布时间02年09月05日 09时18分方法:通过对干扰鲎试验准确性干扰因素的分析(包括鲎试剂本身、操作条件、配制原料等),提出了鲎试验中应注意的问题。
结果:只要克服了检查中的干扰因素,鲎法具有比家兔法更简便、快速、灵敏度高、重现性好等优点。
鲎试验是利用鲎的变形细胞与微量内毒素产生凝集反应的现象,作为判断供试品中细菌内毒素限量是否符合规定的一种方法[1]。
它具有比家兔法更简便、快速、灵敏度高、重现性好等优点。
中国药典1995年版已收载细菌内毒素检查法(简称鲎试验),但只用于几种输液的检查。
根据现有的实验证明,凡不干扰细菌内毒素检查或虽有干扰,但可以克服的药品注射剂,将能够全部以鲎法代替家兔热原检查法。
但是该法受到许多因素的影响,故在做鲎试验检查时,应注意下列问题。
1鲎试剂本身1.1鲎试剂灵敏度 为了保证检查细菌内毒素结果的准确性,用于试验的鲎试剂应首先核对灵敏度。
因为在我们的实际工作中,发现鲎试剂均符合药典规定标准前提下,由于生产厂家不同,部分鲎试剂的实测灵敏度与标示值有差异而导致检测同一检品时,用相同标示值的鲎试剂,出现不同结果。
因而先核对灵敏度可避免因鲎试剂本身造成的判断失误。
建议法定部门和生产单位应注意鲎试剂的质量检查。
1.2供试品稀释 在取样品时,一定要熟悉中国药典的内容,不能直接取大输液原液0.1ml进行检查,这是排除干扰因素的简单有效的方法。
因药典已明确规定试验中鲎试剂的灵敏度不超过0.5EU/ml,根据供试品的稀释公式: 供试品稀释倍数= L/λυL :供试品的内毒素限量(1EU/ml)λυ:鲎试剂灵敏度的标示值(EU/ml)故检测大输液均应稀释后才能进行试验,如选用更高灵敏度的鲎试剂,则应增加样品的稀释倍数。
稀释用的细菌内毒素检查用水药典作了规定。
在4h内不得与鲎试剂产生凝集反应。
如果直接用供试品原液试验,就会使供试品的内毒素提高到0.5EU/ml或0.5EU/ml以下,这样,根据目前大输液的生产和贮藏条件,有些就会达不到,鲎法检出的阳性率会提高,兔法复核的机遇也将增多,势必会浪费人力物力。
![[精华]鲎试剂试验方法](https://uimg.taocdn.com/28cbff01caaedd3383c4d3b4.webp)
[精华]鲎试剂试验方法鲎试剂实验方法鲎试剂按实验方法可分为:凝胶法、动态浊度法鲎试剂、终点浊度法鲎试剂、动态显色法鲎试剂、终点显色法鲎试剂。
凝胶法系通过鲎试剂与内毒素产生凝集反应的原理来定性检测或半定量内毒素的方法。
凝胶法是通过观察有无凝胶形成作为反应的终点。
此法操作比较简单,经济,不需要专用测定设备,可以进行定性或半定量测定。
凝胶法鲎试剂常见规格为0.1ml/支或0.2ml/支的单个测试或0.5ml/支至5.2ml/瓶的真空封口西林瓶装的多个测试。
使用时一般应加细菌内毒素检查用水复溶后使用。
厦门市鲎试剂实验厂有限公司的真空封口试管凝胶法鲎试剂是把鲎试剂直接灌装在试管中,在真空中压盖封口的新产品。
使用时直接用样品溶解鲎试剂,不会割伤手,更加简单方便安全。
特异性鲎试剂,即弃G因子鲎试剂,是厦门市鲎试剂实验厂有限公司国内首创的产品,它专一对内毒素起反应,避免了G因子旁路的干扰,使检测结果更加可靠,在药检和临床检验方面是不可或缺的理想检测试剂。
目前厦门市鲎试剂实验厂有限公司提供的各种内毒素检测鲎试剂均为特异性鲎试剂,都能对抗葡聚糖的干扰,只对内毒素起反应。
因此不列为独立品种。
动态浊度法鲎试剂、终点浊度法鲎试剂、动态显色法鲎试剂、终点显色法鲎试剂,这四种方法都是定量检测内毒素的。
这几种定量法鲎试剂统称光度法鲎试剂。
根据检测原理,终点浊度法和动态浊度法都属于浊度法。
浊度法系利用检测鲎试剂与内毒素反应过程中的浊度变化而测定内毒素含量的方法。
终点浊度法未见商品化产品。
动态浊度法(又称动态比浊法)是检测反应混合物的浊度上升某一预先设定的吸光度所需要的反应时间,或是检测浊度增加速度的方法。
动态浊度法的特点为:1. 能准确定量。
2.检测范围宽,可达4个数量级。
3.灵敏度高达0.005EU/ml。
4. 操作简便,系统自动检测分析,一步即成。
5. 经济实用,试剂样品需要量少,可降至50μL。
6. 和微生物检测系统Elx808(配套IU)及专用软件TALgent使用,一次可同时检测多达96个样品。

文件编号:版本:鲎试剂灵敏度复核试验作业指导书修订历史记录[至多存五版的历史修订记录]1.0 目的对细菌内毒素检查试验所用的鲎试剂的灵敏度进行复核。
2.0 职责质量与法规部负责本规程的起草,QC及相关人员执行本规程。
3.0 范围适用于本公司细菌内毒素检查法。
4.0 参考文件2010年版《中国药典》二部附录ⅪE细菌内毒素检查法2010年版《中国药品检验标准操作规范》细菌内毒素检查法《细菌内毒素检查法及其应用》第一版,气象出版社5.0 定义鲎试剂灵敏度复核试验:在细菌内毒素检查法规定的条件下,使鲎试剂产生凝集的内毒素的最低浓度即为鲎试剂的标示灵敏度(λ),用EU/ml表示。
当使用新批号的鲎试剂或试验条件发生了任何可能影响检验结果的改变时,应进行鲎试剂灵敏度复核试验。
反应终点浓度:指鲎试剂灵敏度复核试验中,系列递减的内毒素浓度中最后一个呈阳性结果的浓度。
6.0 设备/工具及物料6.1 设备/工具6.2 物料6.2.1 细菌内毒素工作标准品除另有规定外,使用由中国药品生物制品检定所统一发放的标准品。
6.2.2 细菌内毒素检查用水指内毒素含量小于0.015EU/ml(凝胶法)且对内毒素试验无干扰的灭菌注射用水。
6.2.3 鲎试剂规格一般选用0.25 EU/ml。
7.0 操作步骤7.1 提前30 min开启超净工作台,试验操作过程中不要开启风机,完毕后用75%乙醇擦拭超净工作台。
试验操作过程应防止微生物和细菌内毒素污染。
7.2 制备细菌内毒素标准溶液7.2.1 取细菌内毒素工作标准品1支,轻弹瓶壁使粉末落入瓶底,用砂轮在瓶颈上部划痕,用75%乙醇擦拭后启开,避免玻璃屑落入瓶内。
7.2.2 按照工作标准品说明书,加入细菌内毒素检查用水溶解。
封口膜封口,置漩涡混合器上混匀15 min后用细菌内毒素检查用水进行稀释,制成2.0 λ、1.0 λ、0.5 λ、0.25 λ四个浓度的内毒素标准溶液。
每稀释一步均应在漩涡混合器上混匀30 s。

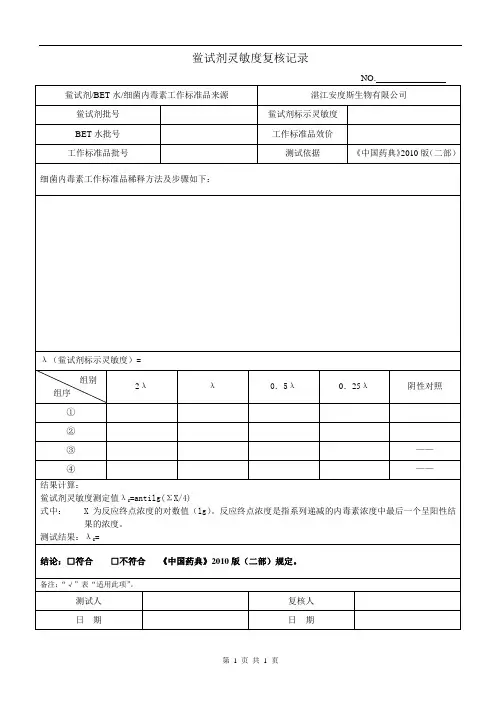
范围:鲎试剂职责:检验室对本规程的实施负责正文:1.内毒素标准溶液的制备1.1取细菌内毒素国家标准品(NSE)或内毒素工作标准品(WSE)一支,轻弹瓶壁,使粉末落入瓶底,再用砂轮在瓶颈上部轻轻划痕,75%酒精棉球擦拭后启开,防止玻璃屑落入瓶内。
1.2按标准品使用说明书用移液管加入规定量的细菌内毒素检查用水(BET)溶解其内容物,用封口膜将瓶口封严。
置旋涡混合器上混合15分钟,然后制备成所需浓度的细菌内毒素标准溶液即2.0λ、1.0λ、0.5λ、0.25λ(λ为所复核鲎试剂的标示灵敏度),每稀释一步均应在旋涡混合器上混合30秒。
若为NSE,可按其使用说明书将其稀释至规定浓度后分装并保存。
2.待复核鲎试剂的准备2.1在制备内毒素标准溶液的同时,取0.1ml/支的鲎试剂18支轻弹瓶壁,使粉末落入瓶底,用砂轮在瓶颈轻轻划痕,75%乙醇棉球擦拭后启开备用,防止玻璃屑落入瓶内,加入0.1mlBET水复溶,使内容物充分溶解,避免产生气泡。
2.2若待复核鲎试剂的规格不是0.1ml/支时,按标示量加入BET水复溶,将复溶后的鲎试剂溶液混匀后每0.1ml分配到10×75mm凝聚管中,要求至少分配18支管备用。
3.加样3.1将已充分溶解的待复核鲎试剂18支(管)放在试管架上,排成5列,其中4支(管)4列分别加入2.0λ、1.0λ、0.5λ、0.25λ的内毒素标准溶液;2支(管)1列分别加入BET水。
内毒素标准溶液和BET水的加样量均为0.1ml/支。
4.加样结束后,用封口膜封口,轻轻混匀,避免产生气泡,连同试管架放入37±1℃水浴或适宜恒温器中,试管架保持水平状态,保温60±2分钟,观察结果。
5.鲎试剂灵敏度复核如最大浓度2.0λ4管均为阳性,最低浓度0.25λ4管均为阴性,阴性对照为阴性,按下式计算反应终点浓度的几何平均值即为鲎试剂灵敏度的复核结果(λc)。
λc=lg- 1 (∑X/4)式中X为反应终点浓度的对数值(lg)。
鲎试剂灵敏度复核原理1 鲎试剂的灵敏度复核鲎试剂是一种病原体检测试剂,用于分析样品中是否存在鲎病毒。
它提供了有效、准确、可靠的检测,并且能够快速和准确地检测出鲎病毒的存在。
灵敏度复核是对鲎试剂灵敏度的一种检验。
本文将简要介绍鲎试剂灵敏度复核的原理。
2 鲎试剂灵敏度复核原理鲎试剂灵敏度复核是通过检测与水力均一系数和介质比容量(VCR)之间的相互关系来进行的。
水力均一系数(FDP)用来衡量样品的灵敏度,是一种量化的指标,它可以测量出检测样品中样品分子数量的值,它可以作为检测决策的依据。
介质比容量(VCR)指标可以衡量检测样品中DNA的质量,它可以用来测量检测分子的大小,它可以作为衡量检测样品的灵敏度的重要参数。
3 所用材料和实验方法用于鲎试剂灵敏度复核的材料包括:NIGP-9576流式细胞术引物、标准分子颗粒(SM)、即用型DNA表达质粒质粒(CTP)、库夫特—威尔斯质粒(KV)及它的完整酶切体(kVCF)、抗体制剂(AM)、核酸定量试剂盒(H∅QT)。
实验步骤主要包括:①用NIGP-9576流式细胞术引物按照要求(1∶15~2∶30)制备测定鲎病毒目标易位基因(TG)的反应混合液,加入与VCR和FDP相对应的原液;②进行表达质粒PCR,并且结合抗体进行抗体表达;③进行激活反应,并以KV或kVF为模版,分解样品;④将所有步骤重复10次,获得完整的酶的灵敏度复核试剂(V∅PoP);⑤最后,用H∅QT试剂盒进行检测,以获得定量的VCR和FDP值,便可得到灵敏度复核结果。
4 结论鲎试剂的灵敏度复核原理是通过VCR和FDP来衡量检测样品中分子数量和大小的,并用H∅QT试剂盒进行检测,以获取定性结果。
只有通过严格的技术测试才能确定样品中分子的灵敏度,确保安全操作。
鲎试剂标准本品为鲎科动物东方鲎(Tachyplecus tridentatus)的血液变形细胞溶解物的无菌冷冻干燥品。
本品含能被微量细菌内毒素激活的凝固酶原(Proclotting enzyme),凝固蛋白原(Coagulagen)其灵敏度以细菌内毒标准品或工作标准品测定,应为标示量的50%-200%。
(一)性状本品为白色或类白色冻干块或粉末,在水生生理盐水中易溶。
(二)鉴别1.取本品按装量加水溶解后,加茚三酮试液《中国药典1990年版》(二部附录162页)0.25ml,加热煮沸1-2分钟,显蓝色紫色。
2.取本品按装量加水溶解后,再加水适当稀释,照分光光度法《中国药典1990年版》(二部附录24页)测定,在270±1nm的波长处有单一吸收峰。
3.取本品按装量加入内毒检查用水溶解后,吸取0.1ml加入0.1ml细菌内毒素工作标准品或标准品50EU,混匀后,于37℃水浴中放置1小时,有凝胶形成。
(三)检查干燥失重:取本品约0.1在g ,在66℃减压干燥至恒得,减失重量不得过5%(中国药典1990年版二部附录55页)。
自身凝集:取本品4支,按装量加入配带的鲎试剂溶剂,溶解后,分别从每支取0.1ml,再分别加入配带的鲎试剂溶剂0.1ml,混匀后,于37±1℃水浴中放置4小时,不得形成凝胶,若有2管以上形成凝胶,判为不合格;若仅有1管形成凝胶,照同样方法,另取8支重复检查,8支均不得形成凝胶。
缓冲能力:任意取5%、10%葡萄糖注射液,氯化钠注射液无菌注射用水或注射用水适量,加稀盐酸调节pH使供试品溶液pH值为2.90-3.00,取此溶液适量与等量鲎试剂溶解液混匀,重复测定,pH值应为6.00-8.00。
(四)灵敏度测定预测:1.取细菌内毒素工作标准品1支,按说明溶解燕稀稀释成1→8等比系列稀释液。
2.取同一批鲎试剂若干支,分别按标示量加入配带的试剂溶剂制成鲎试剂溶液。
取10×75mm试管若干支,分别加入0.1ml鲎试剂溶液,加入内毒素稀释液0.1 ml ,每一稀释液最少作2管,同时作2管阴性对照。