练习2 在恒温、恒压的条件下,向可变容积的
密闭容器中充入3LA和2LB,发生如下反应:
3A(g)+2B(g) xC(g)+yD(g)
达到平衡时,C的体积分数为m%。若维持温度
压强不变,将0.6LA 、0.4LB、4LC、0.8LD作
为起始物质充入密闭容器中,达到平衡时C的体
积分数仍为m%,则X,Y的值分别为(CD)
探究一
恒温恒容条件下等效平衡的条件
1、反应前后气体分子数发生变化的可逆反应 也就是△n(g)≠0的可逆反应
恒温恒容: 2SO2 (g) 途径1起始 2mol 途径2起始 0mol 途径3起始 0.5mol 途径4起始 amol
+ O2(g) 1mol 0mol
0.25?mol bmol
2SO3 (g) 0 2mol
A x=3 y=1
B x=4 y=1
C x=5 y =1
D x=10 y=2
等效平衡小结
条件 等效条件
结果
恒温恒容 (△n(g)≠0)
投料换算成相
同物质表示时
物质的量相同
两平衡各组分百分含 量均相同(n、c相同)
等同等效
恒温恒容 投料换算成相同 两平衡各组分百分
(△n(g)=0)
物质表示时物质
的量成比例
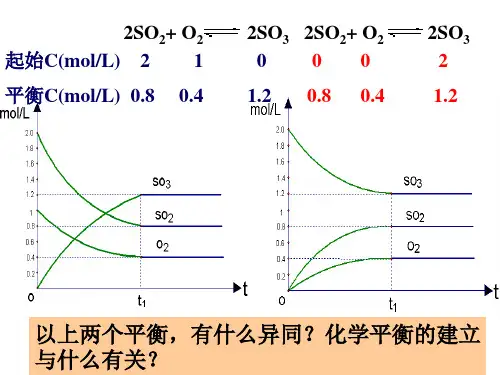
2SO2+ O2 起始C(mol/L) 2 1
平衡C(mol/L) 0.8 0.4
2SO3 2SO2+ O2 0 00
1.2 0.8 0.4
2SO3 2
1.2
以上两个平衡,有什么异同?化学平衡的建立 与什么有关?
结论
1.化学平衡状态的建立与条件(如浓度、 温度、压强)有关,与途径无关, 2.建立平衡状态有4条途径: