兽药残留SPE方法
- 格式:doc
- 大小:268.50 KB
- 文档页数:10

汇总|兽药残留检测前处理类型由于兽药残留种类繁多、在样品中残留水平低、基质复杂、干扰物质多等,使样品前处理技术,即分离纯化技术成为兽药残留分析的重点和难点。
目前,兽药残留的样品前处理方法主要有液液萃取、固相萃取、固相微萃取、免疫亲和色谱、分子印迹、超临界流体萃取、基质固相分散技术、微波辅助萃取、凝胶渗透色谱和超声波辅助提取等。
液液萃取液液萃取(liquid-liquid extraction, LLE)是利用待测物在两种互不相溶(或微溶)的溶剂中分配系数的不同而达到分离纯化的目的,是兽药残留分析中一种常用的前处理技术。
有国外学者将肉类样品用乙腈除蛋白,正己烷脱脂后,加乙酸乙脂液液萃取,利用超高效液相色谱串联质谱技术对肉中的24 种磺胺类药物残留进行了测定。
也有学者等运用液液萃取结合低温纯化技术作为前处理技术,测定了牛奶中大环内酯类抗生素,得到了良好的回收率。
液液萃取对实验条件和仪器要求不高,但操作繁琐、有机溶剂消耗大,污染严重,逐渐被一些新的前处理方法所取代。
固相萃取固相萃取(solid phase extraction, SPE)是目前兽药残留检测中最为常用的一种样品前处理技术。
它是利用固体吸附剂将样品中目标化合物吸附,使其与样品基质及干扰化合物分离,再用洗脱液洗脱下来从而达到分离和富集的目的。
固相萃取技术由于具有操作简单快速、消耗有机溶剂少、样品回收率高、易于自动化等优点,在样品前处理中得到广泛应用。
目前,固相萃取技术已可用在磺胺类、四环素类、阿维菌素类、氯霉素类、喹诺酮类、激素类、β -受体激动剂等多类兽药残留的定量分析中。
有学者采用固相萃取结合液相色谱方法测定了鸡肉组织中的喹诺酮类药物。
对比了Oasis HLB,Oasis MAX, SDB-RPS 三种不同填料固相萃取柱的萃取效率,最终得出SDB-RPS 填料的固相萃取柱的萃取效果最好。
固相微萃取固相微萃取(solid phase microextraction, SPME)技术是20 世纪90 年代兴起的一项新颖的样品净化富集技术,属于非溶剂型选择性萃取法。

农药残留的前处理及检测一、样品前处理以往的提取和净化方法基本上是加入乙腈后用高速组织匀浆后静止或离心,取上清液浓缩后用固相萃取柱净化,上机测定。
目前应用比较多的前处理方法是QuEChERS 方法,其原理是分散固相萃取,减少了浓缩步骤。
1、分散固相选择取决于基质和分析物▪ MgSO4 在所有净化试剂盒中均含有,起到去除水分的作用▪ PSA* 去除极性的有机酸,一些糖类和脂类▪ C18EC 去除脂类和固醇,类胡萝卜素等▪GCB* 去除色素,如叶绿素(对平面结构药物会有吸附)▪ dispersive-SPE (d-SPE)▪无论是EN 还是 AOAC 方法, C18对净化的影响大于PSA针对不同基质的通用净化包,兼顾净化效果与回收率(1)多数蔬菜和水果: PSA+MgSO4去除极性有机酸, 一些糖和少量脂肪类蔬菜和水果>1% Fat, PSA+C18EC+MgSO4去除极性有机酸,糖类,脂肪, 和一些类固醇(2)带色素的蔬菜和水果:PSA+GCB+MgSO4去除极性有机酸,糖类,少量类胡萝卜素和叶绿素,不能用于平面结构农药含有高水平色素含量的水果和蔬菜:PSA+GCB↑+MgSO4去除极性有机酸,糖类,类胡萝卜素和叶绿素,不能用于平面结构农药(3)带有色素和脂肪的蔬菜和水果: PSA+GCB+MgSO4+C18去除极性有机酸,糖类,脂肪,类胡萝卜素和叶绿素,不能用于平面结构农药1、样品前处理流程2、影响农药回收率的因素▪pH敏感农药:提取液的酸碱度▪碱-不稳定农药▪酸-不稳定农药▪酸性农药▪热不稳定农药:萃取放热影响▪平面结构农药:石墨化炭黑的影响(1)碱-不稳定农药如克菌丹、灭菌丹、抑菌灵和其它在QuEChERS 提取之后的碱性PSA 净化步骤中不稳定的农药. 考虑到这些农药的稳定性,因此净化后的样品溶液可以使用甲酸/乙酸调节pH 至5来保证这些化合物的回收率.(2)酸-不稳定农药酸-不稳定农药如乙氧喹啉和吡蚜酮,若回收率不理想,可将提取盐中的0.5 g 柠檬酸二钠盐和1g的柠檬酸三钠盐换成 1.5 g柠檬酸三钠盐,同时控制较低的提取温度来提高回收率。


兽药残留分析中样品前处理方法综述张俊升*,谭梅,杨建鸣,王琼,李良(云南省兽药饲料检测所,云南昆明650021)摘要:样品前处理方法是兽药残留分析的保障,文章介绍了八种目前国内常用的前处理方法:超声波辅助提取、超临界流体萃取、固相萃取、固相微萃取、微波辅助萃取、基质固相分散、加速溶剂萃取、免疫亲和色谱。
现代兽药残留分析方法通常包括样品前处理和测定方法两部分,测定技术是核心,而样品前处理方法是保障。
样品前处理的好坏直接影响到分析的各项指标、成本和效率,占用了将近70%的分析工作量。
兽药残留分析样品的前处理包括提取与净化。
提取是将样品中的目标物溶解分离出来的操作步骤,根据兽药的性质、样品种类、实验条件,可选用的常规提取方法有振荡法、索氏抽提法等。
由于某些样品组成复杂,提取后往往还需经过净化步骤以达到待测物与干扰杂质分离,净化的基本原理主要为液-液作用、液-固作用、液-气作用及化学反应。
柱层析法是最常用的净化方法之一,层析柱填料一般为弗罗里硅土、氧化铝以及活性炭。
经典的样品前处理方法不仅操作繁琐、费时,提取与净化效率低,容易引入误差,且需要使用大量有毒溶剂,另外由于对被测目标物质的最低检出限要求越来越低,其目标物质的稳定性也在随时间发生变化,这给分析测试带来了一定困难,因此亟需发展简单、快速、有效的样品前处理方法。
目前,为适应多种类大批量样品的快速分析,样品前处理的手段在不断更新,并且也逐渐向仪器化、自动化方向发展。
近年来发展较快的方法主要有超声波辅助提取(Sonication-assisted Extraction,SAE)法、超临界流体萃取(Supercritical Fluid Extraction,SFE)法、微波辅助萃取(Microwave Aided Extraction,MAE、固相萃取(Solid Phase Extraction,SPE)、固相微萃取(Sol-id-Phase M icroextraction,SPM E)等方法。

动物性产品中兽药残留的快速检测方法——ELISA & CharmⅡ一、前言:1、现状目前兽医用药几乎占据了所有抗微生物药物的50%,因此食品病原菌、条件致病菌和共生菌不可避免的成了耐药菌。
在过去的50年中大约有100万吨的抗生素被释放到生物圈中。
欧洲动物卫生联盟(European Federation of Animal Health ,FEDESA)对欧盟和瑞士抗生素使用统计数据表明,仅1997年用于人类健康的抗生素达5460吨,用于动物健康的抗生素达3465吨,用于动物生长促进剂的抗生素达1575吨,并有逐年增加的趋势。
在我国,由于兽医用药制度的不完善及一些养殖厂受经济利益的驱使及相应的检测监督体系不健全,药物的滥用现象更为严重,动物产品中兽药的污染时有发生。
其潜在的致癌、致畸作用引起了社会的普遍关注,由于水产品中氯霉素含量过高,欧盟委员会于今年1月作出禁止中国动物源食品进口的协议,使得我国水产品对欧盟出口严重受挫,虽然现在部分产品开始解禁,但形式依然不容乐观;美国、日本等国也开始高度关注我国水产品的质量,并出台一系列相关政策,对我国出口动物性产品进行限制。
在现代文明的世界,健康第一的贸易法则将是关税、价格、质量所不可比拟的,政治上的友好往来无法替代经济贸易中的游戏规则。
2、食品中兽药残留对人类的危害2.1耐药菌株的产生抗生素使用和细菌耐药性永远是互相依存、互相制约的矛盾的两个方面,细菌耐药非正常增加,往往是抗生素的非正常使用的结果。
早在1920-30年青霉素问世时,Dr Fleming就提出了青霉素的耐药性问题。
随着时代的发展和各种新药的出现,耐药性菌株也接踵而至(即包括药物选择压力的结果也包括细菌自身的进化)。
抗生素的副作用以及耐药菌株的存在将严重威胁着人类的健康,而且临床亚治疗水平的抗生素更容易促使抗性基因的转移,比如对动物进行低水平四环素治疗,其粪肠菌群由对四环素敏感逐渐变成抗四环素最后发展成对其它药物也产生抗性。

1 固相萃取(spe)固相萃取就是利用固体吸附剂将液体样品中的目标化合物吸附,使其与样品的基体和干扰化合物分离,然后选用合适的洗脱液洗脱或加热解吸附,达到分离和富集目标化合物的目的。
固相萃取具有高的回收率和富集倍数,减少了溶剂的消耗和废物的产生,是一种对环境友好的分离富集方法。
赵维佳[1]等用固相萃取1次测定小青菜中8种有机磷、有机氯和拟除虫菊酯等农药的残留量,结果表明:8种农药在40 min内可得到很好的分离,检测方法的线性相关系数r≥0 992,回收率为70 87%~85 85%,最低检测限为0 50~1 40 μg/kg。
2 固相微萃取(spme)固相微萃取技术是在固相萃取基础上发展起来的。
固相微萃取以特定的固体(一般为纤维状萃取材料)作为固相提取器将其浸入样品溶液或顶空提取,然后直接gc、hplc等分析[2]。
该技术集采集、萃取、浓缩、进样于一体,所需样品少,重现性好,操作简单。
魏立青等[3]进行spme条件的优化、筛选实验,建立了环境中有机磷杀虫剂的快速检验方法,方法收集17种有机磷杀虫剂,使用spme并结合gc/ms、gc/ms/ms检验方法,结果最低检测浓度为0 01~100 pg/ml,在痕量范围0 1~10 ng/ml内线性回归好,该方法简单、灵敏、迅速、可靠,应用效果理想。
3 膜萃取技术(me)膜萃取是一种基于非孔膜进行分离富集的样品前处理技术。
膜萃取主要分为微孔膜液液萃取(mmlle)、支持液膜萃取(slme)、中空纤维膜液相微萃取(hflpme)等几种模式。
该技术的优点主要是高富集倍数、净化效率高、有机溶剂用量少、成本低以及易于与分析仪器在线联用等。
luthje等[4]将mmlle与gc ms在线联用检测样品中农药及多环芳烃的残留,以甲苯为萃取液,待萃液流速1 00 ml/min,温度50℃、萃取时间50 min,检测水样中吡草胺等16种农药结果的重现性、检测限、萃取率、富集因子等参数。


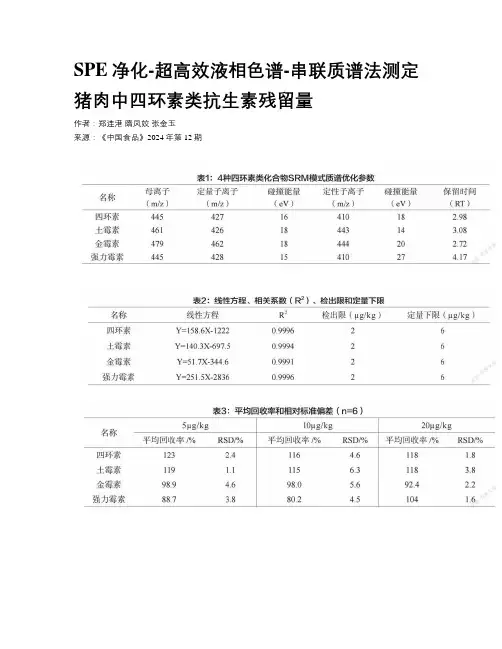
SPE净化-超高效液相色谱-串联质谱法测定猪肉中四环素类抗生素残留量作者:郑连港隋凤姣张金玉来源:《中国食品》2024年第12期四环素类抗生素(Tetracyclines)主要指土霉素(oxytetracycline)、四环素(tetracycline)、金霉素(chlortetracycline)、强力霉素(doxycycline)4种,是一类广谱抗生素,能有效抑制蛋白质的合成,对于治疗动物细菌传染病效果显著,在水产养殖、禽畜养殖等行业有着广泛应用,但却极易造成动物体内药物严重过剩,并随食物链富集,直接或间接对人体造成毒性危害、致畸致癌及其他严重性疾病。
因此,四环素类抗生素的用量和用药期应受到严格管控。
我国对于四环素类抗生素允许残留在猪肉中的浓度标准有着明确规定,其中,土霉素、四环素、金霉素均为200µg/kg,强力霉素(多西环素)为100µg/kg。
四环素类抗生素样品检测的前处理过程常采用固相萃取、液液萃取、固相微萃取等前处理方式。
其中,固相萃取的应用最为广泛,但传统固相萃取柱常采用“等密度法”来填装,选用聚乙烯材质的注射针筒装置为骨架,在装置内上下装有两片聚乙烯或玻璃纤维材质的塞片,并在塞片中间装填一定量的色谱吸附剂(填料),填料要求准确且混合均匀,对填料密度的要求也较高。
因此,传统固相萃取柱填料法操作繁琐,对人员的技术能力要求较高,且填完的固相萃取柱重复性较低。
本文选择市售成品净化柱,采用SPE净化、液相色谱质谱法检测,建立了简单、快捷地检测4种四环素类抗生素的分析方法。
1. 材料与方法1.1 材料与试剂土霉素(CAS:6153-64-6,GSB05-3333-2016)、四环素(CAS:60-54-8,GSB05-3334-2016)、金霉素(CAS:57-62-5,GSB05-3332-2016)、强力霉素(CAS:564-25-0,GSB05-3335-2016),标准物质浓度均为100μg/mL,农业部环境保护科研检测所;甲醇,色谱纯,科密欧;甲酸,色谱纯,科密欧;乙酸乙酯,色谱纯,科密欧;乙二胺四乙酸二钠(Na2EDTA·2H2O)、柠檬酸(C5H8O7·H2O)/磷酸氢二钠(Na2HPO4·12H2O),优级纯,科密欧;实验用水,杭州娃哈哈集团有限公司;SelectCore HLB净化柱,60mg/3mL,苏州纳谱;猪肉粉中四环素、土霉素、金霉素分析质控样MCS-80165。

液相色谱-串联质谱法检测动物产品中兽药残留的应用摘要:本文主要探讨液相色谱-串联质谱法在检测动物产品中兽药残留的应用及效果。
常用的样品前处理方法包括固相萃取(SPE)和液液萃取(LLE)。
固相萃取通过使用特定吸附剂去除干扰物质,从而提高目标化合物的浓缩度和纯度。
液液萃取则利用溶剂的分配系数差异,将目标化合物从基质中转移到有机相中进行富集。
在LC-MS/MS分析条件方面,选择合适的色谱柱对于分离目标兽药很重要。
常用的色谱柱类型包括C18和亲水性柱,具有良好的保留和分离性能。
流动相的组成和温度也需要优化,以实现目标化合物的最佳保留和分离效果。
关键词:液相色谱-串联质谱法;动物产品;兽药残留1动物产品中兽药残留的检测需求与挑战兽药是用于动物领域的诊断、治疗和预防疾病的药物。
在畜牧业中,兽药的使用可以提高动物的生产性能和健康状况。
然而,不当或滥用兽药可能导致兽药残留,在动物产品(如肉类、奶制品和蛋类)中残留下来。
兽药残留可能对人类健康产生潜在风险。
长期暴露于兽药残留物可能导致抗菌耐药性、过敏反应和慢性毒性等问题。
因此,监测和控制动物产品中的兽药残留是保障食品安全和公众健康的重要任务。
液相色谱-串联质谱(LC-MS/MS)由于其高灵敏度、高选择性和广泛的适用性,在兽药残留检测中得到广泛应用。
2样品前处理方法2.1固相萃取(SPE)的应用固相萃取(Solid-Phase Extraction,SPE)是一种常用的样品净化方法,在兽药残留的分析中得到广泛应用。
SPE利用固定在固相柱中的吸附剂对样品进行选择性吸附和洗脱,实现兽药残留的富集和净化。
在SPE过程中,常见的固相材料包括正相、反相和离子交换剂等。
根据目标分析物的特性和样品基质的性质,选择适当的固相材料可以实现针对性的富集和净化效果。
如果目标分析物是亲水性化合物,通常选择正相固相材料进行富集。
正相SPE柱上的吸附剂通常具有极性官能团,能够有效地吸附亲水性化合物。
兽药残留的检测方法
兽药残留的检测方法包括:
1. 高效液相色谱法:将样品中的兽药残留物通过柱子分离,然后使用UV或荧光检测器检测。
2. 质谱法:使用质谱仪检测样品中的兽药残留物,可检测出更低浓度的残留物。
3. 酶联免疫吸附试验法:利用特定的抗体对兽药残留物进行检测,可以进行多重残留的检测。
4. 光谱学方法:使用紫外光谱、红外光谱、拉曼光谱等方法对样品中的兽药残留物进行检测。
5. 火焰原子吸收光谱法:对样品进行预处理后,使用火焰原子吸收光谱仪进行检测。
6. 电化学法:利用电化学传感器对兽药残留物进行检测,具有灵敏度高、实时性好等优点。
QuEChERS法与传统固相萃取法对比检测猪肉中五氯酚残留宋东晓(宁德市食品药品检验检测中心,福建宁德 352000)摘 要:通过对比QuEChERS法与传统固相萃取法(Solid-Phase Extraction,SPE)两种前处理方法,建立高效液相色谱-串联质谱法测定猪肉中五氯酚残留量。
本实验对猪肉中五氯酚钠检出限、定量限、准确度、回收率、基质效应进行考察分析。
对比QuEChERS和SPE两种前处理方法,猪肉中五氯酚钠标液在0.5~25.0 ng·mL-1线性关系良好,相关系数均大于0.999,检出限均为0.1 µg·kg-1,定量限均为0.5 µg·kg-1。
在0.5 µg·kg-1、1.0 µg·kg-1、5.0 µg·kg-1 3水平浓度下进行加标回收,SPE法回收率在107.61%~113.58%,相对标准偏差为3.72%~6.16%,QuEChERS法回收率在88.03%~113.57%,相对标准偏差为2.05%~5.99%。
SPE和QuEChERS法中,五氯酚钠在猪肉中ME值0.264~0.541,均表现出强基质效应。
这两种前处理方法差异不明显,均能满足猪肉中五氯酚钠残留量的检测需求,但QuEChERS法更高效。
关键词:猪肉;五氯酚钠;高效液相色谱-串联质谱法;QuEChERS;传统固相萃取法(SPE)Determination of Sodium Pentachlorophenol Residues in Porkby QuEChERS and SPESONG Dongxiao(Ningde Food and Drug Inspection and Testing Center, Ningde 352000, China) Abstract: A quantitative method for the determination of sodium pentachlorophenol in pork by LC-MS was established by comparing the QuEChERS method with the traditional solid-phase extraction method for pre-treatment. In the experiment, the detection limit, quantification limit, accuracy, recovery rate and matrix effect of sodium pentachlorophenolate in pork were investigated and analyzed. The linear relationship of sodium pentachlorophenol in two pre-processing methods was good in the concentration range of 0.5~25.0 ng·mL-1, the correlation coefficient was greater than 0.999, the detection limit of was 0.1 µg·kg-1, the quantification limit was 0.5 µg·kg-1. At the spiked concentrations of 0.5 μg·kg-1, 1.0 μg·kg-1 and 5.0 μg·kg-1, the recovery was 107.61%~113.58% in SPE, and the corresponding RSD was 3.72%~6.16%. In QuEChERS, the recovery was 88.03%~113.57%, and the corresponding RSD was 2.05%~5.99%. In the SPE and QuEChERS methods, the ME values of sodium pentachlorophenol in pork ranged from 0.264 to 0.541, both of the two pre-processing methods can meet the detection of sodium pentachlorophenolate residue in pork, but the QuEChERS method is more efficient.Keywords:pork; sodium pentachlorophenol; high performance liquid chromatography tandem mass spectrometry; QuEChERS; solid-phase extraction (SPE)五氯酚及其钠盐作为药物,被广泛用于杀虫、杀菌、除草及防腐,但是由于其易溶于水、难降解、持续性污染等特点,易在动植物体内富集,且能通过食物链在人体内蓄积,严重者可致中枢神经系统、肝肾损伤等[1]。
食品中兽药残留的检测技术(常用版)(可以直接使用,可编辑完整版资料,欢迎下载)一、食品中兽药残留的检测技术我国食品安全检测主要应用技术的研究及现状食品工业科技VOL24,(12),2003张志洁林清玉现状分析随着集约化畜牧业的发展,兽药的作用范围也在扩大,有的药物如抗生素、磺胺药、激素等已广泛用于促进畜禽的生长、减少发病率和提高饲料利用率、促进同期发情。
在饲料添加剂中,抗生素用量占有相当大的比重。
兽药的广泛应用使畜牧业在增产的同时,也带来了兽药残留的问题。
八十年代,欧美等国已开始建立了兽药残留检测体系,并制定了较为完善的兽药用量、休药期及有关法律法规。
我国兽药残留检测体系尚不够完备,时常发生因畜产品中药物残留超标而被外国拒绝进口的事件,给我国农产品出口造成很大的经济损失。
“十五”期间,我国将重点加强兽药监察体系和兽药残留检测体系的建设。
农业部每年投入1755 万元用于兽药残留监控,发展了近75 种单个兽药在饲料监控和动物源食品中残留的测定方法。
国家质检总局每年也投入大量资金,针对出口和欧盟监控的需要,建立一些兽药残留的检测方法。
但对于某些禁用兽药(主要是")兴奋剂和激素),其分析方法的灵敏度尚不能满足需要,或大量监控的成本难以承受。
克伦特罗(瘦肉精)的检测方法欧盟和美国FDA立法禁止克伦特罗在肉用畜禽中的使用;规定牛和马肝中的最大残留限量必须小于0.5µg/kg。
我国2001年也实施了鲜冻禽产品不准检出克伦特罗的标准。
对于克伦特罗,农业部已经颁布了采用高效液相色谱筛选和气)质联机验证的饲料测定方法(NY428-2001),但未使用国际认可的确证方法(稳定性同位素稀释技术)。
卫生部组织了肉中克伦特罗中毒控制方法的探索研究,营养与食品安全所和北京市疾病控制中心分别建立了HPLC-紫外与电化学检测方法和GC-MS 方法,正在探索HPLC-MS/MS串联检测方法。
营养与食品安全所、南京农大、华中农大和河南农科院均进行了ELISA试剂盒国产化的研究。
用色谱分析法建立兽药残留分析方法的基本步骤云南农业大学动物营养重点实验室摘要:从分析兽药残留的现状引出色谱分析应用的普遍性,着重介绍了以色谱分析法建立兽药残留分析方法的基本步骤,供从事兽药残留分析的色谱工作者参考。
关键词:兽药残留;高效液相色谱法;色谱法近20年来,兽药(包括药物添加剂)在畜牧业中的应用日益广泛,但是兽药的使用无疑会导致动物体内药物的滞留或蓄积,并以残留的方式进入人体及生态系统。
兽药残留对人类及环境的危害主要是慢性、远期和累积性的,如致癌、发育毒性、体内蓄积、免疫抑制、致敏和诱导耐药菌株等。
动物性食品中的兽药残留已成为公认的农业和环境问题,因此对残留的监测与控制已经是目前国内外兽药研究、开发、使用和管理中的重要内容。
随着兽医学和兽药科学的迅速发展,经过十几年的积累,基于分析化学、药物化学、临床药理与毒理学以及管理科学之上的兽药残留分析已成为一门新兴学科,其中心任务是为动物和动物性食品中的兽药残留监控提供分析手段,内容包括食品残留(药物原形及代谢产物)的含量测定与结构鉴定(静态残留分析)以及组织分布与代谢(动态残留分析)。
残留分析不仅是兽药残留研究和监控的重要基础,而且是兽药代谢、临床药理和生物药剂学等兽药理论及应用研究的必要手段。
与药品分析不同,残留分析的特殊性和复杂性在于痕量、动态的待测物存在于复杂的生物样品中,在于将分析手段与兽药的理化性质、体内过程、存在状态以及药理毒理相结合,在于样品基质和待测组分的不确定性,所以分离和检测是残留分析的两个基本方面,高分辨率和高灵敏度是其发展的两大精髓。
现代色谱和光谱技术,特别是20世纪80年代以来高效液相色谱、毛细管区域电泳、质谱、免疫分析及联用技术在残留分析方面的研究与应用取得了长足进展,利用这些技术可以测定ppb(10-9)~ppt(10-12)水平的残留组分。
人们在努力改进残留分析效能的同时更注重提高分析效率、降低分析成本和减少环境污染。
The determination of antibiotic and pesticide residues in foods: samplepreparation for LC-MS analysisAbstract: In this article, we will discuss SPE strategies prior to tandem LC/MS analysis for sub-ppb determination of chloramphenicol, nitrofuran antibiotic metabolites, and other related substances in animal tissues and in honey. Sample preparation for LC-MS analysis to determinate of antibiotic and pesticide residues in foods is reviewed and prospected .Key words: antibiotic and pesticide residues , food , sample preparation , LC-MS食品中抗生素和农药残留分析:用于LC-MS分析的SPE样品前处理方法Waters公司赵维国摘要:本文将讨论LC-MS分析之前,动物组织和蜂蜜中残留物质的样品前处理策略,其中包括ppb级氯霉素、喹诺酮类、硝基呋喃代谢产物和其它相关物质的固相提取(SPE)方法。
对食品中抗生素和农药残留的LC-MS分析的SPE样品前处理方法进行综述和展望。
关键词:抗生素和农药残留,食品,样品前处理,LC-MS食品中抗生素和其它兽药残留目前正在全球范围内受到广泛的重视。
对于农药和兽药残留的分析而言,所需达到的要求通常取决于毒理学评估的结果,而所期望达到的定量限(LOQ)与合法注册的农业化学品的最大允许残留限量相关。
近年来更加令人担心的是畜牧业和渔业生产中违规非法使用的某些抗生素残留。
这些抗生素没有允许的残留限量,任何被禁用抗生素的存在皆可作为犯罪活动的证据。
本文将讨论串联LC-MS分析之前动物组织和蜂蜜中残留物质的SPE样品前处理策略,其中包括ppb级氯霉素、氟喹诺酮类、硝基呋喃代谢产物和其它相关物质的SPE提取方法。
对食品中抗生素和农药残留的LC-MS分析的SPE样品前处理方法进行了综述和展望。
1固相提取方法SPE的优势SPE是样品前处理的重要手段。
与液液萃取相比,SPE方法简单、快速、重现性好且比较容易实现自动化,是近年来应用非常广泛的样品前处理技术之一。
SPE技术能够有效地净化和浓缩样品,不仅提高检测灵敏度,延长色谱柱寿命,而且能够延长LC-MS系统珍贵的开机时间。
SPE吸附剂:Oasis吸附剂的选择Oasis吸附剂是Waters公司1996年起推出的SPE产品,是Waters继其在业界首推Sep-Pak固相提取产品后,又一个划时代的SPE品牌。
Oasis吸附剂目前有反相机理(HLB)、阳离子交换与反相混合机理(MCX)、阴离子交换与反相混合机理(MAX)、弱阳离子交换与反相混合机理(WCX)、弱阴离子交换与反相混合机理(WCX)五种类型,分别适合于多种未知有机物及碱性、酸性物质的提取 (参见图1:Oasis 吸附剂选择图)。
图1 Oasis 吸附剂选择图2 用于LC-MS 分析的SPE 方法开发示例2.1 牛肉中氟喹诺酮类(Fluoroquinolone)药物的SPE 方法开发氟喹诺酮类药物主要用于预防和治疗动物疾病[1,2],少量使用对动物生长有一定的促进作用。
但是过量使用或使用不当会造成这类药物在畜产品中的长期残留。
而这类残留的药物对人的中枢神经系统会造成不良影响[3],因此,欧盟、北美等国家规定:氟喹诺酮类药物在动物源性食品中的最高限量不得超过10~400µg/kg 。
表1 喹诺酮类药物的最大残留限量(MRL) [7]下面以恩诺沙星为例,介绍如何根据化合物的结构特点,选择样品前处理所用的SPE 小柱和优化提取方法。
图2 恩诺沙星的结构式恩诺沙星是一个两性化合物,同时具有酸性和碱性特征:酸性官能团的pKa ≈ 5,碱性官能团的pKa ≈ 8-9。
恩诺沙星在水中溶解度也与pH 有关:中性条件下微残留标记物动物种类 目标组织 MRL(µg/kg) 达诺沙星(Danofloxacin )牛(Bovine ) 猪(Porcine ) 鸡(Chicken ) 肉(Muscle ) 肝脏(Liver ) 肾脏(Kidney ) 200 400 环丙沙星(Ciprofloxacin ) 恩诺沙星(Enrofloxacin )牛(Bovine )肉(Muscle ) 肾脏(Kidney )30200溶,在酸性或碱性条件下溶解度较好。
因此,可以选用离子交换吸附剂提取。
当pH>6 时,使用阴离子交换填料提取,pH<6 时,使用阳离子交换填料提取。
目前Waters开发了的单柱和双柱串联两种净化法用于氟喹诺酮类药物的SPE样品前处理。
单柱净化法:使用Waters公司的Oasis MAX(6cc/500mg, 186000865)固相提取小柱。
首先称取2g牛肾脏,用30mL 50 mM 磷酸盐缓冲液(pH 7.4)提取,再以10000 rpm速度离心10分钟,取上清液,进行SPE净化。
SPE净化操作步骤如下:1)活化、平衡SPE小柱:1 mL 甲醇, 1 mL 5 M NaOH和1 mL 水2)上样:5 mL的离心上清液3)第一步清洗:1 mL 5 % 氨水4)第二步清洗:1 mL 甲醇5) 洗脱:3 mL 4 % 甲酸甲醇溶液6) 挥干溶剂,用0.4mL 流动相重新定容氟喹诺酮类药物的分析可以用LC/MS或LC/荧光检测方法,本次实验中使用Waters /Micromass Quattro micro API™ (MS/MS)系统,最低检测限(LOQ)可低于20 µg/kg[4]。
LC分离条件等度分离:LC-UV, LC-荧光色谱柱:Atlantis™ dC18,5 μm,4.6 x 150 mm流动相:75% NFPA(0.2%) 水溶液,3% 甲醇,22% 乙腈流速: 1.2 mL/min温度: 30 °C进样体积:30-80 μL 梯度分离:LC-APCI MS色谱柱:Atlantis™ dC18,5 μm,4.6 x 150 mm 流动相:A: 0.2% NFPA*水溶液 B: 甲醇梯度:线性, 在10分钟内 40% B到80% B流速: 0.8 mL/min温度:30 °C进样: 30-80 μL*NFPA 为C4F9-COOH图3 牛肾脏中9种加标氟诺酮类药物SPE提取后的LC/MS/MS 分析此方法已用于合法注册的允许使用抗生素的残留分析。
可以看到,经过单柱SPE 净化、提取,可以得到较好的分析结果。
此外,Waters 还开发了能够去除更多干扰物质,得到更干净本底的双柱串联SPE 净化法。
同样是根据被测物的两性特性,样品先通过Oasis MAX 小柱(6cc 150 mg ,186000370),选择性地保留两性的目标化合物,清洗去除碱性和中性干扰物质。
然后,将从第一根SPE 小柱得到的洗脱液,经过Oasis MCX 小柱(1cc 30 mg ,186000254),再次选择性地保留目标化合物,清洗去除弱酸性干扰物,流程见图4。
加标浓度(ng/g ) 洛美沙星Lomefloxacin 达诺沙星Donofloxacin 氧氟沙星Ofloxation 氟甲喹Flumaquine 诺氟沙星 Norfloxacin 10 76.9[6.5] 75.5[7.7] 85.3[6.2] 75.0[13.5] 70.2[8.2] 100 87.8[5.3] 77.5[7.3] 91.9[7.7] 68.0[6.8] 75.7[5.9]加标浓度(ng/g ) 依诺沙星Enoxacin 环丙沙星Ciprofloxacin 恩诺沙星Enrofloxaxin 沙拉沙星Sarafloxcin 10 69.4[11.0] 70.2[11.3] 73.3[21.3] 71.9[10.9] 10078.7[7.6]80.5[4.7]108.4[5.6]82.0[5.5]图4 牛肾脏中氟喹诺酮类药物的双柱串联SPE 提取流程图5 牛肾脏中氟喹诺酮类药物的SPE 提取结果对比表2 9种氟喹诺酮类药物的回收率及相对标准偏差结果(n=5)从图5可以看到双柱串联SPE法净化的样品本底更加干净,只是回收率略有降低。
可见,选择性各异的SPE小柱和优化的SPE方法为样品前处理提供了更多的选择。
2.2虾中氯霉素(Chloramphenicol)的检测[5]氯霉素的过度使用会使细菌逐渐产生抗药性。
动物性食品中的氯霉素主要来源于带有抗生素的饲料或治疗时使用的抗生素。
目前,美国、加拿大、英国等国已经明令禁止在食用动物中使用氯霉素,食品中发现任何氯霉素残留即为违法。
氯霉素的最低定量限小于或等于100 ng/kg (0.1 ppb)。
氯霉素微溶于水(2.5 mg/mL),易溶于甲醇,乙酸乙酯,乙醇和丙酮,不溶于 (正)己烷,其结构如下:图6 氯霉素结构式美国FDA2003年的提取方法:1)乙酸乙酯(含2%氨水)提取组织中的氯霉素;2)挥干溶剂,并用0.05%醋酸溶解残留物;3)正己烷多次液液萃取;4)SPE C18小柱进行净化,甲醇洗脱,挥干。
用水溶解,过滤。
该方法的缺点是:用正己烷进行多次的液液萃取。
Waters 公司充分利用Oasis® HLB 小柱独特的富集和净化能力,避免液液萃取繁琐复杂的操作以及正己烷的使用,开发出适合LC/MS分析的操作简单、回收率高、步骤少的净化方法,而且该方法更容易标准化,具体操作如下:1)用乙酸乙酯(10+5ml)提取虾组织(5g),挥干溶剂2)用1mL 50:50 甲醇/水溶解残留物3)用20mL水稀释上述溶液,振荡或超声后,离心。
4)取上清液,通过Oasis® HLB 小柱(6cc ,200mg ,WAT106202),30%甲醇水溶液清洗,80%甲醇水溶液洗脱5)挥干洗脱溶剂,用流动相重新定容,过滤,待测。
2.3 蜂蜜中硝基呋喃类药物代谢产物(Nitrofuran metabolites)[6]硝基呋喃类药物是欧盟国家禁止使用的一类兽药,包括呋喃它酮、呋喃唑酮、呋喃西林和呋喃妥因等。
由于硝基呋喃类药物在动物体内容易代谢,因而在其生理基质中很少发现该类药物的原药,检测的目标化合物通常为它们与组织中蛋白结合的代谢产物:5-甲基吗啡-3-氨基-2-唑烷基酮(AMOZ),3-氨基-2-唑烷基酮(AOZ),氨基脲(SEM) ,1-氨基-乙内酰脲(AHD)。