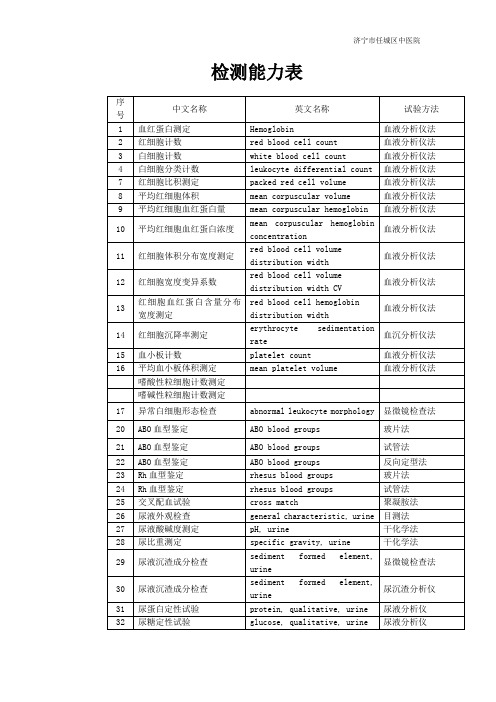
检测能力表
- 格式:doc
- 大小:367.50 KB
- 文档页数:11



表7检测机构综合能力评定表核查组组长签名:检测机构负责人签名:注:①检测机构检测人员不少于10人,根据所申请的检测项目,还需满足以下要求:地基基础工程检测:具有3年以上工程桩检测工作经验,并具备高级或者中级职称的持证上岗人员不得少于4名,每检测项目(方法)持证上岗编审人员不得少于3人(钻孔取芯法机长、编审人员还应分别取得机长、编审培训证),报告编写人还应具备工程类相关专业高级或者中级职称,报告审核人还应具备工程类相关专业高级职称或注册岩土工程师资格。
主体结构工程检测:具有3年以上结构工程检测工作经验,并具备高级或者中级职称的持证上岗人员不得少于4名,每检测项目(方法)持证上岗检测人员不得少于3人,报告审核人还应具备工程类相关专业高(中)级职称或注册一级结构工程师资格。
钢结构工程检测:具有3年以上钢结构检测工作经验,并具备高级或者中级职称的持证上岗人员不得少于4名,每检测项目(方法)持证上岗检测人员不得少于3人,报告审核人还应具备工程类相关专业高(中)级职称或注册一级结构工程师资格。
射线法、超声波法的报告编审人还应具备相应检测方法报告编审上岗证。
建筑幕墙检测:具有3年以上建筑幕墙检测工作经验,并具备高级或者中级职称的持证上岗人员不得少于4名,每检测项目持证上岗检测人员不得少于3人,报告审核人还应具备工程类相关专业高级职称。
见证取样检测:具有3年以上相应专业工作经验,并具备高级或者中级职称的持证上岗人员不得少于3名;每检测项目持证上岗检测人员不得少于3人,报告审核人还应具备工程类相关专业高级或者中级职称。
②现场核查结束前未能提供所抽取资料时,视为资料缺失,该项核查不予通过;③所有证据资料均需有效签署。
无故不予签署应记录为:“不满足”;④★:评定结果均为满足时,实验室通过核查。

附表1 申请资质认定检测能力表注○1“检测产品/类别”按领域类别、产品类别、产品,或领域类别、参数类别、参数分类排序。
如申请工程既有产品又有参数须分别填表;②具备检测产品全部参数能力的,不必注明所检参数;只具备检测产品部分参数能力的,在“说明”中注明能检或不能检的参数名称;③申请资质认定的检测能力,依据规范一般为国家、行业、地方规范,其他规范或方法应在“说明”中予以注明;④“限制范围或说明”指对采用的规范、方法、量程、客户等的限制。
⑤多场所的实验室,应按地点分别填写本表。
附表2.1机构负责人签名:日期:2012年2月27日附表2.2授权签字人申请表实验室名称:重庆鸿远职业危害检测评价有限责任公司注:申请人每人填写一张;授权签字人申请表实验室名称:重庆鸿远职业危害检测评价有限责任公司注:申请人每人填写一张;附表3重庆鸿远职业危害检测评价有限责任公司组织机构框图重庆市质量技术监督局①独立法人的画出本实验室内、外(行政或业务指导)部关系;②非独立法人的画出本实验室在母体法人中所处位置、与实验室相关的部门;③直接(属行政)关系用实线连接,间接(属业务指导)关系用虚线连接;④有独立帐号的,请在此页的空白处加盖有本实验室名称和开户银行帐号的印章。
附表4实验室人员一览表第页共页备注栏内填写:“正式人员”、“合同制人员”6 / 7附表5仪器设备(规范物质)配置一览表注○1申请时,该表的前五列与《申请书》附表1对应,为了简化此表的填写,参数相同的不重复填写。
序号可以不连续。
○2溯源方式填写:检定、校准、自校准等;○3多场所的实验室,按地点分别填写本表。
7 / 7。

序号名称1重量差异/装量差异《中国药典》2015年版四部通则 0100美国药典第41版附录<905>英国药典2018年版附录Ⅻ C 欧洲药典第9版2.9.52装量/最低装量《中国药典》2015年版四部通则0100;0942美国药典第41版附录<755><905><31>英国药典2018年版附录Ⅻ C5欧洲药典第9版2.9.173可见异物《中国药典》2015年版四部通则 0904只用第一法美国药典第41版附录<790>英国药典2018年版附录ⅩⅢ B欧洲药典第9版2.9.204溶散时限《中国药典》2015年版四部通则0108;09215金属性异物《中国药典》2015年版四部通则 01056每瓶总揿(吸、喷)次《中国药典》2015年版四部通则 0111;0112;0113一药品7泄漏率《中国药典》2005年版二部附录I L8每揿(吸、喷)主药含量《中国药典》2015年版四部通则 0112;01139喷出总量《中国药典》2015年版四部通则 011310喷射速率《中国药典》2015年版四部通则 011311每喷(揿)喷量《中国药典》2015年版四部通则 0112;011312溶化性《中国药典》2015年版四部通则 0100;0104;018813沉降体积比《中国药典》2015年版四部通则 0105;0106;0123;012614外观均匀度《中国药典》2015年版四部通则 011515溶解度《中国药典》2015年版四部凡例16分散均匀性《中国药典》2015年版四部通则 010117吸收系数《中国药典》2015年版四部通则 040118溶液的透光率《中国药典》2015年版四部通则 0401限制范围类别(产品/项目/参数)吉林省药品检验所检验检测能力表产品/项目/参数说明依据的标准(方法)名称及编号(含年号)序号序号名称19吸光度《中国药典》2015年版四部通则 040120相对密度《中国药典》2015年版四部通则 0601美国药典第41版附录<841>只用第一法英国药典2018年版附录ⅤG欧洲药典第9版2.2.5日本药局方第17版一般试验法2.56只用第一法21馏程《中国药典》2015年版四部通则 061122熔点《中国药典》2015年版四部通则 061223旋光度/比旋度《中国药典》2015年版四部通则 0621美国药典第41版附录<781>英国药典2018年版附录Ⅴ F 欧洲药典第9版2.2.7日本药局方第17版一般试验法2.49一药品24折光率《中国药典》2015年版四部通则 0622美国药典第41版附录<831>欧洲药典第9版2.2.6日本药局方第17版一般试验法2.4525黏度《中国药典》2015年版四部通则 0633不用第三法26pH值/酸度/酸碱度/碱度《中国药典》2015年版四部通则 0631美国药典第41版附录<791>英国药典2018年版附录ⅤL欧洲药典第9版2.2.3日本药局方第17版一般试验法2.5427氮《中国药典》2015年版四部通则 070428乙醇量《中国药典》2015年版四部通则 0711美国药典第41版附录<611>英国药典2018年版附录ⅧF欧洲药典第9版2.9.1029酸值《中国药典》2015年版四部通则 0713;230330皂化值《中国药典》2015年版四部通则 071331羟值《中国药典》2015年版四部通则 071332碘值《中国药典》2015年版四部通则 071333杂质《中国药典》2015年版四部通则 0713序号名称34维生素A 《中国药典》2015年版四部通则 072135维生素D 《中国药典》2015年版四部通则 072236氯化物《中国药典》2015年版四部通则 0801美国药典第41版附录<221>欧洲药典第9版2.4.4日本药局方第17版一般试验法1.0337硫酸盐《中国药典》2015年版四部通则 0802美国药典第41版附录<221>欧洲药典第9版2.4.13日本药局方第17版一般试验法1.1438硫化物《中国药典》2015年版四部通则 0803一药品39硒《中国药典》2015年版四部通则 080440氟《中国药典》2015年版四部通则 080541氰化物《中国药典》2015年版四部通则 0806只用第一法42铁盐《中国药典》2015年版四部通则 0807美国药典第41版附录<241>欧洲药典第9版2.4.9日本药局方第17版一般试验法1.1043重金属《中国药典》2015年版四部通则 0821美国药典第41版附录<231>44砷盐《中国药典》2015年版四部通则 0822美国药典第41版附录<211>45铵盐《中国药典》2015年版四部通则 0808欧洲药典第9版2.4.1日本药局方第17版一般试验法1.0246干燥失重《中国药典》2015年版四部通则 0831美国药典第41版附录<731>英国药典2018年版附录Ⅸ D 欧洲药典第9版2.2.32日本药局方第17版一般试验法2.4147水分《中国药典》2015年版四部通则 0832;0713序号名称48炽灼残渣《中国药典》2015年版四部通则 0841美国药典第41版附录<281>英国药典2018年版附录Ⅸ A 欧洲药典第9版2.4.16日本药局方第17版一般试验法2.4449易炭化物《中国药典》2015年版四部通则 084250残留溶剂《中国药典》2015年版四部通则 086151溶液颜色《中国药典》2015年版四部通则 0901美国药典第41版附录<631>欧洲药典第9版2.2.2日本药局方第17版一般试验法2.65一药品52澄清度《中国药典》2015年版四部通则0902美国药典第41版附录<641>欧洲药典第9版2.2.153不溶性微粒《中国药典》2015年版四部通则 0903美国药典第41版附录<788>英国药典2018年版附录ⅩⅢ A 欧洲药典第9版2.9.19日本药局方第17版一般试验法6.07,6.0854结晶性《中国药典》2015年版四部通则 0981只用第一法55粒度《中国药典》2015年版四部通则 0982;0104;010556粒度和粒度分布《中国药典》2015年版四部通则 098257渗透压摩尔浓度《中国药典》2015年版四部通则 0632美国药典第41版附录<785>英国药典2018年版附录ⅤN欧洲药典第9版2.2.35日本药局方第17版一般试验法2.4758崩解时限《中国药典》2015年版四部通则0921美国药典第41版附录<701>英国药典2018年版附录Ⅻ A、Ⅻ B欧洲药典第9版2.9.1日本药局方第17版一般试验法6.09序号名称59融变时限《中国药典》2015年版四部通则 0922英国药典2018年版附录Ⅻ A2欧洲药典第9版2.9.260溶出度《中国药典》2015年版四部通则 0931不用第四、五法美国药典第41版附录<711>只用一、二法英国药典2018年版附录Ⅻ B1只用一、二法欧洲药典第9版2.9.3只用一、二法日本药局方第17版一般试验法6.10只用一、二法61释放度《中国药典》2015年版四部通则 0931不用第四、五法美国药典第41版附录<711>只用一、二法英国药典2018年版附录Ⅻ B1只用一、二法欧洲药典第9版2.9.3只用一、二法日本药局方第17版一般试验法6.10只用一、二法62含量均匀度《中国药典》2015年版四部通则 0941美国药典第41版附录<905>英国药典2018年版附录Ⅻ C3欧洲药典第9版2.9.6日本药局方第17版一般试验法6.02一药品63片剂脆碎度《中国药典》2015年版四部通则 0923美国药典第41版附录<1216>英国药典2018年版附录ⅩⅦ G 欧洲药典第9版2.9.7日本药局方第17版通则 G664性状《中国药典》2015年版二部/一部/四部美国药典第41版英国药典2018年版欧洲药典第9版日本药局方第17版65容量分析《中国药典》2015年版二部/一部/四部美国药典第41版英国药典2018年版欧洲药典第9版日本药局方第17版66重量分析《中国药典》2015年版二部/一部/四部67不溶物《中国药典》2015年版四部通则 018368含膏量《中国药典》2015年版四部通则 012269总固体《中国药典》2015年版四部通则 018570耐热性《中国药典》2015年版四部通则 012271喷射试验《中国药典》2010年版一部附录ⅠZ序号名称72药材和饮片取样《中国药典》2015年版四部通则 021173显微鉴别《中国药典》2015年版四部通则 200174无机离子《中国药典》2015年版二部/一部75药材和饮片中的杂质《中国药典》2015年版四部通则 230176灰分《中国药典》2015年版四部通则 230277羰基值《中国药典》2015年版四部通则 230378膨胀度《中国药典》2015年版四部通则 210179过氧化值《中国药典》2015年版四部通则 0713;230380有机氯类农药残留量《中国药典》2015年版四部通则 234181有机磷类农药残留量《中国药典》2015年版四部通则 2341一药品82注射剂有关物质《中国药典》2015年版四部通则 240083甲醇量《中国药典》2015年版四部通则 087184浸出物《中国药典》2015年版四部通则 220185鞣质含量《中国药典》2015年版四部通则 220286挥发油《中国药典》2015年版四部通则 220487发泡量《中国药典》2015年版四部通则 010188出芽率《中国药典》2015年版 一部156页89铅、镉、砷、汞、铜《中国药典》2015年版四部通则 232190松紧度《中国药典》2015年版四部522页91脆碎度《中国药典》2015年版四部522页92乳酸菌制剂检验《卫生部药品标准》二部第六册附录493抗生素微生物检定《中国药典》2015年版四部通则120194异常毒性《中国药典》2015年版四部通则1141英国药典2018年版附录ⅩⅣ E 欧洲药典第9版2.6.995热原《中国药典》2015年版四部通则1142美国药典第41版附录<151>英国药典2018年版附录ⅩⅣ D 欧洲药典第9版2.6.8日本药局方第17版一般试验法4.04序号名称96细菌内毒素《中国药典》2015年版四部通则1143美国药典第41版附录<85>英国药典2018年版附录Ⅹ Ⅳ C 欧洲药典第9版2.6.14日本药局方第17版一般试验法4.0197降压物质《中国药典》2015年版四部通则114598溶血与凝聚《中国药典》2015年版四部通则114899出血毒《国家药品监督管理局国家药品标准化学药品地方标准上升国家标准》第九册62页、十六册88页100神经毒《国家药品监督管理局国家药品标准化学药品地方标准上升国家标准》第十六册88页一药品101无菌《中国药典》2015年版四部通则1101美国药典第41版附录<71>英国药典2018年版附录ⅩⅥ A欧洲药典第9版2.6.1日本药局方第17版一般试验法4.06《中国药典》2015年版四部通则1105不用MPN法102微生物限度《中国药典》2015年版四部通则1106《中国药典》2015年版四部通则1107美国药典第41版附录<61><62>英国药典2018年版附录Ⅹ ⅥB(1、2)欧洲药典第9版2.6.12-2.6.13日本药局方第17版一般试验法4.05103过敏反应《中国药典》2015年版四部通则1147《国家药品监督管理局国家药品标准化学药品地方标准上升国家标准》第九册215页(MTT法)《国家食品药品监督管理总局国家药品标准WS1-XG-019-2016》(MTT法)104活力(性)测定《国家药品监督管理局国家药品标准化学药品地方标准上升国家标准》 第九册35页(白细胞计数法)《国家药品监督管理局国家药品标准化学药品地方标准上升国家标准》第十六册82页(呼吸活性测定法)序号名称进口药品注册标准 X20030248(呼吸活性测定法)104活力(性)测定《国家药品监督管理局国家药品标准化学药品地方标准上升国家标准》第十六册104页 、118页(T细胞活性测定法)《国家药品监督管理局国家药品标准新药转正标准》第27册191页(T细胞活性测定法)国家食品药品监督管理局国家药品标准WS1-XG-037-2000-2008(T细胞活性测定法)105凝血酶效价《中国药典》2015年版二部106胰蛋白酶效价《中国药典》2015年版二部107胰淀粉酶效价《中国药典》2015年版二部108胰脂肪酶效价《中国药典》2015年版二部109胃蛋白酶效价《中国药典》2015年版二部110抑肽酶效价《中国药典》2015年版二部111降纤酶效价《国家药品监督管理局国家药品标准化学药品地方标准上升国家标准》第十六册88页112尿激酶效价《中国药典》2015年版二部113糜蛋白酶效价《中国药典》2015年版二部国家药品监督管理局国家药品标准 WS1-(X-109)-2012Z一药品国家食品药品监督管理局国家药品标准WS1-(X-052)-2001Z-2010国家药品监督管理局国家药品标准 WS1-(X-111)-2000Z-2005国家药品监督管理局国家药品标准 WS1-XG-053-2000-2005 116核糖含量《国家药品监督管理局国家药品标准化学药品地方标准上升国家标准》 第十六册103页117皮肤刺激试验国家食品药品监督管理总局《药物刺激性、过敏性和溶血性研究技术指导原则》(2014年)118血管刺激性试验国家食品药品监督管理总局《药物刺激性、过敏性和溶血性研究技术指导原则》(2014年)119皮肤过敏试验国家食品药品监督管理总局《药物刺激性、过敏性和溶血性研究技术指导原则》(2014年)120溶血试验国家食品药品监督管理总局《药物刺激性、过敏性和溶血性研究技术指导原则》(2014年)121皮内刺激试验国家食品药品监督管理总局《药物刺激性、过敏性和溶血性研究技术指导原则》(2014年)114蚓激酶效价115免疫原性序号名称122肌内刺激试验国家食品药品监督管理总局《药物刺激性、过敏性和溶血性研究技术指导原则》(2014年)123直肠刺激试验国家食品药品监督管理总局《药物刺激性、过敏性和溶血性研究技术指导原则》(2014年)124急性毒性试验国家食品药品监督管理总局《药物刺激性、过敏性和溶血性研究技术指导原则》(2014年)125眼刺激性试验国家食品药品监督管理总局《药物刺激性、过敏性和溶血性研究技术指导原则》(2014年)126药材和饮片检定《中国药典》2015年版四部通则 0212127二氧化硫残留量《中国药典》2015年版四部通则 2331只用第一、三法128防腐剂《中国药典》2015年版二部只测羟苯甲酯、羟苯乙酯、羟苯丙酯、苯扎溴铵129制药用水电导率《中国药典》2015年版四部通则 0681一药品130组胺类物质《中国药典》2015年版四部通则1146国家药品监督管理局国家药品标准WS1-XG-004-2006《中国药典》2015年版二部132等电点《中国药典》2015年版四部通则 0541《中国药典》2015年版四部通则 0301(一般鉴别)美国药典第41版附录<191>欧洲药典第9版2.3日本药局方第17版一般试验法1.09《中国药典》2015年版四部通则 0401(紫外-可见分光光度法)美国药典第41版附录<857>英国药典2018年版附录Ⅱ B 欧洲药典第9版2.2.25133鉴别日本药局方第17版一般试验法2.24《中国药典》2015年版四部通则 0402(红外分光光度法)美国药典第41版附录<197><854>英国药典2018年版附录Ⅱ A 欧洲药典第9版2.2.24日本药局方第17版一般试验法2.25131胰激肽原酶效价序号名称《中国药典》2015年版四部通则 0501(纸色谱法)《中国药典》2015年版四部通则 0502(薄层色谱法)美国药典第41版附录<621>英国药典2018年版附录Ⅲ A欧洲药典第9版2.2.27日本药局方第17版一般试验法2.03《中国药典》2015年版四部通则 0512(高效液相色谱法)美国药典第41版附录<621>英国药典2018年版附录Ⅲ D欧洲药典第9版2.2.29日本药局方第17版一般试验法2.01一药品133鉴别《中国药典》2015年版四部通则 0521(气相色谱法)美国药典第41版附录<621>英国药典2018年版附录Ⅲ B 欧洲药典第9版2.2.28《中国药典》2015年版四部通则 0541(电泳法)《中国药典》2015年版四部通则 0542(毛细管电泳法)《中国药典》2015年版四部通则 0514(分子排阻色谱法)英国药典2018年版附录Ⅲ C 欧洲药典第9版2.2.30《中国药典》2015年版四部通则 0513 (离子色谱法)《中国药典》2015年版四部通则 0612 (熔点)《中国药典》2015年版四部通则 0703(氧瓶燃烧法)《中国药典》2015年版二部/一部(容量分析法)美国药典第41版英国药典2018年版欧洲药典第9版日本药局方第17版《中国药典》2015年版二部/一部美国药典第41版英国药典2018年版欧洲药典第9版日本药局方第17版序号名称《中国药典》2015年版四部通则 0431(液相色谱-质谱法)《中国药典》2015年版四部通则 0431(气相色谱-质谱法)133鉴别《中国药典》2015年版四部通则 0412(电感耦合等离子体质谱法)不用高效液相色谱-电感耦合等离子体质谱联用法《中国药典》2015年版四部通则 0451(X射线衍射法)只用第二法美国药典第41版附录<941>英国药典2018年版附录ⅩⅤⅡQ欧洲药典第9版2.9.33日本药局方第17版一般试验法2.58《中国药典》2015年版四部通则 0401(紫外-可见分光光度法)美国药典第41版附录<857>英国药典2018年版附录Ⅱ B欧洲药典第9版2.2.25日本药局方第17版一般试验法2.24一药品《中国药典》2015年版四部通则 0402(红外分光光度法)美国药典第41版附录<197><854>英国药典2018年版附录Ⅱ A欧洲药典第9版2.2.24 134有关物质日本药局方第17版一般试验法2.25《中国药典》2015年版四部通则 0406(原子吸收分光光度法)美国药典第41版附录<852>《中国药典》2015年版四部通则 0405(荧光分析法)《中国药典》2015年版四部通则 0407(火焰光度法)《中国药典》2015年版四部通则 0501(纸色谱法)《中国药典》2015年版四部通则 0502(薄层色谱法)美国药典第41版附录<621>英国药典2018年版附录Ⅲ A欧洲药典第9版2.2.27日本药局方第17版一般试验法2.03序号名称《中国药典》2015年版四部通则 0511(柱色谱法)《中国药典》2015年版四部通则 0512(高效液相色谱法)美国药典第41版附录<621>英国药典2018年版附录Ⅲ D欧洲药典第9版2.2.29日本药局方第17版一般试验法2.01《中国药典》2015年版四部通则 0521(气相色谱法)美国药典第41版附录<621>英国药典2018年版附录Ⅲ B欧洲药典第9版2.2.28《中国药典》2015年版四部通则 0541(电泳法)《中国药典》2015年版四部通则 0542(毛细管电泳法)一药品134有关物质《中国药典》2015年版四部通则 0514(分子排阻色谱法)英国药典2018年版附录Ⅲ C 欧洲药典第9版2.2.30《中国药典》2015年版四部通则 0513(离子色谱法)《中国药典》2015年版四部通则 0621(旋光度测定法)美国药典第41版附录<781>英国药典2018年版附录Ⅴ F 欧洲药典第9版2.2.7日本药局方第17版一般试验法2.49《中国药典》2015年版四部通则 0701(电位滴定法与永停滴定法)美国药典第41版附录<541>欧洲药典第9版2.2.19;2.2.20;2.2.65日本药局方第17版一般试验法2.50《中国药典》2015年版四部通则 0702(非水溶液滴定法)美国药典第41版附录<541>序号名称《中国药典》2015年版四部通则 0703(氧瓶燃烧法)《中国药典》2015年版四部通则 0704(氮测定法)美国药典第41版附录<461>英国药典2018年版附录Ⅷ H欧洲药典第9版2.5.9日本药局方第17版一般试验法1.08《中国药典》2015年版二部/一部(容量分析法)美国药典第41版英国药典2018年版欧洲药典第9版日本药局方第17版《中国药典》2015年版二部/一部(重量分析法)一药品134有关物质《中国药典》2015年版二部/一部美国药典第41版英国药典2018年版欧洲药典第9版日本药局方第17版《中国药典》2015年版四部通则 0431(液相色谱-质谱法)《中国药典》2015年版四部通则 0431(气相色谱-质谱法)《中国药典》2015年版四部通则 0412(电感耦合等离子体质谱法)不用高效液相色谱-电感耦合等离子体质谱联用法《中国药典》2015年版四部通则 0451(X射线衍射法)只用第二法美国药典第41版附录<941>英国药典2018年版附录ⅩⅤⅡQ欧洲药典第9版2.9.33日本药局方第17版一般试验法2.58135含量测定/效价测定《中国药典》2015年版四部通则 0401(紫外-可见分光光度法)美国药典第41版附录<857>英国药典2018年版附录Ⅱ B欧洲药典第9版2.2.25日本药局方第17版一般试验法2.24序号名称《中国药典》2015年版四部通则 0402(红外分光光度法)美国药典第41版附录<197><854>英国药典2018年版附录Ⅱ A欧洲药典第9版2.2.24日本药局方第17版一般试验法2.25《中国药典》2015年版四部通则 0406(原子吸收分光光度法)美国药典第41版附录<852>《中国药典》2015年版四部通则 0405(荧光分析法)《中国药典》2015年版四部通则 0407(火焰光度法)《中国药典》2015年版四部通则 0501(纸色谱法)一药品135含量测定/效价测定《中国药典》2015年版四部通则 0502(薄层色谱法)美国药典第41版附录<621>英国药典2018年版附录Ⅲ A欧洲药典第9版2.2.27日本药局方第17版一般试验法2.03《中国药典》2015年版四部通则 0511(柱色谱法)《中国药典》2015年版四部通则 0512(高效液相色谱法)美国药典第41版附录<621>英国药典2018年版附录Ⅲ D欧洲药典第9版2.2.29日本药局方第17版一般试验法2.01《中国药典》2015年版四部通则 0521(气相色谱法)美国药典第41版附录<621>英国药典2018年版附录Ⅲ B欧洲药典第9版2.2.28《中国药典》2015年版四部通则 0541(电泳法)《中国药典》2015年版四部通则 0542(毛细管电泳法)序号名称《中国药典》2015年版四部通则 0514(分子排阻色谱法)英国药典2018年版附录Ⅲ C欧洲药典第9版2.2.30《中国药典》2015年版四部通则 0513(离子色谱法)《中国药典》2015年版四部通则 0621(旋光度测定法)美国药典第41版附录<781>英国药典2018年版附录Ⅴ F欧洲药典第9版2.2.7日本药局方第17版一般试验法2.49《中国药典》2015年版四部通则 0701(电位滴定法与永停滴定法)美国药典第41版附录<541>欧洲药典第9版2.2.19;2.2.20;2.2.65日本药局方第17版一般试验法2.50《中国药典》2015年版四部通则 0702(非水溶液滴定法)美国药典第41版附录<541>一药品135含量测定/效价测定《中国药典》2015年版四部通则 0703(氧瓶燃烧法)《中国药典》2015年版四部通则 0704(氮测定法)美国药典第41版附录<461>英国药典2018年版附录Ⅷ H欧洲药典第9版2.5.9日本药局方第17版一般试验法1.08《中国药典》2015年版四部通则 0721(维生素A测定法)《中国药典》2015年版四部通则 0722(维生素D测定法)《中国药典》2015年版四部通则1201(抗生素微生物检定法)《中国药典》2015年版四部通则1208(肝素生物测定法)《中国药典》2015年版四部通则1211(胰岛素生物测定法)序号名称《中国药典》2015年版四部通则 1212(精蛋白锌胰岛素注射液延缓作用测定法)《中国药典》2015年版四部通则 1210(缩宫素生物测定法)《中国药典》2015年版二部/一部(容量分析法)美国药典第41版英国药典2018年版欧洲药典第9版日本药局方第17版135含量测定/效价测定《中国药典》2015年版二部/一部(重量分析法)《中国药典》2015年版二部/一部美国药典第41版英国药典2018年版欧洲药典第9版日本药局方第17版《中国药典》2015年版四部通则 0412(电感耦合等离子体质谱法)不用高效液相色谱-电感耦合等离子体质谱联用法一药品136高分子聚合物《中国药典》2015年版四部通则 0514137分子量与分子量分布《中国药典》2015年版四部通则 0514138黄曲霉毒素《中国药典》2015年版四部通则 2351139拟除虫菊酯类农药残留量测定《中国药典》2015年版四部通则 2341《中国药典》2015年版四部通则 0406(原子吸收分光光度法)140元素分析《中国药典》2015年版四部通则 0412(电感耦合等离子体质谱法)不用高效液相色谱-电感耦合等离子体质谱联用法141中药指纹图谱《中国药典》2015年版一部《新药转正标准》第66册195页、196页《中国药典》2015年版二部520页143升压素《中国药典》2015年版四部通则1205144升压物质《中国药典》2015年版四部通则1144142抗Xa、抗Ⅱa因子效价序号名称145凝点《中国药典》2015年版四部通则0613146冻力强度《中国药典》2015年版四部547页一药品147初黏力的测定《中国药典》2015年版四部通则 0952148持黏力的测定《中国药典》2015年版四部通则 0952149聚合酶链式反应法《中国药典》2015年一部1pH值《中国药典》2015年版三部通则06312氮测定《中国药典》2015年版三部通则07043蛋白质《中国药典》2015年版三部通则0731,31244氯化钠《中国药典》2015年版三部通则31075钠离子《中国药典》2015年版三部通则31106钾离子《中国药典》2015年版三部通则31097辛酸钠《中国药典》2015年版三部通则31118吸光度《中国药典》2015年版三部通则04019热稳定性试验《中国药典》2015年版三部二 生物制品《中国药典》2015年版三部通则3403(免疫双扩散法)《中国药典》2015年版三部通则3404(免疫电泳法)10鉴别试验《中国药典》2015年版三部194页(单向免疫扩散)《中国药典》2015年版三部通则3402(免疫斑点法)11水分《中国药典》2015年版三部通则0832《中国药典》2015年版三部通则0541 (电泳法)只用第二、五法《中国药典》2015年版三部通则0512(高效液相色谱法)12纯度序号名称13人血白蛋白多聚体测定《中国药典》2015年版三部通则312114人免疫球蛋白类制品IgG单体加二聚体测定《中国药典》2015年版三部通则312215热原《中国药典》2015年版三部通则114216无菌《中国药典》2015年版三部通则110117细菌内毒素《中国药典》2015年版三部通则114318异常毒性《中国药典》2015年版三部通则114119乙肝表面抗原《中国药典》2015年版三部20外观《中国药典》2015年版三部21装量/装量差异《中国药典》2015年版三部制剂通则22最低装量《中国药典》2015年版三部通则0942二生物制品23人血液制品中糖及糖醇含量《中国药典》2015年版三部通则312024人血白蛋白铝残留量《中国药典》2015年版三部通则320825激肽释放酶原激活剂(PKA)《中国药典》2015年版三部通则3409《中国药典》2015年版三部(放射免疫法)《中国药典》2015年版三部(酶联免疫法)27枸橼酸离子含量《中国药典》2015年版三部通则310828可见异物《中国药典》2015年版三部通则0904只用第一法29聚乙二醇残留量《中国药典》2015年版三部通则320230凝固活力《中国药典》2015年版 三部274页31人凝血酶活性《中国药典》2015年版三部通则342232牛血清白蛋白残留量《中国药典》2015年版三部通则341126乙肝表面抗体(抗HBs)序号名称33抗补体活性(ACA)《中国药典》2015年版三部通则341034抗A、抗B血凝素《中国药典》2015年版三部通则342535活化的凝血因子活性《中国药典》2015年版三部通则342336人凝血因子II效价《中国药典》2015年版三部通则351737人凝血因子VII效价《中国药典》2015年版三部通则351838人凝血因子IX效价《中国药典》2015年版三部通则351939人凝血因子X效价《中国药典》2015年版三部通则352040人凝血因子VIII效价《中国药典》2015年版三部通则352141人免疫球蛋白中白喉抗体效价《中国药典》2015年版三部通则351342 血凝素含量《中国药典》2015年版三部194页43肝素含量《中国药典》2015年版三部通则3424二生物制品44磷酸三丁酯残留量《中国药典》2015年版三部通则320545聚山梨酯80残留量《中国药典》2015年版三部通则320346硫柳汞含量《中国药典》2015年版三部通则3115只用第一法《中国药典》2015年版三部(酶联免疫法)《中国药典》2015年版三部通则340848游离甲醛含量《中国药典》2015年版三部通则320749卵清蛋白含量《中国药典》2015年版三部(酶联免疫法)50复溶时间《中国药典》2015年版三部51真空度《中国药典》2015年版三部52渗透压摩尔浓度《中国药典》2015年版三部通则063253不溶性微粒《中国药典》2015年版三部通则090347抗生素残留量。
申请资质认定检测能力表
第2页共5页
第3页共5页
第4页共5页
第5页共5页
注:①“检测产品/类别”按领域类别、产品类别、产品,或领域类别、参数类别、参数分类排序。
如申请项目既有产品又有参数须分别填表;
②具备检测产品全部参数能力的,不必注明所检参数;只具备检测产品部分参数能力的,在“说明”中注明能检或不能检的参数名称;
③申请资质认定的检测能力,依据标准一般为国家、行业、地方标准,其他标准或方法应在“说明”中予以注明;
④“限制范围或说明”指对采用的标准、方法、量程、客户等的限制。
⑤多场所的实验室,应按地点分别填写本表。
⑥★表示扩项的检测项目。