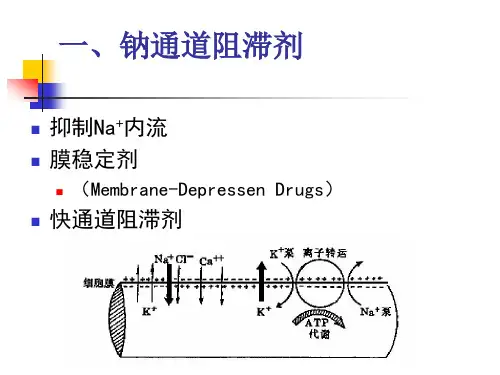
钠通道阻滞药
- 格式:ppt
- 大小:992.00 KB
- 文档页数:25

Ⅰc类钠通道阻滞药(一)病因1、高血压引起的心律失常众所周知,长期的高血压会导致心脑肾眼底等脏器和血管的损害。
高血压对心脏的早期损害常常是对心房的作用,Dernellis JM等对28例原发性未经治疗的高血压患者与20例健康者作比较,发现高血压患者左房的最大容积增加,左房功能受损,用依那普利和(或)thrazide治疗16周后,血压控制,左房最大容积显著减少,左房功能恢复。
有作者也发现长期高血压导致左房容积增加,左房被动排空功能下降,左房收缩泵功能增加,并被认为这是在高血压左室肥厚的一种代偿机制。
由于高血压导致左室后负荷增加,左房压增加,左房的助力泵功能、管道功能、储存器功能发生改变,左房容积增大,引起左房扩大,因此在无二尖瓣瓣膜病和弧立性房颤的情况下,左房的大小可以反映高血压的历史。
左房结构和功能的变化在非勺形高血压患者中尤为明显。
动物模型的组织学研究已证明,心房纤维的拉长或脂肪沉积,其结果导致心房肌的丢失,增加发展成房颤的倾向。
当房颤发生在心脏结构异常时,高血压是最常见原因,高血压导致房颤有许多机制,其中之一是左室后负荷增加和左房结构的改变,左房结构改变与左房舒张压增高、电生理的改变呈线性关系;另外,可能更多直接或复杂的涉及长期形态学、电生理方面的问题,左房分泌的物质还逐渐减少左室顺应性,而左房的扩大又与左室顺应性下降有关。
一个较大的左房内径伴随着慢性房颤进行性发展。
高血压患者的左房比健康者增大,随着左房增大发生房性心律失常严重程度也逐步增加,年龄越大,高血压病史越长,左房扩大的程度也越重,发生房颤的机率也越高。
本组资料中高龄组(80岁)发生持续性房颤为33.77%,明显高于其他年龄组,这和Framingham研究相一致,年龄、高血压是发生房颤的危险因素。
提示年龄、高血压病史、左房大小是影响高血压房性心律失常的重要因素。
二尖瓣返流加重了左房、左室的扩大,左房、左室的扩大又反过来加重二尖瓣返流的程度,最终导致心脏扩大,心律失常加重,心功能恶化。



抗心律失常药知识学习一、概述(一)Ⅰ类:钠通道阻滞药Ⅰa 类:适度阻滞钠通道,降低 Vmax,延长复极过程,延长 ERP 更明显,代表药:奎尼丁,普鲁卡因胺。
Ⅰb 类:轻度阻滞钠通道,轻度降低 Vmax,降低自律性,缩短或不影响 APD。
代表药:利多卡因、苯妥英。
Ⅰc 类:明显阻滞钠通道,显著降低 Vmax。
代表药:普罗帕酮、氟卡尼。
(二)Ⅱ类:β肾上腺素受体阻断药降低自律性,减慢房室传导,代表药:普奈洛尔、美托洛尔(三)Ⅲ类:钾通道阻滞药延长 APD、ERP 药,代表药为胺碘酮(四)Ⅳ类:钙通道阻滞药降低自律性,减慢房室传导,代表药:维拉帕米、地尔硫卓利多卡因不宜口服,静脉给药。
(一)药理作用轻度阻滞 Na+通道1. 对激活态和失活态的 Na+通道均有阻断作用2. 减慢浦氏纤维的 4 相除极速率,降低自律性。
3. 对心肌梗死区缺血的组织(处于失活态)其阻断作用强4.缩短 APD,相对延长 ERP(二)临床应用本品为窄谱抗心律失常药,仅用于室性心律失常,特别适用于危急病例。
苯妥英钠1.口服吸收慢,常静脉给药.2.作用与利多卡因相似.3.用于治疗室性心律失常,对强心甙中毒更有效。
4.不良反应较多普萘洛尔(一)药理作用1.降低窦房结、心房和浦氏纤维的自律性,在运动和情绪激动时明显;2.降低儿茶酚胺所致的迟后除极;3.减慢房室结传导,延长 ERP 。
(二)临床应用室上性心律失常,对窦性心动过速,尤其与交感神经过度兴奋有关的效果更好;运动和情绪激动,嗜铬细胞瘤、甲亢引起的室性心律失常均有效。
单用奎尼丁或强心苷治疗房颤不显著时,合用此药效果更显著。
对心梗患者,能缩小梗死范围,降低死亡率。
可减少肥厚型心肌病所致的心律失常。
胺碘酮(一)药理作用阻滞 K+通道,Na+通道,Ca2+通道,非竞争性阻断、受体,广谱抗心律失常药。
1.降低窦房结和浦氏纤维的自律性,2.减慢房室结、浦氏纤维的传导速度,3.延长复极化过程,显著延长心房和浦氏纤维的 APD 和ERP,延长 Q-T 间期和 QRS 波。



第四章钠通道激动剂、阻滞剂第一节概述钠通道的一个重要特性就是具有特异的激动剂和阻滞剂。
这些激动剂和阻滞剂主要是神经毒素和作用于中枢及心脏钠通道的药物。
钠通道是许多特异性天然动植物神经毒素作用的靶器。
这些毒素可调节钠通道的各种功能活性,包括通道的电导、激活和失活等,进而影响电信号产生与传导过程,使动物麻痹,甚至死亡。
电压门控型钠通道上至少存在7个不同的神经毒素结合靶位点(见图2-6-1)。
河豚毒素(tetrodotoxin,TTX)、蛤蚌毒素(saxitoxin,STX)和芋螺毒素(conotoxin,CTX)作用于位点1,阻断通道外口,但不改变通道动力学和门控性质;蟾毒素(batrachotoxin,BTX)、木藜芦毒素(grayanotoxin ,GTX)和乌头碱(aconitine)等作用于位点2,可持续激活钠通道;北非蝎α-毒素(North African scorpion α-toxin),海洋海葵毒素(Sea-anemone toxins, ATX)它们分别从北非蝎和海葵中分离和提炼出来的碱性水溶性多肽毒素,作用于位点3,其受体部位在通道外侧,使钠通道缓慢失活,并增强其持续激活。
表2-4-1列出了电压门控性钠通道(VGSC)的毒素结合位点及生理效应。
钠通道蛋白的提纯,就是利用它与毒素选择性的结合而进行的。
首先用非离子的清洁剂(detergent) 使可兴奋膜上的钠通道蛋白溶解,然后再通过选择性毒素与该蛋白结合。
最后再用常规生化方法进行纯化。
许多毒素对钠通道有选择性结合作用,主要工作是在神经细胞上发现的。
虽然在骨骼肌细胞与心肌细胞膜上均有钠通道,而且其分子结构与神经细胞上的钠通道相似,但它们对毒素的亲和力并不相同。
例如,心肌细胞钠通道对TTX的亲和力比脑及骨骼肌细胞弱100-1000 倍。
表2-4-1 电压门控性钠通道(VGSC)的毒素结合位点结合位点神经毒素生理效应1 河豚毒素(Tetrodotoxin ,TTX)离子通道阻滞→抑制离子转运蛤蚌毒素(Saxitoxin,STX)μ-芋螺毒素(μ-Conotoxins,μ-CTX)2 藜芦定(Veratridine)持续激活蟾毒素(Batrachotoxin ,BTX)乌头碱(Aconitine)木藜芦毒素(Grayanotoxin,GTX)3 北非蝎α-毒素(North African scorpion α-toxin)缓慢失活; 增强持续激活海洋海葵毒素(Sea-anemone toxins, ATX)δ-Atracotoxins4 北非蝎β-毒素(American scorpion β-toxin) 短暂反复激活;电压依赖性激活移向更负的电位5 短裸甲藻毒素(Brevetoxins , PbTx)西加鱼毒素(Ciguatoxins , CTX) 反复激活;持久活化→电压依赖性激活移向更负的电位6 合成除虫菊酯(Pyrethroids)DDT反复激活和/或阻滞; 激活、失活和去活变慢未经确定的位点DPI 201-106局麻药(Local anaesthetics)延长动作电位离子通道阻滞作用于钠通道的具有药理作用的药物主要为钠通道阻滞药,包括作用于中枢的局部麻醉药、全麻药、抗癫痫药、抗惊厥药及作用于心脏的I类抗心律失常药。

第四章钠通道激动剂、阻滞剂第一节概述钠通道的一个重要特性就是具有特异的激动剂和阻滞剂。
这些激动剂和阻滞剂主要是神经毒素和作用于中枢及心脏钠通道的药物。
钠通道是许多特异性天然动植物神经毒素作用的靶器。
这些毒素可调节钠通道的各种功能活性,包括通道的电导、激活和失活等,进而影响电信号产生与传导过程,使动物麻痹,甚至死亡。
电压门控型钠通道上至少存在7个不同的神经毒素结合靶位点(见图2-6-1)。
河豚毒素(tetrodotoxin,TTX)、蛤蚌毒素(saxitoxin,STX)和芋螺毒素(conotoxin,CTX)作用于位点1,阻断通道外口,但不改变通道动力学和门控性质;蟾毒素(batrachotoxin,BTX)、木藜芦毒素(grayanotoxin ,GTX)和乌头碱(aconitine)等作用于位点2,可持续激活钠通道;北非蝎α-毒素(North African scorpion α-toxin),海洋海葵毒素(Sea-anemone toxins, ATX)它们分别从北非蝎和海葵中分离和提炼出来的碱性水溶性多肽毒素,作用于位点3,其受体部位在通道外侧,使钠通道缓慢失活,并增强其持续激活。
表2-4-1列出了电压门控性钠通道(VGSC)的毒素结合位点及生理效应。
钠通道蛋白的提纯,就是利用它与毒素选择性的结合而进行的。
首先用非离子的清洁剂(detergent) 使可兴奋膜上的钠通道蛋白溶解,然后再通过选择性毒素与该蛋白结合。
最后再用常规生化方法进行纯化。
许多毒素对钠通道有选择性结合作用,主要工作是在神经细胞上发现的。
虽然在骨骼肌细胞与心肌细胞膜上均有钠通道,而且其分子结构与神经细胞上的钠通道相似,但它们对毒素的亲和力并不相同。
例如,心肌细胞钠通道对TTX的亲和力比脑及骨骼肌细胞弱100-1000 倍。
表2-4-1 电压门控性钠通道(VGSC)的毒素结合位点结合位点神经毒素生理效应1 河豚毒素(Tetrodotoxin ,TTX)离子通道阻滞→抑制离子转运蛤蚌毒素(Saxitoxin,STX)μ-芋螺毒素(μ-Conotoxins,μ-CTX)2 藜芦定(Veratridine)持续激活蟾毒素(Batrachotoxin ,BTX)乌头碱(Aconitine)木藜芦毒素(Grayanotoxin,GTX)3 北非蝎α-毒素(North African scorpion α-toxin)缓慢失活; 增强持续激活海洋海葵毒素(Sea-anemone toxins, ATX)δ-Atracotoxins4 北非蝎β-毒素(American scorpion β-toxin) 短暂反复激活;电压依赖性激活移向更负的电位5 短裸甲藻毒素(Brevetoxins , PbTx)西加鱼毒素(Ciguatoxins , CTX) 反复激活;持久活化→电压依赖性激活移向更负的电位6 合成除虫菊酯(Pyrethroids)DDT反复激活和/或阻滞; 激活、失活和去活变慢未经确定的位点DPI 201-106局麻药(Local anaesthetics)延长动作电位离子通道阻滞作用于钠通道的具有药理作用的药物主要为钠通道阻滞药,包括作用于中枢的局部麻醉药、全麻药、抗癫痫药、抗惊厥药及作用于心脏的I类抗心律失常药。

临床钠通道阻滞剂、β受体阻滞剂、钙通道阻滞剂等常用抗心律失常药物作用机制和临床应用Ⅰ类药物(钠通道阻滞剂)Ⅰ类药物抑制峰钠电流可降低心房、心室肌和心脏传导系统动作电位(AP)幅度和最大除极速率,增高兴奋阈值,减慢传导,抑制异位自律性和阻断折返激动。
0相除极幅度降低,继发钙内流减小,抑制心肌收缩力,可加重心功能不全。
Ⅰa类。
Ⅰa类药物阻滞钠通道开放,与钠通道解离时间中等,阻滞强度中等;可抑制快速激活的延迟整流钾电流,延长动作电位时程、有效不应期和QTc间期;对多种类型心律失常有效,因抑制传导、延长QTc间期及致心律失常作用,可增加病死率。
Ⅰb类。
Ⅰb类药物阻滞钠通道开放及失活,与钠通道解离时间短,对正常心肌的INa抑制作用弱,抑制晚钠电流作用相对明显,可缩短APD和ERP,消除折返;抑制INa作用在心肌缺血等病理情况下增强,对浦肯野纤维作用强于心室肌,可提升电复律疗效;对房室传导和心肌收缩力影响小;用于室性快速性心律失常,对房性心律失常无效。
大剂量Ⅰb类药物可抑制自律性,减慢室内及房室传导,抑制心肌收缩力。
Ⅰc类。
Ⅰc类药物阻滞钠通道失活,与钠通道解离时间长,抑制钠通道作用强;减慢心房和心室内传导,延长QRS及H⁃V间期,延长房室结双径路的快径逆传和房室旁道的ERP,阻滞心肌细胞肌浆网雷诺丁受体(RyR2)介导的钙释放,轻度抑制IKr和IKur;可治疗多种类型的房性和室性心律失常;抑制心肌收缩力作用强,可诱发或加重心功能不全,可能升高除颤/起搏的阈值。
莫雷西嗪抑制INa且缩短ERP,属于Ⅰb或Ⅰc类。
Ⅰd类。
选择性晚钠电流抑制剂,缩短APD和QT间期,降低复极离散度,增大复极储备和复极后不应期,治疗浓度不影响INa和室内传导。
代表药物雷诺嗪,用于治疗慢性心肌缺血,对LQTS3型和冠心病合并的心律失常有作用,可减少冠心病特别是非ST段抬高型心肌梗死合并的室早、短阵室速和房颤。
静脉制剂用于危重患者,可联合其他药物治疗顽固性电风暴。

钠离子通道调节剂
钠离子通道调节剂是一种药物,用于调节神经元细胞膜上的钠离子通道的活性。
这些药物可以增强或减弱钠离子通道的功能,从而影响神经元的兴奋性和传导速度。
钠离子通道调节剂被广泛应用于治疗多种疾病,包括癫痫、焦虑症、抑郁症、神经性疼痛和肌肉痉挛等。
这些药物一般被分为三类:钠通道阻滞剂、钠通道激动剂和钠通道调节剂。
钠通道阻滞剂包括利多卡因、普鲁卡因和利福卡因等,可以通过阻止钠离子通道的打开来减少神经元的兴奋性,从而阻止癫痫发作和减轻神经性疼痛。
钠通道激动剂包括氯丙嗪和咪唑仑等,可以通过增强钠离子通道的活性来增加神经元的兴奋性,从而减轻抑郁症和焦虑症等疾病的症状。
钠通道调节剂包括卡马西平和加巴喷丁等,可以通过调节钠离子通道的活性,来改善神经元的兴奋性和传导速度,从而治疗多种疾病。
需要注意的是,钠离子通道调节剂有一定的副作用,如头晕、恶心、嗜睡等。
因此,在使用这些药物时,应当严格按照医生的指示使用,并定期复查身体状况。
- 1 -。
心律失常钠通道阻滞剂的适应症和使用方法心律失常是指心脏搏动的频率、节律或传导异常,导致心脏无法有效地泵血。
钠通道阻滞剂是一类用于治疗心律失常的药物,通过阻断心肌细胞中的钠通道,延缓心肌动作电位的上升速度,减少心室肌细胞的自律性和窦房结传导速度,从而起到抑制心律失常的作用。
本文将介绍心律失常钠通道阻滞剂的常见适应症和使用方法。
一、适应症1. 心房纤颤/心房扑动:心房纤颤和心房扑动是最常见的心律失常类型之一。
心房纤颤是心脏房颤电位持续不规律的快速扑动,心房扑动是快速有规律的心房搏动。
心房纤颤和心房扑动会导致心率增快、心排血量降低,容易诱发血栓形成,增加卒中和心力衰竭的风险。
钠通道阻滞剂可以用于控制心房率,减少心房颤动发作的频率,改善心功能,预防并发症的发生。
2. 室上性心动过速:室上性心动过速是由室上性逸搏点或折返机制引起的心动过速。
钠通道阻滞剂可以通过抑制室上性逸搏点或改变折返路径来减慢心动过速的发作频率和控制心率。
3. 心室颤动:心室颤动是一种高度危险的心律失常,可导致心脏骤停和猝死。
在急诊情况下,静脉注射钠通道阻滞剂可以恢复正常的心律并挽救患者生命。
二、使用方法1. 药物种类和剂量选择:常用的心律失常钠通道阻滞剂包括普鲁卡因胺、利多卡因和奎尼丁等。
具体的药物选择和剂量应根据患者的病情和身体状况来确定,需在医生指导下使用。
2. 给药途径:心律失常钠通道阻滞剂可以通过口服、静脉注射或皮下注射等多种途径给药。
具体给药途径和方法需遵循医生的建议。
3. 注意事项:a. 药物过敏史:患者应告知医生有无对药物或相关成分过敏史,以免发生过敏反应。
b. 副作用监测:使用心律失常钠通道阻滞剂期间,患者应定期进行心电图检查及血药浓度监测,以评估药物疗效和副作用。
c. 妊娠和哺乳期:孕妇和哺乳期妇女在使用心律失常钠通道阻滞剂时需要特别谨慎,应咨询医生,并严格遵守医嘱。
结论心律失常钠通道阻滞剂是治疗心律失常的重要药物之一,常用于控制心房纤颤/心房扑动、室上性心动过速和心室颤动等疾病。
抗心律失常药钠通道阻滞剂一、钠通道阻滞剂作用原理图1,钠通道阻滞剂作用原理钠离子通道阻滞剂阻断钠离子内流,抑制心肌动作电位,减慢心传导。
二、钠通道阻滞剂分类1、I类:钠通道阻滞药1〕Ⅰa:适度阻滞钠通道,降低动作电位0相上升速率,不同程度抑制心肌细胞膜K、Ca2通透性,延长复极过程。
〔奎尼丁、普鲁卡因胺〕2〕Ⅰb:轻度阻滞钠通道,轻度降低动作电位0相上升速率,促进K外流,降低自律性,缩短或不影响动作电位时程。
〔苯妥英钠、利多卡因〕3〕Ⅰc:明显阻滞钠通道,显著降低动作电位0相上升速率和幅度,减慢传导性的作用最为明显。
〔普罗帕酮、氟卡尼〕2、II类:β肾上腺素受体阻断药阻断心脏β受体,抑制交感神经兴奋所致的起搏电流、钠电流和L-型钙电流增加,表现为减慢4相除极速率而降低自律性,降低动作电位0相上升速率而减慢传导性。
〔普萘洛尔〕3、III类:延长动作电位时程药抑制多种钾电流,延长A〕1〕药理作用:膜稳定作用〔↓Na,↑K〕I 仅作用于希-浦系统;↓自律性,↓APD、ERPII增加房室结0相除极速率,加快传导III加快强心苷中毒所致0期除极减慢,改善传导2〕临床应用主要用于室性心律失常,特别是强心苷中毒所致室性心律失常〔首选〕。
3〕不良反响静注过快可引起低血压、窦性心动过缓、孕妇禁用〔致畸〕。
3、普罗帕酮〔Propafenone,心律平〕1〕药理作用:具局麻作用I ↓浦氏纤维自律性;II ↓心房、心室、浦氏纤维传导速度;III 延长APD和ERP;IV 轻度肾上腺素受体阻断作用和钙通道阻滞2 体内过程: 首过效应明显,血浆蛋白结合率>90%3 临床应用: 室上性和室性早搏、心动过速;预激综合征伴发心动过速或心房纤颤。
4 不良反响:消化道反响;严重可致传导阻滞,心衰加重;由于其减慢传导程度超过延长ERP程度,抑制折返,引发心律失常。
临床医学基础知识:抗心律失常药物的分类及主要特点根据Vaughan Williams分类法,将抗心律失常的药物依据它们的电生理机制分成I-IV类:I类:钠通道阻滞药,能阻滞心肌细胞快钠通道,抑制Na+内流。
根据阻滞钠通道特性和程度的不同,以及对K+通道和APD影响的差异又将其分为IA、IB、IC三个亚类。
IA类:代表药有奎尼丁、普鲁卡因胺和丙吡胺等。
本类药阻滞开放态的钠通道,对钠通道的阻滞作用强度介于IB 和IC类之间,能适度阻滞心肌细胞膜钠通道,降低Vmax、减慢传导;另外,该类药不同程度地降低心肌细胞膜对K+、Ca2+的通透性,延长APD和ERP。
它们在心肌的作用部位广泛。
奎尼丁【特点】该药除了能够适度阻滞心肌细胞膜钠通道外,尚能抑制K+外流和Ca2+内流。
除对心肌的这些直接作用外,它还具有拮抗a受体及拮抗M胆碱受体的间接作用。
口服吸收效果好。
IB类:代表药有利多卡因、苯妥英钠和美西律等。
本类药在0相去极化时结合于开放状态的钠通道。
在钠通道阻滞药中,IB类与钠通道的亲和力最小,易解离,轻度阻滞心肌细胞膜钠通道。
能降低自律性,对传导的影响比较复杂。
此外,该类药促进K+外流,缩短APD,相对延长ERP。
主要作用于心室肌和希-浦氏纤维系统。
利多卡因为局部麻醉药,1963年用于治疗心律失常,是目前防治急性心肌梗死及各种心脏病并发快速室性心律失常的常用药物。
该药只能通过静脉途径给药,毒性发生率低。
是钠通道阻滞药中最具有临床价值的药物。
【特点】主要作用于希-浦氏纤维系统和心室肌细胞,对心房几乎无作用。
①降低自律性,该药在治疗浓度时能减慢4相去极速率,降低浦氏纤维自律性;但对正常窦房结的自律性无明显影响,仅在其功能异常时才有抑制作用;②改善传导性,治疗量的lidocaine对浦氏纤维的传导速度无明显影响,但在心肌缺血时可通过抑制0相Na+内流而明显减慢传导。
对低血钾或心肌组织牵张而部分去极化的浦氏纤维,则因促进3相K+外流而引起超极化,故可加速传导,有利于消除折返性心律失常。