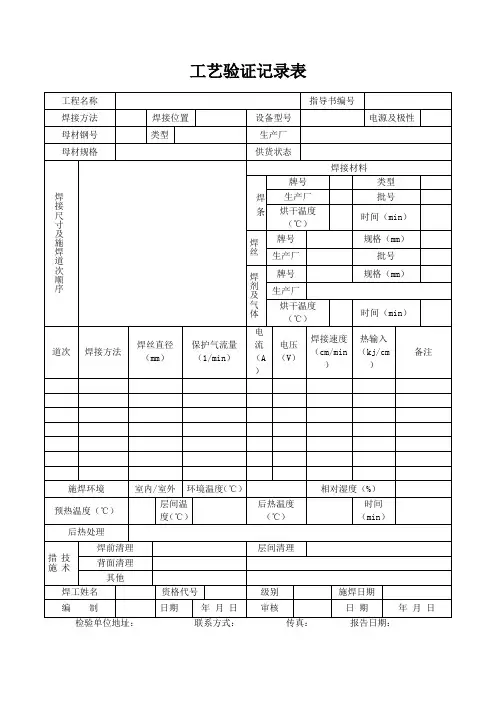
工艺验证记录表
- 格式:doc
- 大小:30.50 KB
- 文档页数:2

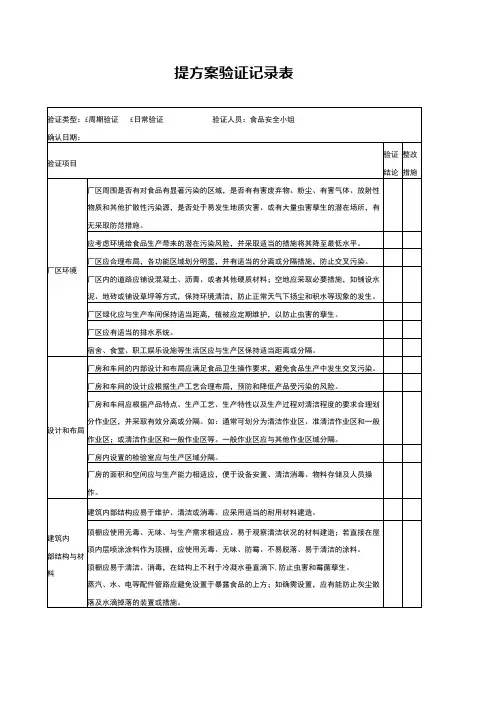
冲压工艺纪律检查记录表检查时间检查时间 : 检查人:检查人: 序号序号考核项目考核项目分值分值 被检查者被检查者 得分得分 备注备注1 产品图样、工艺文件不齐全完好,作业指导书未悬挂现场2 2操作者不熟悉技术标准,不知道自已所在岗位、工序作业指导书的技术要求、检验要求等内容技术要求、检验要求等内容 33原始记录原始记录: :51. 记录填写不符合规定要求记录填写不符合规定要求,,漏项漏项2. 记录数据不真实记录数据不真实3. 字迹不清楚正确字迹不清楚正确4. 记录保存不完好记录保存不完好5. 无模具使用记录无模具使用记录4 是否严格按照设备维护保养规定进行设备的保养维护工作并如实填写记录填写记录35 是否严格按照工艺规定的检验频次进行检验并记录3 6 模具安装前未按规定对模具上、下模板及工作台面进行清理;压件前及压件过程中未按规程对模具进行检查清理和润滑;前及压件过程中未按规程对模具进行检查清理和润滑;压件后模具压件后模具清理不彻底,润滑不良,末件丢失。
2 7 野蛮操作,不注意保护冲件及模具,造成冲压件变形、磕碰划伤、脏污,模具部件损伤脏污,模具部件损伤5 8 在模具使用过程中出现的模具损坏情况,生产线没有事故记录,不及时将损坏情况上报及时将损坏情况上报3 9 模具出现严重磨损、定位不准、工件误差,带病运转,不及时上报 3 10 工位器具未定置摆放,产品件摆放超出,地面有产品件等不良情况 2 11 板材、毛坯料、冲压件有锈蚀、磕碰、脏、划伤、坑包或其它缺陷未修复转下序未修复转下序3 12 不认真执行首件、末件检验,未按有关程序交检。
2 13 首件首件//末件放置是否合适并有标识末件放置是否合适并有标识2 14 检验员对首件质量判定不及时有错检/错判错判//误判的情况误判的情况3 15 每批生产工序结束后操作者是否主动交检验员检查产品件 3 16 巡检员对转序件进行确认合格后是否在《产品追溯记录卡》上加盖自己的检验章,自己的检验章,2 17 压件时双料叠压,二次冲压,模具内压入异物等情况发生 5 18 检验过程中的抽检比例,检验方法是否符合要求5 19 生产过程发现质量异常应是否立即处理,并填写《产品异常通知单》,追查原因,并矫正及作成记录防止再发。

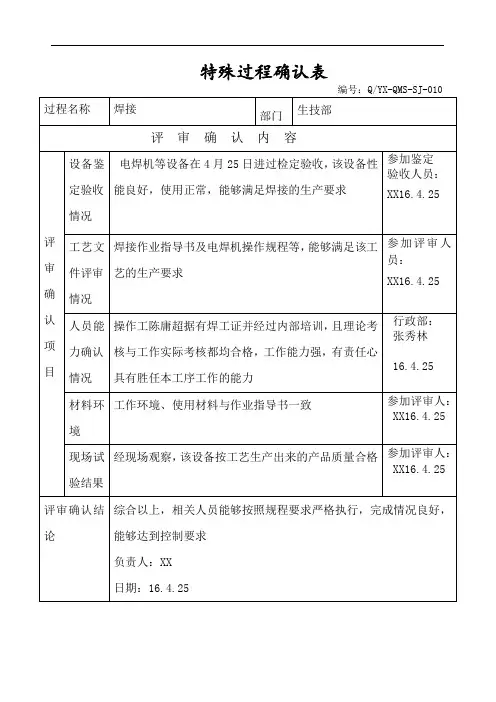

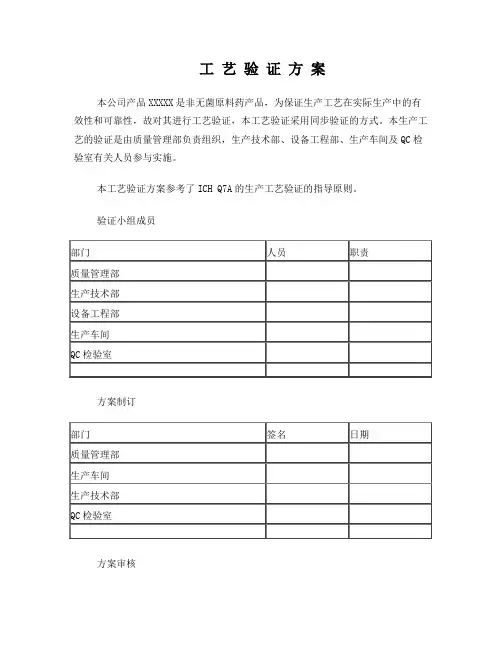
工艺验证方案本公司产品XXXXX是非无菌原料药产品,为保证生产工艺在实际生产中的有效性和可靠性,故对其进行工艺验证,本工艺验证采用同步验证的方式。
本生产工艺的验证是由质量管理部负责组织,生产技术部、设备工程部、生产车间及QC检验室有关人员参与实施。
本工艺验证方案参考了ICH Q7A的生产工艺验证的指导原则。
验证小组成员方案制订方案审核方案批准目录1. 基本情况 61.1. 概述 61.2. 生产工艺 61.2.1. 生产工艺流程图 61.2.2. 生产工艺的详细描述 61.2.3. 关键工艺步骤和参数 62. 验证目的 73. 验证前提 73.1. 工艺环境包括公用系统情况 73.2. 工艺设备情况 73.3. 所用原辅料和包装材料情况 73.4. 所用文件的准备情况 83.5. 人员情况 84. 验证方案 84.1. 验证计划 84.2. 第一步反应(生产XXXXX粗品)的验证(应包括所有重点考察的生产关键参数、结晶、离心、干燥) 84.2.1第一步反应(生产XXXXX粗品)关键工艺参数验证 84.2.2第一步反应收率情况验证 94.2.3第一步反应中间体的质量情况验证 94.3. 粗品精制工序的验证 104.3.1溶解脱色验证 104.3.2 结晶工序验证 104.3.3 分离工序验证 114.3.4 干燥工序验证 124.3.5小批成品收率情况验证 124.3.6小批成品的质量情况验证 134.4批混合工艺的验证 134.4.1批混合工序关键工艺参数验证 134.4.2批混合效果的验证 134.5最终成品的质量情况验证 145. 偏差处理 146.验证结果评定与结论: 151. 基本情况1.1. 概述本公司生产的XXXXX是非无菌原料药产品,为保证生产工艺在实际生产中的有效性和可靠性,采取同步验证的方式来验证XXXXX的整个生产工艺过程(说明是按变更管理规程而进行的验证)。
1.2. 生产工艺1.2.1. 生产工艺流程图应有洁净区的标识。


验证方案1概述XXXXX为公司一个主要生产品种,已对现行制备工艺进行了多次小试及中试,工艺稳定,各步中间体及成品质量符合规定。
为满足规模生产能力,制备小型玻璃器皿放大为反应罐,生产场地由实验室改为在公司二车间。
二车间的厂房设施、公用系统、关健设备均已进行了验证,空调净化系统、工艺用水系统已进行了验证,本次随生产工艺验证进行同步再验证。
所用原辅材料、内外包材均是由合格供应商提供的符合我公司质量标准的产品;公司的各级人员经过了相应规范意识和操作技能的培训。
已建立了系统化的生产质量管理文件体系并经过培训和试运行。
公司已具备工艺验证条件,准备进行工艺验证,证明在现有厂房设施、生产设备、机构人员和各项管理制度和规程整体运行下,工艺稳定可靠。
本产品生产工艺及使用的设备见《XXXXX生产工艺规程》。
验证批生产按现行生产质量程序正常进行。
2验证目的为评价XXXXX生产的工艺规程的可行性和重现性,根据GMP要求制定本验证方案,对其生产过程进行验证,以保证在正常生产条件下,生产出质量合格、均一、稳定产品。
3职责车间验证的组织实施;生技部经理负责工艺验证方案和报告的起草;工程部负责设备的正常运行、仪器仪表校验;QA 负责现场监控和取样;QC 负责按计划完成工艺验证方案中相关检验任务,确保检验结论正确可靠;质量部经理负责工艺验证方案及报告的审核;生产副总经理负责工艺验证方案及报告的批准。
4验证小组成员4验证工艺规程编码《XXXXX饮片生产工艺规程》STP-SC001-00 5验证批量猪胆膏原料150kgXXXXX成品约33kg6工艺流程图(见下页)911 .生产过程参数确认(记录见附表1)12 验证工序及内容粗品制备:主要工艺参数及设备参数皂化时间、温度:12小时/102~105℃皂化液冷却温度:至室温酸化PH值:调PH值至3记录填写:填写规范、准确及时、真实、完整,按规定修改验证项目(记录见附表2)●生产过程和关键参数确认验证方法:在生产过程中由QA全过程跟踪监控,按验证记录要求,独立观察记录关键过程参数,工序操作结束后与工艺规程、批记录核对。
工艺验证报告工艺验证报告项目代号:实施单位:编制:审核:批准:___年月工艺验证报告No.共页第1页一、工艺验证时间工艺验证完成时间:年月日至年月日二、工艺验证类别首台份(OTS样车)□___线□小批(PP节拍认证\FEU)□SOP批量提升□现产品改进□零部件三、验证地点冲压□焊装□涂装□总装四、验证依据产品设计技术标准,工艺设计指标、工艺方案、工艺路线、流程、生产纲领、工艺文件。
五、验证人员及资质验证组组长:验证组成员:姓名单位职务/职称姓名单位职务/职称六、验证情况一)工艺路线、流程验证该项目工艺路线、流程经过试制验证基本符合工艺设计要求,但需要进行流程修订,包括冲压、焊装、涂装和总装。
详见[工艺流程修订表]。
二)工艺装备验证1、冲压模具本项目共有模具套数,其中大型模具套和小冲模具套。
在本次验证中,共验证了套模具,其中存在问题项,包括严重不合格项、一般不合格项、可接受项和需整改再验收项。
详见[模具验证记录表]。
2、工装本项目共有工装套数,在本次验证中,共验证了套工装,其中存在问题项,包括严重不合格项、一般不合格项、可接受项和需整改再验收项。
详见[工装验证记录表]。
3、设备冲压设备与模具匹配满足生产要求。
冲压设备部分与模具不匹配,不能满足生产需求,详见[冲压设备验证记录表]。
焊装设备型号、数量满足生产需求。
焊装设备型号、数量不满足生产需求,详见[焊装设备验证记录表]。
涂装设备满足生产需求。
涂装设备不满足生产需求,详见[涂装设备验证记录表]。
总装设备满足生产需求。
总装设备不满足生产需求,详见[总装设备验证记录表]。
4、工位器具冲压共需种,本次验证种,合格满足使用要求的种,需进行改进的种,详见[冲压工位器具验证记录表]。
焊装共需种,本次验证种,合格满足使用要求的种,需进行改进的种,详见[焊装工位器具验证记录表]。
涂装共需种,本次验证种,合格满足使用要求的种,需进行改进的种,详见[涂装工位器具验证记录表]。
86(300mg)工艺验证方案86 (300mg) PROCESS VALIDATIONPROTOCOL86(300mg)86 (300mg )工艺验证方案共35 页第1 页PROCESS VALIDATIONPROTOCOL修订记录History 文件编号File code版本Version页数PageV-0382(P)V 01共35页***公司86(300mg )工艺验证方案86 (300mg) PROCESS VALIDATIONPROTOCOL作者签名 Signature of th authoro共 35 页第 2 页您的签名表明这份文件的准备(编制/修订)符合企业验证主计划、工艺验证主计划、GMP 规范和企 业生产的要求,并且充分反映了工艺验证全过程中应完成的必要任务,可以付诸对86 工艺验证的实施。
The signature means the drafting/revising confirms to validation master plan, process validation master plan, GMP,and in-house specifications. It includes all the contents need to be validated that can be applied to the process validationof 86 tablets.审核签名 Checking signature您的签名表明您已经仔细审阅了本文件,确认它正确并已全面反映了验证任务,可以付诸对 86 工艺验证的实施。
The signature means the protocol is checked thoroughly and carefully. It includes all the contents need to bevalidated that can be applied to the process validation of 86 tablets.批准签名 Approv a Signaturer您的签名表明这份文件符合企业验证主计划、工艺验证主计划、企业生产检验标准以及现行的 GMP规范,并且在此包含的文件和信息是充分的,并可直接应用。