硅和二氧化硅 ppt课件1
- 格式:ppt
- 大小:2.31 MB
- 文档页数:19










第1节硅无机非金属材料第1课时单质硅与二氧化硅1.掌握Si、SiO2的性质。
重点2.认识Si和SiO2在生产中的应用。
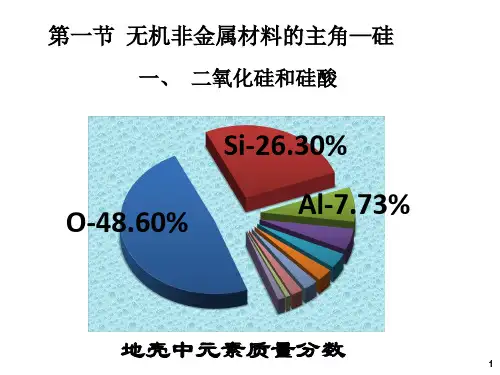
1.硅的分布与存在(1)分布:硅在自然界中分布广泛,在地壳中居第二位,仅次于氧,是构成矿物和岩石的基本元素。
(2)存在:自然界中没有游离态的硅,全部以化合态的形式存在。
2.半导体材料(1)特点:特指导电能力介于导体和绝缘体之间的一类材料。
(2)常见的半导体材料:最早使用的是锗(Ge),现在最广泛使用的是硅。
3.硅单质(1)物理性质①单质硅有晶体硅和无定形硅两种。
②晶体硅是灰黑色、有金属光泽、硬而脆的固体。
③导电性介于导体和绝缘体之间。
(2)化学性质(填写相应的化学方程式,下同)(3)制取与提纯粗硅:2C +SiO 2=====高温Si +2CO↑ Si +2Cl 2=====△SiCl 4SiCl 4+2H 2=====高温Si(纯)+4HCl(4)用途:半导体材料,太阳能电池,硅合金。
[探究·升华][认知升华]硅的特性(1)Si 的还原性大于C ,但C 却能在高温下还原出Si : SiO 2+2C=====高温Si +2CO↑。
(2)非金属单质跟碱液的作用一般无H 2放出,但Si 与碱液(如NaOH 溶液)反应放出H 2:Si +2NaOH +H 2O===Na 2SiO 3+2H 2↑。
(3)非金属单质一般不跟非氧化性酸作用,但Si 却能与HF 作用:Si +4HF===SiF 4↑+2H 2↑。
(4)非金属单质一般不导电,但Si 为半导体,有一定的导电能力。
[题组·冲关]1.下列关于碳和硅的叙述中,不正确的是( ) A .氧化物都能与碱溶液反应B .单质在加热时都能与氧气反应C .碳和硅两种元素都有能导电的单质D .常温下,碳和硅的单质化学性质都不活泼【解析】 碳的氧化物有CO 和CO 2,CO 不能与碱溶液反应。
【答案】 A2.在高温下,碳与硅可形成SiC 。