柔红霉素、盐酸多柔比星和盐酸表柔比星的HPLC分析
- 格式:pdf
- 大小:323.87 KB
- 文档页数:2

化疗患者静脉通路管理
化疗药物在静脉给药过程中意外渗漏的发生率为0.1%~6%。
外渗的后果有多种,可表现为轻度红斑、局部不适或疼痛、组织坏死、皮肤溃疡以及深部结构如肌腱和神经损伤。
根据化疗药物外渗后对组织的损伤程度,可以将化疗药物分为两类:
1.发疱性化疗药物外渗后可以引起局部组织坏死的药物。
如:盐酸多柔比星、盐酸表柔比星、吡柔比星、柔红霉素、放线菌素D、丝裂霉素、长春新碱、长春瑞宾、光辉霉素、氮芥、长春花碱、更生霉素等。
2.非发疱性化疗药物
(1)刺激性化疗药物:外渗后可以引起灼伤或轻度炎症而无坏死的药物。
如卡氮芥、卡铂、奥沙利铂、氮烯咪胺、依托泊苷、链脲霉素、伊立替康、托泊替康、博来霉素等。
(2)无明显刺激作用的药物:如环磷酰胺、异环磷酰胺、甲氨蝶呤、氟脲嘧啶、阿糖胞苷、顺珀、米托蒽醌、平阳霉素、门冬酰胺酶等。
还有一些药物如:紫杉醇、多西他赛、吉西他滨等药物。
虽然在各类文献报道中都没有对外周静脉刺激的报道,但在临床使用的过程中如多西他赛,紫杉醇有皮肤溃烂及坏死现象。
药物外渗后会给患者带来很大的痛苦,所以我们建议化疗要选择中心静脉置管,这样杜绝化疗药物外渗的现象。
在以上的药物中,发疱性的药物是必须做picc置管或中心静脉置管来做,刺激性药物建议用静脉留置针来输入,不主张用钢针输入化疗药物。
另外持续静脉。

脂质体多柔比星治疗淋巴瘤的疗效以及安全性分析【摘要】目的:探讨观察在治疗淋巴瘤患者的过程中,使用脂质体多柔比星进行治疗的临床疗效,为临床治疗提供依据。
方法:选取2019年10月~2021年2月间接受治疗的淋巴瘤患者共100例为研究对象,所有患者均使用脂质体多柔比星进行治疗,对患者的临床资料进行回顾性分析,统计分析患者的治疗有效率、不良反应发生率以及生存率。
结果:①对于治疗有效率,总治疗有效率为74.00%,其中完全缓解有57例,占比57.00%,不问缓解有17例,占比17.00%。
②在不良反应发生率方面,总不良反应发生率为57.00%,胃肠道不适发生率为40.00%,心电图异常发生率为50.00%,肝损害发生率为31.00%。
③在生存率方面,对选取的患者进行随访发现,一年、两年、三年生存率分别为85.00%(85/100)、75.00%(75/100)、55.00%(55/100)。
结论:对于患有淋巴瘤的患者,使用脂质体多柔比星进行治疗,会加大治疗的疗效,延缓病情的发展,提升患者的生存率,值得临床推广及应用。
【关键词】淋巴瘤;脂质体多柔比星;安全性分析淋巴瘤是起源于淋巴造血系统的恶性肿瘤,主要表现为无痛性淋巴结肿大,肝脾肿大,全身各组织器官均可受累,伴发热、盗汗、消瘦、瘙痒等全身症状,根据瘤细胞分为非霍奇金淋巴瘤(NHL)和霍奇金淋巴瘤(HL)两类【1】,这两类淋巴瘤对患者的免疫系统均会造成非常严重的影响,随着病情的不断恶化,肿瘤在向周边扩散转移,会对患者的生命安全造成及其严重的危害【2】。
因此很多医学科研工作者一直致力于淋巴瘤的研究中,希望可以通过合理的手段延缓患者病情的发展,提高患者的生存几率。
多柔比星能成功地诱导多种恶性肿瘤的缓解,包括急性白血病、淋巴瘤、软组织和骨肉瘤、儿童恶性肿瘤及成人实体瘤,尤其用于乳腺癌和肺癌。
此次研究对道中道(菏泽)制药有限公司的100名淋巴瘤患者进行研究治疗,分析观察在治疗过程中,使用脂质体多柔比星进行治疗的临床疗效,现将具体情况报道如下:1资料与方法1.1一般资料选取2019年10月~2021年2月间收治的接受治疗的淋巴瘤患者共100例为研究对象,所有患者均经过严格的检查和诊断,并符合相关诊断标准。

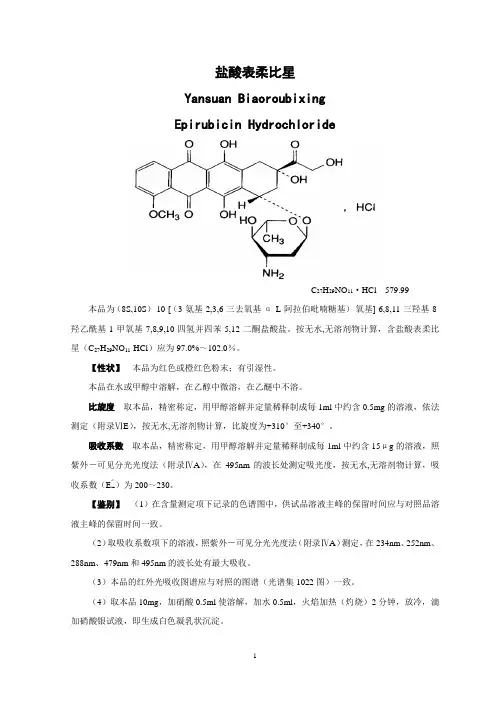
盐酸表柔比星Yansuan BiaoroubixingEpirubicin HydrochlorideC27H29NO11·HCl 579.99 本品为(8S,10S)-10-[(3-氨基-2,3,6-三去氧基-α-L-阿拉伯吡喃糖基)-氧基]-6,8,11-三羟基-8-羟乙酰基-1-甲氧基-7,8,9,10-四氢并四苯-5,12-二酮盐酸盐。
按无水,无溶剂物计算,含盐酸表柔比星(C27H29NO11·HCl)应为97.0%~102.0%。
【性状】本品为红色或橙红色粉末;有引湿性。
本品在水或甲醇中溶解,在乙醇中微溶,在乙醚中不溶。
比旋度取本品,精密称定,用甲醇溶解并定量稀释制成每1ml中约含0.5mg的溶液,依法测定(附录ⅥE),按无水,无溶剂物计算,比旋度为+310°至+340°。
吸收系数取本品,精密称定,用甲醇溶解并定量稀释制成每1ml中约含15μg的溶液,照紫外-可见分光光度法(附录ⅣA),在495nm的波长处测定吸光度,按无水,无溶剂物计算,吸收系数(E1%1cm)为200~230。
【鉴别】(1)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(2)取吸收系数项下的溶液,照紫外-可见分光光度法(附录ⅣA)测定,在234nm、252nm、288nm、479nm和495nm的波长处有最大吸收。
(3)本品的红外光吸收图谱应与对照的图谱(光谱集1022图)一致。
(4)取本品10mg,加硝酸0.5ml使溶解,加水0.5ml,火焰加热(灼烧)2分钟,放冷,滴加硝酸银试液,即生成白色凝乳状沉淀。
【检查】酸度取本品,加水制成每1ml中含5mg的溶液,依法测定(附录VI H),pH 值应为4.0~5.5。
溶液的澄清度取本品5份,各10mg,分别加水5ml溶解后,溶液应澄清;如显浑浊,与1号浊度标准液(附录ⅨB)比较,均不得更浓。


盐酸多柔比星脂质体注射液化疗后出现皮肤黏膜炎症及神经毒性的1例卵巢癌患者的中西医护理发表时间:2016-04-21T15:17:48.927Z 来源:《中西医结合护理》2015年11月第11期作者:江玲霞[导读] 浙江省中医院盐酸多柔比星脂质体注射液是盐酸多柔比星的脂质体制剂.浙江省中医院浙江杭州 310006[中图分类号] R246.7 [文献标识码] A [文章编号]1672-5018(2015)11-51-01盐酸多柔比星脂质体注射液是盐酸多柔比星的脂质体制剂,该剂型克服了游离的阿霉素药物心脏毒性大的缺陷,脱发、呕吐等毒性反应明显减少,常用于乳腺癌、卵巢癌和多发性骨髓瘤等恶性肿瘤一线化疗药。
其最常见的不良反应为骨髓抑制(药物说明书上指出发生率50%),其他少见的不良反应(发生率<5%)有手掌-足底红斑性感觉迟钝、恶心呕吐、口腔溃疡等。
我科2014年收治1例盐酸多柔比星脂质体注射液化疗后出现皮肤黏膜炎症及神经毒性症状的卵巢癌患者,经积极治疗和中西医对症护理,患者最终痊愈出院,现将护理体会报道如下:1 病例资料患者,女性,63岁,前期肿瘤诊疗于浙江省肿瘤医院进行,2013年5月因腹胀行CT检查和腹水穿刺诊断为卵巢癌。
从2013年6月6日开始于艾素+顺铂方案化疗1次,艾素+卡铂方案化疗4次。
2013年11月5日于浙江省肿瘤医院行全麻下经腹子宫全切+双附件切除+选择性盆腔淋巴结切除+大网膜切除+肠粘连松解术,术后病理示:左卵巢中分化子宫内膜样腺癌伴坏死。
术后予艾素+卡铂方案化疗4次。
化疗后出现肝损,黄疸,CT检查示:肝脾占位性病变,考虑转移性肿瘤可能,肝脏病灶较前增大。
2014年9月17日,2014年10月10日予盐酸多柔比星脂质体注射液化疗,21天后出现“Ⅲ度口腔溃疡,四肢指端麻木伴有轻度运动障碍属Ⅲ度神经毒性,手指指腹、脚趾指腹、四肢指缝、腋下、大腿内侧多发水泡”,于2014年10月31日入住我院治疗。


盐酸多柔比星脂质体注射液仿制药1研究技术指导原则2(征求意见稿)34一、概述5盐酸多柔比星脂质体注射液是采用硫酸铵梯度法将盐6酸多柔比星包裹于PEG化脂质体内形成的特殊注射剂。
7本指导原则结合盐酸多柔比星脂质体注射液的制剂特8点,提出仿制药开发过程中药学研究、非临床研究和生物等9效性研究的技术要求,旨在为该仿制药的研发提供技术指导。
10本指导原则仅代表药品监管部门目前对于本品的观点11和认识。
在符合现行法规的要求下,可采用替代的研究方法,12建议提供详细的研究资料或与监管机构进行沟通。
13二、整体研究思路14作为仿制药,应当按照国家局发布的《化学仿制药参比15制剂遴选与确定程序》选择参比制剂。
16盐酸多柔比星脂质体注射液为经静脉注射给药的脂质17体制剂,应基于产品特征,采取逐步递进的对比研究策略,18首先进行仿制药与参比制剂药学和非临床的全面对比研究;19然后进行人体生物等效性研究;必要时进行临床研究。
若药20学研究和(或)非临床研究结果提示仿制药与参比制剂不一21致,建议优化后重新开展研究1。
22作为注射剂仿制药,除满足仿制药注册申报的要求外,23还应符合《化学药品注射剂仿制药质量和疗效一致性评价技24术要求》、《化学药品注射剂仿制药(特殊注射剂)质量和25疗效一致性评价技术要求》等。
26三、技术要求27(一)药学研究281、处方29仿制药的处方应与参比制剂一致,辅料种类和用量通常30应与参比制剂相同2。
31氢化大豆磷脂酰胆碱(HSPC)、胆固醇、甲氧基聚乙二32醇磷脂酰乙醇胺(MPEG-DSPE)是本品的关键成分,应按33相关要求进行登记和关联,或由制剂注册申请人一并提供研34究资料3。
仿制药应与参比制剂选择相同来源(天然的或合35成的)的脂质辅料,制定严格的内控标准,并提供研究资料36证明仿制药所采用的脂质辅料与参比制剂中的脂质辅料相37似(如,各组分比例)。
382、制备工艺39应采用硫酸铵梯度法制备,主要步骤包括:1)空白脂质40体的制备,2)硫酸铵梯度的形成,3)活性药物的装载。

盐酸多柔比星脂质体的制备及体外释放研究
王秋云;岳占国;潘颖彬
【期刊名称】《海峡药学》
【年(卷),期】2024(36)2
【摘要】目的制备盐酸多柔比星脂质体(DOX-Lip),并研究其体外释放行为。
方法采用硫酸铵梯度法制备DOX-Lip,通过单因素考察硫酸铵溶液pH、油水比、挤出次数、超滤次数、孵育温度和时间对DOX-Lip包封率的影响。
再以包封率为评价指标,采用正交试验进行处方工艺优化,并评价其体外释放行为。
结果经最优处方工艺制备的DOX-Lip为类圆球形,分布均匀。
平均粒径为85 nm~87
nm(PDI=0.052~0.078),Zeta电位为-15 mV~-16 mV,包封率为96%~97%。
体外释放与市售参比制剂相似,具有明显的缓释性。
结论采用最优处方工艺制备DOX-Lip稳定可行,具有明显的缓释特征,体外释放与参比制剂相似,为该产品的生物等效性评价提供研究基础。
【总页数】5页(P9-13)
【作者】王秋云;岳占国;潘颖彬
【作者单位】广州玻思韬控释药业有限公司
【正文语种】中文
【中图分类】R94
【相关文献】
1.盐酸多柔比星脂质体体外释放度测定
2.盐酸伊立替康、二氢杨梅素复方脂质体的制备及其体外释放研究
3.盐酸多柔比星磁性热敏脂质体的制备和理化性质研究
4.表柔比星-白藜芦醇复方脂质体的制备及体外抗肿瘤作用研究
5.盐酸多柔比星脂质体的制备及体外质量评价
因版权原因,仅展示原文概要,查看原文内容请购买。

同一色谱条件测定柔红霉素、盐酸多柔比星和盐酸表柔比星作者:刘思迪来源:《中国科技博览》2014年第10期[摘要]目的:建立柔红霉素、盐酸多柔比星和盐酸表柔比星的高效液相色谱分析方法。
方法:色谱柱为Agilent HC-C18(250mm×4.6mm ,5m);柱温为30℃;流速为1.0mL·min-1;流动相为十二烷基硫酸钠溶液-乙腈-甲醇(500∶500∶60,用磷酸调pH2.2);检测波长为254nm。
结果:柔红霉素保留时间19.7min,盐酸多柔比星保留时间10.9min,盐酸表柔比星保留时间12.4min;三种化合物进样量在0.12g范围内与峰面积积分值呈良好线性关系;平均回收率为98.4%~99.0%,RSD为0.45%(n=5);结论:本方法灵敏度高、准确,可以对盐酸多柔比星类化合物进行定性定量分析。
[关键词] 柔红霉素;盐酸多柔比星;盐酸表柔比星比较中图分类号:TH365 文献标识码:A 文章编号:1009-914X(2014)10-0391-01柔红霉素和盐酸多柔比星为蒽环类抗生素,盐酸多柔比星是柔红霉素的C-14位的羟化产物,盐酸多柔比星氨基糖部分4’位异构化的活性相当、但毒性减少的盐酸表柔比星,是联合国世界卫生组织推荐的治疗肿瘤化疗的基本药物,在国际和国内市场同类药物中占有较大的份额。
目前盐酸多柔比星类化合物主要是通过化学半合成法,问题是化学合成目标产物时可能含有其他的组份,质量控制需要各组份精确分析,因此定性和定量分析就很重要。
2005版药典中有介绍盐酸多柔比星类化合物的分析方法,但没有柔红霉素、盐酸多柔比星和盐酸表柔比星三种化合物的分析方法,故参照有关文献,以高效液相色谱法建立盐酸多柔比星类化合物的分析方法。
1 材料1100型高效液相色谱仪包括包括G2170AA型PC化学工作站、G1311A型四元梯度泵、G1314A型可变紫外检测器(美国Agilent公司);ALC-1100.4精密天平(Sarforius公司);KQ250DB型数控超声波清洗器(昆山超声仪器厂)。

柔红霉素盐酸多柔比星和盐酸表柔比星的HPLC分析摘要本文通过高效液相色谱(HPLC)的方法对柔红霉素、盐酸多柔比星和盐酸表柔比星进行分析。
实验使用的是InertSustain C18柱,采用乙腈和50mM磷酸缓冲液的梯度洗脱,检测波长为210nm。
实验结果表明,在最佳条件下,柔红霉素、盐酸多柔比星和盐酸表柔比星的峰面积与浓度呈良好的线性关系,其线性范围分别为5-100μg/mL、2-100μg/mL和2.5-100μg/mL,相关系数均大于0.999。
背景柔红霉素、盐酸多柔比星和盐酸表柔比星都属于广谱抗生素,具有广泛的临床应用价值。
为了保证其质量和安全性,需要对其进行质量控制。
HPLC是一种高效、准确、可靠的分析方法,已被广泛应用于药物质量控制的实验室研究中。
本文通过HPLC的方法对柔红霉素、盐酸多柔比星和盐酸表柔比星进行分析,以期为药品生产和质量检验提供技术支持。
实验方法实验药品柔红霉素、盐酸多柔比星和盐酸表柔比星均为化学纯品,购自Sigma-Aldrich。
仪器设备HPLC仪器型号为Waters e2695,检测器型号为Waters 2998 PDA;色谱柱为InertSustain C18(4.6mm×250mm,5μm)。
实验条件流速:1.0mL/min;检测波长:210nm;进样量:10μL;流动相A:乙腈;流动相B:50mM磷酸缓冲液;洗脱方案:0-5min,95% A;5-12min,95%-60% A;12-17min,60% A;17-19min,60%-95% A;20-25min,95% A。
样品制备将柔红霉素、盐酸多柔比星和盐酸表柔比星分别加入50mL容量瓶中,加入5mL甲醇溶解,使用紫外分光光度计分别测定其波长最大处的吸收峰值(λmax)以确定检测波长。
将各样品中的药物加标准液分别制成浓度为1mg/mL的药物标准溶液。
然后将标准溶液进行适当稀释,得到3个不同浓度的药物标准曲线溶液。
高效液相法测定注射用盐酸表柔比星的含量盐酸表柔比星为阿霉素的主体异构体,是阿霉素氨基糖部分中 C4羟基的反式构型,它既可直接嵌入 DNA,与 DNA的双螺旋结构形成复合物,阻断依赖于 DNA的 RNA形成,又有形成超氧基自由基的动能本品为半合成的第二代蒽环类抗癌抗生素。
主要药理作用为直接嵌入DNA,与其双螺旋结构形成复合物,从而阻断RNA合成,它还可形成超氧基自由基团,因此本药既可作用于细胞核,又可影响瘤细胞的细胞膜和其运转系统,属细胞周期非特异性药物。
我们采用高效液相色谱法测定唑来膦酸制剂含量,建立本品含量测定方法[1-4]。
1.仪器与试药Agilent 1200 Series高效液相色谱仪(DAD检测器),色谱柱Waters C18? 5μm?4.6×150mm表柔比星对照品(含量:99.8%),盐酸多柔比兴对照品,来源均为中检院,注射用盐酸表柔比星由哈药集团生物工程公司提供,其它试剂均为色谱纯,乳糖及羟苯甲酯为处方中辅料,均为药用级辅料。
2.方法与结果色谱条件与系统适用性试验??用十八烷基硅烷键合硅胶为填充剂,以甲醇:水:乙腈(35:45:20)为流动相,流速为2.0ml/min,检测波长为254nm。
理论塔板数以表柔比星计不低于8000。
测定法??取本品,精密称定,用流动相溶解并制成每1ml 含0.5mg的溶液,精密量取20μl注入液相色谱仪,记录色谱图,另精密称取对照品,同法测定。
按外标法以峰面积计算,即得。
2.1 系统适用性取盐酸表柔比星及盐酸多柔比星对照品,加流动相溶解制成0.5mg/ml的溶液,按照测定法进样,考察分离度,结果盐酸表柔比星与多柔比星分离度为4.5,符合规定,峰纯度监测结果表明峰纯度符合规定,说明表柔比星与其它杂质峰亦可有效分离。
2.2 专属性试验取表柔比星、空白辅料(乳糖、羟苯甲酯),分别加流动相溶解,按照拟定方法进样测定,结果盐酸表柔比星与其它物质可有效分离,盐酸表柔比星峰纯度符合规定,表明辅料不干扰含量测定。
盐酸多柔比星脂质体英文名称:Doxorubicin Hydrochloride Liposome Injection【成份】活性成份为盐酸多柔比星,是从一种波塞链霉菌表灰变种培养液中提取得到的蒽环类细胞毒性抗生素。
【性状】●一种脂质体制剂,系将盐酸多柔比星包封于聚乙二醇化(PEG化)的,表面结合有甲氧基聚乙二醇(MPEG)的脂质体中,可以保护脂质体免受单核巨噬细胞系统(MPS)识别,从而延长其在血液循环中的时间。
●为无菌、半透明红色混悬液,每瓶10ml,含盐酸多柔比星2mg/ml,是用于单剂量静脉滴注的浓缩液。
【适应症】可用于低CD4(<200CD4淋巴细胞/mm3)及有广泛皮肤粘膜内脏疾病的与艾滋病相关的卡波氏肉瘤(AIDS-KS)病人。
可用作全身化疗药物,或者用作治疗病情有进展的AIDS-KS病人的二线化疗药物,也可用于不能耐受下列两种以上药物联合化疗的病人:长春新碱、博莱霉素和多柔比星(或其他蒽环类抗生素)。
脂质体多柔比星在国外还被批准用于乳腺癌、卵巢癌和多发性骨髓瘤等恶性肿瘤。
【用法用量】应为每2-3周静脉内给药20mg/m2,给药间隔不宜少于10天,因为不能排除药物蓄积和毒性增强的可能。
病人应持续治疗2-3个月以产生疗效。
为保持一定的疗效,在需要时继续给药。
用250毫升5%葡萄糖注射液稀释,静脉滴注30分钟以上。
禁止大剂量注射或给用未经稀释的药液。
建议滴注管与5%葡萄糖滴注管相连接以进一步稀释并限度地减少血栓形成和外渗危险。
禁用于肌肉和皮下注射。
肝功能不全病人:对少数肝功能不全病人(胆红素值达4mg/dl)给予20mg/m2,血浆清除率和清除半衰期未见变化。
然而在取得进一步的经验之前,根据以往盐酸多柔比星的使用经验,对于肝功能不全的病人的给药量要减少。
建议当胆红素高于以下数值时考虑减少用量:血清胆红素1.2-3.0mg/dl,用常用量的;大于3mg/dl时用常用量的。
肾功能不全病人:由于多柔比星由肝脏代谢和经胆汁排泄,故使用时剂量不需作调整。
盐酸表柔比星混合杂质对照品的研究与制备闻宏亮;蒋孟虹;杨美成;秦峰;刘浩;胡昌勤【摘要】目的研究盐酸表柔比星的杂质谱并制备混合杂质对照品.方法通过对盐酸表柔比星杂质谱的研究,选择合适的目标杂质;采用控速降解条件结合添加工艺杂质,优化制备工艺,研制了混合杂质对照品;以质谱法和单体对照品对照法,鉴定了混合杂质对照品中各主要杂质.结果制备了含有6种主要杂质的盐酸表柔比星混合杂质对照品,可用于有机杂质峰的确认.结论在杂质谱研究基础上,研制混合杂质对照品,不仅可有效评价色谱体系对各杂质的分离效能,还可快速准确归属多个杂质色谱峰,为分析杂质来源、评价样品质量提供依据.【期刊名称】《中国抗生素杂志》【年(卷),期】2017(042)001【总页数】6页(P46-51)【关键词】盐酸表柔比星;杂质谱;混合杂质对照品;制备;质谱法【作者】闻宏亮;蒋孟虹;杨美成;秦峰;刘浩;胡昌勤【作者单位】上海市食品药品检验所,上海201203;上海市食品药品检验所,上海201203;上海市食品药品检验所,上海201203;上海市食品药品检验所,上海201203;上海市食品药品检验所,上海201203;中国食品药品检定研究院,北京100050【正文语种】中文【中图分类】R978.1药物中的杂质与药物的安全性、有效性密切相关,随着公众对药品安全的日益关注,对杂质的控制已成为药品质量控制的重要项目。
人用药品注册技术要求国际协调会(ICH)已经制定了与杂质控制相关的切实可行的指导原则[1],多个国家药典也在附录中设有专门的杂质检查通则[2-5]。
胡昌勤等[6]阐述了化学药品中杂质控制的现状与策略,指出杂质控制理念已由纯度控制、限度控制转变为杂质谱控制,即对药品中的每个杂质依据其特性分别控制。
但药品中的杂质来源复杂、种类繁多,制备单个杂质对照品耗时耗力,且有时无法获得,因此急需建立快速归属多个杂质峰的方法,以加强药品杂质控制。
盐酸表柔比星属于广谱抗肿瘤抗生素,收载于多个国家药典[2-5],由于其杂质分离纯化工艺复杂、制备成本高,无法长期获得大量杂质对照品,目前均采用相对保留时间法归属各特定杂质峰。
盐酸多柔比星脂质体注射液质量标准盐酸多柔比星脂质体注射液质量标准: 从简到繁的探索1. 引言:多柔比星脂质体注射液简介随着医疗技术的不断进步,脂质体药物逐渐受到重视。
盐酸多柔比星脂质体注射液作为一种新型靶向药物,被广泛应用于药物治疗领域。
本文将探讨盐酸多柔比星脂质体注射液的质量标准与大家分享。
2. 盐酸多柔比星脂质体注射液质量标准的定义在研究盐酸多柔比星时,为了保证药物的质量和疗效,必须制定一系列的质量标准。
这些标准包括药物的理化性质、药典规定的要求以及国际公认的药物质量标准。
3. 药物的理化性质盐酸多柔比星脂质体注射液的理化性质是评估其质量的重要指标之一。
药物的外观应该符合药典规定的要求,如无悬浮物、无变色、无固体等。
溶解度、浓度和pH值等理化性质也需要进行精确的测量和分析。
4. 药典规定的要求各国药典对盐酸多柔比星脂质体注射液的质量标准也有明确的规定。
国际药典要求该药物的含量应在指定范围内,符合药物的活性成分含量。
5. 国际公认的药物质量标准国际药物质量标准是全球医药品质量控制的重要参考。
对于盐酸多柔比星脂质体注射液,国际上也有着共识的标准。
这些标准包括成分分析、物理性质、纯度、稳定性及微生物控制等方面。
6. 盐酸多柔比星脂质体注射液质量标准的回顾与总结盐酸多柔比星脂质体注射液的质量标准需要以药物的理化性质为基础,符合药典规定的要求,并且遵循国际公认的药物质量标准。
通过严格的质量控制和监管体系,有效保证了盐酸多柔比星脂质体注射液的质量和疗效。
个人观点与理解作为一名撰写此文的写手,我对盐酸多柔比星脂质体注射液的质量标准有着深刻的理解。
我认为制定科学、严格的质量标准是保证药物质量的重要手段,有助于保证患者的用药安全和治疗疗效。
在制定质量标准时应注重风险评估和数据支持,确保标准的科学性与可操作性。
质量标准应与不同地区、医疗机构和监管要求相适应,避免药物质量在生产、运输和使用过程中产生差异。
结语通过对盐酸多柔比星脂质体注射液质量标准的探讨与总结,我们了解到质量标准是保证药物质量的重要手段。
盐酸多柔比星脂质体工艺
盐酸多柔比星是一种广泛应用的药品,它能帮助治疗抗炎、抗感
染等疾病。
脂质体作为一种有效的药物传递系统,口服给药可以提高
生物利用度,改善药效,因此盐酸多柔比星脂质体的研究与开发备受
关注。
下面,我们将会详细介绍如何制备盐酸多柔比星脂质体。
首先,需要制备盐酸多柔比星。
该药品的制备方法可参照国家药
典标准操作。
常规使用乙醇或者酸性溶液作为溶解剂,再加入类固醇
类脂质体成分即可制备得到盐酸多柔比星脂质体。
其次,需要制备脂质体成分。
可以使用基磷脂、胆固醇等成分,
根据实际需要添加一些美容成分、抗氧化剂等物质,为药品制备提供
更好的载体。
再者,需要将盐酸多柔比星和脂质体成分进行混合,制备盐酸多
柔比星脂质体。
具体方法如下:
1、将脂质体成分溶解于无水醇,如甲醇,乙醇等;
2、将盐酸多柔比星溶解在醇中,并加入到脂质体成分所溶解的
醇中;
3、循序渐进地加入合适的量水,并边搅拌边蒸发醇,最终制备
得到盐酸多柔比星脂质体。
需要注意的是:制备过程中,应遮光处理,避免光的照射;同时,温度应严格控制,避免高温和冷冻现象发生。
最后制备好的脂质体成
品应在阴凉处保存。
制备工艺不仅决定着产品质量,还与制备成本直
接相关,需要不断优化和改进,不断提高药品的品质和医疗应用效果。
总之,盐酸多柔比星脂质体的制备方法相对繁杂,需要严格遵循
操作流程和控制各项指标,才能制备出高质量的产品。
相信在后续的
研究和应用中,盐酸多柔比星脂质体仍然将有广泛的应用前景。