第十五章氧族元素
- 格式:pptx
- 大小:800.85 KB
- 文档页数:56

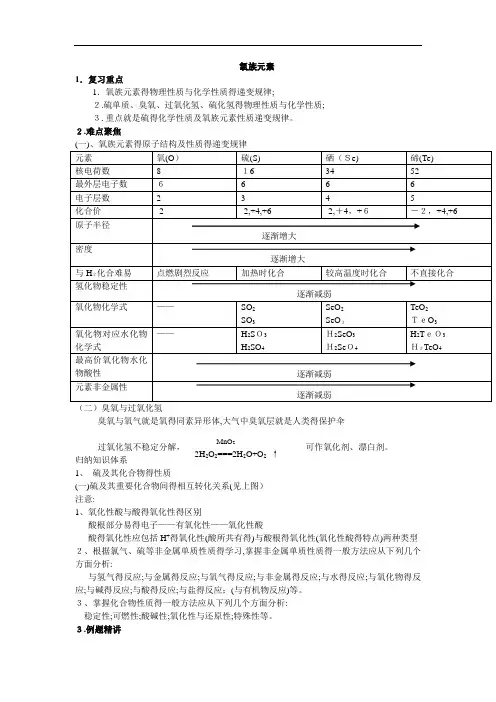
2H 2O 2===2H 2O+O 2 ↑ MnO 2 氧族元素1.复习重点1.氧族元素得物理性质与化学性质得递变规律;2.硫单质、臭氧、过氧化氢、硫化氢得物理性质与化学性质;3.重点就是硫得化学性质及氧族元素性质递变规律。
2.难点聚焦(二)臭氧与过氧化氢臭氧与氧气就是氧得同素异形体,大气中臭氧层就是人类得保护伞过氧化氢不稳定分解,可作氧化剂、漂白剂。
归纳知识体系1、 硫及其化合物得性质(一)硫及其重要化合物间得相互转化关系(见上图)注意:1、氧化性酸与酸得氧化性得区别酸根部分易得电子——有氧化性——氧化性酸酸得氧化性应包括H +得氧化性(酸所共有得)与酸根得氧化性(氧化性酸得特点)两种类型 2、根据氯气、硫等非金属单质性质得学习,掌握非金属单质性质得一般方法应从下列几个方面分析:与氢气得反应;与金属得反应;与氧气得反应;与非金属得反应;与水得反应;与氧化物得反应;与碱得反应;与酸得反应;与盐得反应;(与有机物反应)等。
3、掌握化合物性质得一般方法应从下列几个方面分析:稳定性;可燃性;酸碱性;氧化性与还原性;特殊性等。
3.例题精讲[例1]哪些实验事实说明氯元素得非金属性比硫元素强,并用原子结构知识加以解释。
解析:目前,已学习过多种非金属元素,通过卤族、氧族元素得学习可得出,比较两种非金属元素得非金属性相对强弱一般可根据以下几方面得实验事实:①非金属单质与H2化合得难易以及氢化物得稳定性大小;②最高价氧化物对应水化物得酸性强弱;③非金属单质间得置换反应。
答案:可以说明氯元素非金属性比硫元素强得主要实验事实有:①氯气与氢气反应时光照可发生爆炸,反应剧烈,硫单质加热变为蒸气才可与H2化合,且H2S不如HCl稳定;②H2SO 4得酸性不如HClO4强;③H2S与Cl2反应可生成硫单质;④铁与Cl2反应生成FeCl3,而硫与铁反应生成FeS。
S、Cl两原子电子层数相同,但Cl原子最外层电子数较多,且Cl原子半径比S原子小,最外层电子受原子核得引力较大,故氯元素非金属性应比硫元素强。
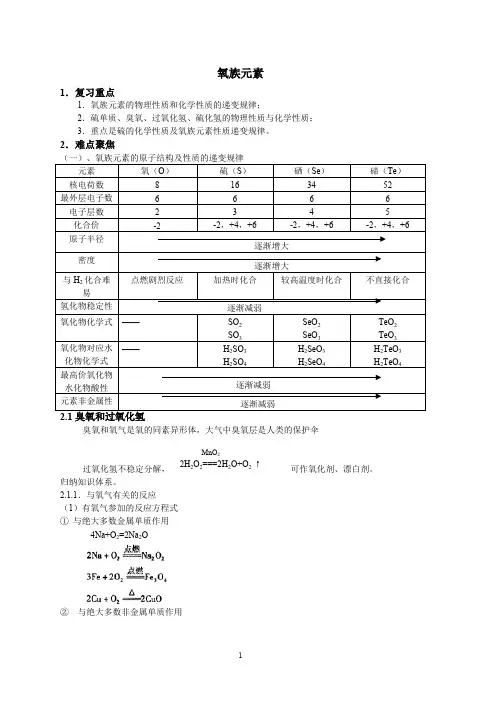
4Na+O2=2Na2O③与非还原性化合物作用2NO+O2=2NO24FeS2+11O22Fe2O2+8SO2④与有机物作用⑤在空气中易被氧化而变质的物质a.氢硫酸或可溶性硫化物:2H2S+O2=2S↓+2H2Ob.亚硫酸及其可溶性盐2H2SO3+O2=2H2SO4,2Na2SO3+O2=2Na2SO4c.亚铁盐、氢氧化亚铁4Fe(OH)2+O2+2H2O=4Fe(OH)3d.苯酚e.氢碘酸及其可溶性碘化物4HI+O2=2H2O+2I2⑥吸氧腐蚀(如:铁生锈)负极:2Fe—4e—=2Fe2+正极:O2+4e—+2H2O=4OH—Fe2++2OH—=Fe(OH)24Fe(OH)2+O2+2H2O=4Fe(OH)32Fe(OH)3=Fe2O3+3H2O(2)生成氧气的反应方程式)硫单质的反应 ①H2S H2+S↓②③H2S+X2=2HX+S↓(X2是指卤素单质,即Cl2,Br2,I2)④H2S+Pb(Ac)2=PbS↓+2HAc⑤H2S+CuSO4=CuS↓+H2SO4⑦FeS+2HCl=FeCl2+H2S↑(H2S的实验室制法)一、硫及其化合物的性质(一)硫及其重要化合物间的相互转化关系(见上图)注意:1、氧化性酸与酸的氧化性的区别酸根部分易得电子——有氧化性——氧化性酸酸的氧化性应包括H+的氧化性(酸所共有的)与酸根的氧化性(氧化性酸的特点)两种类型2、根据氯气、硫等非金属单质性质的学习,掌握非金属单质性质的一般方法应从下列几个方面分析:反应;与金属的反应;与氧气的反应;与非金属的反应;与水的反应;与氧化物的反应;与碱的反应;与酸的反应;与盐的反应;(与有机物反应)等。
3、掌握化合物性质的一般方法应从下列几个方面分析:稳定性;可燃性;酸碱性;氧化性和还原性;特殊性等。
2.5 二氧化硫的物理性质无色、有刺激性气味的有毒气体;密度比空气大;易溶于水(1∶40);(可用于进行喷泉实验,如SO2、HCl、NH3);易液化(-10℃)4、SO2的化学性质1)、酸性氧化物能和碱反应生成盐和水:SO2+2NaOH===Na2SO3+H2O与水反应生成相应的酸:SO2+H2O===H2SO3(二氧化硫的水溶液使紫色石蕊试液变红)二氧化硫溶于水形成的亚硫酸只能存在于溶液中,它很不稳定,容易分解成水和二氧化硫,故二氧化硫溶于水的反应是可逆反应。




一、氧族元素的性质1、相似性①单质与金属的反应(与大多数金属直接化合)②化合价为—2、+4、+6(氧一般无正价,除OF2中)。
③氧、硫、硒、碲的气态氢化物(碲不能直接与氢气化合),通式为H2R,它们的稳定性逐渐减弱,即热稳定性:H2O>H2S>H2Se>H2T e,其中后三者水溶液都是弱酸。
④硫、硒、碲都有两种氧化物RO2和RO3,对应水化物通式为H2RO3、H2RO4。
2、递变性同一主族元素从上至下,电子层数逐渐增多,原子半径逐渐增大,失电子能力依次增强,得电子能力依次减弱。
因此,氧族元素依氧、硫、硒、碲的顺序,非金属性逐渐减弱。
3、根据元素周期律的有关知识,比较氧族元素与同周期元素非金属性的强弱在同一周期中,从左至右,核电荷数依次增多,原子半径逐渐减小,失电子能力逐渐减弱,得电子能力逐渐增强。
以第三周期V A、ⅥA、ⅦA族磷、硫、氯元素为例,非金属性从磷到氯依次增强,可从以下性质证实:①与氢气化合难易:(P与H2的反应很难进行)②气态氢化物稳定性:HCl>H2S>PH3;③最高价氧化物对应水化物的酸性:HClO4>H2SO4>H3PO4④与变价金属反应时,氧化产物价态越高,则单质氧化性越强:P很难跟金属反应。
例1.下列关于氧族元素的叙述正确的是()A.氧族元素都能直接跟氢气化合,生成气态氢化物B.它们的含氧酸只有H2RO4形式C.氧族元素固体单质都不导电D.氧族元素中氧的非金属性最强解析:氧族元素中氧、硫是典型的非金属元素,硒、碲虽是非金属,但也具有金属的某些性质。
氧族元素单质与氢气化合能力逐渐减弱,氧气与氢气点燃下就直接化合,硫与氢气在加热条件下化合,硒与氢气的化合温度则更高些,碲与氢气一般不能直接化合。
氧族元素的单质中,氧气和硫不能导电,硒是半导体、而碲能够导电。
氧族元素的含氧酸有H2RO3和H2RO4形式两种。
答案:D二、单质硫1、物理性质淡黄色晶体,俗称硫磺,难溶于水、密度比水大,微溶于酒精,易溶于CS2,所以洗涤试管壁附着的硫单质,可用CS2将其溶解。



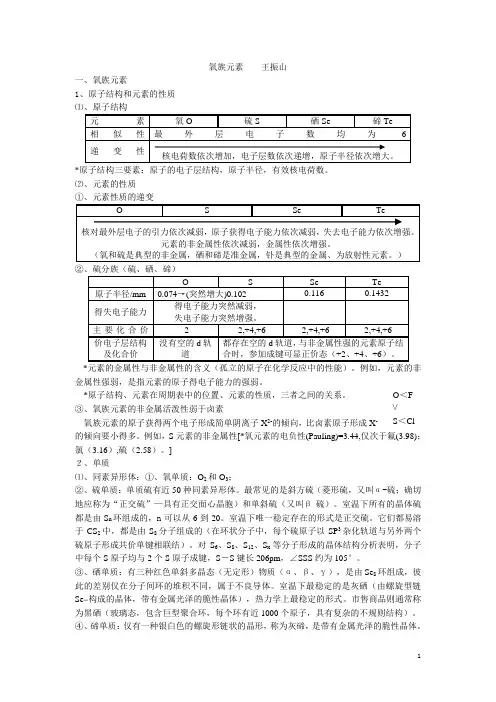
氧族元素 王振山一、氧族元素1、原子结构和元素的性质 ⑴、原子结构*原子结构三要素:原子的电子层结构,原子半径,有效核电荷数。
⑵、元素的性质 ①、元素性质的递变②、硫分族(硫、硒、碲)*元素的金属性与非金属性的含义(孤立的原子在化学反应中的性能)。
例如,元素的非金属性强弱,是指元素的原子得电子能力的强弱。
*原子结构、元素在周期表中的位置、元素的性质,三者之间的关系。
③、氧族元素的非金属活泼性弱于卤素氧族元素的原子获得两个电子形成简单阴离子X 2-的倾向,比卤素原子形成X -的倾向要小得多。
例如,S 元素的非金属性[*氧元素的电负性(Pauling)=3.44,仅次于氟(3.98);氯(3.16),硫(2.58)。
] 2、单质⑴、同素异形体:①、氧单质:O 2和O 3;②、硫单质:单质硫有近50种同素异形体。
最常见的是斜方硫(菱形硫,又叫α-硫;确切地应称为“正交硫”—具有正交面心晶胞)和单斜硫(又叫β-硫)。
室温下所有的晶体硫都是由S n 环组成的,n 可以从6到20。
室温下唯一稳定存在的形式是正交硫。
它们都易溶于CS 2中,都是由S 8分子组成的(在环状分子中,每个硫原子以SP 3杂化轨道与另外两个硫原子形成共价单键相联结)。
对S 6、S 8、S 12、S x 等分子形成的晶体结构分析表明,分子中每个S 原子均与2个S 原子成键,S -S 键长206pm ,∠SSS 约为105°。
③、硒单质:有三种红色单斜多晶态(无定形)物质(α、β、γ),是由Se 8环组成,彼此的差别仅在分子间环的堆积不同,属于不良导体。
室温下最稳定的是灰硒(由螺旋型链Se ∞构成的晶体,带有金属光泽的脆性晶体),热力学上最稳定的形式。
市售商品则通常称为黑硒(玻璃态,包含巨型聚合环,每个环有近1000个原子,具有复杂的不规则结构)。
④、碲单质:仅有一种银白色的螺旋形链状的晶形,称为灰碲,是带有金属光泽的脆性晶体。