高一化学必修2共价键
- 格式:ppt
- 大小:346.50 KB
- 文档页数:20

第2课时共价键三维目标1.知识与技能(1)知道共价键的概念;(2)了解极性键和非极性键的概念;(3)能用电子式表示共价化合物的形成过程。
2.过程与方法(1)通过对共价键形成过程的学习,培养学生抽象思维和综合概括的能力;(2)通过离子键和共价键的学习,培养学生对微观粒子运动的想象力。
3.情感态度与价值观(1)培养学生用对立统一规律认识问题;(2)通过对共价键形成过程的分析,培养学生怀疑、求实、创新的精神;(3)培养学生由个别到一般的研究问题的方法,使学生领会从宏观到微观,从现象到本质的认识事物的科学方法。
教学重点共价键和共价化合物的概念理解;化学反应的本质理解。
教学难点共用电子对的理解;极性键和非极性键的理解。
课前准备多媒体平台:共价键形成的动画。
教学过程知识回顾回顾氯化钠的形成,离子键的概念、实质、形成条件。
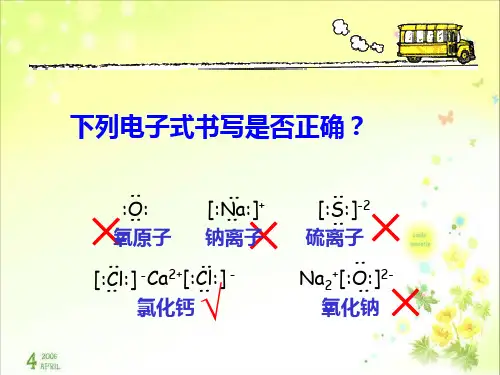
复习原子、离子、分子的电子式以及离子化合物的形成过程的书写。
写出下列物质的电子式:Mg3N2、PH3、K2O导入新课我们知道钠在氯气中燃烧生成氯化钠,由于钠原子容易失去1个电子形成阳离子,氯原子容易得到1个电子形成阴离子,然后钠离子和氯离子间通过静电作用形成了氯化钠这种离子化合物。
那我们在初中学习过的共价化合物HCl的形成和NaCl的形成一样吗?H2和Cl2在点燃或光照的情况下,H2和Cl2分子分别被破坏形成氢原子和氯原子,当氢原子和氯原子相遇时是通过什么样的方式结合在一起的呢?是通过阴阳离子间静电作用结合在一起的吗?推进新课[分析]两种非金属元素的原子化合时,原子间并不是一方失去电子形成阳离子,一方得到电子形成阴离子来形成相互作用力的,而是原子间共用最外层上的电子,形成共用电子对以使原子双方均达到稳定的电子层结构。
共用电子对同时受到两个原子核的吸引,从而将两个原子紧密地联系在一起,如同双面胶把两个小球黏在一起。
[投影]氯原子之间通过共价键形成氯气分子的动画。
[分析]我们以氯原子为例来探讨一下氯分子的形成。

第二章分子结构与性质第二节分子的空间结构2.3.1共价键的极性【教材分析】本节是在学习了共价键和分子的立体构型的基础上,进一步来认识分子的一些性质,包括共价键的极性和非极性,并由此引出一些共价分子的性质及其应用;范德华力、氢键及其对物质性质的影响,特别是物质的熔沸点及溶解性等;教学时要注意引导学生运用“物质结构决定物质性质,性质反映结构”的观念来理解和解释分子的性质。
【课程目标】教学重点:极性分子与非极性分子的判断教学难点:极性分子与非极性分子的判断【教学过程】【情境引入】微波炉的加热原理任务一:分子的极性【讲解】分子的极性(1)极性分子:分子的正电中心和负电中心不重合,使分子的某一部分呈正电性,另一部分呈负电性,这样的分子是极性分子。
如HCl、H2O等。
(2)非极性分子:分子的正电中心和负电中性重合,使分子没有带正电和带负电的两部分,这样的分子是非极性分子。
如P4、CO2等。
【设疑】为什么水分子内部正电中心和负电中心不重合?共用电子对在两原子周围出现的机会是否相同?即共用电子对是否偏移?【讲解】有些共用电子对的两个原子由于电负性不同,那么共用电子对在两原子周围出现的机会便不同,即共用电子对发生偏移。
有些共用电子对的两个原子由于电负性相同,那么共用电子对在两原子周围出现的机会相同,即共用电子对不发生偏移。
根据共用电子对是否偏移,可以将共价键分为极性键和非极性键。
任务二:键的极性【讲解】2.键的极性以HCl分子为例,HCl分子是由不同元素的原子构成的,Cl原子的电负性大于H原子,致使共用电子对发生偏移,那么会使H原子呈正电性、Cl原子呈负电性。
以Cl2分子为例,Cl2分子是由同种元素的原子构成的,每个Cl原子的电负性相同,致使共用电子对不发生偏移,使成键原子呈电中性。
【讲解】判断分子的极性可依据分子中的化学键的极性向量和。
从向量的角度认识分子的极性,若分子中共价键的极性的向量和等于0,则分子中没有带正电和带负电的两部分,为非极性分子,如BF3、CH4等。

第2课时共价键一、共价键1.形成过程(以Cl2形成为例)(1)用电子式表示Cl2的形成过程:________________________________________________________________________(2)HCl的形成过程与NaCl的形成过程比较:由图示可知二者的形成过程不一样。
由于形成HCl的过程是双方各供应一个e-形成____________为两个原子共用,从而使双方共同达到____________。
而形成NaCl的过程为Na失去一个电子形成Na+,Cl得到一个电子形成Cl-,这样形成____________。
之所以消灭这种现象,是由于H、Cl都缺少一个电子就可以达到稳定结构,所以二者形成____________,而Na与Cl为活泼金属与活泼非金属,金属______电子而非金属______电子,所以有电子的______。
2.概念原子间通过____________所形成的相互作用。
3.分类(1)极性共价键(简称极性键)由____________形成共价键,原子吸引电子的力量______,共用电子对将偏向________________的一方,所以________________的原子显负电性,________________的原子显正电性,像这样共用电子对______的共价键叫做极性共价键,简称极性键。
(2)非极性共价键(简称非极性键)由________形成共价键,两个原子吸引电子的力量______,共用电子对________任何一个原子,成键原子因此而______电性,这样的共价键叫做非极性共价键,简称非极性键。
4.离子键与共价键的区分键型离子键共价键概念使阴、阳离子结合成化合物的____作用叫做离子键原子之间通过共用______所形成的相互作用叫做共价键成键方式通过____电子达到稳定结构通过形成共用______达到稳定结构成键粒子成键元素活泼____元素与活泼______元素之间(特殊:NH4Cl、NH4NO3等铵盐只由非金属元素组成,但含有离子键)______元素之间(特殊:AlCl3等由金属和非金属组成,但含有共价键)5.共价化合物概念:以____________形成分子的化合物。

《共价键的极性》教学设计一、课标解读《共价键的极性》是选择性必修模块2物质结构与性质的主题2:微粒间的相互作用与物质的性质中的内容,课程标准(《普通高中化学课程标准(版修订)》)对这部分内容的要求具体如下:1.内容要求(1)知道共价键可分为极性和非极性共价键;(2)知道分子可以分为极性分子和非极性分子,知道分子极性与分子中键的极性、分子的空间结构密切相关。
2.学业要求(1)能利用电负性判断共价键的极性;(2)能根据分子结构特点和键的极性来判断分子的极性,并据此对分子的一些典型性质及其应用作出解释。
二、教材分析本节内容选自高中化学人教版选择性必修二《物质结构与性质》第2章“分子的结构与性质”第3节分子的性质第一课时。
本节是在学习了共价键和分子的立体构型的基础上,进一步来认识分子的极性,能从共用电子对是否发生偏移的角度认识键的极性的实质是成键原子分别带正电和负电。
掌握分子极性和分子中键的极性、分子的空间结构密切相关。
能从微观角度理解共价键的极性和分子极性的关系,培养学生微观辨识的科学素养,通过键的极性对物质性质的影响的探析,形成“结构决定性质"的认知模型。
鲁科版教材中内容的编排顺序与人教版中不同,在鲁科版中共价键的极性安排在第一节共价键的分类中,而分子的极性安排在第三节,两个内容的学习较为分散。
在鲁科版教材中安排了分子极性的实验:用带静电的橡胶棒分别靠近水流和四氯化碳,观察流向,给学生认识分子极性提供了感性认识,便于学生直观感知。
三、学情分析教学中要充分考虑学生已有的知识基础,已学习了共价键、电负性、酸的电离常数等知识,通过上一节的学习,学生也了解了常见分子的空间构型,这些都为本节课学习共价键的极性和分子的极性做好了知识铺垫。
能力方面,学生从微观角度理解并解释宏观性质的能力比较欠缺,需要进一步通过本节内容的学习进行强化。
四、素养目标【教学目标】1.知道共价键可分为极性共价键和非极性共价键;能利用电负性判断共价键的极性。


第二单元微粒之间的相互作用力第二课时:共价键【三维目标】知识与技能目标:使学生理解共价键的概念,初步掌握共价键的形成;学会用电子式表示共价键,学会用结构式表示共价键以及共价分子;学会判断离子化合物和共价化合物;初步了解用球棍模型、比例模型表示分子结构;了解有机化合物中碳的成键特点和成键方式。
过程与方法目标:通过对共价键形成过程的教学,培养学生抽象思维和综合概括能力;通过学生利用球棍模型拼有机分子,锻炼学生多角度思维的能力和创新能力。
情感态度与价值观目标:培养学生用对立统一规律认识问题;通过对共价键形成过程的分析,培养学生怀疑、求实、创新的精神;培养学生由个别到一般的研究问题的方法以及从现象到本质的认识事物的科学方法。
【教学重点】共价键的概念和形成;离子化合物和共价化合物的判断。
【教学难点】用电子式、结构式表示共价键以及共价分子。
【教学过程】【复习】离子键的概念、形成条件、电子式。
【过渡】下面再来学习化学键中的另一种类型——共价键。
【分析讲评】Cl2分子是由两个Cl原子结合而成的,那么两个Cl原子是如何结合到一起形成Cl2分子的呢?(电子式表示形成过程:Cl× + Cl×——→Cl Cl )(组成元素都是非金属,都想得到电子形成稳定结构,谁都不易失去电子;最终办法是相互妥协,各拿出一个电子来公用,形成共用电子对,从而都达到稳定的结构。
)(共用电子对为两个原子所共有)【板书】一共价键1定义:原子间通过共用电子对所形成的强烈的相互作用。
共价键可存在于单质、共价化合物、离子化合物中。
2共价化合物:仅含共价键的化合物。
3形成条件:①非金属元素之间:H2、O2、N2、HCl 、CO2、H2O 、NH3、CH4、电子式表示:H2、HCl 、H2O 、NH3、CH4、(讲评各原子如何满足稳定结构)注意:电子没有完全得失,所以没有形成离子,依然为原子;相同原子不能合并在一起;②非金属元素与不活泼的某些金属元素之间:AlCl3、BeCl2、(8e-不是唯一的稳定结构,在共价化合物中,有的原子最外层电子数少于8e-,而有的原子最外层电子比8e-多.)【练习】电子式的书写:O2、CO2、N2、CCl4、【引导认识】①两个原子间不仅可以形成1个电子对,还可形成2个或3个电子对。



第二章分子的结构与性质第一节共价键一、共价键1.共价键的概念和特征原子间通过共用电子对所形成的相互作用。
【注】所有共价键都有饱和性,并不是所有共价键都具有方向性,如两个s电子形成共价键时就没有方向性。
2.形成条件同种非金属元素或者不同种非金属元素原子之间,某些金属原子与非金属原子之间形成共价键。
如AlCl3、BeCl2、FeCl3等所含化学键为共价键。
3.共价键的类型(按成键原子的原子轨道重叠方式分类)(1)σ键π键的电子云形状与σ键的电子云形状有明显差别:每个π键的电共价单键为σ键;共价双键中有一个σ键,另一个是π键;共价三键由一个σ键和两个π键构成。
【总结】σ键与π键的比较轴对称镜面对称【注】①s轨道与s轨道形成σ键时,电子并不是只在两核间运动,只是电子在两核间出现的概率大。
②因s轨道是球形的,故s轨道与s轨道形成σ键时,无方向性。
两个s轨道只能形成σ键,不能形成π键。
③两个原子间可以只形成σ键,但不能只形成π键。
例1.有关CH2===CH—C≡N分子中所含化学键数目的说法正确的是() A.3个σ键,3个π键B.4个σ键,3个π键C.6个σ键,2个π键D.6个σ键,3个π键【答案】D[共价单键为σ键,双键中含1个σ键和1个π键,三键中含1个σ键和2个π键,故CH2===CH—C≡N分子中含6个σ键和3个π键。
]例2.关于σ键和π键的比较,下列说法不正确的是()A.σ键是轴对称的,π键是镜面对称的B.σ键是“头碰头”式重叠,π键是“肩并肩”式重叠C.σ键不能断裂,π键容易断裂D.氢原子只能形成σ键,氧原子可以形成σ键和π键【答案】C[σ键较稳定,不易断裂,而不是不能断裂。
]二、键参数——键能、键长与键角1.键能(1)键能是指气态分子中1 mol化学键解离成气态原子所吸收的能量。
键能的单位是kJ·mol-1。
键能通常是298.15_K、101_kPa条件下的标准值。
例如,H—H 的键能为436.0 kJ·mol—1。
第二章分子结构与性质第一节共价键课前回顾:1.化学键:(1)定义:是指相邻的原子之间强烈的相互作用。
(2)分类:化学键包括:共价键、离子键、金属键。
共价键包括:极性键和非极性键2.化学反应的本质是旧化学键的断裂和新化学键形成的过程。
断裂化学键需要吸收能量,形成化学键需要放出能量,导致化学反应过程中能量变化(吸热或放热)。
3.由离子键构成的化合物叫做离子化合物,离子化合物中一定含有离子键,可能含有共价键。
以共用电子对形成的化合物叫做共价化合物。
共价化合物中只含有共价键,但只含共价键的物质不一定是共价化合物,如O2、N2等单质中只含有共价键。
注:并不是所有的物质都含有化学键,例如:稀有气体一、共价键(一)定义:原子间通过共用电子对所形成的相互作用叫做共价键。
(二)本质:是在原子之间形成共用电子对。
共价键形成的原因是成键原子相互接近,原子轨道发生重叠,自旋方向相反的未成对电子形成共用电子对。
特征概念作用存在情况饱和性每个原子所能形成的共价键的总数或以单键连接的原子数目是一定的饱和性决定了分子的组成。
所有的共价键都具有饱和性方向性在形成共价键时,原子轨道重叠的越多,电子在核间出现的概率越大,所形成的共价键就越牢固,因此共价键将尽可能沿着电子出现概率最大的方向形成,所以共价键具有方向性方向性决定了分子的空间结构。
并不是所有共价键都具有方向性:通常电负性相同或差值较小的非金属元素原子之间形成共价键,大多数电负性之差小于1.7的金属与非金属原子之间形成共价键。
(五)表示方法1、用一条短线表示一对共用电子所形成的共价键,如H-H2、用“=”表示原子间共用两对电子所形成的共价键,如C=C3、用“≡”表示原子间共用三对电子所形成的共价键,如C≡Cσ键π键成键示意图(常见类型)原子轨道重叠方式“头碰头”重叠“肩并肩”重叠对称类型轴对称镜面对称原子轨道重叠程度大小键的强度轨道重叠程度大,键的强度较大,键越牢固轨道重叠程度较小,键比较容易断裂,不如σ键牢固活泼性不活泼活泼成键规律共价单键是σ键;共价双键中一个键是σ键,另一个键是π键;共价三键中一个键是σ键,另外两个键是π键旋转情况以形成σ键的两个原子核的连线为轴,任意一个原子可以绕轴旋转,并不破坏σ键的结构以形成π键的两个原子核的连线为轴,任意一个原子并不能单独旋转,若单独旋转则会破坏π键的结构存在情况能单独存在,可存在于任何含共价键的分子或离子中不能单独存在,必须与σ键共存,可存在于共价双键和共价三键中联系只有在形成σ键后,余下的p轨道才能形成π键实例CH4、OH-N≡N中既含有σ键,又含有π键2②并不是所有的分子都含有σ键二、键参数——键能、键长与键角(一)键能:1.概念:气态分子中1mol化学键解离成气态原子所吸收的能量称为键能。
《共价键》教学设计一、课标解读“共价键”是《普通高中化学课程标准(版修订)》中模块2物质结构与性质的主题2微粒间的相互作用与物质的性质中的内容。
1.内容要求认识原子间通过原子轨道重叠形成共价键,了解共价键具有饱和性。
知道根据原子轨道的重叠方式,共价键可分为σ键和π键等类型。
2.学业要求能说出共价键的主要类型、特征和区别。
能比较σ键和π键的联系和区别。
能说明H2、Cl2、HCl、乙烷、乙烯和乙炔等典型物质的成键类型。
二、教材分析本节内容的功能价值是提高学生的宏观辨识与微观探析能力,能从原子、分子水平分析常见物质及其反应的微观特征,能从宏观与微观结合的视角对物质及其变化进行分类和表征。
新旧人教版教材在本节内容上没有较大的改动。
新教材将旧教材中“我们学过电子云,如何将电子云的概念来进一步理解共价键呢?”改为“我们学过原子轨道,如何将原子轨道的概念来进一步理解共价键呢?”将“电子云”变更为“原子轨道”,使得化学用语更加规范。
新人教版教材注重前后知识衔接的逻辑关系,前面学习的内容,在后续内容中不断得到应用。
在第一章第一节《原子结构》中运用电子云轮廓图形象地描述了原子轨道,到本节中再介绍共价键时,可以直接采用原子轨道相互重叠而形成共价键的过程,简明扼要地阐明了共价键的本质和特征,体现了原子轨道与共价键知识的前后衔接。
三、学情分析构成物质的微粒之间存在着相互作用。
通过必修一化学键的学习,学生已经初步了解了什么是共价键,通过第一章第一节《原子结构》的学习,学生已经学会运用电子云轮廓图形象地描述了原子轨道,并掌握常见元素基态原子的核外电子排布式和轨道表示式。
在本节中再介绍共价键时,可以直接采用原子轨道相互重叠而形成共价键的过程,简明扼要地阐明了共价键的本质和特征体现了原子轨道与共价键知识的前后衔接。
本节课的学习也会对之后《分子的空间结构》的学习打下基础。
高二学生处于具体思维向抽象思维发展的中期,学生具有一定的抽象思维能力及空间想象能力,但仍需要借助一定的直观教学手段帮助学生理解三维空间想象能力。