泮托拉唑注射液说明书--海南卫康
- 格式:doc
- 大小:37.50 KB
- 文档页数:4
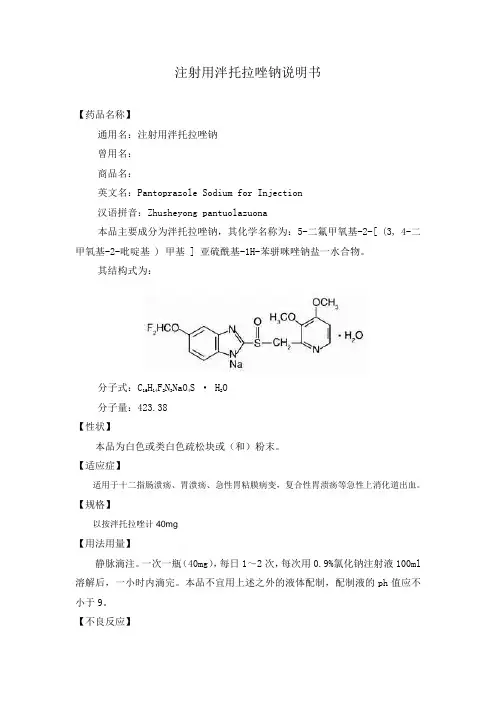
注射用泮托拉唑钠说明书【药品名称】通用名:注射用泮托拉唑钠曾用名:商品名:英文名:Pantoprazole Sodium for Injection汉语拼音:Zhusheyong pantuolazuona本品主要成分为泮托拉唑钠,其化学名称为:5-二氟甲氧基-2-[ (3, 4-二甲氧基-2-吡啶基 ) 甲基 ] 亚硫酰基-1H-苯骈咪唑钠盐一水合物。
其结构式为:分子式:C16H14F2N3NaO4S · H2O分子量:423.38【性状】本品为白色或类白色疏松块或(和)粉末。
【适应症】适用于十二指肠溃疡、胃溃疡、急性胃粘膜病变,复合性胃溃疡等急性上消化道出血。
【规格】以按泮托拉唑计40mg【用法用量】静脉滴注。
一次一瓶(40mg),每日1~2次,每次用0.9%氯化钠注射液100ml 溶解后,一小时内滴完。
本品不宜用上述之外的液体配制,配制液的ph值应不小于9。
【不良反应】偶见头晕、失眠、嗜睡、恶心、腹泻、便秘、皮疹和肌肉疼痛等症状,但程度较轻。
【禁忌】对本品过敏者或严重肝功能不全者禁用。
【注意事项】①应用本品时应首先排除癌症的可能,因为本品治疗可减轻胃癌症状,从而延误诊断。
②肝、肾功能不全者慎用,根据需要酌情较轻。
【孕妇及哺乳期妇女用药】本品禁用。
【儿童用药】未进行该项实验且我可靠参考文献。
【老年患者用药】老年患者应用泮托拉唑后药代动力学(清除率、半衰期、生物利用度)无明显变化,因此老年人不需要改变剂量。
【药物相互作用】1.在体内较高剂量的泮托拉唑不改变安定的清除率,其血清浓度不受安定的影响,表明安定不影响泮托拉唑的代谢。
2.泮托拉唑与氨茶碱、华法令、避孕药、苯妥英钠、氨基比林、地高辛、双氯芬酸、美托洛尔及抗酸剂等之间无相互作用。
【药物过量】大药剂使用时可出现心律不齐,转氨酶升高,肾功能改变,粒细胞降低等。
【药理毒理】本品通过特异性的作用于胃粘膜壁细胞,降低壁细胞中的H+、K+-ATP酶的活性,从而抑制胃酸的分泌。

商品名称:泮托拉唑肠溶片(潘妥洛克) 通用名称:泮托拉唑肠溶片规格: 40mg×7片/盒,双铝泡罩成份: 潘妥洛克40mg×7片主要成份为泮托拉唑(Pantoprazole)倍半水合钠盐化学名:5-二氟甲氧基-2-[(3,4-二甲氧基-2-吡啶甲基)亚硫酰]-1氢苯并咪唑钠倍半水合物分子式:C16H14F2NaO4S×1.5H2O分子量:432性状: 本品为黄色肠溶衣片,除去包衣后显白色或类白色。
用法用量: 本品若无医师处方,应按下述方法服用,请遵守这些方法,否则可能疗效不佳。
对伴有幽门螺杆菌感染的十二指肠溃疡或胃溃疡须用联合疗法根除感染。
潘妥洛克与抗菌药物的联合使用可采取下述任何一种方案:a、1片潘妥洛克肠溶片×2/日+1000mg阿莫西林×2/日+500mg 克拉霉素×2/日b、1片潘妥洛克肠溶片×2/日+500mg甲硝唑×2/日+500mg克拉霉素×2/日c、1片潘妥洛克肠溶片×2/日+1000mg阿莫西林×2/日+500mg甲硝唑×2/日在联合疗法中,有甲硝唑的方案仅在其他方案不能根除幽门螺杆菌感染的情况下方予使用。
若患者无联合疗法的指征,如检查幽门螺杆菌阴性,潘妥洛克可按下述剂量单独使用,除非另有医师处方:a、十二指肠溃疡、胃溃疡和反流性食管炎患者一般每日服用1片潘妥洛克肠溶片。
b、个别病例,特别是在其它治疗方法无效的情况下,可将剂量加倍(即每日2片潘妥洛克肠溶片)。
注意:a、肾功能受损和老年患者每日潘妥洛克的剂量一般不应超过40mg,但有些情况例外。
b、为根除幽门螺杆菌感染而使用联合疗法时,老年患者在1周治疗中也使用常规剂量(40mg×2/日)的潘妥洛克。
c、严重肝功能受损衰竭的患者剂量应减少至隔日1片(40mg)潘妥洛克。
功能主治(适应症): 1.十二指肠溃疡2.胃溃疡3.中重度反流性食管炎4.与下述药物配伍用能够根除幽门螺杆菌感染(1)克拉霉素和阿莫西林(2)克拉霉素和甲硝唑(详见用药方法)以减少该微生物感染所致的十二指肠溃疡与胃溃疡的复发。


亲爱的朋友,很高兴能在此相遇!欢迎您阅读文档潘妥洛克说明书,这篇文档是由我们精心收集整理的新文档。
相信您通过阅读这篇文档,一定会有所收获。
假若亲能将此文档收藏或者转发,将是我们莫大的荣幸,更是我们继续前行的动力。
潘妥洛克说明书潘妥洛克适用于十二指肠溃疡,胃溃疡,中、重度反流性食管炎。
下面是我们整理的,希望对大家有所帮助。
潘妥洛克商品介绍通用名:泮托拉唑肠溶片生产厂家:德国TakedaGmbH批准文号:注册证号Hxx0162药品规格:40mg*14片【商品名】潘妥洛克【通用名】泮托拉唑肠溶片【汉语拼音】PanTuoLaZuoChangRongPian【英文名】PantoprazoleEnteric-CoatedTablets【主要成分】每片潘妥洛克肠溶片含:45.1mg泮托拉唑钠盐倍半水合物(相当于40mg泮托拉唑)。
【性状】本品为黄色肠溶衣片,除去包衣后显白色或类白色。
【适应症】十二指肠溃疡,胃溃疡,中、重度反流性食管炎,与下述药物配伍用能够根除幽门螺杆菌感染:克拉霉素和阿莫西林,或克拉霉素和甲硝唑,或阿莫西林和甲哨唑(详见用药方法)以减少该微生物感染所致的十二指肠溃疡与胃溃疡的复发。
提示:潘妥洛克不用于治疗病变轻微的胃肠道疾患,如神经性消化不良。
在应用潘妥洛克治疗胃溃疡前,须除外胃与食道的恶性病变,以免因症状缓解而延误诊断。
反流性食管炎的诊断应经内镜检查核实。
【用法用量】本品若无医师处方,应按下述方法服用,请遵守这些方法,否则可能疗效不佳。
对伴有幽门螺杆菌感染的十二指肠溃疡或胃溃疡须用联合疗法根除感染。
潘妥洛克与抗菌药物的联合使用可采取下述任何一种方案:a、1片潘妥洛克肠溶片×2/日+1000mg 阿莫西林×2/日+500mg克拉霉素×2/日;b、1片潘妥洛克肠溶片×2/日+500mg甲硝唑×2/日+500mg克拉霉素×2/日;c、1片潘妥洛克肠溶片×2/日+1000mg阿莫西林×2/日+500mg甲硝唑×2/日。

【通用名】注射用泮托拉唑钠【英文名】PANTOPRAZOLE SODIUM FOR INJECTION【拼音名】ZHUSHEYONG PANTUOLAZUONA【药品类别】抗酸药及抗溃疡病药【化学名】5-二氟甲氧基-2-[(3,4-二甲氧基-2-吡啶基)甲基]亚硫酰基-1H-苯骈咪唑钠盐一水合物【结构式】【分子式】C16H14F2N3NaO4S·H2O【分子量】【性状】本品为白色或类白色疏松块或粉末,专用溶媒为无色的澄明液体。
【药理毒理】本品为胃壁细胞质子泵抑制剂,在中性和弱酸性条件下相对稳定,在强酸性条件下迅速活化,其pH依赖的活化特性,使其对H+、K+-ATP酶的作用具有更好的选择性。
本品能特异性地抑制壁细胞顶端膜构成的分泌性微管和胞浆内的管状泡上的H+、K+-ATP酶,引起该酶不可逆性的抑制,从而有效地抑制胃酸的分泌。
由于H+、K+-ATP 酶是壁细胞泌酸的最后一个过程,故本品抑酸能力强大。
它不仅能非竞争性抑制促胃液素、组胺、胆碱引起的胃酸分泌,而且能抑制不受胆碱或H2受体阻断剂影响的部分基础胃酸分泌。
本品与其它药物伍用时,具有药物间相互作用小的优点。
本品通过肝细胞内的细胞色素P450酶系的第I系统进行代谢,同时也可以通过第II系统进行代谢。
当与其它通过P450酶系代谢的药物伍用时,本品的代谢途径可以通过第II 酶系统进行,从而不易发生药物代谢酶系的竞争性作用,减少体内药物间的相互作用。
无致突变、致癌和致畸作用。
【药代动力学】本品具有较高的生物利用度,首次口服时即可以达到70%~80%,达峰时间1小时,有效抑酸达24小时。
静脉注射与口服给药的生物利用度比值为。
口服40mg 时的tmax为2~4小时,Cmax约为2~3μg/ml,清除半衰期约为小时。
约80%的口服或静注本品的代谢物经尿中排泄,肾功能不全不影响药代动力学,肝功能不全时可延缓清除。
t1/2、清除率和表观分布容积与给药剂量无关。

注射用泮托拉唑钠说明书【药品名称】通用名:注射用泮托拉唑钠曾用名:商品名:英文名:Pantoprazole Sodium for Injection汉语拼音:Zhusheyong pantuolazuona本品主要成分为泮托拉唑钠,其化学名称为:5-二氟甲氧基-2-[ (3, 4-二甲氧基-2-吡啶基 ) 甲基 ] 亚硫酰基-1H-苯骈咪唑钠盐一水合物。
其结构式为:分子式:C16H14F2N3NaO4S · H2O分子量:423.38【性状】本品为白色或类白色疏松块或粉末,专用溶媒为无色的澄明液体。
【药理毒理】本品为胃壁细胞质子泵抑制剂,在中性和弱酸性条件下相对稳定,在强酸性条件下迅速活化,其pH依赖的活化特性,使其对H+、K+-ATP酶的作用具有更好的选择性。
本品能特异性地抑制壁细胞顶端膜构成的分泌性微管和胞浆内的管状泡上的H+、K+-ATP酶,引起该酶不可逆性的抑制,从而有效地抑制胃酸的分泌。
由于H+、K+-ATP酶是壁细胞泌酸的最后一个过程,故本品抑酸能力强大。
它不仅能非竞争性抑制促胃液素、组胺、胆碱引起的胃酸分泌,而且能抑制不受胆碱或H2受体阻断剂影响的部分基础胃酸分泌。
本品与其它药物伍用时,具有药物间相互作用小的优点。
本品通过肝细胞内的细胞色素P450酶系的第I系统进行代谢,同时也可以通过第II系统进行代谢。
当与其它通过P450酶系代谢的药物伍用时,本品的代谢途径可以通过第II 酶系统进行,从而不易发生药物代谢酶系的竞争性作用,减少体内药物间的相互作用。
无致突变、致癌和致畸作用。
【药代动力学】本品具有较高的生物利用度,首次口服时即可以达到70%~80%,达峰时间1小时,有效抑酸达24小时。
静脉注射与口服给药的生物利用度比值为1.2。
口服40mg时的t max为2~4小时,C max约为2~3μg/ml,清除半衰期约为1.1小时。
约80%的口服或静注本品的代谢物经尿中排泄,肾功能不全不影响药代动力学,肝功能不全时可延缓清除。


新产品调研之泮托拉唑---一、概况泮托拉唑钠是在奥美拉唑的基础上基于Me-too药物设计原理,对母体结构进行改造后发现的药效更好的药物,泮托拉唑钠是由德国百克顿有限公司(BydG ulden)首先研制,于1994年在南非首次上市,商品名:潘妥洛克(Pantoloc®),至今已在美国、英国、德国等二十多个国家获准上市,,是继奥美拉唑,兰索拉唑之后全球第三个质子泵抑制剂,主要用于治疗十二指肠和胃溃疡及缓解中至重度的反流性食管炎. 同其它质子泵抑制剂相比,在弱酸条件下稳定,在强酸条件下很快被激活与其它药物相互作用小,其特点是在代谢过程中不易与细胞色素P45 0作用而氧化失效,生物利用度较之奥美拉唑提高7倍,在与其它药物配用时安全性和有效性均高于奥美拉唑和兰索拉唑,在弱酸性环境下也较奥美拉唑和兰索拉唑稳定。
泮托拉唑钠原料药为白色或类白色疏松块状物或粉末.市场主要是注射用泮托拉唑钠粉针,肠溶片和肠溶胶囊. 。
1、制剂情况2、原料药情况【原料药名称】Pantoprazole Sodium【中文名称】泮托拉唑钠【CAS登记号】138786-67-1【结构式】【化学名称】5-二氟甲氧基-2-[[(3,4-二甲氧基-2-吡啶基)-甲基]亚磺酰基]-1H-苯并咪唑钠一水合物。
【分子式】C16H14F2N3NaO4S·H2O【分子量】423.383、制剂处方资料【性状】本品为白色或类白色疏松块状物或粉末。
辅料为:甘露醇、依地酸二钠。
3.1适应证和用途适用于十二指肠溃疡、胃溃疡、急性胃粘膜病变,复合性胃溃疡等急性上消化道出血。
3.2药理毒理药理作用:泮托拉唑为质子泵抑制剂,通过与胃壁细胞的H+-K+ATP酶系统的两个位点共价结合而抑制胃酸产生的最后步骤。
该作用呈剂量依赖性并使基础和刺激状态下的胃酸分泌均受抑制。
本品与H+-K+ATP酶的结合可导致其抗胃酸分泌作用持续24小时以上。
毒理研究遗传毒性:泮托拉唑的人淋巴细胞染色体畸变试验、中国仓鼠卵巢细胞/HGPRT 正向突变试验及二次小鼠微核试验中的一次结果均为阳性,而大鼠肝脏DNA共价结合试验结果难以判断。

泮托拉唑适应症①十二指肠溃疡po,40mg/d,2和4周后愈合率分别为68%和96%。
国外多中心研究对比发现本品40mg/d与奥美拉唑20mg/d在2及4周的愈合率与症状缓解率均无明显差异。
②胃溃疡对于急性溃疡本品与奥美拉唑疗效无差异,但对于H2受体拮抗剂治疗无效的胃溃疡患者,本品40~80mg/d,8周愈合率为96.7%,12周愈合率达99%。
③反流性食管炎林万隆等总结了国外泮托拉唑对反流性食管炎的疗效,本品40mg/d疗效优于H2受体拮抗剂,与奥美拉唑20mg/d相似,④幽门螺杆菌本品与2种抗菌药物联合应用治疗HP感染,其疗效与其他PPIs与抗菌药物合用的结果相似,HP感染根除率接近或达到90%以上。
药物相互作用与奥美拉唑和兰索拉唑不同,本品在代谢过程中有一个转硫基作用且对细胞色素P450依赖性酶的抑制作用较弱,所以对同时通过该酶代谢的其他合用药物影响较小。
不良反应大多较轻微,发生率约为 2.5%,包括头痛、头晕、嗜睡、恶心、腹泻和便秘、皮疹及肌肉痛。
中文题名泮托拉唑代谢和立体选择性药物动力学研究副题名外文题名论文作者谢智勇著导师钟大放指导学科专业药物分析学研究领域\研究方向学位级别博士学位授予单位沈阳药科大学学位授予日期2005论文页码总数156页关键词泮托拉唑药物分析药物代谢动力学质子泵抑制剂液相色谱-质谱联用(LC/MS)馆藏号B SLW 2008 R975 3【中文摘要】选择性长效质子泵抑制剂泮托拉唑,主要用于治疗胃、十二指肠溃疡和反流性食管炎等胃肠道高分泌疾病,其结构中含有一手性中心硫原子,临床现在以消旋体形式给药。
前期对泮托拉唑代谢和动力学的研究表明,泮托拉唑经肝药酶进行广泛代谢,代谢途径包括亚砜氧化为砜或还原为硫醚、O-去甲基化、芳... >> 详细【外文摘要】Pantoprazole, a chiral benzimidazole sulfoxide derivative, is an irreversible proton pump inhibitor which is used clinically as racemate in the treatment of reflux esophagitis,Zoliinger-Ellison syndrome, peptic ulcers, and other acid-related, hypersecretory gastrointestinal disorders. In previous studies on the metabolism and pharmacokinetics of pantoprazole, it is extensively metabolized in the liver through the cytochrome P450 system and also exhibits polymorphic metabolism in humans. Pantoprazole undergoes metabolic pathways including sulfoxide oxidation and reduction (cataly zed mainly by CYP3A4),O-demethylation and aromatic hydroxylation (catalyzed by CYP2C19 and CYP3A4). The demethylated and hydroxylated metabolites then undergo phase II metabolism (glucuronidation or sulfation). In the EMs, the AUC of l-pantoprazole was slightly higher than that of d-pantoprazole. However, significant differences in the AUC (approximately 3 times greater for the d-pantoprazole than that for the l-pantoprazole) were observed in the PMs. It is important for complete understanding of the absorption, distribution, metabolism,and excretion of pantoprazole enantiomers, and for development of pantoprazole enantiomer, to gain further understanding of pantoprazole metabolism and stereoselective pharmacokinetics and its mechanism.The thesis aimed to isolate and identify metabolites of pantoprazole, to investigate pantoprazole metabolism in microbial model and in mammals. The stereoselective pharmacokinetics of pantoprazole was studied by assays for simultaneous determination of pantoprazole and its metabolites in different biological matrices and its mechanism was also revealed. It would offer some references and inspirations for the development of chiral drugs.1. Isolation and identification of pantoprazole metabolites A total of fifteen metabolites of pantoprazole were isolated from the biotransformed culture sample of pantoprazole by Cunninghamella blakesleeana AS 3.153 and urine sample of rat after multi-dose oral administration of pantoprazole and identified by NMR and ESI-MS. They were 8 phase I metabolites, 4 glucuronides, 2 N-acetylcysteine metabolites, and one glucoside, which could be used as reference substances in the studies on metabolism and stereoselective pharmacokinetics of pantoprazole. Using multi-stage ion trap mass spectrometric analysis, the characteristic fragment ions of pantoprazole and its metabolites were obtained. The collision-induced dissociation of protonated pantoprazole and its metabolites proceeds mainly via the following well-defined fragmentation pathways: The MS²spectra of glucuronides, N-acetylcysteine metabolites,and glucosides were dominated by an abundant loss of 176 (glucuronic acid - H₂O), 129 (CH₂=C(COOH)NHCOCH₃), and 162 Da (glucose - H₂O), respectively. After this dominating dissociation, the protonated phase I metabolites were formed. If it was a sulfone derivative, there was one characteristic fragment ion formed by the loss of 64 Da (SO₂). If it was a sulfine derivative, there were two characteristic fragment ions formed by the losses of 33 (·SH) and 34 Da (H₂S). When the sulfoxide functionality has not been changed, The MS²spectrum of the protonated metablite only provided one characteristic fragment ion, which was formed by the cleavage of C₂-S bond of the benzimidazole. Sometimes, there were some fragment ions formed by the losses of 20 (HF), 40 (2×HF), and 68 Da (HOCHF₂).2. The metabolism of pantoprazole in the microbial model and in mammals and their comparison Metabolites of pantoprazole in the microbial model of C. blakesleeana AS3.153 and in mammals (rat, dog, and human) were investigated by LC/MS〒method. A total of 37 metabolites were found andidentified by comparisons of their chromatographic behaviors,ESI-MS, and MS/MS spectra to those of pantoprazole, pantoprazole sulfone, pantoprazole thioether, and 15 isolated standards. These metabolites included 4'-O-demethyl-pantoprazole (RM8), 6-hydroxy-pantoprazole (RM13), conjugated metabolites of RM13 with glucuronic acid and sulphuric acid (RM16-RM19),5'-hydroxy-pantoprazole (RM14), rearranged metabolites (RM26), conjugated metabolites of pantoprazole sulfone with glucuronic acid (RM20 and RM21),4'-O-demethyl-pantoprazole sulfone (RM1), 6-hydroxy-pantoprazole sulfone (RM22), 1'-N-oxidic-pantoprazole sulfone (RM23), conjugated metabolites of RM22 with glucuronic acid and sulphuric acid (RM24 and RM25), conjugated metabolites of pantoprazole thioether with glucose (MM5 and MM6), 4'-O-demethyl-pantoprazole thioether (RM11), conjugated metabolites of RM11 with glucuronic acid (RM12), 6-hydroxy-pantoprazole thioether (RM2),conjugated metabolites of RM2 with glucuronic acid and sulphuric acid (RM3-RM5),6-hydroxy-4'-O-demethyl-pantoprazole thioether (RM6), conjugated metabolites of RM6 with glucuronic acid and sulphuric acid (RM9 and RM10), benzimidazole-related metabolites (RM27, RM30, RM34, and RM35), and pyridine-related metabolites (RM28,RM29, RM31-RM33). The major metabolic pathways of pantoprazole in the microbial model and in mammals were oxidation and reduction of the sulfoxide functionality,4'-O-demethylation, 6-hydroxylation, 5'-hydroxylation, 1'-N-oxidation, rearrangement and conjugation with glucuronic acid, sulphuric acid, glucose, and glutathione. Secondary metabolism via these pathways was also evidenced. Two new metabolic pathways (conjugation with glucose and glutathione) were found in this study.Pantoprazole was extensively metabolized both in the microbial model and in mammals (rat, dog, and human) to produce 6 and 35 metabolites, respectively. Except for that metabolites of RM2, RM7, RM11, and RM15 were the phase I metabolites of pantoprazole in the microbial model and in mammals, there were some differences in phase II metabolic reactions of pantoprazole between the microbial model and mammals.Only two glucosides were present in the microbial model, whereas the phase II metabolites of pantoprazole were found to be glucuronides (9 metabolites), sulfates (5 metabolites), and two N-acetylcysteine metabolites in mammals.3. Studies on the stereoselective pharmacokinetics and its mechanism of pantoprazole Using the assay for simultaneous determination of pantoprazole enantiomers and its two metabolites (pantoprazole sulfone and pantoprazole thioether) in plasma, the chiral inversion of pantoprazole enantiomers (d-pantoprazole in human and pantoprazole enantiomers in dog and rats) and the stereoselective pharmacokinetics of pantoprazole in rats have been studied. The stereoselective distribution of pantoprazole enantiomers after multi-dose oral administration of pantoprazole enantiomers to rat at 25 ㎎/㎏has been investigated by the LC/MS/MS method for simultaneous determination of parent drug and its four metabolites (pantoprazole thioether, pantoprazole sulfone, 4'-O-demethyl -pantoprazole thioether, 6-hydroxy-pantoprazole thioether) in tissues. Moreover, the stereoselective metabolism of pantoprazole enantiomers in rats liver microsomes has also been studied by another LC/MS/MS method of simultaneous determination of its three metabolites (pantoprazole sulfone, 4'-O-demethyl-pantoprazole thioether, 6-hydroxy-pantoprazole).These results indicated that the chiral inversion of pantoprazole enantiomers could not occur in mammals (human, dog, and rat), and pantoprazole has an enantioselective pharmacokinetics profile in Wistar rats. The concentrations of l-pantoprazole in plasma and tissues (liver, stomach, duodenum, small intestine intestine content, large intestine, and cecum) were higher than those of d-pantoprazole. The in situ absorption study showed no evidence of enantioselective absorption of the two enantiomers fromthe intestine and the protein binding of pantoprazole enantiomers may not influence the enantioselective disposition of pantoprazole after oral administration. Whereas, the metabolism of pantoprazole enantiomers in rat liver microsomes were enantioselective, which was mainly contributed to the different pharmacokinetics of pantoprazole enantiomers. These metabolic pathways included 4'-O-demethylation and 6-hydroxylation (catalyzed by CYP2C19), and oxidation of the sulfoxide functionality (catalyzed by CYP3A4).4. Pharmacokinetics of l-pantoprazole The studies of stereoselective pharmacodynamics ofpantoprazole enantiomers have proved the eudomer was l-pantoprazole. In order to develop a single optical isomer, the pharmacokinetics of l-pantoprazole has been studied in this investigation.l-Pantoprazole is rapidly absorbed after oral administration, with T〒approximately 23 and 16 min in dog and rats, respectively. l-Pantoprazole is subjected to low first-pass hepatic extraction, as reflected in an estimated absolute oral bioavailability of 63.9% and 88.9% in dog and rats,respectively.l-Pantoprazole and its two metabolites (pantoprazole sulfone and pantoprazole thioether) are mainly distributed to gastrointestines (stomach, small intestine,large intestine, and cecum), which are useful to its therapy of hypersecretory gastrointestinal disorders.In the present study, a total of fifteen metabolites of pantoprazole were isolated and identified by NMR and ESI-MS, moreover, a total of 37 metabolites were observed in microbial model and in mammals by the analysis of LC/MS〒. Two new metabolic pathways,conjugation with glucose and glutathione, were found. The stereoselective pharmacokinetics and its mechanism of pantoprazole, as well as pharmacokinetics of l-pantoprazole conducted by an HPLC and two LC/MS/MS methods, and they would be useful for chiral drugs development and design.KEY WORDS: Pantoprazole; Metabolism; Stereoselective pharmacokinetics; Chiral drugs;Proton pump inhibitors; Liquid chromatography-mass spectrometry; Microbial models;Cytochrome P450隐藏【相关检索】窗体顶端序号申请号专利名称100816583.1新型药用组合物299112872.9泮托拉唑钠冻干粉针剂及制备方法302109182.X手性泮托拉唑盐及其制备方法4200610047741.0一种治疗胃食管反流疾病与功能性消化不良的药物5200810001189.0一种泮托拉唑钠冻干粉针剂及其制备方法6200810088954.7泮托拉唑钠脂质体冻干制剂及其制备方法7200810024532.3一种无定形S-泮托拉唑钠及其制备方法、应用8200810024533.8S-泮托拉唑钠9200680015425.3由无症状性胃-食管返流引起的睡眠障碍的治疗中的质子泵抑制剂10200510023469.8泮托拉唑钠冻干粉针剂及其制备方法1101819379.X泮托拉唑冻干制剂和泮托拉唑注射剂1202813961.5苯并咪唑型化合物的改进制备方法13200310112607.0泮托拉唑钠肠溶微丸14200480020488.9制备质子泵抑制剂的异构纯前体药物的方法15200410022415.5含有环糊精衍生物和胃壁细胞质子泵抑制剂的药物组合物16200380104409.8用于制备泮托拉唑(pantoprazole)的方法17200480012129.9含有泮托拉唑作为活性成分的剂型18200410097130.8泮托拉唑或其盐的口服肠溶微丸及其制备工艺19200480022239.3制备2-[(吡啶基)甲基]亚磺酰基取代的苯并咪唑和新型泮托拉唑氯化衍生物的方法20200610085227.6一种泮托拉唑钠肠溶微丸21200480035251.8泮托拉唑多颗粒制剂22200610172184.5手性质子泵抑制剂的制备方法23200610156621.4泮托拉唑钠冻干粉针剂及其制备方法24200710010273.4手性亚砜类化合物的制备方法25200610045806.8一种治疗幽门螺旋杆菌感染的复方口服制剂26200710021608.2注射剂用胶塞的质量标准及其检测方法27200710023577.4一种质子泵抑制剂分散片28200710023576.X一种质子泵抑制剂咀嚼片29200710099342.3一种含有多潘立酮泮托拉唑钠的缓释制剂及其制备方法30200810012623.5四个抗溃疡药物毛细管电泳手性分离分析方法31200810150111.5光学纯泮托拉唑的制备方法32200810163437.1泮托拉唑及其钠盐肠溶缓释微丸制剂33200710093154.X一种泮托拉唑钠肠溶片及其制备方法34200910000896.2一种泮托拉唑及其盐的合成方法35200910019756.X一种泮托拉唑钠化合物及其制法36200910128639.7含有泮托拉唑作为活性成分的剂型37200810045020.5手性亚砜类化合物的制备新方法38200910014975.9一种复乳法制备的泮托拉唑钠亚微乳冻干制剂39200910016385.X泮托拉唑钠在治疗胆囊炎中的新应用40200810038527.8泮托拉唑钠肠溶微丸41 200810110447.9S-泮托拉唑及盐的新制备方法42 200910230611.4一种泮托拉唑钠亚微乳固体制剂43 200910154928.4泮托拉唑及其钠盐口腔崩解片44 201010045827.6泮托拉唑钠的组合药物45 201010000492.6一种泮托拉唑钠的组合药物及其制备方法46 200910077100.3一种以泮托拉唑钠为主要成分的肠溶固体制剂及其制备方法47 200910265378.3含有泮托拉唑的中西药组合物48 200910223918.1一种注射用泮托拉唑钠冻干药物组合物及其制备方法49 200910080240.6一种含有左旋泮托拉唑镁的药物制剂及其制备方法50 200910080241.0一种含有右旋泮托拉唑镁的药物制剂及其制备方法51 201010281487.7注射用泮托拉唑钠配制工艺52 200910060079.6泮托拉唑与多潘立酮的联合用药物。

注射用S-泮托拉唑钠中间产品标准
【性状】本品为无色澄清液体
【pH值】依法测定(中国药典2010年版二部附录Ⅵ H),PH值应为11.2~12.5
【含量范围】中间产品范围9.00~11.00mg/ml[以S-泮托拉唑(C16H15F2N3O4S)计]
【含量测定】避光操作。
照高效液相色谱法(中国药典2010年版二部附录Ⅴ D)测定。
色谱条件与系统适用性试验用十八烷基硅烷键合硅胶为填充剂;以0.01mol/L磷酸氢二钾溶液(用磷酸调节pH值至7.0)-乙腈(65:35)为流动相,检测波长为289nm,柱温为25℃,流速为每分钟1.0ml。
理论板数按S-泮托拉唑峰计算不低于2500。
测定法取本品4瓶,加溶剂〔0.001mol/L氢氧化钠溶液-乙腈(1:1)〕溶解并转移至同一100ml量瓶中,用溶剂稀释至刻度,摇匀,精密量取适量,用溶剂定量稀释制成每1ml中约含S-泮托拉唑40μg的溶液,精密量取20μl,注入液相色谱仪,记录色谱图。
另取S-泮托拉唑钠对照品适量,精密称定,加溶剂溶解并定量稀释制成每1ml中含S-泮托拉唑40μg的溶液,同法测定。
按外标法以峰面积计算,即得。
【微生物污染水平】正常检测
【中间产品密度】正常检测。
注射用丹参多酚酸盐与注射用泮托拉唑钠存在配伍禁忌发表时间:2016-02-22T14:18:49.563Z 来源:《健康世界》2015年20期供稿作者:王丽[导读] 内蒙古鄂尔多斯市中心医院 017000 对科室及有关文献、指南报到的药物间配伍禁忌情况、实例,组织全体医护人员安全用药学习,提高警惕,促进合理、有效、准确用药。
王丽内蒙古鄂尔多斯市中心医院 017000目前,临床用药种类繁多,很多药物之间存在配伍禁忌是护理人员在临床实践过程中发现的。
2015年4月,我科发现注射用丹参多酚酸盐与注射用泮托拉唑钠存在配伍禁忌。
为避免或减少临床护理工作中的一些不必要的差错和事故,维护患者的安全及健康,现报道如下。
临床资料患者,男,65岁,因冠心病,心绞痛,高血压,胃溃疡入院。
遵医嘱给予5%葡萄糖溶液250ml+注射用丹参多酚酸盐100mg静脉滴注,接着更换0.9%氯化钠100ml+注射用泮托拉唑钠40mg静脉滴注时茂菲滴管内出现液体为黄绿色反应,无浑浊及沉淀。
立即更换输液器,严密观察患者病情变化,经观察未发生不良用药反应,患者主诉无不适症状。
注射用丹参多酚酸盐为浅棕色疏松块状物,50mg/瓶,由上海绿谷制药有限公司生产,有活血、化瘀、通脉的作用,用于冠心病稳定型心绞痛。
注射用泮托拉唑钠为白色或类白色疏松块或粉末,40mg/瓶,由海南卫康有限公司生产,适用于十二指肠溃疡、胃溃疡、急性胃粘膜病变,复合性胃溃疡等急性上消化道出血。
为证实两种药物存在配伍禁忌的情况,查阅《306种药物配伍禁忌表》及药品使用说明书,均无此两种药物的配伍禁忌说明。
实验方法及结果为进一步证实注射用丹参多酚酸盐与注射用泮托拉唑钠存在配伍禁忌,通过与医院药师委员会共同进行实验,我们用一次性注射器抽取丹参多酚酸盐稀释液与泮托拉唑钠稀释液混合时,针管内液体即刻出现黄绿色反应,同时静置30分钟、60分钟均未发生任何改变。
临床应用及实验均表明注射用丹参多酚酸盐与注射用泮托拉唑钠存在配伍禁忌。
注射用头孢孟多脂钠与注射用泮托拉唑钠存在配伍禁忌头孢曲松钠为白色结晶性粉末,无臭,在水中易溶解,适用于敏感菌所致的感染。
注射用泮托拉唑钠(国产)为白色疏松块状物。
适用于十二肠溃疡、胃溃疡、急性胃黏膜病变、复合性胃溃疡等急性上消化道出血。
在临床实践中发现二者存在配伍禁忌。
标签:头孢孟多脂钠;泮托拉唑钠;配伍禁忌本科2015年1月收治多例进行治疗的十二指肠球部溃疡病患者,遵医嘱给予输入注射用头孢孟多脂钠与注射用泮托拉唑钠2种药物输入过程中出现了白色混浊絮状物,现报告如下:1材料注射用头孢孟多脂钠为类白色结晶性粉末,由上海新亚药业有限公司生产,批号H10870009,规格为0.5g/支,适用于敏感细菌所致的肺部感染、尿路感染、胆道感染、皮肤软组织感染、骨和关节感染以及败血症、腹腔感染等。
注射用泮托拉唑钠为类白色疏松块状物,由海南卫康制药(潜山)有限公司生产,批号H20083910规格为40mg/支,具有抑酸作用:用于十二指肠溃疡、胃溃疡、急性胃粘膜病变,复合性胃溃疡等引起的急性上消化道出血。
2配伍禁忌多例患者在入院后行注射用头孢孟多脂钠3g加0.9%生理盐水100ml与注射用泮托拉唑钠40mg加0.9%生理盐水100ml静脉输液,上述2种药物序贯使用时输液器中均立即出现白色混浊,继而出现白色絮状物,振动后不消失,立即更换输液器及输液体,同时给患者及家属充分解释,观察患者未诉不适,保留换下液体及输液器以备检查,记录药名,厂家,生产日期,批号,配药时间,输液时间签名,及时上报药学部。
3讨论注射用头孢孟多脂钠与注射用泮托拉唑钠存在配伍禁忌,提示护理人员在进行静脉用药时应注意以下几点①此2种药物不能在同一静脉通路中借用三通管同时使用上述2种药物②此2种药物输注过程中要输入0.9%生理盐水20ml,冲管间隔开后再使用③在用药之前要查阅成药的说明书并注意与其相关说明,此种药物说明书上均未注明其相互间的配伍禁忌,注射用头孢孟多脂钠说明书上只说明本药品不能与含有钙或镁的溶液有配伍禁忌,说明书上无其他相关说明,次种药物说明书上均未说明其相互间的配伍情况,且临床应用广泛,如临床需要两药联用,为避免药物反应,护理人员应在应用此药物时给予0.9%生理盐水冲管或间隔输入,避免药物之间配伍反应给患者造成的不必要损害,建议临床上在任何时为静脉输注注射用头孢孟多脂钠时,用生理盐水冲管或更换输液器,以免发生药物配伍禁忌的不良反应,若出现配伍反应,应立即更换输液器,严密观察患者反应,做好解释及心理安抚工作,同时也提醒临床在用药过程中应重视药物之间的相互作用,护士在日常护理工作中,要严密观察药物性质有无变化,若出现配伍反应应做好药物不良反应上报工作,确保用药安全。
注射泮托拉唑钠注意事项
一、注射泮托拉唑钠注意事项二、胃不好的人要少吃什么食物三、胃溃疡会变成胃癌吗
注射泮托拉唑钠注意事项1、注射泮托拉唑钠注意事项
泮托拉唑钠适用于十二指肠溃疡、胃溃疡、急性胃粘膜病变,复合性溃疡等引起的急性上消化道出血。
对本品过敏者或严重肝功能不全者禁用。
应用本品时应首先排除癌症的可能,因为本品治疗可减轻胃癌症状。
从而延误诊断。
肝、肾功能不全者慎用,根据需要酌情减量。
药物相互作用:在体内较高剂量的泮托拉唑不改变安定的消除率,其血清浓度不受安定的影响,表明安定不影响泮托拉唑的代谢。
泮托拉唑与氨茶碱,华法令、避孕药、苯妥英钠、硝苯吡啶、氨基比林、地高辛、双氯芬酸、美托洛尔及抗酸剂等药物之间无相互作用。
2、泮托拉唑钠肠溶片饭前吃还是饭后吃呢
泮托拉唑钠肠溶片正确的服用方法: 泮托拉唑钠肠溶片口服,每日早晨餐前40mg(1片)。
十二指肠溃疡疗程通常为2~4周,胃溃疡和反流性食管炎疗程通常为4~8周。
泮托拉唑钠肠溶片,主要成分是泮托拉唑钠,适用于活动性消化性溃疡(胃、十二指肠溃疡)反流性食管炎和卓艾氏综合症。
泮托拉唑钠肠溶片口服后吸收迅速、完全,单次口服40mg后2~3小时左右即可达血药浓度峰值,其口服制剂的绝对生物利用度为77%,泮托拉唑的血浆蛋白结合率为98%,主要在肝脏代谢为去甲基泮托拉唑硫酸酯。
泮托拉唑的半衰期1小时左右,去甲基泮托拉唑硫酸酯的半衰期1~5小时。
80%的代谢产物通过肾脏排出,其余经胆汁进入粪便排出。
3、泮托拉唑钠注射有什么作用。
核准日期:2007年02月24日修订日期:2013年02月19日2014年08月29日2016年11月28日2017年10月09日2019年08月09日泮托拉唑钠肠溶片40mg说明书请仔细阅读说明书并在医师指导下使用。
【药品名称】通用名称:泮托拉唑钠肠溶片商品名称:潘妥洛克®英文名称:Pantoprazole Sodium Enteric-Coated Tablets汉语拼音:Pan Tuo La Zuo Na Chang Rong Pian【成份】本品主要成份为:泮托拉唑(Pantoprazole)倍半水合钠盐。
化学名称:5-二氟甲氧基-2-[(3,4-二甲氧基-2-吡啶甲基)亚磺酰]-1-氢-苯并咪唑倍半水合钠盐化学结构式:分子式:C16H14F2N3NaO4S × 1.5H2O分子量:432.4【性状】本品为黄色肠溶衣片,除去包衣后显白色或类白色。
【适应症】-十二指肠溃疡-胃溃疡-中、重度反流性食管炎-与下述药物配伍用能够根除幽门螺杆菌感染:-克拉霉素和阿莫西林,或-克拉霉素和甲硝唑,或-阿莫西林和甲硝唑(详见用药方法)以减少该微生物感染所致的十二指肠溃疡与胃溃疡的复发。
提示泮托拉唑不用于治疗病变轻微的胃肠道疾患,如神经性消化不良。
在应用泮托拉唑治疗胃溃疡前,须除外胃与食道的恶性病变,以免因症状缓解而延误诊断。
反流性食管炎的诊断应经内镜检查核实。
【规格】40mg/片,每片潘妥洛克肠溶片含:45.1 mg 泮托拉唑倍半水合钠盐(相当于40mg泮托拉唑)。
【用法用量】本品若无医师特殊处方,应按下述方法服用,请遵守这些方法,否则可能疗效不佳。
对伴有幽门螺杆菌感染的十二指肠溃疡或胃溃疡须用联合疗法根除感染。
泮托拉唑与抗菌药物的联合使用可采取下述任何一种方案:a.1片泮托拉唑钠肠溶片× 2次/日+ 1000 mg 阿莫西林× 2次/日 + 500 mg 克拉霉素× 2次/日b. 1片泮托拉唑钠肠溶片× 2次/日+ 500 mg甲硝唑× 2次/日+ 500 mg克拉霉素× 2次/日c.1片泮托拉唑钠肠溶片× 2次/日+ 1000 mg阿莫西林× 2次/日+ 500 mg甲硝唑× 2次/日在联合疗法中,有甲硝唑的方案仅在其他方案不能根除幽门螺杆菌感染的情况下方予使用。
药品名称:
通用名称:注射用泮托拉唑钠
英文名称:Pantoprazole Sodium for Injection
商品名称:注射用泮托拉唑钠
成份:
本品主要成份为泮托拉唑钠。
辅料为甘露醇、依地酸二钠。
主要用于
1.消化性溃疡出血。
2.非甾体类抗炎药引起的急性胃粘膜损伤和应激状态下溃疡大出血的发生。
3.全身麻醉或大手术后以及衰弱昏迷患者防止胃酸反流合并吸入性肺炎。
规格:
60mg(以泮托拉唑计)
静脉滴注。
一次40—80mg,每日1—2次,临用前将10ml 0.9%氯化钠注射液注入冻干粉小瓶内,将溶解后的药液加入0.9%氯化钠注射液100—250ml中稀释后供静脉滴注。
静脉滴注,要求15—60分钟内滴完。
本品溶解和稀释后必须在4小时内用完,禁止用其他溶剂或其他药物溶解和稀释。
不良反应:
偶见头晕、失眠、嗜睡、恶心、腹泻、便秘、皮疹、肌肉疼痛等症状。
大剂量使用时可出现心律不齐,转氨酶升高,肾功能改变,粒细胞降低等。
1.对本品过敏者禁用。
2.妊娠期与哺乳期妇女禁用。
1.本品抑制胃酸分泌的作用强,时间长,故应用本品时不宜同时再服用其它抗酸剂或抑酸
剂。
为防止抑酸过度,在一般消化性溃疡等病时,不建议大剂量长期应用(卓一艾综合征例外)。
2.肾功能受损者不须调整剂量;肝功能受损者需要酌情减量。
3.治疗溃疡时应排除胃癌后才能使用本品,以免延误诊断和治疗。
孕妇及哺乳期妇女用药:
孕妇及哺乳期妇女禁用。
儿童用药:
尚无儿童静脉应用本品的经验。
老年用药:
老年人用药剂量无须调整。
药物相互作用:
本品与肝脏细胞色素P450酶的亲和力较低,并有Ⅱ期代谢的途径,因而与通过细胞色
素P450酶系代谢的其他药物相互作用较奥美拉唑和兰索拉唑少。
泮托拉唑为质子泵抑制剂,通过与胃壁细胞的H<SUP>+- K<SUP>+ATP酶系统的两个位点共价结合而抑制酸产生的最后步骤。
该作用呈剂量依赖性并使基础和刺激状态下的胃酸分泌均受抑制。
本品H<SUP>+-
K<SUP>+ATP酶的结合可导致其抗胃酸分泌作用持续24小时以上。
毒理研究:
1.遗传毒性:
泮托拉唑的人淋巴细胞染色体畸变试验、中国仓鼠卵巢细胞/HCPRT正向突变试验及二次小鼠微核试验中的一次结果均为阳性,而大鼠肝脏DNA共价结合试验结果难以判断。
Ames试验、大鼠肝细胞程序外DNA合成试验(UDS)、AS52/GPT哺乳动物细胞正向基因突变试验、小鼠淋巴瘤L5178Y细胞胸腺嘧啶激酶突变试验及体内大鼠骨髓细胞染色体畸变试验结果均为阴性。
2.生殖毒性:
1.雄性大鼠经口给予泮托拉唑500mg/kg/d(按体表面积折算为临床推荐口服剂量
的98倍),雌性大鼠经口给予泮托拉唑450mg/kg/d(按体表面积折算为临床推荐口
服剂量的88倍)时,生育力及生殖行为未见明显异常。
2.大鼠静脉给予泮托拉唑20mg/kg/d(按体表面积折算为临床推荐口服剂量的4
倍),家兔静脉给予泮托拉唑15mg/kg/d(按体表面积折算为临床推荐口服剂量的6
倍),对生育力和胎仔均未见明显损害。
泮托拉唑及其代谢产物可以从家兔乳汁中分
泌。
3.致癌性:
1.SD大鼠连续24个月经口给予泮托拉唑0.5- 200mg/kg/d,胃底出现剂量依赖性
的肠嗜铬样细胞增生及良性和恶性的神经内分泌细胞瘤。
当剂量为50和200mg/kg/d
(按体表面积折算为临床推荐口服剂量的10和40倍)时,前胃出现良性鳞状细胞乳
头状瘤和恶性鳞状细胞癌。
泮托拉唑还导致极少数大鼠出现胃肠道肿瘤,包括
50mg/kg/d剂量时偶尔出现十二指肠腺癌,以及200mg/kg/d剂量时胃底出现良性息
肉和腺癌。
泮托拉唑给药剂量0.5 - 200 mg/kg/d时,大鼠剂量依赖性地出现肝细胞
腺瘤和肝癌,200 mg/kg/d剂量还可使大鼠甲状腺囊泡细胞瘤和囊泡细胞癌的发生率
增加。
SD大鼠6个月和12个月的毒性研究中也偶见肝细胞腺瘤和肝癌。
2.Fischer344大鼠连续24个月经口给予泮托拉唑5-50mg/kg/d(按体表面积折算
为临床推荐口服剂量的1-10倍),胃底剂量依赖性出现肠嗜铬样细胞增生及良性和
恶性的神经内分泌细胞瘤。
但该试验的剂量选择不足以支持对泮托拉唑潜在致癌性的
充分评价。
3.B6C3Fl小鼠连续24个月经口给予泮托拉唑5-150mg/kg/d(按体表面积折算为
临床推荐口服剂量的0.5 -15倍),同样出现胃底肠嗜铬样细胞增生;雌鼠在
150mg/kg/d剂量时,肝细胞腺瘤和肝癌的发生率升高。
上述啮齿类动物的致癌性研究结果提示本品只有一定的致癌性,但此结果与临床的相关性尚不清楚。
药代动力学:
本品具有较高的生物利用度,静脉注射与口服给药的生物利用度比值为1.2。
约80%静注本品的代谢物经尿中排泄,肾功能不全不影响药代动力学,肝功能不全时可延缓清除。
T1/2清除率和表观分布容积与给药剂量无关。
性状:
本品为白色或类白色疏松块状物或粉末。
贮藏:
避光、密闭,在阴凉处保存,不超过20℃。
包装:
西林瓶装,1瓶/盒。
24个月
执行标准:
《中国药典》2010年版二部
批准文号:
国药准字H20083911
生产企业:
海南卫康制药(潜山)有限公司
药物分类:
抑酸/抗反流/治疗溃疡的药物。