土壤中有机磷分组
- 格式:wps
- 大小:24.00 KB
- 文档页数:4

⼟壤磷贵州⼟壤磷素肥⼒磷是植物⽣长发育所必需的⼤量营养元素之⼀。
它既是植物体内许多重要有机化合物的组分,同时⼜以多种⽅式参与植物体内各种代谢过程。
⼟壤[1]是植物磷营养的主要来源,⽣产上⼈们通过向⼟壤中施加磷肥来提⾼⼟壤中磷的含量,由于磷是以沉积的形式存在和贮存的,⽽且,在⼟壤中具有特定的化学⾏为,使其在当季作物的利⽤率仅为10%~25% [2]。
为此⼟壤中磷的含量、存在形态及其有效性对作物磷素吸收极为重要,成为当今关注的热点问题。
贵州位于我国西南,居云贵⾼原东部,是介于四川盆地和⼴西丘陵之间的岩溶⾼原⼭区。
省内地带性⼟壤以黄壤为主,还有红壤、黄棕壤等⼟壤呈酸性或强酸性,⼟壤中活性铁、铝含量较⾼,可溶性磷多与铁、铝相结合,转化为难溶性磷酸铁、磷酸铝等形态⽽被固定,其有效磷含量不⾼[3]。
⼈们通过在⼟壤中施加磷肥来提⾼⼟壤中磷的含量,但是,随着磷肥的⼤量施⽤,我国各区耕地⼟壤速效磷含量呈显著增加趋势,部分耕层⼟壤速效磷含量表现为过量累积,导致农⽥⽣态系统⽔体富营养化,给环境带来不利影响,⽂章通过对磷素在⼟壤中存在的状态,⼟壤对磷的固定积累以及提⾼磷的有效性展开综述,以期为提⾼作物对⼟壤磷的吸收利⽤⽅⾯研究提供参考。
1.贵州⼟壤磷素肥⼒利⽤现状贵州位于我国西南,居云贵⾼原东部。
其具有低纬度、⾼海拔,⾃然条件复杂,地貌多种多样,母岩组合复杂,⽓候变化悬殊,⼟壤类型较多,从亚热带的红壤到暖温带的棕壤都有分布的特点。
其中,以黄壤分布⾯积最多,遍及贵州⾼原的主体部分。
贵州⼟壤pH 值在3.1~8.9范围。
通常林草地⼟壤与耕地⼟壤之间有⼀定的差异。
全省耕地⼟壤以微酸性(pH 5.5~6.5) 所占⾯积⽐例最⼤,为35.7%。
由于黄壤地区温暖湿润;地形以低⼭丘陵为主;旱地⾯积分布较⼴;是我国农业⽣产的主要区域之⼀,由于对⼟地资源的不合理利⽤;多数旱地⼟壤侵蚀严重;引起⼟壤养分流失;导致⼟壤退化,在农业⽣产上磷肥施⽤是提⾼作物产量的有效措施之⼀;然⽽当季施⽤磷肥的利⽤率⼀般为10%~25%;⼤量磷肥在⼟壤中积累;当地表径流和⼟壤侵蚀发⽣时;⼟壤磷由陆地向⽔体迁移;这不仅造成磷矿资源的损失与浪费;⽽且会加速附近⽔体富营养化的产⽣。


土壤速效磷组分1. 简介土壤中的磷(Phosphorus)是植物生长所必需的营养元素之一,对于植物的生长和发育具有重要作用。
土壤中的磷主要以有机磷和无机磷两种形式存在,其中速效磷是植物能够直接吸收利用的主要形式。
本文将介绍土壤速效磷的组分,包括速效磷的来源、形态、含量等内容,以及对速效磷的测定方法和调控措施。
2. 速效磷的来源速效磷主要来自于土壤中的有机磷和无机磷。
有机磷是由植物和动物遗体、粪便等有机物分解产生的,其中包含的磷以有机磷酸形式存在。
无机磷主要来自于土壤中的矿物质,如磷酸钙、磷酸铁等。
速效磷的来源多样化,包括有机肥料、无机肥料、有机物分解产物等。
有机肥料中的速效磷主要来自于有机磷,如动物粪便中的有机磷酸。
无机肥料中的速效磷主要来自于无机磷,如磷酸二铵、磷酸一铵等。
3. 速效磷的形态速效磷在土壤中以不同的形态存在,主要包括磷酸盐、有机磷酸和磷酸酯等。
磷酸盐是速效磷的主要形态,包括磷酸一铵、磷酸二铵、磷酸二钙等。
磷酸盐溶解度较高,容易被植物吸收利用。
有机磷酸是速效磷的另一种形态,主要来自于有机物分解产生的有机磷。
有机磷酸在土壤中较稳定,需要通过微生物的作用才能转化为无机磷形式,被植物吸收利用。
磷酸酯是速效磷的一种次要形态,主要存在于土壤中的有机物中。
磷酸酯的溶解度较低,不容易被植物吸收利用。
4. 速效磷的含量土壤中的速效磷含量是评价土壤肥力的重要指标之一。
速效磷含量的高低对作物的生长和产量有着直接的影响。
速效磷含量的测定方法主要有树脂吸附法、提取液法和酶解法等。
树脂吸附法是目前应用较广泛的测定方法,通过树脂吸附土壤中的速效磷,再用酸溶解树脂,测定溶液中的磷含量。
提取液法是将土壤样品与提取液进行反应,利用提取液中的酸或碱溶解土壤中的速效磷,再测定溶液中的磷含量。
酶解法是利用酶解剂将土壤中的有机磷转化为无机磷,再测定无机磷的含量。
土壤速效磷的含量与土壤类型、施肥措施、有机质含量等因素密切相关。




土壤中有机磷的测定实验方案设计土壤中磷知识总结I、土壤中磷的来源及分布:土壤中的磷素来源于成土矿物、有机物质和含磷化学肥料。
土壤全磷量不能作为当季作物的土壤供磷的水平指标,但可作为表示土壤潜在肥力的一项指标。
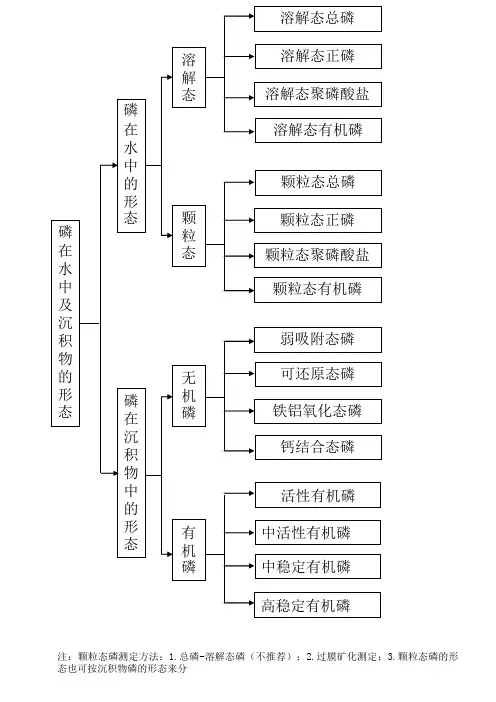
土壤磷素分为无机形态和有机形态。
无机形态的磷约占全磷的50%〜90%,主要包括磷酸钙类化合物(Ca-P)、磷酸铁类化合物(Fe-P)、磷酸铝类化合物(AI-P )和表面为氧化铁胶膜所封闭的闭蓄态磷(O-P)。
风化程度较高的土壤,如红壤以O-P和Fe-P为主,风化程度较低的土壤以Ca-P 和AI-P 为主。
有机形态的磷约占全磷10%〜50%,主要以磷脂、植素、核酸和核蛋白形式存在。
土壤有机磷含量与土壤有机质含量密切相关。
土壤有效磷是指当季作物所能吸收的磷。
土壤中磷移动性很小。
作物吸收的磷主要是土壤溶液中的H2PO- 4和HPO2 4-。
U、磷的营养功能:1、磷是植物体内重要化合物的组成元素;2、磷能加强光合作用和碳水化合物的合成与运转;3、促进氮素代谢;4、磷能促进脂肪代谢;5、提高作物对外界环境的适应性川、作物磷素营养失调的症状缺磷时,各种代谢过程受到抑制,植株生长迟缓、矮小、瘦弱、直立、根系不发达,成熟延迟、籽实细小、植株叶小、叶色暗绿或灰绿、缺乏光泽,主要是细胞发育不良致使叶绿素密度相对提高,同时,Fe的吸收间接地促进叶绿素合成,使叶色暗,严重缺磷时,在不少作物茎叶上明显地呈现紫红色的条纹或斑点(花青苷)甚至叶片枯死脱落,症状一般从基部老叶开始。
逐渐向上部发展。
缺磷造成玉米果穗秃顶,油菜脱荚,棉花和果树落蕾、落花,甘薯及马铃薯薯块变小,耐贮性变差。
磷素过剩,谷类无效分蘖,秕粒增加,叶肥厚而密,植株早衰。
由于磷过多,而引起的病症,通常以缺Zn、Fe、Mg 等的失绿症表现出来。
W土壤中磷的测定方法:测定土壤速效磷的方法选择,酸性土壤一般采用盐酸氟化铵或氢氧化钠一草酸钠法来提取,石灰性土壤或中性土壤采用碳酸氢钠来提取。

土壤中全磷测定土壤全磷分析土壤全磷测定要求把无机磷全部溶解,同时把有机磷氧化成无机磷,因此测定的第一步是样品分解,第二步是溶液中磷的测定。
一、HClO4–H2SO4消煮,钼蓝比色法1.方法原理在高温条件下,土壤中含磷矿物及有机磷化合物与高沸点的H2SO4和强氧化剂HClO4作用,分解成正磷酸盐而进入溶液。
在一定酸度下,正磷酸根与钼酸铵作用生成磷钼杂多酸,在还原剂的作用下形成“钼蓝”,使溶液呈蓝色。
蓝色深浅与磷的含量成正比,可用分光光光度法于700nm处测定。
2.仪器设备分光光度计消煮炉3.试剂(1)浓H2SO4;(2)70%~72%HClO4;(3)2,4-二硝基酚指示剂:0.2g 溶于100 mL水中;(4)4 mol?L-1氢氧化钠溶液;(5)钼锑储存溶液;a浓硫酸153 mL缓缓倒入400 mL水中,b10g 钼酸铵溶于60℃ 300 mL水中,a倒入b中,加入100 mL 5g·L-1的酒石酸锑钾溶液,用水定容摇匀,贮存于棕色试剂瓶中。
(6)钼锑抗显色剂:100 mL钼锑储存溶液中加1.5g抗坏血酸,现配现用。
(7)磷标准贮存溶液(ρ=100 mg·L-1),0.4390g 磷酸二氢钾(105℃烘2h)溶于100 mL水中,加入5mL硫酸,定容至1L;(8)磷标准溶液(ρ=5.00mg·L-1),磷标准贮存溶液准确稀释20倍。
4.操作步骤(1)样品消煮称取100目土样0.3~1 g于50 mL消化管中→ 加少量水润湿后加浓硫酸8mL,摇匀→ 加70~72%高氯酸10滴,摇匀,管口加一个小漏斗→ 加热消煮,至溶液开始转白后继续消煮20min→ 冷却后用水洗入100 mL容量瓶中→ 定容摇匀→ 静置过夜取上清液或用干燥的无磷滤纸过滤。
(同时做空白试验)(2)溶液中磷的比色测定移取澄清液或滤液2~10 mL于50ml容量瓶中→ 加水至约30 mL→ 加二硝基酚指示剂2滴→ 用4 mol?L-1 NaOH调节pH至溶液刚呈黄色→ 加钼锑抗显色剂5 mL→ 定容,摇匀→ 半小时后(高于15℃)于700nm处比色测定标准曲线分别移取5.00mg·L-1磷标准溶液0、1、2、3、4、5mL于50mL 容量瓶中,同上操作,以吸光度为纵坐标,磷浓度为横坐标绘制工作曲线。

第8章土壤中有机磷农药的测定8.1概述长期以来,大面积使用化学农药严重破坏环境和生态,而我国化学农药的使用量是世界平均用量的2.5倍,高毒农药使用量占我国农药使用量的30%[1]。
有机磷农药是上世纪三十年代德国G.Schradev首先发现的,有机磷农药是作为取代有机氯农药而发展起来的新型农药,这种农药较有机氯农药容易降解,对自然环境的污染和生态系统的危害、残留没有有机氯农药普遍和持久。
但事实上,有机磷农药并不是理想高效、低毒、低残留农药,其在环境中的残留也不容忽视[2],并在动物体内富集[3]。
有机磷农药一般为硫代磷酸酯类或磷酸酯类化合物,大多呈结晶状或油状,工业品呈棕色或淡黄色,除敌敌畏和敌百虫之外,大多有蒜臭味。
这类农药除敌百虫、磷胺、甲胺磷、乙酰甲胺磷等易溶于水,其它不溶于水,易溶于有机溶剂如苯、丙酮、乙醚、三氯甲烷及油类。
有机磷农药分子结构一般具有容易断裂的化学键,在酸性和中性溶液中较稳定,遇碱易分解破坏,对光、热、氧均较稳定,略具挥发性,遇高热可异构化,加热遇碱可以加速分解。
有机磷农药是一种神经毒物,作用机制是抑制生物体内的乙酰胆碱酯酶,引起神经系统紊乱,并造成中毒。
另外,有机磷农药迟发性毒性还会对生殖系统造成损害。
印度北部Kanpur市,地表水中马拉硫磷含量达 2.618mg/L,地下水含量高达29.835mg/L[4]。
近年来,我国农药工业迅速发展,农药年产量居世界第二位。
其中,有机磷农药产量占全世界总量的1/3,占全国农药总量的50%以上[5]。
我国近年来用量最大的农药主要是甲拌磷、特丁硫磷、甲胺膦、氧乐果、丙溴磷、乐果、水胺硫磷、杀螟硫磷、辛硫磷、异稻瘟净、马拉硫磷、乙酰甲胺磷、甲基毒死蜱、毒死蜱、三唑磷、敌百虫、敌敌畏、草甘膦等有机磷农药产品年产量约占我国有机磷类农药总产量的90%以上[6]。
8.2相关环保标准和工作需要8.2.1 国内相关标准目前我国的各类环境质量标准和污染物排放标准中,除了危险废物毒性标准中有四种有机磷的排放限值,还没有土壤和沉积物中有机磷的相关质量和排放标准,详见表1。

土壤中磷的形态土壤作为植物生长的基础,其中的营养成分尤为重要。
磷素是土壤中极为重要的营养元素之一。
在土壤中,磷素主要以无机和有机形态存在,这些形态对植物吸收磷素具有不同的影响。
一、土壤中的磷素1. 有机磷有机磷是磷素的有机形态。
常见有机磷包括植物和动物残体、微生物、生物膜等。
有机磷含量较高,但大部分不易被植物直接吸收利用,需要通过微生物酶解等作用转化为无机磷才能为植物所用。
2. 无机磷无机磷是磷素的无机形态,包括三种主要形态:磷酸盐、磷酸根和铁、铝磷酸盐。
其中,可吸收的无机磷主要是磷酸盐和磷酸根,这两种形态是植物吸收磷素的主要来源。
二、磷在土壤中的运移1. 磷的吸附和解吸作用土壤中的矿物质、含铁、铝氧化物或有机质具有吸附磷的作用。
土壤酸化能加强磷的吸附。
然而,当土壤中磷含量过多时会导致溶解磷的释放,使土壤中可供吸收的磷素增加。
2. 土壤中的磷素迁移与消失磷素迁移过程包括表土侵蚀和土壤水质等,这些因素都可导致磷素的消失。
特别是在沿海地区,土壤中的磷素会被带到海洋中,影响海洋环境。
三、影响磷素吸收和利用的因素1. pH值土壤pH值越低,土壤中磷的溶解度就越高;pH值越高,则磷的溶解度越低。
2. 钾钾能够提高土壤中磷的含量,特别是在基质缺乏的土壤中,钾会提高磷的利用率。
3. 钙钙对植物吸收磷的影响主要是通过影响土壤pH值,改变磷的形态和吸收能力。
4. 营养元素平衡磷的吸收和利用与其他营养元素的平衡有密切关系,如氮素、钾素等。
总之,土壤中的磷形态会影响植物的吸收和利用,同时,也会受到土壤pH值、钾和钙等营养元素的影响。
了解这些因素有助于提高土壤中磷的利用率,促进植物健康生长。
土壤有机磷种类
答案:
土壤中的有机磷是指存在于腐殖质和其他有机物中的磷。
在成土过程中,随着土壤有机质的积累,土壤有机磷也随之形成,一般占土壤全磷的20-50%,已知组分的有机磷化合物主要有3类:植素类、核酸类、磷脂。
有机磷分级能够划分出不同性质的土壤有机磷化合物,较好地评价土壤有机磷对植物有效性的高低。
有机磷分级体系(Bowman-Cole法):①活性有机磷:为易矿化、易为植物吸收的组分,主要为核酸、核苷酸和甘油磷酸等;②中活性有机磷:较易矿化、较易为植物利用的组分;③中稳性有机磷:较难矿化、较难为植物利用的组分,主要为富里酸磷;④高稳性有机磷:难为植物利用的组分,主要为胡敏酸磷。
土壤有机磷组分测定(Bowman-Cole法)按土壤有机磷在不同浓度的酸碱溶液中的水解量,分成4组活性不同的有机磷:1.活性有机磷——碳酸氢钠溶液[c(NaHCO3)=0.5mol/L]提取的有机磷;2.中等活性有机磷——硫酸溶液[c(H2SO4)=1.0mol/L]和氢氧化钠溶液[c(H2SO4)=1.0mol/L]提取的有机磷;3.中等稳定性有机磷——富里酸磷:能溶于氢氧化钠溶液[c(NaOH)=0.5mol/L]在pH1~pH1.8的条件下不发生沉淀但难为植物吸收的磷;4.高稳定性有机磷——胡敏酸磷:能溶于氢氧化钠溶液[c(NaOH)=0.5mol/L],在pH1~pH1.8的条件下发生沉淀又难为植物吸收的磷。
一.仪器设备:分光光度计二.试剂:1.硫酸溶液[c(H2SO4)=1.0mol/L]:55ml浓硫酸(H2SO4,ρ=1.84g/cm3,分析纯)慢慢倒入500ml水中,冷却后定容1000ml。
2.氢氧化钠溶液[c(H2SO4)=1.0mol/L]:称取氢氧化钠(NaOH,分析纯)20g溶于500ml 水中,冷却,定容于1000ml。
3.碳酸氢钠溶液[c(NaHCO3)=0.5mol/L,pH8.5]:称取碳酸氢钠(NaHCO3,分析纯)42g 溶于水稀释至1L,用稀硫酸或氢氧化钠溶液调节pH至8.5。
(其余试剂同水中磷的测定)4.无水碳酸钠(Na2CO3,分析纯),磨细通过60孔筛。
5.硫酸溶液[c(1/2H2SO4)=6mol/L]:在800ml蒸馏水中缓慢加入浓硫酸(H2SO4,ρ=1.84g/cm3,分析纯)167ml,同时搅拌,待冷却后,加入蒸馏水定容到1000ml。
6.钼锑贮存溶液:浓硫酸(H2SO4,分析纯)153ml缓慢倒入约400ml蒸馏水中,同时搅拌,放置冷却。
另称10g钼酸铵([(NH4)6Mo7O24·4H2O,分析纯])溶于约60℃的300ml蒸馏水中,冷却。
文献综述内容摘要通过翻看这些文献和参考材料,了解土壤中有机磷分组测定的方法和目前研究达到程度。
找出自己实验研究的方向和如何能弥补目前研究的不足。
生物炭作为土壤改良剂,会增加土壤的吸收能力和生产能力,但是对土壤中有机磷的的分组的影响在各个地区是不一样的,本次实验主要是对沈阳和阜新的土壤进行实验,了解生物炭这种新型的土壤改良剂加入不同量时对不同土壤中总磷,无机磷和有机磷组分的影响,通过对空白组的对照,找出其中的规律,结合其他的微量元素的研究,更好的改良土壤情况,已达到增产增收的目的。
关键字:生物炭;有机磷;总磷;褐土;棕壤1 选题依据磷是植物生长发育必须的大量元素,植物体需要的磷主要是从土壤磷库中获得。
作为土壤磷库的重要组部分,土壤有机磷对土壤肥力和植物营养有着重要的影响;其对植物的作用愈来愈受到关注。
土壤有机磷经过矿化分解而转化为有效态磷,然后供给植物吸收利用。
在无机磷含量较低的土壤上,有机磷的矿化更成为植物吸收磷素的重要来源。
因此,对土壤有机磷进行研究,其重要性可想而知。
随着有机农业和生态学的发展,近年来土壤有机磷在植物营养中的作用日益受到重视。
人们对土壤有机磷的种类、数量和转化也随着研究方法的改善在不断地深入,并有了不少进展。
在土壤中,磷元素主要源于母质的特殊性,不像碳、氢、氧、氮等大部分来自大气,因此在成土过程中,随着土壤有机质的积累,土壤有机磷也随之形成。
土壤中的磷包括无机磷和有机磷两大部分,而有机磷在土壤磷库中占相当大的比例。
从世界范围的土壤看,有机磷在土壤中的比重大约占15%~80%。
我国大部分土壤有机磷占土壤全磷的20%~40%,且有逐年增加的趋势。
天然植被下土壤有机磷含量时常可占总磷量的一半以上,而黑土中的含量更高。
耕地土壤有机磷因为开垦的缘故,其含量时常比同类的自然土壤低一般来说,土壤表层有机磷含量较高,随着深度的增加,有机磷含量逐渐下降。
土壤有机磷含量因土壤母质、土壤类型、土壤特性、土壤质地、植被类型、气候季节变化及土地管理措施而不同。
一般认为,母质全磷量高,其土壤有机磷含量就高;母质全磷量低,其土壤有机磷含量就低。
从土壤类型来看,有机土和有机质土有机磷含量最高,软土和变性土有机磷含量居中,氧化土和某些灰化土有机磷含量最低。
土壤特性(包括土壤有机质量、全氮量和土壤pH等)对有机磷含量的影响比较复杂。
研究表明,土壤有机磷含量和土壤有机质(有机碳)及全氮量具有良好的相关性;酸性土壤含有较多的植酸铁、铝盐,易使有机磷形成沉淀,故酸性土壤比碱性土壤容易积累有机磷。
从土壤质地来看,粘粒、粉砂能够吸附有机磷,泥炭、腐泥的有机磷含量最高,壤质砂土、砂和细砂的有机磷含量最低。
一般来说,森林土壤和草地土壤由于腐殖质积累较多,因此有机磷含量较高。
季节和气候变化对有机磷的影响为:随着气温升高、雨量增加,土壤有机磷的含量上升;土壤有机磷含量因季节不同而呈现周期性变化。
现阶段由于我国对生物炭研究刚刚起步,对生物炭的农用研究较为薄弱。
虽然一些初步研究已展示了生物炭在改善土壤肥力、提高土壤炭库、减少氮素流失方面有较大的力(张文玲等,2009; 刘玉学等,2009;罗凯等,2007),但针对不同域土壤性质的差异,分析生物炭对不同类型土壤磷素的影响还没有系统的研究。
为了了解生物炭对土壤磷素有效性和失风险的影响,本文研究了生物炭在不同类型土壤中磷有效性转化的影响及量化关系和生物对外源磷在不同类型土壤中有效性转化的影响。
不仅为农田土壤科学的施用生物炭提供理论据,而且对提高生物炭的农田磷肥资源有效利用具有重大意义。
2 生物炭介绍生物炭是生物有机材料(也称为生物质)在无氧或低氧环境中低温热裂解后的固体产物。
传统工艺生产的炭大多为块状黑炭或颗粒黑炭,如木炭和竹炭。
现代热裂解工艺生产的生物炭为粉状颗粒。
生物炭通常含碳40%~75%,含少量矿物质和挥发有机化合物,呈碱性,不易为微生物分解。
生物炭的多孔性、巨大表面积及羧基基团赋予生物炭强吸附能力,对土壤具有很好的改良作用。
生物炭在增加土壤肥力,提高作物产量,还表现为:(1)生物炭等够显著提高土壤pH、改变土壤质地、增加盐基交换量,从而引起土壤CEC增加,提高植物对营养元素的吸收效果。
(2)生物炭能够有效调控土壤中营养元素的循环,促进作物对N、P 等元素的吸收。
(3)生物炭的多孔性和表面特性能够为微生物生存提供附着位点和较大空间,同时调控土壤微环境的理化性质,影响和调控土壤微生物的生长、发育和代谢,进而改善土壤肥力。
(4)生物炭能改变有毒元素的形态,降低有毒元素对作物以及对环境的危害,有助于植株正常发育。
3 国内外研究现状国内外许多学者先后提出了多种有机磷分级体系,它们是:1)Bowman-Cole提出的土壤有机磷分级体系及其修正体系;2)Ivanoff等提出的有机土有机磷分级体系;3)Hedley等提出的土壤磷素分级体系及其修正体系;4)Tiessen等提出的土壤磷素分级体系.其中,以1978年Bowman-Cole分级体系和1982年Hedley分级体系最为经典,但更多是采用Bow-man-Cole的分级方法.下面重点介绍这2种分组体系.按照Bowman-Cole法,土壤有机磷可分为4组:活性有机磷,易矿化易为植物吸收;中活性有机磷,较易矿化,同时也较易为植物吸收;中稳性有机磷,较难矿化,且较难为植物吸收;高稳性有机磷,很难矿化,基本不被植物吸收.贺铁等在水稻土上曾对该法进行了验证,结果表明该法具有可行性.而熊恒多和范也宽等则认为,上述方法对土壤有机磷提取不够充分,并且先酸后碱的浸提顺序使测定的中等活性有机磷的含量偏高,因此建议对土样进行用氯仿进行预处理之后,在提取中活性有机磷和稳性有机磷时,把先酸后碱的浸提顺序改为先碱后酸,并采用超声波技术缩短振荡时间和提高浸提效率.Fan等在酸性土壤上的研究指出,对NaOH浸提液进行调酸来分离高稳性有机磷和中稳性有机磷时,最适宜的pH为3.00.改进后的Bowman-Cole法,能显著地提高活性有机磷和稳定性有机磷含量,而中活性有机磷含量则明显下降,这可能与提取的顺序有关.在Hedley等的分级体系中,有机磷和无机磷被划分在不同的组分中,具体为:1)树脂-Pi;2)NaHCO3-P;3)微生物磷;4)NaOH-P;5)超声波/NaOH-P;6)HCl-Pi;7)残余-P.这个体系重要的特点是量化了在土壤循环和土壤磷的生物有效性中不可缺少的微生物磷数量.后来Potter等对该体系进行了修正.他们认为,风干土壤比田间湿润土壤含微生物磷少,在分组时对土样应进行湿润培养,以恢复微生物的活性;另外,由于研磨会使样品中部分微生物磷释放,从而使树脂-Pi增加;由CHCl3熏蒸处理得到的微生物细胞释放的有机磷和无机磷,被吸附到其他的组分中,不能通过NaHCO3浸提出来.由此可知,CHCl3/NaHCO3-P和NaHCO3-P之差可能有负值出现.他们认为,用熏蒸和未经熏蒸的土壤进行连续浸提而得到的浸提液,测定其所有组分含量,然后计算两种处理总含量之差,即为微生物磷含量.4 我的实验特点及展望每个实验都是受实验材料以及实验手法的影响的,因此每个实验也都是独一无二的,我的实验是通过对阜新沈阳两种土中加入不同类型不同量的生物炭,然后对其中的活性有机磷,中等活性有机磷,中稳性有机磷和高稳性有机磷通过浸提等方法,最后测定其吸光度,找出生物炭对其中的无机磷的影响到底是增加,减少还是无影响。
希望这次试验得出的趋势能够对阜新和沈阳地区的土壤改良有一定的指导性意义,并且能够更多的了解生物炭这种土壤改良剂对于本省的土壤的影响。
参考文献:1Agbenin JO, Iwuafor ENO, Ayuba B. 1999. A critical assessment of methods for determining organic phosphorus in savanna soils. Biol Fert Soils, 28: 177~181.2Borie1 F, Rubio R. 2003. Total and organic phosphorus in Chilean volcanic soils fosforo total Y fosforo organic en suelos volcánicos deChile.Gayana Bot, 60(1):69~783Bowman RA. 1989.A sequential extraction procedure with concen-trated sulfuric acid and dilute base for soil organic phosphorus.SoilSci Soc Am J, 53:362~3664Bowman RA,Moir JO. 1993.Basic EDTA as an extractant for soil organic phosphorus.Soil Sci Soc Am J, 57:1516~15185Brookes PC,Powlson DS,Jenkinson DS. 1982.Measurement of mi-crobial biomass phosphorus in soil.Soil Biol Biochem, 14:319~3296Dalal RC. 1977.Soil organic phosphorus.Adv Agron, 29:83~1177Fan Y-K(范业宽) ,Hu X-L(胡晓玲) ,Li S-J(李世俊). 1997.Modification of Bowman-Cole's method to extract stable organic phosphorus and moderately labile organic phosphorus from calcare-ous soil.J Huazhong Agric Univ(华中农业大学学报), 16(5):345~348(in Chinese)8Fan YK,Li SJ. 1998.Fractionation of moderately and highly stableorganic phosphorus in acid soil.Pedosphere, 8(3):261~2669Fen Y-H(冯跃华),Zhang Y-Z(张杨珠).2002.Research progresson the fraction of soil organic phosphorus.J Hunan Agric Univ(Nat Sci)(湖南农业大学学报·自然科学版), 28(3):259~264(in Chinese)10Giuffre L,Piccolo G,Rosell R,et al. 2001.Anthropogenic effect on soil organic phosphorus fractions in tropical munSoil Sci Plant, 32:1621~162811Harrap FEG. e of sodium EDTA in the determination of soil organic phosphorus.JSoil Sci, 14:82~8712Harrison AF. 1987.Trans.He N-Z(何念祖).1990.Soil organicphosphorus—Areview of world literature.Soil Prog(土壤学进展), 18(4):11~19(in Chinese)。