沙门氏菌原始记录表
- 格式:doc
- 大小:34.50 KB
- 文档页数:1
XXX中心
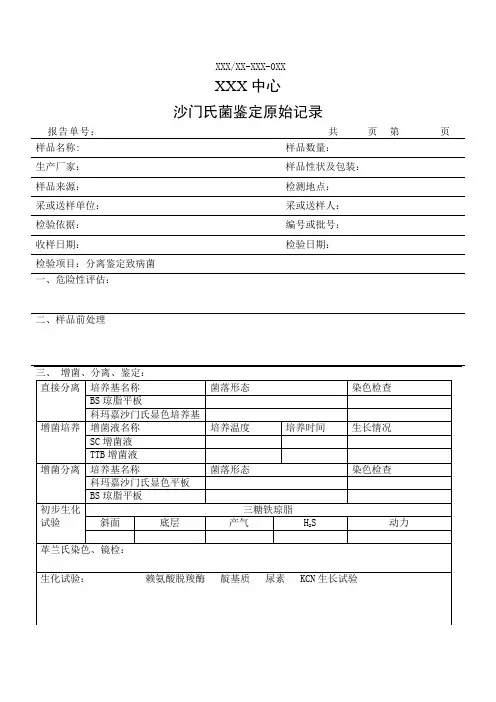
沙门氏菌鉴定原始记录
报告单号:共页第页样品名称: 样品数量:
生产厂家:样品性状及包装:
样品来源:检测地点:
采或送样单位:采或送样人:
检验依据:编号或批号:
收样日期:检验日期:
检验项目:分离鉴定致病菌
一、危险性评估:
二、样品前处理
共页第页
血清学凝集试验:
菌种处理:
终末消毒:
四、使用设备、标准菌株和主要试剂:
1、使用设备
恒温培养箱:
恒温培养箱:
显微镜:
高压蒸汽灭菌器:
生物安全柜:
2、标准菌种来源、菌号及代数
沙门氏菌标准菌株:
3、主要试剂、批号及配制记录
SC增菌液:
TTB增菌液:
BS琼脂平板:
科玛嘉沙门氏显色培养基:
三糖铁琼脂:
沙门氏菌诊断血清:
生化鉴定管:
五、检验结果
检毕时间年月日检测者:复核者:
XXX中心
沙门氏菌鉴定原始记录
报告单号:共页第页样品名称: 样品数量:
样品性状及包装:检测地点:
收样日期:检验日期:
检验依据: GB4789.4-2010
检验项目:分离鉴定沙门氏菌
一、样品前处理
用0.45um滤膜过滤500ml水样,将滤膜无菌手续剪碎,分别取适量滤膜进行如下操作。
共页第页
血清学凝集试验:
盐水对照:
沙门氏菌A-F多价O血清:
O4:
O5:
H多价2:
Hf:
三、检验结果
检毕时间年月日检测者:复核者:。
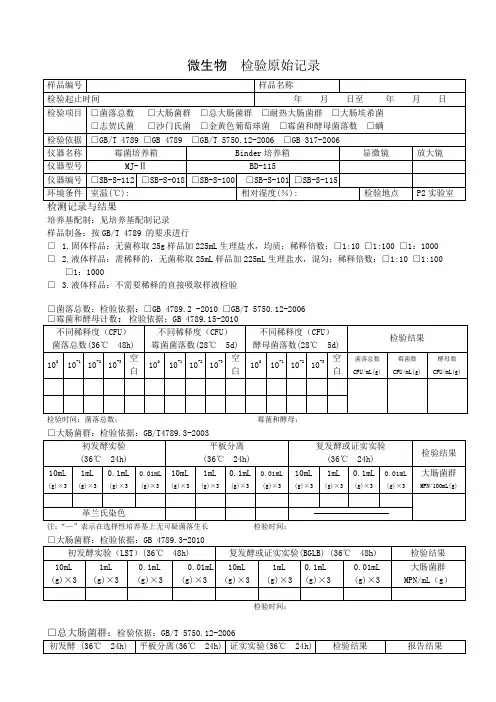
微生物检验原始记录
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进行
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
□大肠菌群:检验依据:GB/T4789.3-2003
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
□大肠菌群:检验依据:GB 4789.3-2010
检验时间:
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
□螨:检验依据 GB 317.4-.10-2006
检测人:复核人:。

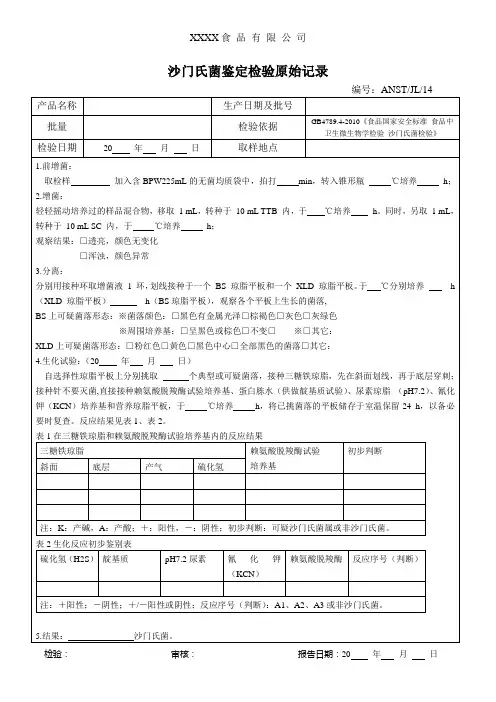
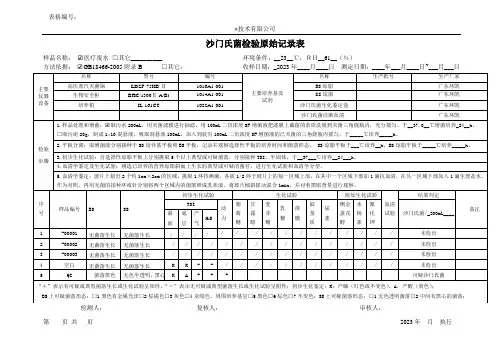
检验原始记录(沙门氏菌)样品编号:疾控检[201 ] 号_______________________________________________检验依据:《年国家食品污染和有害因素风险工作手册》___________ 检验项目:沙门氏菌_________一、培养基及试剂:1、缓冲蛋白胨水(BPVV:生产厂家____________________ 批号 _________________2、四硫磺酸盐煌绿增菌液(TTB):生产厂家 ___________ 批号 _________________3、亚硒酸盐胱氨酸增菌液(SC):生产厂家_____________ 批号 _________________4、沙门氏菌显色平板:生产厂家_________________ 配置日期 __________________5、BS平板:生产厂家 ___________________________ 配置日期 __________________6、三糖铁琼脂(TSI):生产厂家 _________________ 配置日期 _________________7、革兰氏染液:生产厂家___________________________ 批号 __________________&沙门氏菌属诊断血清:生产厂家______________________ 批号 __________________二、样品处理:无菌操作取检样g (mL加入盛有—BPW的无菌均质袋内,固体样品用拍击式均质器拍打1 mins 2min,制成1:10均匀稀释液备用。
液体样品不需均质,振荡混匀。
如需要,测定pH 值,用1mol/L无菌氢氧化钠或盐酸调pH至±。
冷冻产品,应在45C以下不超过15min或2Cs 5C不超过18h解冻。
三、实验记录:25g 检样+BPW225mL------------- BS显色培养基°C放入时间: 取出时间: C放入时间: 取出时间: C放入时间:取出时间:C放入时间:取出时间:C放入时间:取出时间:菌落形态观察1、菌落形态观察:SC转显色培养基:SC转BS平板:TTB转显色培养基:TTB转BS平板:2、鉴定:四、结果报告:沙门氏菌(/25 (g/mL)):检验者:复核者:。
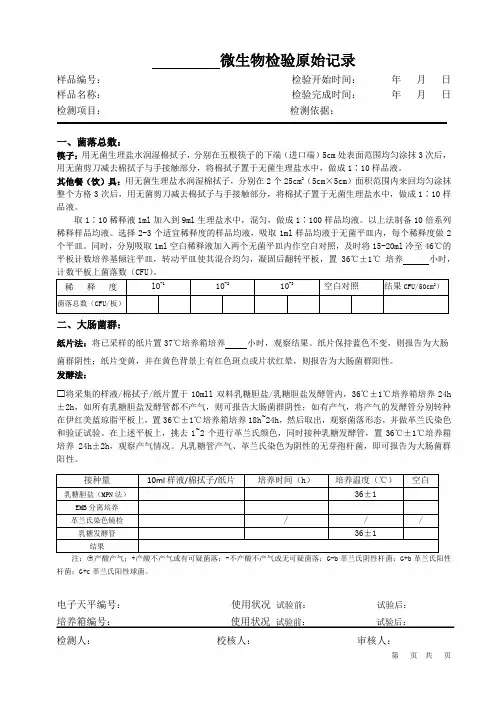
微生物检验原始记录样品编号:检验开始时间:年月日样品名称:检验完成时间:年月日检测项目:检测依据:一、菌落总数:筷子:用无菌生理盐水润湿棉拭子,分别在五根筷子的下端(进口端)5cm处表面范围均匀涂抹3次后,用无菌剪刀减去棉拭子与手接触部分,将棉拭子置于无菌生理盐水中,做成1∶10样品液。
其他餐(饮)具:用无菌生理盐水润湿棉拭子,分别在2个25cm2(5cm×5cm)面积范围内来回均匀涂抹整个方格3次后,用无菌剪刀减去棉拭子与手接触部分,将棉拭子置于无菌生理盐水中,做成1∶10样品液。
取1∶10稀释液1ml加入到9ml生理盐水中,混匀,做成1∶100样品均液。
以上法制备10倍系列稀释样品均液。
选择2-3个适宜稀释度的样品均液,吸取1ml样品均液于无菌平皿内,每个稀释度做2个平皿。
同时,分别吸取1ml空白稀释液加入两个无菌平皿内作空白对照,及时将15-20ml冷至46℃的平板计数培养基倾注平皿,转动平皿使其混合均匀,凝固后翻转平板,置 36℃±1℃培养小时,计数平板上菌落数(CFU)。
二、大肠菌群:纸片法:将已采样的纸片置37℃培养箱培养小时,观察结果。
纸片保持蓝色不变,则报告为大肠菌群阴性;纸片变黄,并在黄色背景上有红色斑点或片状红晕,则报告为大肠菌群阳性。
发酵法:将采集的样液/棉拭子/纸片置于10mll双料乳糖胆盐/乳糖胆盐发酵管内,36℃±1℃培养箱培养24h ±2h,如所有乳糖胆盐发酵管都不产气,则可报告大肠菌群阴性;如有产气,将产气的发酵管分别转种在伊红美蓝琼脂平板上,置36℃±1℃培养箱培养18h~24h,然后取出,观察菌落形态,并做革兰氏染色和验证试验。
在上述平板上,挑去1~2个进行革兰氏颜色,同时接种乳糖发酵管,置36℃±1℃培养箱培养24h±2h,观察产气情况。
凡乳糖管产气、革兰氏染色为阴性的无芽孢杆菌,即可报告为大肠菌群阳性。

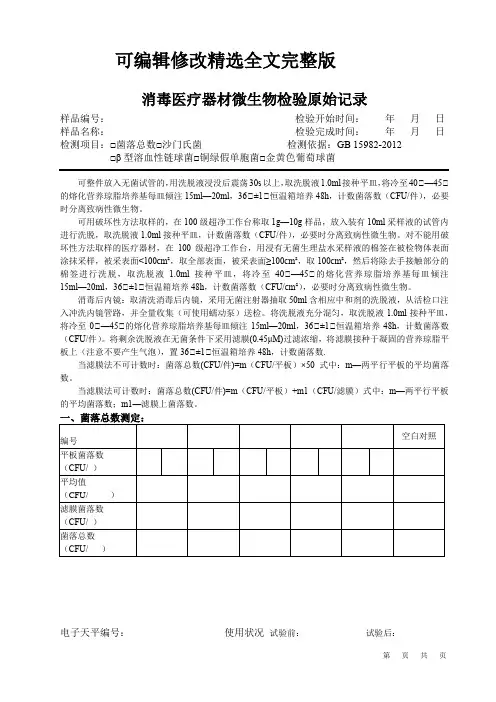
可编辑修改精选全文完整版消毒医疗器材微生物检验原始记录样品编号:检验开始时间:年月日样品名称:检验完成时间:年月日检测项目:□菌落总数□沙门氏菌检测依据:GB 15982-2012□β型溶血性链球菌□铜绿假单胞菌□金黄色葡萄球菌可整件放入无菌试管的,用洗脱液浸没后震荡30s以上,取洗脱液1.0ml接种平皿,将冷至40℃—45℃的熔化营养琼脂培养基每皿倾注15ml—20ml,36℃±1℃恒温箱培养48h,计数菌落数(CFU/件),必要时分离致病性微生物。
可用破坏性方法取样的,在100级超净工作台称取1g—10g样品,放入装有10ml采样液的试管内进行洗脱,取洗脱液1.0ml接种平皿,计数菌落数(CFU/件),必要时分离致病性微生物。
对不能用破坏性方法取样的医疗器材,在100级超净工作台,用浸有无菌生理盐水采样液的棉签在被检物体表面涂抹采样,被采表面<100cm²,取全部表面,被采表面≥100cm²,取100cm²,然后将除去手接触部分的棉签进行洗脱,取洗脱液 1.0ml接种平皿,将冷至40℃—45℃的熔化营养琼脂培养基每皿倾注15ml—20ml,36℃±1℃恒温箱培养48h,计数菌落数(CFU/cm²),必要时分离致病性微生物。
消毒后内镜:取清洗消毒后内镜,采用无菌注射器抽取50ml含相应中和剂的洗脱液,从活检口注入冲洗内镜管路,并全量收集(可使用蠕动泵)送检。
将洗脱液充分混匀,取洗脱液1.0ml接种平皿,将冷至0℃—45℃的熔化营养琼脂培养基每皿倾注15ml—20ml,36℃±1℃恒温箱培养48h,计数菌落数(CFU/件)。
将剩余洗脱液在无菌条件下采用滤膜(0.45μM)过滤浓缩,将滤膜接种于凝固的营养琼脂平板上(注意不要产生气泡),置36℃±1℃恒温箱培养48h,计数菌落数.当滤膜法不可计数时:菌落总数(CFU/件)=m(CFU/平板)×50式中:m—两平行平板的平均菌落数。
微生物检测原始记录一、目的本文档旨在规定微生物检测的原始记录格式和内容,以确保检测过程和结果的准确性和可追溯性。
二、记录格式1、记录纸张:使用A4纸,横向排列,页边距至少留有2cm。
2、记录标题:在页面顶部居中书写“微生物检测原始记录”。
3、日期和实验室名称:在页面右下角书写检测日期和实验室名称。
4、检测样品信息:在页面中部或适当位置填写样品信息,包括样品名称、编号、来源、处理方式等。
5、检测项目和指标:在页面中部或适当位置列出检测项目和指标,如菌落总数、大肠杆菌、沙门氏菌等。
6、检测方法和仪器:在页面中部或适当位置描述检测所采用的方法和使用的仪器设备。
7、检测结果记录:在页面中部或适当位置详细记录每个检测项目的实验数据,并确保数据准确、清晰、可追溯。
8、结论和建议:在页面底部或适当位置总结检测结果,并给出相应建议或处理意见。
9、检测人员签名:在页面右下角或适当位置由检测人员签名,以示负责。
10、备注:根据需要添加其他相关信息,如样品异常情况说明、引用标准、注意事项等。
三、记录内容1、样品信息:样品名称、编号、来源(如生产批次、产地等)、处理方式(如取样、前处理等)。
2、检测项目和指标:根据实际需要确定检测项目和指标,如菌落总数、大肠杆菌、沙门氏菌等微生物指标,以及可能的化学指标等。
3、检测方法:描述微生物检测所采用的方法,如国标法、第三方检测方法等。
同时应注明所用方法的版本号和发布机构。
4、仪器设备:列出在检测过程中使用的所有仪器设备的名称、型号、编号和使用状态等信息。
5、实验数据记录:详细记录每个检测项目的实验数据,包括观察结果、计数结果、吸光度值等。
数据应准确、清晰、可追溯,并附上必要的图表和曲线图。
6、结论和建议:根据检测结果给出相应的结论和建议,如是否符合标准要求,是否需要进一步处理或跟进等。
7、其他信息:根据需要添加其他相关信息,如样品异常情况说明、引用标准、注意事项等。
8、检测人员签名:由检测人员签名,以示负责。
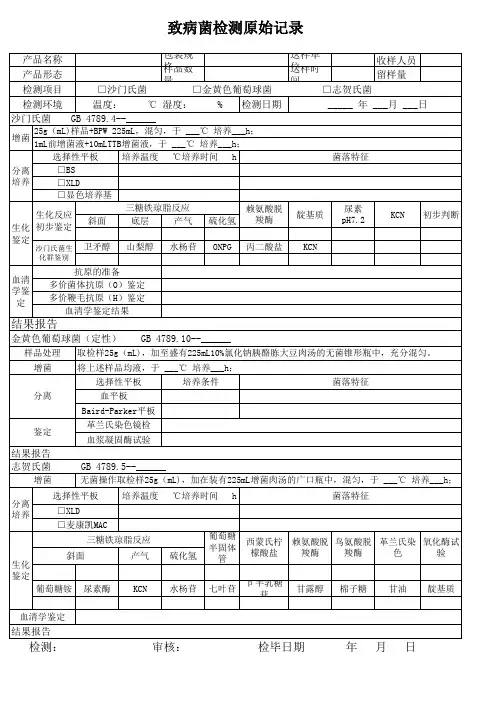
________疾病预防控制中心沙门氏菌检验原始记录共 页 第 页检验者: 审核者: 年 月 日样品编号样品名称检验依据 GB 4789.4-2010检验环境温度 ℃ 湿度 %RH检验日期仪器设备名称、规格型号、精度、编号电子天平: YP-1002 0.01g 105 有计量合格标识,并在检定有效期内. 恒温培养箱: DH6000 0.1℃ 88 有计量合格标识,并在检定有效期内.样品复苏 __月__日_____ 无菌操作,将待检样品磁珠置于10mL 无菌营养肉汤中37℃温育24h 复苏。
前增菌 __月__日_____按无菌操作取待检肉汤1mL ,加入到10 mL BPW 增菌液中,充分混匀,于36±1℃培养4h 。
增菌__月__日_____取1mLBPW 增菌液,转种于10mLSC 增菌液中,于36±1℃培养18~24h 。
检验项目现象结果 分离 培养BS 琼脂平板要求 36±1℃,40h-48h培养 ___日____时至__日____时。
HE 琼脂 平板 要求 36±1℃,18h-24h 培养 ___日____时至__日____时。
____显色平板 要求 36±1℃,18h-24h培养___日____ 时至__日___时。
生化 试验三糖铁琼脂要求 36±1℃,18h-24h 培养 ___日____时至__日____时。
普通琼脂平板 要求 36±1℃,18h-24h 培养 ___日____时至___日____时。
赖氨酸脱羧酶试验 API20E 生化试剂盒 要求 36±1℃,18h-24h 编码 结果 培养___日___时至___日___时。
血清学鉴定实验结果 样品中 沙门氏菌备注。
微生物检验原始记录
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进行
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
□大肠菌群:检验依据:GB/T4789.3-2003
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间:
□总大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
□螨:检验依据 GB 317.4-.10-2006
检测人:复核人:
微生物限度检验记录(复合膜)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:
微生物限度检验记录(铝箔、PVC硬片)
检验人:复核人:
微生物限度检验记录(半成品、成品)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:。
第 页,共 页
沙门氏菌检验原始记录表
检测员: 校核人: 审核人:
年 月 日 年 月 日 年 月 日
样品编号
检测类别
环境条件
温度: ℃ 湿度: %
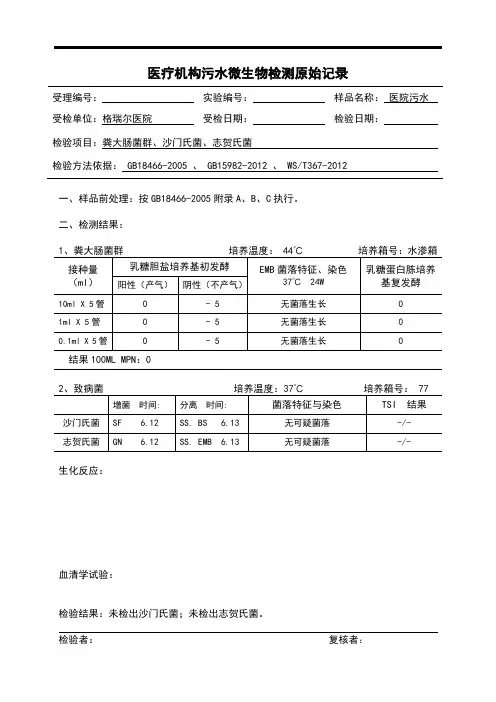
检测标准 医疗水污染物排放标准 医疗机构污水和污泥中沙门氏菌的检验方法 GB18466-2005 附录B
设备名称
设备编号
增菌
□ 污水 移取200mL 污水,用灭菌滤膜抽滤,用100mL 二倍浓度SF 增菌液将滤膜上的杂质洗脱到灭菌三角烧瓶中,摇匀。
37℃下培养12~24h
□ 污泥 称取20g 污泥,加200mL 灭菌水,制成1:10混悬液,移取100mL 混悬液,加入到装有100mL 二倍浓度SF 增菌液的已灭菌三角烧瓶中,摇匀。
37℃下培养24h
检验项目
现象
初判断
分离 培养
SS 培养基平板 37℃培养, h (24~48h )
BS 培养基平板 37℃培养, h (24~48h )
生化试验
表1 在TSI 试验培养基内的反应结果
TSI 培养基 37℃培养, h (18~24h )
初步判断
斜面 底层 产气 硫化氢
注:K :产碱,A :产酸;+:阳性,—阴性:初步判断:可疑沙门氏菌或非沙门氏菌。
表2 生化反应初步鉴定表
葡萄糖
甘露醇 麦芽糖
乳糖 蔗糖 靛基质 硫化氢 动力 尿素酶
注:+阳性;-阴性;+/-阳性或阴性
表3 补做试验(选做)
侧金盏花醇
水杨素 氰化钾
结果判断
注:+:阳性,-:阴性;结果判断:沙门氏菌或非沙门氏菌。
血清学鉴定
盐水 ,多价抗O 型抗血清( A-F ) 。
结果 mL 样品中 沙门氏菌 备注。