无水碳酸钠检验原始记录
- 格式:doc
- 大小:59.00 KB
- 文档页数:4

疾病预防控制中心(卫生监测检验中心)检验者:校核者:第页共页疾病预防控制中心(卫生监测检验中心)检验者:校核者:第页共页疾病预防控制中心(卫生监测检验中心)检验者:校核者:第页共页疾病预防控制中心(卫生监测检验中心)水质类检验原始记录检验者:校核者:第页共页疾病预防控制中心(卫生监测检验中心)水质类检验原始记录疾病预防控制中心(卫生监测检验中心)水质类检验原始记录检验者:校核者:第页共页疾病预防控制中心(卫生监测检验中心)水质类检验原始记录检验者:校核者:第页共页疾病预防控制中心(卫生监测检验中心)水质类检验原始记录检验者:校核者:第页共页GXCDC/QBG03-27-002疾病预防控制中心(卫生监测检验中心)检验者:校核者:第页共页GXCDC/QBG03-27-001疾病预防控制中心(卫生监测检验中心)水质类检验原始记录检验者:校核者:第页共页GXCDC/QBG03-27-002疾病预防控制中心(卫生检测检验中心)水质类检验原始记录检验者:校核者:第页共页GXCDC/QBG03-27-002疾病预防控制中心(卫生检测检验中心)水质类检验原始记录检验者:校核者:第页共页GXCDC/QBG03-27-002疾病预防控制中心(卫生检测检验中心)水质类检验原始记录检验者:校核者:第页共页GXCDC/QBG03-27-002疾病预防控制中心(卫生监测检验中心)水质类检验原始记录详细离子色谱仪记录附后。
标准、样品均进样20μL.。
检验者:校核者:第页共页GXCDC/QBG03-27-002疾病预防控制中心(卫生监测检验中心)水质类检验原始记录详细离子色谱仪记录附后。
标准、样品均进样20μL.。
检验者:校核者:第页共页GXCDC/QBG03-27-002疾病预防控制中心(卫生监测检验中心)详细离子色谱仪记录附后。
标准、样品均进样20μL.。
检验者:校核者:第页共页GXCDC/QBG03-27-002疾病预防控制中心(卫生监测检验中心)水质类检验原始记录详细离子色谱仪记录附后。

食品检验原始记录样品名称:样品编号:检验项目:过氧化值检验日期:检验依据:GB5009.227-2016(第一法)判定依据:/仪器名称仪器编号仪器溯值状态仪器使用记录电子天平000012020.06.10~2021.06.09 ///配制记录三氯甲烷-冰乙酸混合液(4+6):量取40mL三氯甲烷,加入60mL冰乙酸。
混匀即可;碘化钾饱和溶液:称取20g碘化钾,加入10mL新煮沸冷却的超纯水,摇匀后贮于棕色瓶中,放于避光处备用;(要确保溶液中有饱和碘化钾结晶存在)淀粉指示剂(1%):称取0.5g可溶性淀粉,加少量水调成糊状,边搅拌边倒入50mL沸水,再煮沸搅匀后,放冷备用,临用现配;硫代硫酸钠标准溶液(C=0.1mol/L):称取26g硫代硫酸钠,加0.2g无水碳酸钠,溶于1000mL 水中,缓缓煮沸10min,冷却。
放置两周后过滤,标定后使用;(具体标定方法详见GB/T 601-2016)或者购买有证书的硫代硫酸钠标准溶液直接使用;硫代硫酸钠标准使用液1(C=0.01mol/L):准确吸取10mL硫代硫酸钠标准溶液于100mL 容量瓶中,用新煮沸冷却的超纯水定容至刻度,摇匀即得;硫代硫酸钠标准使用液2(C=0.002mol/L):准确吸取20mL硫代硫酸钠标准使用液1于100mL容量瓶中,用新煮沸冷却的超纯水定容至刻度,摇匀即得;实验记录(样品制备过程应避免强光,并尽可能避免带入空气)样品前处理:食用氢化油、起酥油、代可可脂类食品:对液态样品,振摇装有试样的密闭容器,充分混匀后直接取样;对固态样品,选取有代表性的试样置于密闭容器中混匀后取样。
如有必要,将盛有固态试样的密闭容器置于恒温干燥箱中,缓慢加温到刚好使其融化,趁试样为液态时立即取样测定;人造奶油类食品:将样品置于密闭容器中,于60-70℃的恒温干燥箱中加热至融化,振摇混匀后,继续加热至破乳分层并将油层通过快速滤纸到烧杯中,烧杯中滤液即为待测样,(制备出的待测样应澄清)趁待测样为液态时立即取样测定;以小麦粉、谷物、坚果等植物性食品为原料,经油炸、膨化、烘烤、调制、炒制等加工工艺而制成的食品:从所取全部样品中取出有代表性样品的可食部分,在粉碎机中粉碎,将粉碎的样品置于广口瓶中。
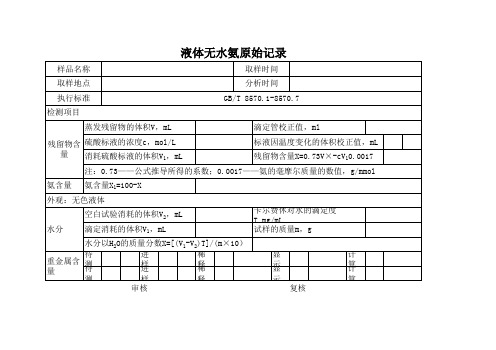

标准溶液的配置标定记录氢氧化钠标准滴定溶液的配置滴定记录① 配制:将氢氧化钠配成饱和溶液,注入塑料桶中密闭放置至溶液清亮,使用时用塑料管虹吸上层清液。
氢氧化钠标准溶液:量取毫升氢氧化钠饱和溶液,注入毫升不含二氧化碳的水中,摇匀。
② 标定:称取克于105℃--110℃电烘箱中干燥至恒重的工作基准试剂邻苯二甲酸氢钾,称准至0.0002克。
溶于毫升不含二氧化碳的水中,加2滴1酚酞指示液,用氢氧化钠溶液滴定至溶液呈粉红色,并保持30s。
同时做空白试验。
③ 计算:氢氧化钠标准滴定溶液的浓度[c(NaOH)],数值以摩尔每升(mol/L)表示,按下列公式计算:c(NaOH)=m 1000(V1 V2)M式中:m-----邻苯二甲酸氢钾的质量的准确数值,单位为克(g); V1----氢氧化钠溶液的体积的数值,单位为毫升(mL); V2---空白试验氢氧化钠溶液的体积的数值,单位为毫升(mL);M----邻苯二甲酸氢钾的摩尔质量的数值,单位为克每摩尔(g/mol)[M(*****4)= 204.22 ]容量分析原始记录检验:审核:检验日期:① 配制:盐酸标准溶液,量取毫升盐酸,注入毫升水中。
② 标定:称取克于270℃--300℃高温炉中灼烧至恒重的工作基准试剂无水碳酸钠,称准至0.0002克。
,溶于50mL水中,加10滴溴甲酚绿一甲基红指示液,用配制好的盐酸溶液滴定至溶液由绿色变为暗红色,煮沸2min,冷却后继续滴定至溶液再呈暗红色,同时做空白试验。
③ 计算:盐酸标准滴定溶液的浓度[c(HCl)]数值以摩尔每升(mol/L)表示,按下列公式计算:c(HCl)=m 1000(V1 V2)M式中:m----无水碳酸钠的质量的准确数值,单位为克(g) V1---盐酸溶液的体积的数值,单位为毫升(mL)V2---空白试验盐酸溶液的体积的数值,单位为毫升(mL) M---无水碳酸钠的摩尔质量的数值,单位为克每摩尔(g/mol)[M (12 Na2CO3)=52.994]容量分析原始记录检验:审核:检验日期:① 配制:硫酸标准溶液,量取毫升硫酸,注入毫升水中。

标准溶液‘配制’及‘标定’原始记录标准溶液编号:有效期:温度修正系数f(mL/L) (GB/T 601-2002 附录A)溶液体积 V(mL)CB(mol/L)平均值(mol/L)计算式:V=(V1-V0)×(1+f/1000)CB=1000m/(M×V)说明:每次滴定必须从“0”开始备注:配制人:标定:复标:审核:标准物质配制(标定)记录编号: CHEC/QBG-075名称:、配制方法:使用天平型号编号室温℃、湿度 %RH配制:取定溶 mL标定:取份:⑴⑵⑶⑷用溶液滴定,滴定消耗量(mL)V1= 、V2= 、V3= 、V4= 、V0= 。
标准溶液浓度计算公式:C=计算结果():C1= C2= C3= C4= C =相对偏差(%):S1= S2= S3= S4=备注:。
配制人:复核人:配制日期:年月日有效期年月日标准溶液配制记录编号: CHEC/QBG-147标准溶液名称:规格:配制方法:仪器名称:溯源标准:温度:℃ 、湿度: %RH 标准溶液拟配浓度:配制或稀释过程:配制日期:年月日有效期:年月日配制人:复核人:0.1mol/L盐酸标准滴定溶液的标定编号:JL/LJ-001-01一、标定方法:GB/T5009.1-2003二、使用仪器:AEL-200电子天平(仪器编号:JYB001)马弗炉(仪器编号:JYC009)三、操作1、量取9ml盐酸,加适量水并稀释至1000ml。
混匀,待标定。
2、标定:精密称取约0.15g在270~300℃干燥至恒量的基准无水碳酸钠,加50ml水使之溶解,加10滴溴甲酚绿-甲基红混合指示液,用本溶液滴定至溶液由绿色转变为紫红色,煮沸2min,冷却至室温,继续滴定至溶液由绿色变为暗紫色。
四、记录和结果1、计算公式:c(HCl)=m/[(V1-V2)×0.0530]0.0530……与1.00ml盐酸标准滴定溶液[c(HCl)=1mol/L]相当的基准无水碳酸钠的质量,g2、数据配制人:复核人:配制日期:复核日期:稀释记录表标准溶液(滴定液)管理工作的基本要求关键词(必填项目):标准溶液、滴定液目的(必填项目):对标准溶液的使用等制定统一的要求,便于统一的管理。
《无机化工产品品质检验》课程项目报告-个人工作页无机化工产品品质检验个人工作过程工作页项目名称:工业碳酸钠产品品质检验项目组:质检员:项目完成时间:始年月日终年月日项目编号:gf12-4项目四:工业碳酸钠产品品质检验任务4.1接受检验任务学生个人作品1⏹学生个人作品2样品交接单⏹学生个人作品3品质检验的工作任务表4.2检测碳酸钠产品中主含量一、工业碳酸钠主含量检验方案1、方法提要2、方法原理3、操作步骤4、注意事项☆方案的解析方案的解析(续)二、检验前准备单1.药品准备单2.仪器准备单3.溶液准备单主含量检测原始记录单HCl标准溶液标定原始记录总碱量测定原始记录主含量检测报告单任务4.3检测碳酸钠产品中原料残留氯化物含量原料残留氯化物含量检验的方案一、工业碳酸钠产品中原料残留氯化物含量检验方案1、方法提要2、方法原理3、操作步骤4、注意事项☆方案的解析二、检验前准备单1.药品准备单2.仪器准备单3.溶液准备单原料残留氯化物含量检测原始记录单AgNO3标准溶液标定原始记录氯化物测定原始记录原料残留氯化物含量检测报告单4.4 检测碳酸钠产品中杂质硫酸盐含量杂质硫酸盐含量检验的方案一、工业碳酸钠产品中杂质硫酸盐含量检验方案1、方法提要2、方法原理3、操作步骤4、注意事项☆方案的解析二、检验前准备单1.药品准备单2.仪器准备单3.溶液准备单杂质硫酸盐检测原始记录单硫酸盐测定原始记录四、数据处理五、硫酸盐检测报告单4.5归纳总结,撰写报告项目检验结果分析与总结1、操作过程出现的问题、现象及解决方法分析讨论2、知识拓展内容、课后学习内容解答记录3、项目实施总结检验报告单表1:项目总成绩表注:满分100分。
项目成绩=个人成绩*70%+团队成绩*30%表2:个人项目成绩汇总表注:满分100分。
每项成绩中,自评占10%,同行评价占20%,教师评价占70%。
表3:个人项目成绩评分标准。
无水碳酸钠
本试剂为白色粉末,暴露于空气中逐渐吸水成为一水合物,溶于水,不溶于乙醇。
分子式: Na2CO3分子量:105.99 ( 按1 9 8 3 年国际原子量)
1 技术要求
1.1 Na2CO3含量不少于:99.8%
2. 试验方法
测定中所需标准溶液、杂质标准液、制剂及制品按GB 601-77 《化学试剂标准溶液制备方法) ) .
G B 6 0 2 -7 7《化学试剂杂质标准液制备方法) ) . GB 603-77《化学试剂制剂及制品制备方法》之规定制备。
2.1 Na2CO3含量测定:
称取2 g 预先于300 ℃干燥恒重的样品,称准至0.0002 g ,溶于50 ml水中,加10滴澳溴甲酚绿一甲基红混合指示液,用1 N盐酸标准溶液滴定至溶液由绿色变为暗红色,煮沸2 min ,冷却,继续滴定至溶液呈暗红色。
:
Na2CO3的百分含量 ( X)按下式计算。
无水碳酸钠含量的实验结果引言:无水碳酸钠,化学式为Na2CO3,是一种无水物质,也是很多实验室中常用的化学试剂。
了解无水碳酸钠的含量对于实验的准确性和结果的可靠性至关重要。
本实验旨在通过一系列实验步骤来测定无水碳酸钠的含量,并得出准确的结果。
实验步骤:1. 预备工作在进行实验之前,首先需要准备好实验所需的仪器和试剂,包括天平、锥形瓶、滴定管、酚酞指示剂和稀硫酸等。
同时,需要保证实验环境的清洁和无尘,以避免外界物质的干扰。
2. 确定标准溶液需要制备一定浓度的标准溶液,用于与待测样品进行滴定反应。
可以选择氯化钠作为标准溶液,浓度可以根据实验需要进行调整,一般为0.1mol/L。
制备标准溶液时,需要精确称取一定质量的氯化钠,并溶解在适量的去离子水中。
3. 处理待测样品将待测样品(无水碳酸钠)称取一定质量,并溶解在适量的去离子水中,得到一定体积的样品溶液。
注意,在称取样品时要避免外界水分和杂质的污染,以确保实验结果的准确性。
4. 滴定反应将待测样品溶液与标准溶液进行滴定反应。
首先,将样品溶液倒入锥形瓶中,加入几滴酚酞指示剂,使溶液变成粉红色。
然后,用滴定管滴加标准溶液,直至溶液颜色由粉红色变为无色。
记录滴定所需的标准溶液体积,即可计算出无水碳酸钠的含量。
5. 数据处理根据实验所得的滴定体积和标准溶液的浓度,可以通过化学计算方法来计算出无水碳酸钠的含量。
具体计算公式如下:含量(mol/L)=标准溶液浓度(mol/L)×滴定体积(mL)/样品溶液体积(L)结果与讨论:根据实验所得的数据和计算结果,可以得出无水碳酸钠的含量。
通过多次实验的平均值和标准差,可以进一步确定结果的准确性和可靠性。
同时,还可以与其他实验室或文献中的数据进行比对,以验证实验结果的正确性。
结论:通过本实验的实验步骤和数据处理,成功测定出了无水碳酸钠的含量。
实验结果的准确性和可靠性对于后续的实验工作和结果的解释具有重要意义。
通过进一步的研究和实验,可以进一步探索无水碳酸钠在化学反应和实验中的应用价值,并为相关领域的研究提供参考和借鉴。
无水硫酸钠(玄明粉)检验记录文件编号:QB-D-QD-SOP-0361.性状本品结果判定:检验人/日期:复核人/日期:4.2 铁盐与锌盐天平编号:取本品 g,加水20ml溶解后,加硝酸(编号:)2滴,煮沸5分钟,滴加氢氧化钠试液(编号:)中和,加稀盐酸(编号:)1ml、亚铁氰化钾试液(编号:)1ml与适量的水使成50ml,摇匀,放置10min,观察(不得发生浑浊或显蓝色)。
结果判定:检验人/日期:复核人/日期:4.3 镁盐取本品1g,加水20ml溶解后,加氨试液(编号:)与磷酸氢二钠试液(编号:)各1ml, (5min内不得发生浑浊)。
结果判定:检验人/日期:复核人/日期:4.4重金属A管:量取2.0ml铅标准溶液(编号:)于25ml纳氏比色管中,加入2mlpH3.5的乙酸盐缓冲溶液(编号:),加水至25ml混匀,备用。
B管:取1支与A管配套的纳氏比色管,加入1.0g试样,加入2mlpH3.5的乙酸盐缓冲溶液(编号:),加水至25ml,混匀,备用。
C管:取1支与A、B管配套的纳氏比色管,加入与B管相同质量的试样,再加入与A管等量的铅标准溶液(编号:)和2mlpH3.5的乙酸盐缓冲溶液(编号:),加水至25ml,混匀,备用。
向各管加入2ml硫代乙酰胺试液(编号:),混匀,于暗处放置2min后,在白色背景下观察, (B 管的色度不得深于A 管的色度,C 管的色度应与A 的色度相当或深于A 管的色度。
)结果判定:检验人/日期: 复核人/日期:4.5 含量测定天平编号: 马弗炉编号:水浴锅编号:取本品,置105℃干燥至恒重后,取 g,精密称定,加水200ml 溶解后,加盐酸(编号: )1ml,煮沸,不断搅拌,并缓缓加入热氯化钡试液(编号: )(约20ml ),至不在生成沉淀,置水浴上加热30min ,静置1h ,用无灰滤纸或称定重量的古氏坩埚滤过,沉淀用水分次洗涤,至洗液不在显氯化物的反应,干燥,并炽灼至恒重 ,精密称定,与0.6086相乘,即得供试品中含有硫酸钠的重量 。