钢中锰含量的测量
- 格式:doc
- 大小:13.00 KB
- 文档页数:3
实验钢中锰含量(w Mn)的测定一、实验导读1.钢材的化学成分钢铁是由多种元素组成的合金,除铁元素外,普通钢材中还含有碳、硅、锰等元素。
而合金钢则可能含有铬、钛、镍、铝、钒等元素。
钢材中通常还有硫、磷等有害元素,需要严格控制其含量。
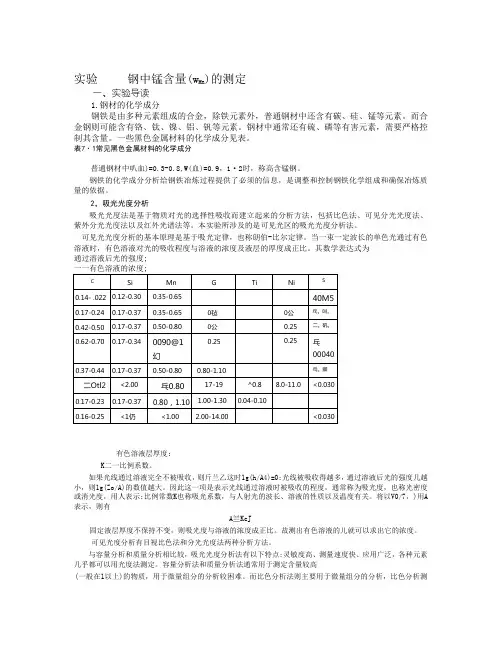
一些黑色金属材料的化学成分见表。
表7·1常见黑色金属材料的化学成分普通钢材中叭血)=0.3-0.8,W(血)=0.9,1·2时,称高含锰钢。
钢铁的化学成分分析给钢铁冶炼过程提供了必须的信息,是调整和控制钢铁化学组成和确保冶炼质量的依据。
2,吸光光度分析吸光光度法是基于物质对光的选择性吸收而建立起来的分析方法,包括比色法、可见分光光度法、紫外分光光度法以及红外光谱法等。
本实验所涉及的是可见光区的吸光光度分析法。
可见光光度分析的基本原理是基于吸光定律,也称朗伯-比尔定律。
当一束一定波长的单色光通过有色溶液时,有色溶液对光的吸收程度与溶液的浓度及液层的厚度成正比。
其数学表达式为通过溶液后光的强度;有色溶液层厚度;K二一比例系数。
如果光线通过溶液完全不被吸收,则斤兰乙这时1g(h/A4)=0;光线被吸收得越多,通过溶液后光的强度几越小,则1g(Zo/A)的数值越大。
因此这一项是表示光线通过溶液时被吸收的程度,通常称为吸光度,也称光密度或消光度,用人表示;比例常数K也称吸光系数,与人射光的波长、溶液的性质以及温度有关。
将以V0/7,)用A 表示,则有A兰KcJ固定液层厚度不保持不变,则吸光度与溶液的浓度成正比。
故测出有色溶液的儿就可以求出它的浓度。
可见光度分析有目视比色法和分光光度法两种分析方法。
与容量分析和质量分析相比较,吸光光度分析法有以下特点:灵敏度高、测量速度快、应用广泛,各种元素几乎都可以用光度法测定。
容量分析法和质量分析法通常用于测定含量较高(一般在1以上)的物质,用于微量组分的分析较困难。
而比色分析法则主要用于微量组分的分析,比色分析测量物质的浓度一般为10",-10"6ml·L"1(相当于0·叨1-0·0叨 1)。

实验报告钢铁中锰含量的测定——银盐氧化光度法班级:应111-1姓名:王海花学号:201169503147指导老师:王老师一.实验目的:1.通过实验,了解钢铁中锰的存在形式,测定意义。
2.了解测定钢铁中锰含量的测定方法。
3.掌握钢铁中锰含量的测定原理。
4.熟练掌握分光光度计的使用,进一步训练移液管、容量瓶的正确使用。
5.掌握用比色法测定钢材中锰含量的方法二.实验原理:1.锰在钢铁中主要以MnC、MnS、FeMnSi或固溶体状态存在。
生铁中一般含锰0.5%~6%,普通碳素钢中锰含量较低,含锰0.8%~14%的为高锰钢,含锰12%~20%的铁合金称为镜铁,含锰60%~80%的铁合金称为锰铁。
2.锰溶于稀酸中,生成锰(Ⅱ)。
锰化物也很活泼,容易溶解和氧化。
在化学反应中,由于条件的不同,金属锰可部分或全部失去外层价电子,而表现出不同的价态,分析上主要有锰(Ⅱ)、锰(Ⅲ)、锰(Ⅳ)、锰(Ⅶ),少数情况下亦有锰(Ⅵ),这就为测定锰提供了有利条件。
3.常用测定方法:一般碳素钢,低合金钢,生铁试样常以HNO3(1+3)或硫磷混酸溶解。
难溶的高合金钢以王水溶解,加HClO4或H2SO4冒烟溶解。
溶解试样的酸主要依靠H2SO4,HCl,HNO3,因H2SO4-HCl可使MnS分解。
HNO3分解碳化物(Mn3C)生成CO2逸出,加磷酸可使Fe3+配合成无色而消除Fe3+的干扰。
同时因为磷酸的存在,防止了MnO2沉淀的生成和HMnO4的分解。
4.主要反应方程式:3MnS+12HNO3=3Mn(NO3)2+6HNO3+3SO2+6H2O3Mn3C+28HNO3=29Mn(NO3)2+3CO2+10NO+14H2OMnS+H2SO4=MnSO4+H2S2AgNO3+(NH4)2S2O8=Ag2S2O8+2NH4NO3Ag2S2O8+2H2O=Ag2O2+2H2SO45Ag2O2+2 Mn(NO3)2+6HNO3=2HMnO4+10AgNO3+2H2O三.实验仪器及试剂:1.实验仪器:721型分光光度计,分析天平,容量瓶(50mL),移液管(1ml,2ml,3ml),滴管,洗耳球,电炉2.实验试剂:硝酸溶液(1:3),王水(1浓硝酸+3浓盐酸)硫磷混酸(700ml水中加入150ml磷酸及硫酸150ml,摇匀),0.5%硝酸银溶液,20%过硫酸铵溶液,5%EDTA,锰标准溶液(0.1mg/ml)四.实验步骤:1.溶样:钢样0.2630g于50ml烧杯,加5mlH2O,15ml王水溶解,(可稍热)2mlHClO4加热至冒白烟2min冷却,加硫磷混酸10ml加热至冒白烟,除尽Cl-冷却,定量转移至50ml容量瓶定容,摇匀,备用。

钢铁中锰含量的测定方法在咱们的日常生活中,钢铁无处不在,真是个“大块头”,可不管是家里的锅碗瓢盆,还是城市的高楼大厦,它们背后都少不了锰这个小家伙的身影。
说到锰,很多人可能会想,这东西到底有什么用?简单来说,锰能提升钢铁的硬度和韧性,让钢铁更加坚固耐用。
今天我们就来聊聊怎么测定钢铁中锰的含量,别担心,我会把这事儿说得简单明了,让你听得懂,甚至还可能会忍不住哈哈大笑。
1. 锰的“身世”背景1.1 什么是锰?首先,咱们得搞清楚锰是个啥玩意儿。
锰(Mn)是一种金属元素,虽然它听起来有点陌生,但它在钢铁中的地位可是相当高的哦。
想象一下,如果把钢铁比作一个超级英雄,锰就是它的“助力神器”,让它在打斗中更加强壮有力。
没有锰,钢铁就像是没了超能力的英雄,任人宰割。
1.2 锰的作用锰不仅提升了钢铁的抗拉强度,还能改善它的抗氧化性能。
这就像是在给钢铁穿上了一件防弹衣,让它在风雨中也能挺立不倒。
而且,锰还对钢铁的成型和焊接有很大的帮助,这可真是太重要了,钢铁生产可离不开它!2. 如何测定锰含量2.1 准备工作接下来,我们就要进入正题,开始测定钢铁中锰的含量了。
首先,我们得准备一些工具,听上去有点像科学实验,但其实没那么复杂。
你需要的主要有试管、试剂、还有一个电子天平,别忘了保护眼睛的护目镜,安全第一,毕竟咱可不想给自己来个“惊心动魄”的实验场面。
2.2 测定步骤1. 取样:从钢铁中取一小块样品,这就像从蛋糕上切一块,确保它的“内心”也是充满了锰。
2. 溶解:将样品放入酸中溶解,这一步是为了让锰从钢铁的“牢笼”里逃出来,露出真实的身姿。
3. 反应:加入特定的试剂,锰会和它发生反应,产生颜色变化。
这就像魔术表演,等着看这神奇的一刻。
4. 测量:最后,使用分光光度计测量颜色的深浅,通过标准曲线来计算锰的含量。
这一刻,就像侦探解谜一样,谜底即将揭晓。
3. 注意事项与总结3.1 注意事项在进行测定的时候,有几点需要特别注意。

组别:成员:
钢铁中锰含量的测定
一、母液制备:
试剂:a、硝酸:1+3、b、过硫酸铵:10%。
操作步骤:称取100 mg试样于100ml钢铁量瓶中,加20ml预热的硝酸,待试样基本溶解后,加10ml过硫酸铵,低温加热至大气泡,取下流水冷却至室温,用水定容、摇匀。
二、锰的测定:过硫酸铵氧化光度法。
试剂:a、硝酸银溶液:0.1% (用1+4的硝酸配制)
b、过硫酸铵溶液:10%
分析操作:
1、溶样及显示
准确移取母液5.0ml于100ml钢铁量瓶中,加入10ml硝酸银溶液,10ml过硫酸铵溶液,加热至冒小气泡、取下、流水冷至室温,以水定容。
2、测定
摇匀后,于530nm,1-2cm比色杯,水作参比,以标样同上操作,作检量线(以下同)。
三、填写结果,完成质检报告单(背面)
莱芜市金威新材料有限公司质检报告单。

一、实验目的1. 学习并掌握钢中锰含量的测定方法。
2. 熟悉使用分光光度法测定试样浓度的基本操作。
3. 了解混合酸在钢中锰含量测定中的作用。
二、实验原理钢中锰含量的测定主要基于比色法,通过分光光度法测定试样溶液中锰离子的浓度。
锰离子在特定条件下,其溶液的颜色深度与浓度成正比。
实验中,常用的方法是将锰离子还原为低价态,再通过特定的显色反应,使溶液呈现一定的颜色,利用分光光度计测定其吸光度,从而计算出锰的含量。
三、实验仪器与试剂1. 仪器:- 分光光度计- 移液管- 容量瓶- 比色管- 滴定管- 磁力搅拌器- 电子天平2. 试剂:- 硫酸(H2SO4)- 硝酸(HNO3)- 混合酸(硫酸与硝酸按一定比例混合)- 还原剂(如草酸)- 锰标准溶液- 染料(如邻苯二酚)- 水为去离子水四、实验步骤1. 样品准备:准确称取一定量的钢样,加入适量的混合酸,在磁力搅拌器上加热溶解。
2. 氧化处理:将溶解后的样品溶液在加热条件下,加入适量的氧化剂,使锰离子氧化为高价态。
3. 显色反应:在酸性条件下,加入还原剂将高价态锰离子还原为低价态,再加入染料,使溶液呈现一定的颜色。
4. 吸光度测定:将显色后的溶液用分光光度计测定吸光度。
5. 标准曲线绘制:配制一系列已知浓度的锰标准溶液,分别测定其吸光度,绘制标准曲线。
6. 计算锰含量:根据实验测得的吸光度,从标准曲线上查得对应的锰离子浓度,进而计算出钢中锰的含量。
五、实验结果与分析1. 标准曲线绘制:根据实验数据绘制标准曲线,发现吸光度与锰离子浓度呈良好的线性关系。
2. 钢中锰含量的测定:根据实验测得的吸光度,从标准曲线上查得锰离子浓度,计算出钢中锰的含量。
3. 混合酸的作用:实验中发现,使用混合酸可以有效提高锰离子的氧化率和显色反应的灵敏度。
硫酸在混合酸中起到稳定溶液pH值的作用,硝酸则具有氧化性,有助于锰离子的氧化。
六、实验结论1. 本实验采用分光光度法测定钢中锰含量,操作简便,结果准确。


一、实验目的1. 了解锰在钢铁中的存在形式及其测定意义。
2. 掌握用比色法测定钢材中锰含量的原理和方法。
3. 熟练掌握分光光度计的使用,以及移液管、容量瓶等实验仪器的正确操作。
二、实验原理锰在钢铁中主要以固溶体状态存在,根据锰含量的不同,可将钢铁分为高锰钢、锰铁等。
锰溶于稀酸中,生成锰离子。
在化学反应中,金属锰可表现出不同的价态,分析上主要有锰(II)、锰(III)、锰(V)等。
本实验采用比色法测定钢材中锰含量,通过分光光度计测定锰离子的吸光度,进而计算出锰含量。
三、实验仪器及试剂1. 实验仪器:- 型分光光度计- 分析天平- 容量瓶- 移液管- 吸量管- 滴管- 洗耳球- 电炉2. 实验试剂:- 硝酸溶液- 王水- 浓硝酸- 浓盐酸- 硫磷混酸(水中加入磷酸及硫酸,摇匀)- 硝酸银溶液- 过硫酸铵溶液- 锰标准溶液(锰含量已知)四、实验步骤1. 准备标准溶液:根据锰含量,配制一系列已知浓度的锰标准溶液。
2. 样品预处理:将待测样品用王水溶解,加入适量的硫磷混酸,煮沸后冷却至室温。
3. 比色:取一定量的样品溶液,加入过量的硝酸银溶液,使锰离子与银离子反应生成白色沉淀。
将沉淀过滤、洗涤、干燥,称量其质量。
4. 标准曲线绘制:将标准溶液按照相同步骤进行处理,绘制标准曲线。
5. 样品测定:将样品溶液按照比色步骤进行处理,测定其吸光度。
6. 计算锰含量:根据样品溶液的吸光度,从标准曲线上查得对应的锰含量,计算样品中锰的含量。
五、实验结果与分析1. 标准曲线绘制:根据实验数据,绘制标准曲线。
2. 样品测定:将样品溶液进行比色,测定其吸光度。
3. 计算结果:根据样品溶液的吸光度,从标准曲线上查得对应的锰含量,计算样品中锰的含量。
4. 结果分析:将实验测定的锰含量与理论值进行比较,分析误差来源。
六、实验结论通过本次实验,掌握了用比色法测定钢材中锰含量的原理和方法。
实验结果表明,该方法具有较高的准确度和可靠性,为钢铁生产中锰含量的质量控制提供了技术支持。


钢铁中锰含量的测定实验报告实验目的:通过重量分析法测量给定钢锭中锰的含量。
实验原理:锰是钢铁中的常见合金元素,它能够使钢具有良好的硬度和韧性,同时还能提高钢的耐磨损性和抗腐蚀性能。
因此,锰合金钢在工业生产中使用较为普遍。
本实验采用浓硝酸将样品中的锰完全溶解,然后再通过比色法来测量其浓度,从而计算出样品中锰的含量。
实验仪器和药品:1.恒重天平2.分析天平3.酸洗玻璃器皿4.密码锁保险柜5.2N硝酸6.去离子水7.KMnO₄(二氧化锰)8.FeSO₄(硫酸亚铁)9.H₂SO₄(硫酸)实验步骤:1.在恒重天平上称取约1克左右的样品(钢锭)。
2.将样品加入酸洗玻璃器皿中,加入足量的2N硝酸,并将其密封。
3.将加有样品的酸洗玻璃器皿放入加热器中进行加热,直至样品完全溶解。
4.在加热的过程中,用分析天平称取一定比例的KMnO₄和FeSO₄,分别放置于两个玻璃烧杯内备用。
5.将一定量的去离子水加入玻璃烧杯中,然后分别加入已称好的KMnO₄和FeSO₄,搅拌均匀,使其完全退色。
6.将上述溶液依次加入原样中,使其达到定容(一般为100ml)。
7.将上述溶液振荡均匀,并取一定体积的样品(一般为25ml)加入2N硝酸校正瓶中,制成样品稀释液。
8.取校正瓶中的样品稀释液,用比色管进行比色,测定其AB值。
9.参照比色管上的色板,找到对应的AB值,根据铁漏斗的倒数和样品稀释液的配比,计算出样品中锰的含量。
实验结果:在本次实验中,我们分别进行了3次测量,得出的结果如下所示:第一次测量:锰含量为0.033%第二次测量:锰含量为0.031%第三次测量:锰含量为0.032%实验结论:经过三次测量,我们得出了钢锭中锰的含量分别为0.033%、0.031%、0.032%。
取其平均值,可以得出样品中锰的平均含量为0.032%左右。
因此,我们可以得出结论:本次实验通过重量分析法,准确地测量出了给定钢锭中锰的含量。

实验报告钢铁中锰含量的测定——银盐氧化光度法班级:应091-4姓名:任晓洁学号:200921501428指导老师:王老师一.实验目的:1.通过实验,了解钢铁中锰的存在形式,测定意义。
2.了解测定钢铁中锰含量的测定方法。
3.掌握钢铁中锰含量的测定原理。
4.熟练掌握分光光度计的使用,进一步训练移液管、容量瓶的正确使用。
5.掌握用比色法测定钢材中锰含量的方法二.实验原理:1.锰在钢铁中主要以MnC、MnS、FeMnSi或固溶体状态存在。
生铁中一般含锰0.5%~6%,普通碳素钢中锰含量较低,含锰0.8%~14%的为高锰钢,含锰12%~20%的铁合金称为镜铁,含锰60%~80%的铁合金称为锰铁。
2.锰溶于稀酸中,生成锰(Ⅱ)。
锰化物也很活泼,容易溶解和氧化。
在化学反应中,由于条件的不同,金属锰可部分或全部失去外层价电子,而表现出不同的价态,分析上主要有锰(Ⅱ)、锰(Ⅲ)、锰(Ⅳ)、锰(Ⅶ),少数情况下亦有锰(Ⅵ),这就为测定锰提供了有利条件。
3.常用测定方法:一般碳素钢,低合金钢,生铁试样常以HNO3(1+3)或硫磷混酸溶解。
难溶的高合金钢以王水溶解,加HClO4或H2SO4冒烟溶解。
溶解试样的酸主要依靠H2SO4,HCl,HNO3,因H2SO4-HCl可使MnS分解。
HNO3分解碳化物(Mn3C)生成CO2逸出,加磷酸可使Fe3+配合成无色而消除Fe3+的干扰。
同时因为磷酸的存在,防止了MnO2沉淀的生成和HMnO4的分解。
4.主要反应方程式:3MnS+12HNO3=3Mn(NO3)2+6HNO3+3SO2+6H2O3Mn3C+28HNO3=29Mn(NO3)2+3CO2+10NO+14H2OMnS+H2SO4=MnSO4+H2S2AgNO3+(NH4)2S2O8=Ag2S2O8+2NH4NO3Ag2S2O8+2H2O=Ag2O2+2H2SO45Ag2O2+2 Mn(NO3)2+6HNO3=2HMnO4+10AgNO3+2H2O三.实验仪器及试剂:1.实验仪器:721型分光光度计,分析天平,容量瓶(50mL),移液管(1ml,2ml,3ml),吸量管(5mL),滴管,洗耳球,电炉2.实验试剂:硝酸溶液(1:3),王水(1浓硝酸+3浓盐酸)硫磷混酸(700ml水中加入150ml磷酸及硫酸150ml,摇匀),0.5%硝酸银溶液,20%过硫酸铵溶液,5%EDTA,锰标准溶液(0.1mg/ml)四.实验步骤:1.溶样:钢样0.25-0.3g于50ml烧杯→加5mlH2O,10-15ml王水溶解,(可稍热)→2mlHClO4→加热至冒白烟2min→冷却→加硫磷混酸10ml→加热至冒白烟,除尽Cl-→冷却,定量转移至50ml容量瓶定容,摇匀,备用。

钢中锰含量的测定实验报告实验报告:钢中锰含量的测定
实验目的:
本实验旨在测定某钢材中锰的含量,并了解钢中非金属元素的分析方法和测定原理。
实验原理:
钢材中锰的含量可通过测定钢材溶液中过氧钼酸钠-铵铁硫酸复合物(PMA)溶解后,生成的锰(VII)酸根离子的吸光度来计算。
实验步骤:
1. 取样:将待测钢材切成小块,加入密封瓶中。
用玻璃片将密封瓶密封,避免空气进入导致钢材氧化。
2. 溶解:取一定量的样品后,加入浓硝酸使其完全溶解;加入稀氨水并调节pH值为8-10;加入500mg/L的过氧钼酸钠-氨铁硫酸复合物,并摇匀。
3. 吸收:于蓝色时立即测定吸光度。
保持室内环境不变,重复三次实验并取平均值。
4. 统计计算:根据标定曲线计算出锰含量。
实验数据:
1. 样品质量:0.3565g
2. 溶液取量:20ml
3. 吸光度计测量波长:880nm
4. 吸光度测定值:0.425
数据处理:
根据溶液的配制方法和吸光度的测量值,则此钢材样品中锰元素的含量为:15.48mg/L
结论:
经过本次实验,我们学会了一种钢中锰含量的测定方法,并成功测定了某一钢材中锰的含量为15.48mg/L。
此实验具有重要的意义,可为制定相关钢铁标准提供依据和参考。
钢中锰含量的测定实验报告钢中锰含量的测定实验报告摘要:本实验旨在通过化学分析方法测定钢中锰的含量。
首先,将待测样品溶解,并添加适量的试剂进行反应,生成可测定的化合物。
然后,利用分光光度计测量反应产物的吸光度,根据标准曲线计算出样品中锰的含量。
实验结果表明,该方法可以准确测定钢中锰的含量。
引言:钢是一种重要的金属材料,其性能与组成密切相关。
锰是钢中常见的合金元素之一,它可以显著提高钢的硬度、强度和耐磨性。
因此,准确测定钢中锰的含量对于控制钢材质量具有重要意义。
本实验采用化学分析方法,通过测量反应产物的吸光度来确定钢中锰的含量。
实验步骤:1. 样品溶解:取一定量的待测样品,将其溶解于酸性溶液中。
酸性溶液可以将钢中的锰溶解出来,并防止其他金属离子的干扰。
2. 反应生成:向样品溶液中加入适量的试剂,使其与溶解出的锰离子发生反应,并生成可测定的化合物。
本实验中,选择硫代硫酸钠作为试剂,与锰离子反应生成紫色的锰酸锌。
3. 吸光度测量:将反应产物溶液转移到分光光度计比色皿中,设置适当的波长,测量其吸光度。
锰酸锌的吸光度与其浓度成正比,因此可以根据吸光度值推算出锰的含量。
4. 标准曲线绘制:制备一系列不同浓度的锰标准溶液,分别测量其吸光度,并绘制标准曲线。
通过标准曲线,可以将吸光度值转化为锰的浓度。
5. 锰含量计算:根据待测样品的吸光度值和标准曲线,计算出样品中锰的含量。
结果与讨论:通过实验测量,得到了一系列标准曲线上的吸光度值和对应的锰浓度。
通过待测样品的吸光度值,可以在标准曲线上找到对应的锰浓度,并计算出样品中锰的含量。
实验结果表明,该方法可以准确测定钢中锰的含量。
然而,实验中可能存在一些误差。
首先,样品的制备过程中,可能存在溶解不完全或者其他杂质的存在,这会影响到测定结果的准确性。
其次,反应过程中可能存在其他金属离子的干扰,导致测定结果偏高或偏低。
为了减小误差,可以在实验前进行样品的预处理,确保样品的纯度和溶解度。
钢铁中锰的测定
钢铁中锰的测定是一种常见的化学分析方法,用于快速、准确地测定钢铁中的锰的含量。
钢铁中锰的测定的基本原理是:将钢铁中的锰以锰酸钠的形式进行氧化,再将其与铁黄素溶液发生反应,然后进行光度测定,用以检测其发生反应时光度改变的情况,最后由原料
中锰量得知其光度改变的程度,从而计算出钢铁中锰的含量。
此外,还需要在测定痕量锰时进行消杂处理,以除去其可能含有的其他金属离子和有机物,从而减小干扰因素,保证测定结果的准确性。
整个测定钢铁中锰的过程大致分为如下几个步骤:首先通过分子筛、离心选择最佳样品,
其含锰量应至少达到200毫克;然后配制试液,主要是将滤液或样品中的有机物等去除,消去其潜在干扰;紧接着将钢铁样品发生氧化反应,形成锰酸钠溶液;在此基础上,将其
与铁黄素溶液混合发生反应;最后进行光度测定,得出固溶体中锰的含量,最终确定其中
的锰含量。
由于钢铁对环境和生物的影响非常重大,因此对钢铁中锰的测定及其合理的管控非常重要。
测定的准确性和锰的含量将直接关系到钢铁的质量,从而确保产品的安全性和可靠性。
综上所述,钢铁中锰的测定是一种可靠、准确的方法,用于快速检测其中锰的含量,为钢铁的生产提供了重要保障,确保我们使用的产品符合标准要求。
FCLHSDHJGMn 004低合金钢—锰含量的测定—高氯酸氧化-亚铁滴定法F_CL_HS_DHJG_Mn_ 004低合金钢—锰含量的测定—高氯酸氧化-亚铁滴定法1 范围本推荐方法用高氯酸氧化-亚铁滴定法测定碳素钢、低合金钢、硅钢和纯铁中锰的含量。
本方法适用于碳素钢、低合金钢、硅钢和纯铁中质量分数大于1%的锰含量的测定。
2 原理试料经硝酸、磷酸分解,在磷酸存在下以高氯酸将锰氧化至三价,以N-苯基邻氨基苯甲酸为指示剂,用亚铁标准滴定溶液滴定,由标准滴定溶液消耗量计算锰的质量分数。
钒、铈有干扰可用系数扣除法消除,系数值是每1%的钒相当于1.08%的锰,每1%的铈相当于0.39%的锰。
3 试剂分析中,除另有说明外,仅使用分析纯的试剂和蒸馏水或与其纯度相当的水。
3.1硝酸,ρ约1.42g/mL3.2磷酸,ρ约1.69g/mL3.3高氯酸,ρ约1.67g/mL3.4高氯酸—盐酸—氢氟酸混合酸300mL高氯酸中缓缓加入170mL盐酸(边摇边加),然后加入30mL氢氟酸(ρ约1.15g/mL)混匀,储于塑料瓶中。
3.5N-苯基邻氨基苯甲酸溶液,2g/L每100 mL溶液含0.2g碳酸钠。
3.6重铬酸钾标准溶液,c(1/6K2Cr2O7)=0.064 mol/L称取6.2758g预先置于105~110℃干燥并达到恒量,在干燥器中冷却至室温的重铬酸钾基准试剂(质量分数大于99.9%),精确至0.0001g。
置于250mL烧杯中,加100 mL水、数滴硫酸溶液(1+1),加热溶解,冷却至室温,移入2000 mL容量瓶中,以水稀释至刻度,混匀。
放置一周后方可使用。
3.7硫酸亚铁铵标准滴定溶液,c(Fe2+)=0.064mol/L3.7.1配制称取25g硫酸亚铁铵置于烧杯中,加100mL水,40 mL硫酸,搅拌至全部溶解,再用水稀释至1000mL,经充分混匀放置一周后标定。
3.7.2标定准确移取25.00 mL 重铬酸钾标准滴定溶液(0.064mol/L)于500mL烧杯中,加约200mL 水,20 mL硫酸(1+1),用待标定硫酸亚铁铵标准滴定溶液(0.064mol/L)滴定至淡黄色,加入5~6滴N-苯基邻氨基苯甲酸溶液(2g/L),继续用硫酸亚铁铵标准滴定溶液(0.064mol/L)滴定至樱桃红色变为亮绿色为终点。
钢中锰的含量测定1.概述钢是由多种元素组成的合金,其中含有元素的总类和含量决定了钢的性质,因此钢的化学成分分析是冶炼过程中必不可缺的工作。
利用成分分析结果进行适时调控,可以确保冶炼质量。
本实验通过分光光度法测定钢中锰的含量。
使用分光光度计,利用有色溶液对单色光的吸收程度来确定物质含量,称为分光光度法。
此方法灵敏度较高,适用于微量组分的测定,测定浓度下限可达0.1~1μg·g-1。
2.实验目的(1)了解分光光度分析的基本原理;(2)学习通过分光光度分析测定微量元素的方法;(3)掌握分光光度计的使用,完成钢中锰含量的测定;3.实验原理通常看到的白光为复合光,它由不同波长的光组成。
受人的视觉分辨能力的限制,人们所看到的红光、黄光等是含一定波长范围的色光,各种色光也是一种复合光。
仅具有某一种波长的光称为单色光。
当某一波长的单色光照射到有色溶液时,该溶液对光的吸收程度与液层厚度b成正比。
这一关系为朗伯(Lamber)所发现,称为朗伯定律,数学表达式为lgI0/I =k1b之后比耳(Beer)又指出,当单色光通过液层厚度一定的有色溶液时,溶液对光的吸收程度与溶液浓度c成正比,这一关系称为比耳定律,数学表达式为lgI0/I=k2c将朗伯定律与比耳定律结合可得到lgI0/I=kbc其中,lgI0/I项表明了溶液对光的吸收程度,称为吸光度,用符号A表示。
I/I0表示入射光透过溶液的程度,称为透光度(以%表示为透光率),以T表示,则A=lgI0/I=lg1/T=kbc若液层厚度b的单位为cm,浓度的单位为mol·L-1,则常数k用ε表示:A=εbc其中,ε称为摩尔吸光系数,其单位是L·(mol·cm)-1。
从上式可知,当入射光通过的液层厚度一定时,吸光度A与溶液中吸收物质的浓度成正比。
若配制不同浓度的标准溶液,测定其吸光度A,画出曲线,此曲线称为工作曲线。
然后测定未知试样有色溶液的吸光度。
钢中锰含量的测量
1.实验目的
(1)了解用分光光度法测定钢中锰含量的原理和方法;
(2)熟练掌握分光光度计的使用,进一步训练移液管、容量瓶的正确使用;
(3)练习作图法处理实验数据。
2.实验原理
将已知质量的钢样溶解于由硝酸、硫酸和磷酸组成的混合酸中。
Fe+6HN03 = Fe(N03)3+3NO2十+3H20
Mn+4HN03 = Mn(N03)2+2N02十+2H20
Fe3++2H3PO4 = H3[Fe(P04)2] +3H+
Ag+
2Mn2++5S2O82-+8H20 = 2MnO4-+10SO42-+16H+
所得到的MnO4-溶液,以空白试样为参比液,可用分光光度计在波长530nm处测定其吸光度。
将一系列已知浓度的Mn04-标准溶液,按上述相同方法处理后,用分光光度计测出它们的吸光度。
以吸光度(A)为纵坐标,标准溶液浓度(c)为横坐标作图,得到A与c的关系曲线,叫工作曲线。
通过工作曲线可查到样品溶液的吸光度所对应的浓度,进而可换算出钢样中锰的含量,
3.仪器与试剂
仪器:721型分光光度计,分析天平,容量瓶(50mL),移液管(10mL),吸量管(5mL),滴管,洗耳球,酒精灯。
试剂:HN03-H2S04—H3P04的混合酸(1:1:1) 1%AgN03,KMn04标准溶液
(含Mn 1mg·mL-1),(NH4)2S2O8 (15%),钢样。
4.实验内容
(1)标准KMn04系列溶液的配制:用移液管吸取10mL的标准KMnO4溶液
于100mL容量瓶中,用去离子水稀释至刻度。
盖上瓶盖后摇匀备用。
另取6只50ml容量瓶。
每只容量瓶按表5—4用量,用移液管(或吸量管)分别加入备用的标准KMn04溶液、混合酸、(NH4)2S2O8和AgN03,并用去离子水稀释至刻度,盖上瓶塞后摇匀。
(2)钢样的处理及钢样溶液的配制:
用分析天平准确称量一份钢样(60~
80mg),放人50mL烧杯中,加入17mL混合酸,在通风橱中用低温电势板加热,使钢样溶解,待棕色N02气体不再产生时,加入10mL (NH4)2S2O8和3mL AgN03溶液,继续加热至沸腾。
煮沸lmin后即可停止加热。
待溶液冷却至室温后,全部转移到50mL溶量瓶中,用去离子水稀释至刻度,盖上瓶塞,摇匀(3)溶液吸光度的测定:将分光光度计波长调至530nm(使用方法参见第二章2.4节),使用0.5cm 比色皿装待测液,以空白试样为参比液,分别测定5个标准KMnO4溶液及钢样溶液的吸光度。
5.数据处理
以溶液的吸光度为纵坐标,KMn04浓度为横坐标,在坐标纸上作
出标准系列溶液的A-c关系工作曲线。
由钢样溶液的吸光度在工作曲线上查出其相应的浓度,计算钢样中锰的含量。
6.思考题
(1)在本实验中,分光光度计的波长为何要调在530nm处?
(2)使用移液管、容量瓶配制溶液的操作中,应注意哪些方面?
(3)如何根据钢样溶液中MnO4-的浓度计算钢样中锰的含量?。