影响化学平衡的条件
- 格式:doc
- 大小:52.50 KB
- 文档页数:4

高二化学影响化学平衡的条件【本讲主要内容】影响化学平衡的条件 1. 化学平衡移动2. 影响化学平衡的因素3. 勒沙特列原理【知识掌握】【知识点精析】 (一)化学平衡移动1. 从正、逆反应速度是否相等分析:化学平衡状态是指在一定条件下正反应速率与逆反应速率相等的动态平衡状态。
这种平衡是相对的,改变反应的某些条件,可以使正、逆反应发生不同的改变(也可能只改变正、逆反应速率的一种速率),原平衡状态被破坏,一定时间后,在新的条件下又建立新的平衡状态,这一过程就是化学平衡的移动。
*2. 从浓度商和平衡常数分析:对于一个一般的可逆反应:aA + bB cC + dD ,在平衡状态时,平衡常数K=ba d c B A D C ][][][][,浓度商Q 与K 具有相同的表达式,但其浓度(或压力)不像K 那样特指平衡态。
当Q = K 时,反应处于平衡状态; 当Q < K 时,反应向着正方向进行; 当Q > K 时,反应向着逆方向进行。
同样,欲破坏化学平衡状态,必须使Q ≠K 。
(二)影响化学平衡的因素mA(g)+nB(g)pC(g)+qD(g)+Q (放热),△ng =p +q -(m +n)思考:若在气体混合物中充入惰性气体,对化学平衡的移动有无影响?解析:应分恒温恒压和恒温恒容两种情况进行讨论。
①恒温恒压:充入惰性气体,密闭容器的体积增大,各组分浓度同等程度降低,其效果相当于减小平衡混合物的压强,因此,平衡向反应气体体积增大方向移动。
如对合成氨反应来说,则向逆反应方向移动。
图象如下:②恒温恒容:充入惰性气体,似乎总压强增大了,但实际上容器体积不变,对平衡混合物各组成浓度不变,即原各气体分压不变,增大的惰性气体的分压与平衡体系无关,所以平衡不发生移动。
图象如图所示:注意①以上讨论适合于不与平衡混合物各组分反应的多种气体。
不一定真为惰性气体。
②如可逆反应前后气态物质总物质的量不变,则化学平衡不受压强影响,上述恒温恒压、恒温恒容两情况都不会使化学平衡移动。
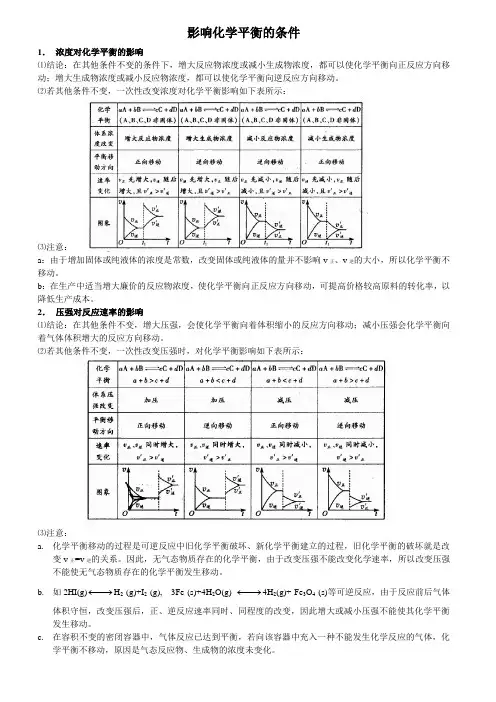
影响化学平衡的条件1. 浓度对化学平衡的影响⑴结论:在其他条件不变的条件下,增大反应物浓度或减小生成物浓度,都可以使化学平衡向正反应方向移动;增大生成物浓度或减小反应物浓度,都可以使化学平衡向逆反应方向移动。
⑵若其他条件不变,一次性改变浓度对化学平衡影响如下表所示:⑶注意:a :由于增加固体或纯液体的浓度是常数,改变固体或纯液体的量并不影响v 正、v 逆的大小,所以化学平衡不移动。
b :在生产中适当增大廉价的反应物浓度,使化学平衡向正反应方向移动,可提高价格较高原料的转化率,以降低生产成本。
2. 压强对反应速率的影响⑴结论:在其他条件不变,增大压强,会使化学平衡向着体积缩小的反应方向移动;减小压强会化学平衡向着气体体积增大的反应方向移动。
⑵若其他条件不变,一次性改变压强时,对化学平衡影响如下表所示:⑶注意:a. 化学平衡移动的过程是可逆反应中旧化学平衡破坏、新化学平衡建立的过程,旧化学平衡的破坏就是改变v 正=v 逆的关系。
因此,无气态物质存在的化学平衡,由于改变压强不能改变化学速率,所以改变压强不能使无气态物质存在的化学平衡发生移动。
b. 如2HI(g)−→←H 2 (g)+I 2 (g), 3Fe (s)+4H 2O(g) −→←4H 2(g)+ Fe 3O 4 (s)等可逆反应,由于反应前后气体体积守恒,改变压强后,正、逆反应速率同时、同程度的改变,因此增大或减小压强不能使其化学平衡发生移动。
c. 在容积不变的密闭容器中,气体反应已达到平衡,若向该容器中充入一种不能发生化学反应的气体,化学平衡不移动,原因是气态反应物、生成物的浓度未变化。
例如可逆反应2SO 2(g)+O 2 (g) −→←2SO 3(g),达到平衡后,在温度和体积不变的情况下充入Ar ,因c(SO 2)、c(O 2)、c(SO 3)均未发生变化,故会化学平衡不移动。
d. 在容积可变的恒压容器中,充入一种不能发生化学反应的气体,此时虽然总压强不变,但各气态物质的浓度改变,则应考虑平衡发生移动的问题。


影响化学平衡的条件说课稿影响化学平衡的条件说课稿1一、说教材1、教材的地位和作用课题:高中化学第二册第二章第三节《影响化学平衡的条件》《影响化学平衡的条件》是中学化学的重要理论之一。
本节教材在本章中起到承上启下的作用,通过对本章的学习,既可以使学生加深对溶解平衡的化学理论的理解,又为以后学习电离平衡奠定了基础,对学生后续的学习有着深远的影响。
通过本章的学习,使学生能够进一步学习应用理论分析,研究,联系实际解决问题的能力。
2、教材简析教材分析:本节教材由三部分构成:第一部分,化学平衡移动;第二部分,影响化学平衡的条件,化学平衡移动;第三部分,勒夏特列原理。
其中第一部分是基础,第二部分是整节教材的核心,第三部分是对本节课的总结和升华。
3、教学目标的确定根据《大纲》的要求、教材编排意图及学生的实际情况,拟定以下教学目标:认知目标――理解掌握浓度、压强、温度等外界条件对化学平衡的影响。
技能目标――通过本节课的教学,培养学生分析问题,解决问题,创造性思维的能力和自学能力。
素质教育目标――对学生进行辩证唯物主义教育,培养学生热爱科学、勇于探索的精神。
4、重点及难点的确定重点:浓度,压强,温度对化学平衡的影响难点:1、平衡移动原理的应用。
2、平衡移动过程的速率――时间图。
确立依据:对化学平衡移动原理的学习很重要,所以讨论“浓度,压强,温度等条件对化学平衡的影响”成为本节课的重点。
由于理论付诸实践有一定的难度,因此平衡移动原理的利用和移动过程中的速率――时间图成为本节的难点。
二、高学情分析二学生已经具备独立思考问题能力,而且思维活跃,掌握了影响化学反应速率的理论,以此为契机在教学中变探究为验证,激发学生学习的主动性,并培养学生严谨求实的科学态度。
三、说教法由于本节教材地位的重要性,结合学生实际情况,采取以下教学方法:1、通过演示实验,启发学生总结,归纳出浓度,压强,温度等条件改变对化学平衡影响。
2、通过对外界条件对速率影响理论复习,采取启发式教学,使学生从理论上认识平衡移动规律。

证对市爱幕阳光实验学校高三化学影响化学平衡的条件及效平衡一、教学内容:影响化学平衡的条件及效平衡二、教学目标:理解浓度、温度、压强、催化剂对化学平衡影响的一般规律;掌握勒沙特列原理及其用;了解效平衡原理;掌握化学平衡图像题的解题规律和方法三、教学、难点:条件对化学平衡的影响,效平衡原理和化学平衡图像题的解题规律四、教学过程:〔一〕化学平衡的移动,条件对化学平衡的影响及勒沙特列原理:化学平衡移动的实质是外界因素破坏了衡状态时v正= v逆的条件,使正、逆反速率不再相,然后在的条件下到达正、逆反速率重相。
也就是说,化学平衡的移动是:平衡状态→不平衡状态→平衡状态〔1〕浓度对化学平衡的影响:当其他条件不变时,增大反物浓度或减小生成物浓度,平衡向正反方向移动;增大生成物浓度或减小反物浓度平衡向逆反方向移动。
说明:①固体及纯液体的浓度是一值,不因量的多少而改变,所以增加或减少固体及纯液体的量,不会影响平衡状态。
②在可逆反中,为了尽可能利用某一反物,经常用过量的另一种物质和它作用。
③在生产中,也可以不断将生成物从反体系中别离出来,那么平衡将不断向生成产物的方向移动。
〔2〕压强对化学平衡的影响:当其他条件不变时,在有气体参加反的平衡体系中,增大压强使平衡向气体体积缩小的方向移动;减小压强使平衡向气体体积增大的方向移动。
说明:①压强的改变对化学平衡的影响只针对有气体参加且气体体积在反前后有变化的平衡体系。
对于固体或溶液间的反,改变压强对速率衡没有影响;对反前后气体分子总数保持不变的可逆反,改变压强只能改变反速率,对平衡无影响。
②增大压强无论平衡移动方向如何,平衡状态里的速率一大于衡状态的速率;减小压强无论平衡移动方向如何,平衡状态里的速率一小于衡状态的速率。
③在反体系中充入与反无关的气体时:a、在恒温恒压下,充入与反无关的气体,容器的总压强保持不变,但平衡混合气体的分压减小,可通过降低压强平衡向体积增大的方向移动判断平衡移动方向;b在恒温下,充入与反无关的气体,容器的总压强增大,但平衡混合气体的分压保持恒,因此,平衡不移动。

化学平衡的条件与影响因素化学平衡是指化学反应达到了一种稳定状态,反应物与生成物的浓度或活性不再发生明显变化。
在化学平衡状态下,反应物和生成物之间的正反应速率相等。
化学平衡受到一定的条件和影响因素的制约。
影响化学平衡的条件1. 温度:温度的改变可以影响反应的平衡状态。
根据Le Chatelier原理,当温度升高时,平衡反应往吸热反应方向移动;当温度降低时,平衡反应往放热反应方向移动。
因此,温度的改变可以改变平衡时反应物和生成物的比例。
2. 压力(气相反应):对于气相反应,压力的改变会影响反应的平衡。
根据Le Chatelier原理,当压力增加时,平衡反应往可减少摩尔体积的方向移动;当压力减少时,平衡反应往可增加摩尔体积的方向移动。
3. 浓度(溶液反应):对于溶液反应,浓度的改变会影响反应的平衡。
根据Le Chatelier原理,当某一反应物或生成物的浓度增加时,平衡反应往减少该物质浓度的方向移动;当某一反应物或生成物的浓度减少时,平衡反应往增加该物质浓度的方向移动。
4. 催化剂:催化剂对化学平衡没有影响。
催化剂可以加速正反应和逆反应的速率,但对平衡状态的稳定性无影响。
影响化学平衡的因素1. 反应物的浓度:反应物浓度的增加会使平衡反应往生成物的方向移动,而反应物浓度的减少会使平衡反应往反应物的方向移动。
2. 反应物的活性:反应物的活性可以影响反应的平衡,活性较高的反应物更容易参与反应。
3. 反应物和生成物之间的相互作用:反应物和生成物之间的相互作用可以改变反应的平衡状态。
比如,当产物的浓度增加时,反应物与生成物之间可能发生反应,使得平衡反应往反应物的方向移动。
综上所述,化学平衡受到温度、压力、浓度和催化剂等条件的影响,同时反应物的浓度、活性和相互作用也会对反应的平衡产生影响。
理解这些条件和因素对于掌握化学平衡的基本原理和应用具有重要意义。

第二章第三节 影响化学平衡的条件一、教学目的:1、 使学生理解浓度、温度和压强等条件对化学平衡的影响2、 使学生理解化学平衡移动的原理3、 通过对化学平衡移动原理的教学,培养学生科学的思维方法和辩证唯物主义观点。
二、教学重点:浓度、压强和温度对化学平衡的影响三、教学难点:平衡移动原理的理解和应用四、教学方法:实验探究 讨论分析五、教学过程:【第一课时】【复习】影响化学反应速率的因素有哪些?1、什么是化学平衡,化学平衡时有哪些主要的特征?化学平衡受哪些因素的影响?2、如果我们向一个处于化学平衡的反应中增加反应物的量,经过一段时间后,它还会平衡吗?(溶解平衡相联系)。
【引入】从上述的分析中,我们得知化学平衡只有在一定的条件下才能维持,如果我们在改变外界条件(温度、浓度、压强)时,平衡状态会发生改变,经过一段时间又会重新建立一个新的平衡状态。
【板书】第三节 影响化学平衡的条件【讲述】我们研究化学平衡,目的在于能建立更好的化学平衡,提高物质的转化率,提高产量,为此,我们就要研究如何建立更好的化学平衡,这节课我们就此来展开讨论学习。
【板书】一、浓度对化学平衡的影响【实验探究】实验原理:FeCl 3 +3KSCN Fe(SCN) 3(血红色)+3KCl结论分析:讨论归纳出浓度对化学平衡的移动情况。
【小结】增大反应物的浓度(或减少生成物的浓度),可使平衡向正方向移动。
【思考】为什么增加反应物的浓度,能使平衡向正反应方向移动呢?(能否从化学反应速率的角度分析)【分析并板书】当可逆反应达到平衡时,正反应速率和逆反应速率相等。
【练习】1.下列反应在容器中建立化学平衡:SO 2+NO 2 NO +SO 3,若在容器中通入一定量的O 2,此时反应将会发生的变化是 ( A )A.平衡向正反应方向移动B.平衡将向逆反应方向移动C.平衡不发生移动D.不使平衡移动,但容器内压强增大2. 在溴水中存在着下列平衡:Br 2+H 2O HBr +HBrO,在溶液中加入CCl 4,则溴水层的颜色将变浅或褪色,平衡将向逆反应方向移动,溶液的PH 值将增大。

1.化学平衡移动可逆反应的平衡状态是在一定条件下(浓度、温度、压强)建立起来的,当条件发生改变时,原平衡状态被破坏,并在新条件下建立起新的平衡。
此过程可表示为:(1)化学平衡移动:可逆反应中就化学平衡的破坏、新化学平衡的建立的过程。
(2)化学平衡移动的原因:反应条件的改变,移动的结果是正逆反应速率发生变化,平衡混合物中各组分的含量发生相应的变化。
(3)化学平衡移动的特征:○1从反应速率来看:若有v正=v逆到v正≠v逆某条件下平衡,再到这样的过程表明化学平衡发生了移动。
○2从混合物组成来看:各组分的含量从保持一定到条件改变时含量发生变化,最后在新条件下保持新的一定,同样表明化学平衡发生了移动。
(4)化学平衡移动的方向:○1若外界条件改变,引起v正>v逆时,正反应占优势,化学平衡向正反应方向移动。
○2若外界条件改变,引起v正<v逆时,逆反应占优势,化学平衡向逆反应方向移动。
○3若外界条件改变,引起v正和v逆都发生变化,如果v正和v逆能保持相等,化学平衡就没有发生移动。
2.影响化学平衡的条件参加反应的物质的性质是影响化学平衡的内在因素,影响化学平衡的外界条件主要有浓度、压强和温度等。
外界条件的改变对化学平衡的影响实质上是通过改变正、逆反应速率来实现的。
(1)浓度对化学平衡的影响○1结论:在其他条件不变的情况下,增大反应物浓度或减少生成物的浓度,都可以使化学平衡向正反应方向移动;增大生成物浓度或减少反应物的浓度,都可以使化学平衡向逆反应方向移动。
2增大反应物浓度增大生成物浓度减小反应物浓度减小生成物浓度a.由于增加固体或纯液体的浓度是常数,改变固体或纯液体的量并不影响v正、v逆的大小,所以化学平衡不移动。
b.在溶液中进行的反应,如果稀释溶液,反应浓度减小,生成物浓度也减小,v正、v逆的量减小,但减小的程度不同,总的结果使化学平衡向反应方程式中化学计量增大的方向移动。
c.在生产中适当增大廉价的反应物浓度,使化学反应向正反应方向移动,可提高价格较高原料的转化率,以降低生产成本。

影响化学平衡的三个因素1.浓度(1)可能影响化学反应速率和平衡移动的是浓度而不是质量、物质的量、体积。
若质量、物质的量、体积等的改变不能使浓度改变,则化学反应速率和平衡不改变。
(2)对于溶液中进行的离子反应,改变不参与反应的离子的浓度,速率和平衡一般不移动,如FeCl3+3KSCN≒Fe(SCN)3+3KCl,增加c(K+)或c(Cl-),不会影响化学反应速率和平衡。
(3)浓度的变化一定会带来反应速率的变化,但不一定导致化学平衡的移动。
如同等程度地增大反应各物质浓度,平衡向反应前后气体化学计量数之和减少的方向移动:同等程度地减少反应各物质浓度,平衡向反应前后气体化学计量数之和增大的方向移动;但对于反应前后气体化学计量数之和相等的反应,同等程度地改变反应各物质的浓度,平衡不移动。
(4)浓度改变瞬间时的正(逆)反应速率与反应物(生成物)浓度的变化成同一趋势,与生成物(反应物)浓度变化无关。
经常可以先判断平衡移动的方向,再由此判断外界条件改变瞬间,正、逆反应速率的相对大小。
(5)温度一定时,固体、纯液体的浓度一般认为是一常数,所以,改变固体、纯液体的量,其浓度仍不变,化学反应速率和平衡无影响;但改变固体的表面积(如“块状粉末状”),化学反应速率会增大或减小。
(6)H2O作为纯液体,虽然它的浓度为一常数(液态时),但对于在溶液中发生的反应,改变H2O的量往往会导致其他物质的浓度增大或减少,从而引起化学反应速率和平衡的移动,如Al3++3H2O ≒Al(OH)3+3H+,加水,其他反应物和生成物的浓度下降。
使υ正、υ逆均下降且平衡右移;另外,H2O作溶质,其他物质作溶剂进行的化学反应,此时H2O的浓度不再是一常数,改变H2O的量,会引起H2O 的浓度改变从而影响速率和平衡;最后注意水蒸气参加的反应,它的浓度亦不是一常数;可能随外界条件的改变而改变。
2.压强(1)只有压强的变化能引起反应物质的浓度改变时,平衡才有可能移动。
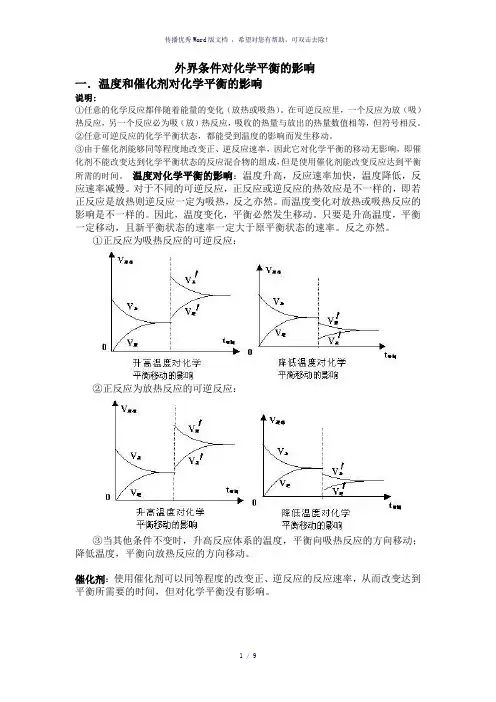
外界条件对化学平衡的影响一.温度和催化剂对化学平衡的影响说明:①任意的化学反应都伴随着能量的变化(放热或吸热)。
在可逆反应里,一个反应为放(吸)热反应,另一个反应必为吸(放)热反应,吸收的热量与放出的热量数值相等,但符号相反。
②任意可逆反应的化学平衡状态,都能受到温度的影响而发生移动。
③由于催化剂能够同等程度地改变正、逆反应速率,因此它对化学平衡的移动无影响,即催化剂不能改变达到化学平衡状态的反应混合物的组成,但是使用催化剂能改变反应达到平衡所需的时间。
温度对化学平衡的影响:温度升高,反应速率加快,温度降低,反应速率减慢。
对于不同的可逆反应,正反应或逆反应的热效应是不一样的,即若正反应是放热则逆反应一定为吸热,反之亦然。
而温度变化对放热或吸热反应的影响是不一样的。
因此,温度变化,平衡必然发生移动。
只要是升高温度,平衡一定移动,且新平衡状态的速率一定大于原平衡状态的速率。
反之亦然。
①正反应为吸热反应的可逆反应:②正反应为放热反应的可逆反应:③当其他条件不变时,升高反应体系的温度,平衡向吸热反应的方向移动;降低温度,平衡向放热反应的方向移动。
催化剂:使用催化剂可以同等程度的改变正、逆反应的反应速率,从而改变达到平衡所需要的时间,但对化学平衡没有影响。
【例1】对于合成氨反应来说,使用催化剂和采用高压,对这两项作用的叙述正确的是()A.都能提髙反应速率,对平衡无影响B.都不能缩短达到平衡所用的时间,但对平衡有影响C.都能缩短达到平衡所用的时间,只有压强对平衡有影响D.催化剂能缩短达到平衡所用的时间,而压强不能变式探究1在密闭容器中下列反应达平衡时,若降低温度可使混合气体平均相对分子质量减小的是()A. 4NH3(g)+5O2(g)4NO(g)+6H2O(g) (正反应为放热反应)B.N2(g)+3H2(g)2NH3(g) (正反应为放热反应)C.2SO3(g)2SO2(g)+O2(g) (正反应为吸热反应)D.H2(g)+I2(g)2HI(g) (正反应为放热反应)变式探究2如图中曲线a表示放热反应X(g)+Y(g)Z(g)+M (g)+N(s),进行过程中X 的转化率随时间变化的关系。
30化学平衡的影响的条件一、化学平衡移动1、概念:一定条件下,某可逆反应达平衡后,当改变某条件〔浓度、温度、压强〕,平衡混合物各组分的浓度也就随之改变,因而在新的条件下达到新的平衡。
这种由于条件的改变而使旧的平衡破坏和在新的条件下达到新的平衡的过程叫做化学平衡移动。
2、外界原因:改变了条件3、本质原因:V正≠V逆4、移动方向判断的依据:勒夏特列原理。
二、影响化学平衡的条件:勒夏特列原理如果改变影响平衡的一个条件(如浓度、压强或温度),平衡就向着能够减弱这种改变的方向移动。
改变影响平衡的一个条件化学平衡移动方向化学平衡移动结果增大反应物浓度向正反应方向移动反应物浓度减小减小反应物浓度向逆反应方向移动反应物浓度增大增大生成物浓度向逆反应方向移动生成物浓度减小减小生成物浓度向正反应方向移动生成物浓度增大增大体系压强向气体体积减小的反应方向移动体系压强减小减小体系压强向气体体积增大的反应方向移动体系压强增大升高温度向吸热反应方向移动体系温度降低降低温度向放热反应方向移动体系温度升高注意:①、固体、纯液体的浓度当作一个不变的量,所以增加固体或纯液体并不能改变浓度。
在实际生产中,往往采用增大易取得的或成本较低的物质的方法,使平衡正向移动,同时提高成本较高的原料的利用率〔转化率〕。
②、压强——要有气态物质存在,改变压强(使容器内气体的浓度发生改变),才可能使平衡移动。
A、充入与反应无关的气体如稀有气体要分析容器是恒容(不移)、还是恒压(向扩体方向移);反应式左右两边气体化学计量数和不变(无论上述那种均不变)B、颜色的改变要注意是一个动态变化的过程,先变?后变?C、平衡不移动,并不表示颜色不会变,因为颜色深浅决定于有色物质的浓度。
如:2NO2 N2O4(红棕色) 〔无色〕增大压强,颜色先深后浅;减小压强,颜色先浅后深。
③、温度——所有化学反应均具有能量变化,温度改变,化学平衡一定移动。
④、催化剂——只改变反应速率,而平衡不移动。
影响化学平衡的因素影响化学平衡的因素是高考重点考察的知识点。
影响化学平衡的因素主要有三个:1.浓度对化学平衡的影响当一个化学反应达到平衡的时候,其它反应条件不变,只改变其中任何一种反应物或生成物的浓度,就会改变正反应或逆反应的反应速率,使它们不再相等,从而使平衡移动。
在达到平衡的反应里,减小任何一种生成物的浓度,平衡会向正反应的方向移动;减小任何一种反应物的浓度,平衡会向逆反应的方向移动。
由此可见,在其它条件不变的情况下,增大反应物的浓度,或减小生成物的浓度,都可以使平衡向着正反应的方向移动;增大生成物的浓度或减小反应物的浓度,都可以使平衡向着逆反应的方向移动。
在生产上,往往采用增大容易取得的或成本较低的反应物浓度的方法,使成本较高的原料得到充分利用。
例如,在硫酸工业里,常用过量的空气使二氧化碳充分氧化。
2.压强对化学平衡的影响处于平衡状态的反应混合物里,不管是反应物或生成物,只要有气态物质存在,那么改变压强也常常会使化学平衡移动。
在其它条件不变的情况下,增大压强,会使化学平衡向着气体体积缩小的方向移动;减小压强,会使平衡向着气体体积增大的方向移动。
在有些可逆反应里,反应前后气态物质的总体积没有变化,在这种情况下,增大或减小压强就不能使化学平衡移动。
固态物质或液态物质的体积,受压强的影响很小,可以略去不计。
因此,平衡混合物都是固体或液体的,改变压强不能使平衡移动。
3.温度对化学平衡的影响在吸热或放热的可逆反应里,反应混合物达到平衡状态以后,改变温度也会使化学平衡移动。
在其他条件不变的情况下,温度升高,会使化学平衡向着吸热反应的方向移动;温度降低会使化学平衡向着放热反应的方向移动。
4.催化剂对化学平衡的影响由于催化剂能够以同样倍数增加正反应和逆反应的速率,因此它对化学平衡的移动没有影响,也就是说它不能改变达到化学平衡状态的反应混合物的百分组成。
但是使用了催化剂,就能够改变反应达到平衡所需的时间。
影响化学平衡的因素总的来说是以下几点:如果增大反应物浓度,平衡向正反应方向移动,移动的结果,反应物浓度减少;升高温度平衡向吸热方向移动,移动的结果体系温度降低;增大压强平衡向缩小体积方向移动,移动的结果体系压强降低。
化学反应达到平衡状态的条件
1. 封闭系统:在严格封闭的系统中,没有任何物质可以进出系统,保持反应物质总量不变。
2. 反应物质浓度:当反应物质浓度达到一定的值,它们之间的反应速度达到一定的水平,使得反应物质的消耗和生成达到动态平衡。
3. 温度:温度的变化会影响反应物质的反应速度。
当温度升高时,反应速度会加快,并且平衡位置会向生成物方向移动。
4. 压力:对于气相反应,改变压力会对平衡位置产生影响。
高压力可以推动平衡位置向生成物方向移动。
5. 反应的物质性质:反应物质间的相互作用是影响化学反应达到平衡状态的重要因素。
在某些情况下,化学反应在任何条件下都很难达到平衡状态。
第三节 影响化学平衡的条件 【第二课时】自主学习(预习提纲)一、化学平衡的移动:1.定义: 可逆反应中,旧化学平衡的 、新化学平衡的 过程叫做化学平衡的移动.2.实质当外界条件变化时, v (正) v (逆),平衡被破坏;在新的条件下, v ′(正) v ′(逆)时,建立新的平衡状态.也就是说,化学平衡的移动是原平衡状态——不平衡状态——新平衡状态的转化.3.研究对象:已经建立 的体系;本质原因:v (正) v (逆)二、影响化学平衡的条件及规律:1、浓度对化学平衡的影响实验原理:Cr 2O 2-7+H 2O 2CrO 2-4+2H +橙色 黄色实验步骤:①取两支试管各加入5 mL 0.1 mol·L -1K 2Cr 2O 7溶液。
②向一支试管中滴加1 mol·L -1HNO 3溶液,观察并记录溶液的颜色。
③向另一支试管中滴加1 mol·L -1NaOH 溶液,观察并记录溶液颜色的变化。
的浓度,平衡向逆反应方向移动,溶液橙色加深;增加OH -的浓度,减小H +的浓度,平衡向正反应方向移动,溶液黄色加深。
基本规律:增大反应物浓度或减小生成物浓度,平衡向正反应方向移动;减小反应物浓度或增大生成物浓度,平衡向逆反应方向移动。
[实验2-4]在KSCN + FeCl 3 KCl + Fe (SCN )3反应平衡体系中,继续加入FeCl 3溶液的瞬间, FeCl 3的浓度 ,Fe (SCN )3的浓度 (填“增大”、“减小”或“不变”) ;V 正 ,V 逆 (填“增快”、“减慢”或“不变”); 因而V 正 V 逆(填“=”或“≠”),致使平衡 (填“移动”或“不移动”)。
随着平衡向 (填“正反应方向”或“逆反应方向”)的移动,FeCl 3的浓度 ,Fe (SCN )3的浓度 (填“增大”、“减小”或“不变”) ;V 正 ,V 逆 (填“增快”、“减慢”或“不变”);最后V 正 V 逆(填“=”或“≠”),达到新的平衡状态。
影响化学平衡的主要因素及其在科研和生产实践中的
应用
影响化学平衡的主要因素包括温度、压力、浓度、反应物质量等。
以下是它们在科研和生产实践中的应用:
1. 温度:温度对化学反应速率和平衡常数均有影响。
在科研中,研究反应热、热力学参数等,可以优化反应条件和提高反应效率。
在生产实践中,控制反应温度有助于提高产品质量和纯度。
2. 压力:对于含气反应,压力可以影响气相反应物的活性,从而影响反应速率和平衡常数。
在科研中,通过控制压力,可以实现反应机理的解析和反应路径的优化。
在生产实践中,合理选择反应器的压力参数可以提高反应质量和产量。
3. 浓度:化学反应速率与反应物浓度的关系是一个重要的研究对象,在科研中可以通过测定反应速率对浓度的依赖性,研究反应机理和反应路径。
在生产实践中,通过控制反应物的浓度可以达到最佳反应条件。
4. 反应物质量:对于多组分反应,反应物之间的质量比例是一个重要的影响因素。
在科研中,可以通过控制反应物质量比例,研究反应机理和反应路径。
在生产实践中,最优化反应物质量比例可以提高反应产率和质量。
总之,了解化学平衡的影响因素及其应用对于科研和生产实践具有重要意义。
第三节影响化学平衡的条件
[学习目标]
1.明确化学平衡移动的概念;
2.掌握浓度、温度、压强等条件对化学平衡移动的影响;
3.理解勒沙特列原理的涵义,并能结合实际情况进行应用;
4.通过知识的应用,培养学生分析问题和解决问题的能力。
[知识重点]
1.化学平衡的移动原理; 2. 化学平衡移动在实际中的应用;
3. 化学平衡的有关计算。
.
[知识要点]
1.化学平衡的移动:
2.影响化学平衡的条件及规律
①浓度的影响:
浓度的改变V正、V逆的变化结果平衡移动的方向增大反应物的浓度
减小生成物的浓度
增大生成物的浓度
减小反应物的浓度
....
②压强的影响:
压强的改变V正、V逆的变化结果平衡移动的方向压强增大
(体积缩小)
压强减小
(增大体积)
㈠必须,压强变化才有
意义。
㈡压强
....的影响的区别。
......的影响与对化学平衡
..对化学反应速率
③温度的影响:
温度的改变V正、V逆的变化结果平衡移动的方向
升高温度
降低温度
④催化剂对化学平衡影响。
注意:催化剂
....的影响的区别
...对反应速率
....的影响与其对化学平衡
总结:
即勒沙特列原理。
[例题分析]
例 1.在稀氨水中存在如下平衡:NH3+H2O NH3·H2O NH4++OH-在下列情况下, NH3,NH4+,OH-的浓度如何变化?
①加入少量NH4Cl晶体:[ OH-] ,[ NH4+] 。
②加入少量HCl:[ NH3] ,[NH4+] 。
③加入少量NaOH晶体: [ NH3] ,[NH4+] 。
例2.可逆反应:A+3B2C+2D+热量,达到平衡时,要使正反应速率加快,平衡向正反应方向移动,且A的转化率增大,可采取的措施是( )
A 增大压强
B 升高温度
C 使用催化剂
D 增大B的浓度
[巩固练习]
1.可逆反应:NH 4HS(固) NH3(气)+H2S(气),在某温下达平衡。
下列各情形中,不能使平衡发生移动的是()
A 移走一部分NH4HS
B 恒压条件下,充入氦气
C 其他条件不变时,充入SO2
D 容器容积不变时,充入氦气
2.反应CaCO3(固) CaO3(固) + CO2(气),在不同温度下CO2的平衡压强如下表: 温度℃550 650 750 850 897
压强 Pa ×101×102×103×104101×105
按要求填空:(1)若升高CaCO3分解平衡体系的温度,同时给反应容器加压,则平衡;
A 向左移动
B 向右移动
C 不移动
D 无法确定平衡移动方向
(2)在一个与外界不能进行热交换的密闭容器中,足量的CaCO3在850℃建立了分解平衡。
若将该容器的容积扩大为原来的2倍,当重新达到平衡时容器内的温度将,CO2的平衡压强将 4. 94×104,理由是
3.有 a 、b两个极易导热的密闭容器,a 保持容积不变,b 中的活塞可上下移动,以保持内外压强相等。
在相同条件下将 3 mol A,1 mol B 分别同时混合于a、b两容器中,发生反应 3 A(气)+B(气) 2C(气)+D (气)(1)达平衡时,a 中A 的浓度为M mol/L,C的浓度为Nmol/L,b中A的浓度为m mol/L,C的浓度为n mol/L,则M m;N n;(填①<②>③=④无法比较)
(2)保持温度不变,按下列配比分别充入a、b两容器,达平衡后,a中C的浓度为N mol/L的是(),b中C的浓度为n mol/L的是()
+2molB B. 3molA+2molC +1molB+1molD
D. 2molC+1molD E .++1molC+
(3)若将2molC和2molD充入a中,保持温度不变,平衡时A的浓度为Wmol/L,C的浓度为Ymol/L,则W和M,Y和N之间的关系为W M ,Y N (4)保持温度不变,若将4molC和2molD充入a中,平衡时A的浓度为Rmol/L则 A R=2M B R<M C M<R<2M D R>2M ( )
4.在高温下,反应2HBr (气) H2+Br2-热量,达到平衡状态,要使混合气体颜色加深,可采取的方法是()
A 减小压强
B 缩小体积
C 升高温度
D 增大氢气的浓度
5.可逆反应A(气)+nB(气)2C(气)+热量,在一定温度下,反应物B的转化率与压强有如下图所示的关系,那么n值一定是 )
A n>1
B n≥1
C n=1
D n≤1
6.在密闭容器中通入体积比为1:3的气体X和气体Y,在一
定条件下,可逆反应X+3Y=PZ达到平衡时,有50%的Y转化为
Z,反应前与平衡时容器内的压强比(同温下)是4:3,则系
数P是()
A 1
B 2
C 3
D 4
7.容积为1L的固定的密闭容器中充入2molNH3,在一定条件下发生下列反应:2NH3=3H2+N2,达到平衡时C(N2)为L。
若维持原温度和体积不变,按下列物质的量加入起始物质,达到平衡时,容器内C(N2)不能维持的是
A 1molN2+3molH2
B 2molNH3+1molHe
C 2molN2+3molH2
D ++
8.A(气)+2B(气)C(气)+2D(气)在恒温下达到平衡,能充分说明这一事实的是
A 反应容器不再变化
B 各反应物的浓度不再变化
C 单位时间内生成CmolA,则同时生成2nmolB
D 反应容器内A、B、C、D四种物质生成速率相等
9.温度,催化剂不变,向某一固定体积的密闭容器内按下列各组物质的量(mol),加入SO2,O2和SO3,反应达平衡状态时,SO3气体浓度最大的一组是( )
A B C D
SO2 6 3 5
O2 2 0 1
SO30 4 2 1
2
件,则指定物质的浓度及平衡如何变化。
①增加C,平衡,[CO] 。
②减小密闭容器体积,保
持温度不变,则平衡,[CO2] 。
③通入N2,保持密闭容器体积和温度不变,则平衡,[CO] 。
④通入N2,密闭容器体积增大,保持温度不变,则平衡,[CO2] 。
11.某温度时有如下反应:S2Cl2(液、无色)+Cl2(气)2SCl2(液、红色)+,在容器中达到平衡,下列说法不正确的是()
A 升高温度,而压强不变,液体颜色变浅
B 温度不变,而缩小容器体积,液体颜色加深
C 温度不变,而增大容器容积,S2Cl2的转化率降低
D 温度降低,而体积不变,Cl2的转化率降低
12.下列事实不能用勒沙特列原理来解释的是()
A 氮氢合成氨需要较高温度(约500℃)
B 饱和NaCl溶液中通入HCl气体有晶体析出
C 工业上制取硫酸,利用催化剂有利于SO3的生成
D 用饱和NaHCO3溶液收集CO2气体
13.一定温度下,某密闭容器中发生如下可逆反应:
CO(气)+H2O(气)CO2(气)+H2(气)—Q,当反应达到平衡时,测得容器中各物质均为nmol。
欲使H2(气)的平衡浓度增大一倍,在其它条件不变时,下列措施中可采用的是()
A 升高温度
B 增大压强
C 再通入nmolCO和nmol H2O(气)
D 再通入2nmol CO2(气)和2nmol H2(气)
14.在某固定容积的密闭容器中存在化学平衡:a A(气)=b B(气)+c C(气),在温度不变的条件下,再充入一定量的A 物质,重新达到平衡时,下列判断中正确的是
A 若a=b+c时,B的物质的量分数变大
B 若a=b+c时,B的物质的量分数不变
C 若a>b+c时,A的转化率不变
D 若a<b+c时,A的转化率变小
15.反应2SO2+O22SO3,在一定条件下达到平衡,SO2的起始浓度为8mol/L,平衡转化率为25%,O2的起始浓度为2mol/L,求平衡时反应混合物中各组分的百分含量。
若将O2的起始浓度加大至4mol/L,SO2的起始浓度不变,平衡时测得SO3的浓度为L,求SO2,O2各自的转化率。