高二化学弱电解质的电离
- 格式:ppt
- 大小:542.00 KB
- 文档页数:17

高二化学知识点总结(水溶液中的离子平衡)高二化学知识点总结第三章水溶液中的离子平衡一、弱电解质的电离1、定义:电解质:在水溶液中或熔化状态下能导电的化合物,叫电解质。
非电解质:在水溶液中或熔化状态下都不能导电的化合物。
强电解质:在水溶液里全部电离成离子的电解质。
弱电解质:在水溶液里只有一部分分子电离成离子的电解质。
2、电解质与非电解质本质区别:电解质——离子化合物或共价化合物非电解质——共价化合物注意:①电解质、非电解质都是化合物②SO2、NH3、CO2等属于非电解质③强电解质不等于易溶于水的化合物(如BaSO4不溶于水,但溶于水的BaSO4全部电离,故BaSO4为强电解质)——电解质的强弱与导电性、溶解性无关。
3、电离平衡:在一定的条件下,当电解质分子电离成离子的速率和离子结合成时,电离过程就达到了平衡状态,这叫电离平衡。
4、影响电离平衡的因素:A、温度:电离一般吸热,升温有利于电离。
B、浓度:浓度越大,电离程度越小;溶液稀释时,电离平衡向着电离的方向移动。
C、同离子效应:在弱电解质溶液里加入与弱电解质具有相同离子的电解质,会减弱电离。
D、其他外加试剂:加入能与弱电解质的电离产生的某种离子反应的物质时,有利于电离。
5、电离方程式的书写:用可逆符号弱酸的电离要分布写(第一步为主)6、电离常数:在一定条件下,弱电解质在达到电离平衡时,溶液中电离所生成的各种离子浓度的乘积,跟溶液中未电离的分子浓度的比是一个常数。
叫做电离平衡常数,(一般用Ka表示酸,Kb表示碱。
)表示方法:ABA++B- Ki=[ A+][B-]/[AB]7、影响因素:a、电离常数的大小主要由物质的本性决定。
b、电离常数受温度变化影响,不受浓度变化影响,在室温下一般变化不大。
C、同一温度下,不同弱酸,电离常数越大,其电离程度越大,酸性越强。
如:H2SO3>H3PO4>HF>>H2CO3>H2S>HClO二、水的电离和溶液的酸碱性1、水电离平衡:水的离子积:KW= c[H+]·c[OH-]25℃时,[H+]=[OH-] =10-7 mol/L ; KW= [H+]·[OH-] = 1_10-14注意:KW只与温度有关,温度一定,则KW值一定KW不仅适用于纯水,适用于任何溶液(酸、碱、盐)2、水电离特点:(1)可逆(2)吸热(3)极弱3、影响水电离平衡的外界因素:①酸、碱:抑制水的电离 KW〈1_10-14②温度:促进水的电离(水的电离是吸热的)③易水解的盐:促进水的电离 KW 〉1_10-144、溶液的酸碱性和pH:(1)pH=-lgc[H+](2)pH的测定方法:酸碱指示剂——甲基橙、石蕊、酚酞。

弱电解质的电离平衡常数教学设计(人教版选修4)【教学过程】板块一:课前回顾1、请写出CH3COOH的电离方程式:影响弱电解质电离平衡的因素之后,在学习电离常数之前,先进行上一节已学新知识的巩固应用)板块二:电离常数表达式一、电离常数(K)表达式1、概念:在一定温度下,当弱电解质在水溶液中达到电离平衡时,溶液中电离出的各离子与未电离的分子的的比值是一个常数。
2、表达式:(以醋酸为例)K=(设计意图:类比第二章化学平衡常数,学生很快的类比迁移至电离常数的概念和表达式)【练一练】1、请写出HClO、H2S的电离常数表达式(提示:分子中含有两个或两个以上可电离H+的多元弱酸的电离是分步进行的。
)(设计意图:对电离常数的表达式进行巩固训练,同时通过题目提出多元弱酸分步电离对应多个电离常数)板块三:电离常数的影响因素二、电离常数的影响因素【自主思考】1、两种酸HA与HB的电离常数为K1、K2,若K1<K2,能说明电离程度大小和酸性强弱吗?结论一:结论二:(设计意图:由第二章化学平衡常数的意义是可以反映出化学反应进行的限度迁移至电离常数可以反映酸性强弱,由学生进行自主思考。
通过表格所提供的两组数据来由学生自行观察总结出电离常数的影响因素)【练一练】2、下列说法正确的是()A.电离平衡常数受溶液浓度的影响B.电离平衡发生移动,电离平衡常数一定改变C.电离常数大的酸溶液中C(H+)一定比电离常数小的酸溶液中大D.电离常数的大小首先由物质的性质决定,外因受温度影响(设计意图:设计与知识点相匹配的对应练习帮助学生对所学知识进行及时巩固训练)板块四:电离常数的应用三、电离常数的应用酸性由强到弱顺序:结论:①②(设计意图:通过表格数据呈现来比较酸性强弱和电离常数大小的关系,强化这一知识点)【实验设计】请设计实验证明CH3COOH、H2CO3、H3BO3的酸性强弱。
(可供选择的药品:1mol/L醋酸溶液、饱和硼酸溶液、饱和碳酸钠溶液、氢氧化钠溶液)动脑完成验证性探究实验设计并上台来展示,提升实验动手能力)【练一练】4、已知H212(1)H2S溶液中存在哪些阴阳离子?(2)试比较这些离子的浓度大小?(设计意图:第3题是针对电离常数、电离程度和酸性强弱的再一次强化训练;第4题则是分步电离强弱的变式体现:水溶液中的主要存在离子浓度大小比较)【拓展应用】CH3COOH稀溶液加水稀释,对CH3COOH的电离平衡有什么影响?(提示:请从电离常数角度解释)(设计意图:考察的是延伸的一个知识点,浓度商和电离常数的比较应用于电离平衡移动,设在此处,拓宽了电离常数的应用范围,为学生提供了电离平衡移动的有一个解题路径)【巩固练习】1、25 ℃时,K(CH3COOH)=1.75×10-5(1)向0.1mol/L醋酸溶液中加入一定量1mol/L盐酸时,上式中的数值是否发生变化?为什么?(2)若醋酸的起始浓度为0.010mol/L,平衡时c(H+)是多少?(3)醋酸的电离度是多少?注:醋酸的电离常数很小,平衡时的c(CH3COOH)可近视为仍等于0.010mol/L。



化学选修4第三章第一节弱电解质的电离导学案(1)强弱电解质【教学目标】1、会从电离的角度认识强弱电解质的不同并能准确判断强电解质和弱电解质。
2、会正确书写电离方程式【预习案】1、复习初中化学pH值与溶液酸碱性的关系, 复习必修1课本30页有关电解质的概念2、阅读选修4课本46-47页有关C(H+)与PH的相互换算内容。
3、阅读选修4课本40页至42页相关内容,完成《百年学典》知识点1的学习和填空。
【探究案】1、从电离的角度如何认识强弱电解质的不同?2、如何书写电离方程式?【教学过程】【温故1】酸性溶液:pH 7 中性溶液:pH 7 碱性溶液:pH 7故pH越小,溶液的越强【温故2】电解质和非电解质常见的电解质是、、和【温故3】酸、碱、盐溶液是怎样导电的?酸、碱、盐溶液的导电性强弱与什么因素有关?【新课学习】【思考1】课本40页学与问酸碱盐都是电解质,在水中都能电离出离子,不同电解质的电离程度是否有区别?【探究1】观察选修4课本40页实验3-1,完成表格填空实验结果说明:等体积、等浓度的醋酸和盐酸与等量镁条反应的剧烈程度不同,而且两种酸的pH也不一样。
这是为什么呢?pH的计算方法:PH=从pH与C(H+)的换算来看,pH不同,则反映出溶液中C(H+)也。
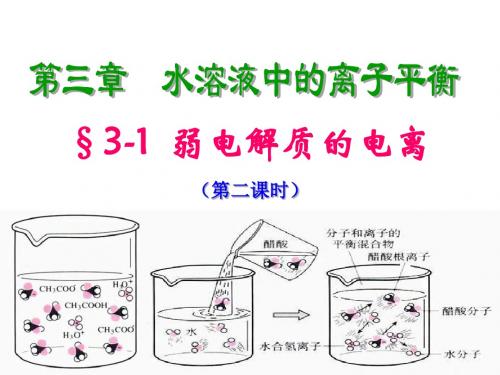
【探究2】同样是一元酸,相同浓度的HCl和CH3COOH溶液中C(H+)为何不同呢?请注意观察课本40页图3-1、3-2,你有何发现?HCl溶液中只有离子和离子,没有分子,说明HCl 电离。
电离方程式为该过程。
CH3COOH溶液中既有离子和离子,还有分子,说明CH3COOH只有发生电离,电离方程式为该过程。
一、强电解质和弱电解质1、概念:强电解质弱电解质★2、常见的强电解质①强酸:HCl、HBr、HI、H2SO4、HNO3、HClO3、HClO4等。
②强碱:NaOH、KOH、Ba(OH)2、Ca(OH)2等。
③绝大多数盐:如NaCl、(NH4)2SO4、BaSO4等。
以下是©⽆忧考⽹为⼤家整理的关于《⾼⼆化学知识点总结:电离平衡》,供⼤家学习参考!⼀、强弱电解质的判断1、电解质和⾮电解质均指化合物,单质和混合物既不是电解质⼜不是⾮电解质。
2、判断电解质的关键要看该化合物能否⾃⾝电离。
如NH3、SO2等就不是电解质。
3、电解质的强弱要看它能否完全电离(在⽔溶液或熔化时),与其溶解性、导电性⽆关。
4、离⼦化合物都是强电解质如NaCl、BaSO4等,共价化合物部分是强电解质如HCl、H2SO4等,部分是弱电解质如HF、CH3COOH、HCN、HNO2、H3PO4、H2SO3、H2CO3、HClO、NH3·H2O等,部分是⾮电解质如酒精、蔗糖等。
⼆、电离平衡1、弱电解质才有电离平衡,如⽔:2H2O =H3O++OH-。
2、电离平衡的特征:等(V电离=V结合≠0)动(动态平衡)定(各微粒浓度⼀定)变3、影响电离平衡的外界条件:温度越⾼,浓度越⼩,越有利于电离。
加⼊和弱电解质具有相同离⼦的强电解质,能抑制弱电解质的电离。
4、电离⽅程式:(1)强电解质完全电离,⽤等号,如:HCl=H++Cl_ NaHSO4=Na++H++SO42-(2)弱电解质部分电离,⽤可逆符号;多元弱酸分步电离,以第⼀步电离为主,电离级数越⼤越困难;且各步电离不能合并。
如:H3PO4 H++H2PO4- H2PO4- H++HPO42- HPO42- H++PO43-三、⽔的离⼦积(Kw)1、由⽔的电离⽅程式可知:任何情况下,⽔所电离出的H+与OH-的量相等.2、Kw=c(H+)·c(OH-),25℃时,Kw=1×10-14。
Kw只与温度有关,温度越⾼,Kw越⼤。
四、溶液的pH1、pH=-lg{c(H+)},溶液的酸碱性与pH的关系(25℃):中性溶液:C(H+)=C(OH-)=1×10-7mol/L pH=7 ,酸性溶液:C(H+)>C(OH-) pH<7,碱性溶液:C(H+)7。