实验9:碘量法测定维生素C
- 格式:ppt
- 大小:88.00 KB
- 文档页数:6

《维生素C含量的测定》教学设计(优秀范文5篇)第一篇:《维生素C含量的测定》教学设计维生素C含量的测定[教学目标](一)知识与技能1.通过实验使学生掌握碘量法测定维生素含量的原理、方法和计算。
2.通过实验使学生熟练酸式滴定管的使用方法。
(二)过程与方法通过实验使学生学会对实验误差进行分析并会采取合理可行的方法减小误差。
(三)情感态度价值观通过实验使学生认识到维生素C对人体的重要作用,从而走出对维生素C的一些认识误区,养成良好的饮食习惯。
[教学重难点]1.教学重点:碘标准溶液滴定维生素C的的实验原理以及酸性的滴定环境。
2.教学难点:酸式滴定管的使用(关于酸式滴定管使用的知识点多而且零碎)。
[教学过程] [教师]1934年4月3日年,美国教授查尔斯•葛兰•金首先分离出人体必需的维生素C,从此人类逐渐远离败血症的折磨,所以在医药上常把维生素C叫做抗坏血酸(ascorbic acid)。
维生素C,无色晶体,是一种水溶性的六碳多羟基内酯化合物,具有很强的还原性,广泛存在于植物组织中,新鲜的水果、蔬菜,特别是枣、辣椒、苦瓜、柿子叶、猕猴桃、柑橘等食品中含量尤为丰富。
除了这些,同学们知道还有哪些水果蔬菜中富含维生素C?[学生](回答)······[教师]大家说得很好,那么你们知道维生素C对人体有哪些作用吗?[学生](回答)······[教师](评价)看来大家课前都做足了功课。
现在老师来总结一下:维生素C在人体内影响胶元蛋白的形成,并且有解毒作用,另外参与多种氧化还原反应、羟化反应,还有防止贫血、可改善过敏体质以及刺激免疫系统的作用,是人体不可缺少的物质。
因此准确测定维生素C的含量,对饮食健康、医疗保健都具有十分重要的意义。
那么,今天我们就来学习维生素含量的测定。
(板书“维生素C含量的测定”)根据我刚才对维生素C的一些介绍,对于本次的实验的方法,大家有没有一些想法?[学生](回答)······[教师](评价)其实,维生素C含量的测定方法大体可以分为滴定法、光度分析法和高效液相色谱法等,而滴定法又有2,6一二氯靛酚法和电位滴定法等,光度分析法又有2,4一二硝基苯肼分光光度法和钼蓝比色法等,至于高效液相色谱法又有HYPERSIL—C8色谱柱法和VenusilXBP—C18柱法等。


维生素C制剂及果蔬中抗坏血酸含量的直接碘量法测定一、实验目的1. 掌握碘标准溶液的配制和标定方法。
2. 了解直接碘量法测定抗坏血酸的原理和方法。
二、实验原理维生素C(Vc)又称抗坏血酸,分子式为C6H8O6。
Vc具有还原性,可被I2定量氧化,因而可用I2标准溶液直接滴定。
其滴定反应式为:C6H8O6+I2=C6H6O6+2HI。
用直接碘量法可测定药片、注射液、饮料、蔬菜、水果等中的Vc含量。
由于Vc的还原性很强,较易被溶液和空气中的氧氧化,在碱性介质中这种氧化作用更强,因此滴定宜在酸性介质中进行,以减少副反应的发生。
考虑到I-在强酸性溶液中也易被氧化,故一般选在pH=3~4的弱酸性溶液中进行滴定。
三、主要试剂1. I2溶液(约0.05mol·L-1):称取3.3g I2和5g KI,置于研钵中,加少量水,在通风橱中研磨。
待I2全部溶解后,将溶液转入棕色试剂瓶中,加水稀释至250mL,充分摇匀,放暗处保存。
2. Na2S2O3标准溶液(约0.01mol·L-1)3. 淀粉溶液(0.2%)4. HAc(2mol·L-1)5. 固体Vc样品(维生素C片剂)6. K2Cr2O7标准溶液(约0.020mol·L-1)7. KIO3标准溶液(约0.002mol·L-1)8. 果蔬样品(如西红柿、橙子、草莓等)9. KI溶液(约25%)四、实验步骤1. I2溶液的标定用移液管移取25.00mL Na2S2O3标准溶液于250mL锥形瓶中,加50mL蒸馏水,5mL 0.2%淀粉溶液,然后用I2溶液滴定至溶液呈浅蓝色, 30s内不褪色即为终点。
平行标定三份,计算I2溶液的浓度。
2. 维生素C片剂中Vc含量的测定准确称取约0.2g研碎了的维生素C药片,置于250mL锥形瓶中,加入100mL新煮沸过并冷却的蒸馏水,10mL 2mol·L-1 HAc溶液和5mL 0.2%淀粉溶液,立即用I2标准溶液滴定至出现稳定的浅蓝色,且在30s内不褪色即为终点,记下消耗的I2溶液体积。

抗坏血酸药品中维生素C 含量的测定一、实验目的1.掌握碘标准溶液的配制注意事项;2.通过维生素C 的测定了解直接碘量法和间接碘量法的过程;3.掌握碘量法测定抗坏血酸药品中维生素C 含量的原理和方法。
二、实验用品 1.仪器全自动分析天平;台秤;碘量瓶;玻璃棒;洗瓶;试剂瓶;烧杯;酸式滴定管;量筒;胶头滴管;容量瓶;移液管;洗耳球。
2.试剂分析纯O H O S 23225Na ⋅,分析纯2I ;7221-r mol 017.0O C K L ⋅标准溶液;)s (KI 、KI 溶液100-1L g ⋅,使用前配制;淀粉指示剂1-g 5L ⋅;)(s a 32CO N ;l HC 溶液1-mol 6L ⋅;败坏血酸片。
三、实验原理抗坏血酸又名维生素C ,分子式686O H C 。
由于分子中的烯二醇基具有还原性,能被2I 定量地氧化成二酮基,其反应式为:碱性条件下可使反应向右进行完全,但因维生素C 还原性很强,在碱性溶液中尤其易被空气氧化,在酸性介质中较为稳定,故反应应在稀酸(如稀乙酸、稀硫酸或偏磷酸)溶液中进行,并在样品溶于稀酸后,立即用碘标准溶液进行滴定。
根据滴定消耗的2I 标准溶液的体积,便可计算出抗坏血酸药品中维生素C 的含量。
计算公式:%100m %100m m 68622⨯=⨯=药品药品维生素O H C I I C M V C W2I 标准溶液的配制和标定:由于通常使用的市售2I 试剂纯度不高,故需先配成近似浓度,然后在进行标定。
2I 微溶于水而易溶于KI 溶液中,但在稀的KI 溶液中溶解得很慢,故配制2I 溶液时应先在较浓的KI 溶液中进行,待溶解完全后再稀释到所需浓度。
2I 溶液可以用32s O A 为基准物对I 2溶液进行标定,但32s O A (俗称砒霜)有剧毒,故用322a O S N 标准溶液进行标定。
322a O S N 标准溶液的配制和标定:固体试剂O H O S N 23225a ⋅通常含有一些杂质,且易风化和潮解,因此,322a O S N 标准溶液采用标定法配制。


简述碘量法测定维生素c的原理
碘量法测定维生素C原理:
维生素C具有很强的碘敏感性,因此可以采用碘量法测定维生素C的含量。
碘量法测定维生素C的原理是:
样品中的维生素C在某特定条件下,把碘溶液中的游离碘转变成有机碘,并产生相应的光学变化,这种光学变化的强度可用以就维生素C的含量,从而实现对维生素C的测定。
碘量法测定维生素C的过程可以分为以下几个步骤:
1.将检测样品通过碘蒸馏技术,将其中的游离碘转变成有机碘,以及将维生素C的其他小分子溶出;
2.将维生素C添加一定浓度的甲萘基四胺,使其转变成碘分子;
3.将维生素C的蒸馏水与作为产生参照光的紫外线照射,观察紫外线光强度的变化,并用以评估有机碘的含量;
4.检测样品的浓度,并和参照光比较,从而确定维生素C的含量。
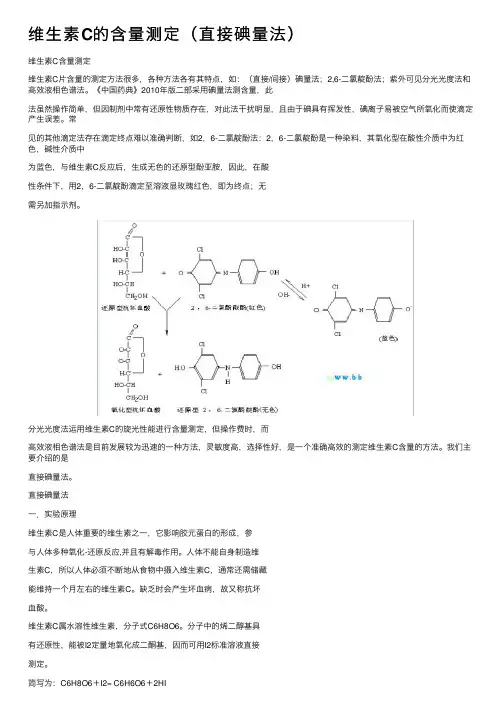
维⽣素C的含量测定(直接碘量法)维⽣素C含量测定维⽣素C⽚含量的测定⽅法很多,各种⽅法各有其特点,如:(直接/间接)碘量法;2,6-⼆氯靛酚法;紫外可见分光光度法和⾼效液相⾊谱法。
《中国药典》2010年版⼆部采⽤碘量法测含量,此法虽然操作简单,但因制剂中常有还原性物质存在,对此法⼲扰明显,且由于碘具有挥发性,碘离⼦易被空⽓所氧化⽽使滴定产⽣误差。
常见的其他滴定法存在滴定终点难以准确判断,如2,6-⼆氯靛酚法:2,6-⼆氯靛酚是⼀种染料,其氧化型在酸性介质中为红⾊,碱性介质中为蓝⾊,与维⽣素C反应后,⽣成⽆⾊的还原型酚亚胺,因此,在酸性条件下,⽤2,6-⼆氯靛酚滴定⾄溶液显玫瑰红⾊,即为终点;⽆需另加指⽰剂。
分光光度法运⽤维⽣素C的旋光性能进⾏含量测定,但操作费时,⽽⾼效液相⾊谱法是⽬前发展较为迅速的⼀种⽅法,灵敏度⾼,选择性好,是⼀个准确⾼效的测定维⽣素C含量的⽅法。
我们主要介绍的是直接碘量法。
直接碘量法⼀.实验原理维⽣素C是⼈体重要的维⽣素之⼀,它影响胶元蛋⽩的形成,参与⼈体多种氧化-还原反应,并且有解毒作⽤。
⼈体不能⾃⾝制造维⽣素C,所以⼈体必须不断地从⾷物中摄⼊维⽣素C,通常还需储藏能维持⼀个⽉左右的维⽣素C。
缺乏时会产⽣坏⾎病,故⼜称抗坏⾎酸。
维⽣素C属⽔溶性维⽣素,分⼦式C6H8O6。
分⼦中的烯⼆醇基具有还原性,能被I2定量地氧化成⼆酮基,因⽽可⽤I2标准溶液直接测定。
简写为:C6H8O6+I2= C6H6O6+2HI使⽤淀粉作为指⽰剂,⽤直接碘量法可测定药⽚、注射液、饮料、蔬菜、⽔果中维⽣素C的含量。
由于维⽣素C的还原性很强,较容易被溶液和空⽓中的氧氧化,在碱性介质中这种氧化作⽤更强,因此滴定宜在酸性介质中进⾏,以减少副反应的发⽣。
考虑到I - 在强酸性中也易被氧化,故⼀般选在pH为3~4的弱酸性溶液中进⾏滴定。
由于碘具有挥发性,碘离⼦易被空⽓所氧化⽽使滴定产⽣误差;⼜由于碘的挥发性和腐蚀性,使碘标准滴定溶液的配制及标定⽐较⿇烦。

直接碘量法测定维生素c含量
维生素C,也被称为抗坏血酸,是一种水溶性维生素。
它在许多生物体内起着重要的生理作用,并且对人体有益。
维生素C含量测定是基于一种叫做碘量法的化学方法。
该方法利用碘酸钾溶液与维生素C反应的化学性质,通过了解反应后剩余的碘酸钾的含量来测定维生素C含量。
碘量法测定维生素C的过程如下:
准备样品:将要测定的样品加入到3%的浓磷酸中,并将其加热到约80℃,然后再冷却。
制备碘酸钾溶液:将20克的碘酸钾加入到1000毫升的蒸馏水中,并充分搅拌,以制备出0.1N的碘酸钾溶液。
测定过程:将取出的样品加入到定容瓶中,加入足够的蒸馏水,直至瓶子充满为止。
然后取出1毫升的样品溶液,并将其加入到滴定瓶中。
加入几滴淀粉溶液。
此时,溶液会变成淡蓝色。
准备滴定剂:将制备好的碘酸钾溶液滴加到另一个滴定瓶中,并加入适量的酒精。
通过滴加,将滴定剂加入到样品溶液中,直至溶液变成深蓝色。
读取数据:记录滴定剂滴入样品溶液的次数,并且根据已知的滴定剂浓度计算出维生素C的含量。
利用碘量法可以准确地测定含有维生素C的食物以及药品的维生素C含量。
然而,由于该测量方法需要使用化学试剂和复杂的实验过程,所以在实践中不太实用。
为了更加方便测量维生素C的含量,也出现了其他测量方法,例如高效液相色谱法和光谱法。
无论使用哪种方法测量维生素C的含量,都可以帮助人们了解他们摄入的营养成分,以及制定更加健康的膳食计划。

分析化学实验果汁中Vc含量的测定以及比较化学学院2008级化学二班方基永果汁中维生素C的含量测定以及比较前言:1.维生素C(Vitamin C ,Ascorbic Acid)又叫L-抗坏血酸,是一种水溶性维生素。
食物中的维生素C被人体小肠上段吸收。
一旦吸收,就分布到体内所有的水溶性结构中,正常成人体内的维生素C代谢活性池中约有1500mg维生素C,最高储存峰值为3000mg维生素C。
正常情况下,维生素C绝大部分在体内经代谢分解成草酸或与硫酸结合生成抗坏血酸-2-硫酸由尿排出;另一部分可直接由尿排出体外。
2.Vc在中国现在中国已经掌握了维生素C生产的领导地位,应该可以彻底解决病毒的问题,只是出产的维生素C大部份都外销,中国人服用维生素C的平均剂量,远逊于欧美和日本。
如果我们普遍认识维他命C对预防和治疗病毒传染病症的原理而大量服用,就可以遏止各种病毒的流行。
流行感冒只是一小事,维他命C的真正效用,会显示在治疗禽流感,SARS和AIDS等更严重的病毒传染病上。
3.正常需求1)、成人及孕早期妇女维生素C的推荐摄入量为100mg/d;2)、中、晚期孕妇及乳母维生素C的推荐摄入量为130mg/d。
注意:每个人对于VC的需求量个体化差异是很大的。
有的人补充少量既可满足,有的人可以达到每天10克甚至更高。
在人类对维生素C的研究史上,卡斯卡特医生(Robert F.Cathcart)早在上世纪70年代初就发现并建立了一套使用维生素C的标准。
当一个人口服维生素C达到相当的量,即24小时0.5~200克时,由于肠道渗透压的改变,会产生轻微的腹泻。
卡斯卡特将略低于此的量叫做“维生素C的肠道耐受量”,也就是一个人能承受的不引起轻微腹泻的量。
因为无酸性的VC,使大量口服维生素C成为可能,那么,每个人就可以根据自身体况的不同去服用。
只要在自己的肠道耐受量之内,效果就会很好。
有趣的是,人体对于VC的肠道耐受量是变化的。
在人体有病的时候,肠道耐受量会大幅度的提升,比如平时1克的耐受量,在急性感染或者患有肿瘤、心脏病等慢性疾病,甚至是感冒的时候,都会有不同程度的耐受量提升。

碘量法测定维生素c的含量原理宝子们,今天咱们来唠唠碘量法测定维生素C含量的原理,可有趣儿啦。
咱先得知道维生素C这小宝贝儿,它在咱们身体里可起着超级重要的作用呢。
在化学世界里,它也有自己独特的脾气。
维生素C有很强的还原性,就像一个小小的还原剂精灵。
那碘量法是咋回事呢?碘啊,它在这个测定里就像一个小侦探。
碘单质有氧化性,这氧化性就像是碘的超能力。
当我们把含有维生素C的样品和碘溶液放在一起的时候,就像一场小小的化学大战开始了。
维生素C这个还原性的小战士,就会和碘这个有氧化性的家伙打起来。
因为维生素C的还原性,它会把碘给还原了。
反应方程式就像是它们战斗的记录,维生素C和碘反应,会让碘变成碘离子。
这个过程啊,就好像是维生素C把碘的氧化性这个“超能力”给夺走了,碘从那个有氧化性的碘单质变成了比较“低调”的碘离子。
在这个反应里,碘单质和维生素C的反应是按照一定的化学计量关系进行的。
就好比是两个人打架,有一定的规则,一个维生素C分子能和一定数量的碘分子反应。
这就给我们测定维生素C的含量提供了线索。
那我们怎么知道有多少碘和维生素C反应了呢?这时候就需要用到淀粉这个小助手啦。
淀粉可神奇了,它就像一个小信号员。
当有碘单质存在的时候,淀粉就会和碘单质结合,然后溶液就会变成蓝色,就像变魔术一样。
但是呢,当所有的碘单质都被维生素C还原成碘离子的时候,这个蓝色就消失了。
我们就可以通过看这个蓝色什么时候消失,来知道有多少碘参与了和维生素C的反应。
比如说,我们先配好已知浓度的碘溶液,然后把含有维生素C的样品加进去。
慢慢的,碘就会和维生素C反应。
我们可以一直滴加碘溶液,直到溶液出现蓝色并且持续一小会儿不消失。
这个时候我们就能根据加入的碘溶液的量来计算维生素C的含量啦。
因为我们知道碘溶液的浓度,也知道加入了多少碘溶液,再根据碘和维生素C反应的化学计量关系,就能算出样品里维生素C的含量了。
这整个过程就像是一场有趣的化学游戏。
维生素C、碘和淀粉它们都扮演着不同的角色。

维生素c含量测定碘量法实验报告
实验目的:
本实验旨在通过维生素c含量测定碘量法,掌握测定维生素c的方法和技能,同时加深对维生素c的认识。
实验原理:
碘量法是一种常用的测定维生素c含量的方法。
其原理是利用维生素c在氯化亚铁和碘酸钾的存在下,被氧化为脱氢抗坏血酸,然后用碘量法测定反应结束时残余的碘量,从而计算出维生素c的含量。
实验步骤:
1.将维生素c样品溶解于少量水中,加入5%的氯化亚铁溶液,使其完全还原。
2.加入2ml的碘酸钾溶液,并用0.1mol/L的氢氧化钠溶液调节溶液pH值为2-3。
3.用0.1mol/L的硫酸滴定溶液滴定反应液,直至溶液呈浅黄色,再加入几滴淀粉指示剂,继续滴定至溶液呈蓝色。
4.测量反应液的体积,计算出维生素c的含量。
实验结果:
在本实验中,我们测定了三个不同维生素c含量的样品,分别为0.1g、0.2g和0.3g。
在滴定过程中,我们发现反应液颜色会在滴定末几滴发生明显变化,这时需谨慎滴加滴定液,避免过度滴定。
最终的实验结果表明,三个样品的维生素c含量分别为0.096g、0.192g和0.284g。
实验结论:
通过本实验,我们掌握了维生素c含量测定碘量法的方法和技能,同时加深了对维生素c的认识。
实验结果表明,维生素c含量与样品添加量成正比,可以通过碘量法准确测定。
实验注意事项:
1.在实验过程中,应注意安全,避免溶液溅出,避免接触皮肤和眼睛。
2.在滴定时,应注意滴定液的速度,避免过度滴定。
3.实验前应检查所用试剂的质量和纯度,避免影响实验结果。
4.实验后应及时清洗实验器材,保持实验室卫生。
维生素c碘量法原理维生素C碘量法原理维生素C是一种重要的水溶性维生素,也称为抗坏血酸。
它在人体内具有多种生理作用,如参与氧化还原反应、促进铁吸收、增强免疫力等。
因此,准确测定维生素C含量对于保障人体健康至关重要。
其中,碘量法是一种常用的测定维生素C含量的方法。
1. 碘量法的基本原理碘量法是利用维生素C作为还原剂,将其氧化成脱氢抗坏血酸(DHA),然后再利用加入过量碘离子与DHA发生反应生成二碘化物(I2)。
在反应中,过量的碘离子被消耗完毕后会出现自由碘(I2),自由碘与淀粉溶液反应形成蓝色复合物。
通过比较样品和标准溶液所需的碘滴定体积来计算样品中维生素C的含量。
2. 碘液制备制备0.05mol/L的I2溶液:将4.95g固体I2称入干燥瓶中,加入约10mL无水乙醇,摇匀,使I2溶解。
再加入适量的去离子水至1000mL,摇匀。
最后,用0.1mol/L的氢氧化钠溶液调节pH至6.5-7.5即可。
3. 标准曲线制备将维生素C标准品称取适量(如10mg),加入10mL 4%三氯乙酸溶液中,在冰浴中搅拌30min。
然后用去离子水稀释至50mL,摇匀后即为1mg/mL的标准溶液。
将该标准溶液分别稀释成不同浓度(如0.05、0.1、0.2、0.4、0.6mg/mL),每个浓度各取一定体积(如1mL)放入试管中,加入4%三氯乙酸溶液调节pH至2-3,然后加入10mL碘液,摇匀并静置15min。
之后用1%淀粉溶液滴定到蓝色消失即可。
4. 样品处理将样品称取适量(如5g),加入50mL 4%三氯乙酸溶液中,在冰浴中搅拌30min。
然后用去离子水稀释至100mL,摇匀后过滤。
取10mL滤液加入试管中,加入4%三氯乙酸溶液调节pH至2-3,然后加入10mL碘液,摇匀并静置15min。
之后用1%淀粉溶液滴定到蓝色消失即可。
5. 计算维生素C含量用标准曲线得出样品所需的碘滴定体积(如V),用下式计算维生素C含量:维生素C(mg/100g)= V×C×1000/m其中,C为标准曲线中维生素C的浓度(mg/mL),m为样品质量(g)。
直接碘量法测VC一.实验目的1.掌握碘标准溶液的配制和标定方法;2.了解直接碘量法测定维生素C 的原理和方法。
二.实验原理维生素C (Vc )又称抗坏血酸,分子式686O H C ,分子量1mol •176.1232/g 。
Vc 具有还原性,可被2I 定量氧化,因而可用2I 标准溶液直接滴定。
其滴定反应式为:。
由于Vc 的还原性很强,较易被溶液和空气中的氧氧化,在碱性介质中这种氧化作用更强,因此滴定宜在酸性介质中进行,以减少副反应的发生。
考虑到-I 在强酸性溶液中也易被氧化,故一般选在pH=3~4的弱酸性溶液中进行滴定。
使用淀粉作为指示剂,用直接碘量法可测定水果中维生素C 的含量。
I 2标准溶液采用间接配制法获得,用Na 2S 2O 3标准溶液标定,反应如下: 2S 2O 32-+I 2 = S 4O 62-+2I-器材和药品1.器材 天平(0.1mg ),碱式滴定管(50 mL)、酸式滴定管(50mL ),碘量瓶(250mL ),移液管(20mL )锥形瓶(250ml )、量筒、棕色瓶(250mL )。
从此以下未整理2.药品 果汁、K 2Cr 2O 7(基准试剂),Na 2S 2O 3(0.02mol·L-1),I 2(0.01 mol·L-1),KI (20%)、HCl,(6mol·L-1),HAc (2mol·L-1),淀粉指示剂(0.5%)。
Na2CO3固体 以上试剂未说明均为分析纯,水为蒸馏水所需试剂的用量及配制方法:1、 0.1 mol·L-1Na 2S 2O 3标准溶液的配制称取25g Na 2S 2O 3·5H 2O ,溶于1000mL 新煮沸并冷却的蒸馏水中,加入0.2gNa2CO3使溶液呈碱性,以防止Na 2S 2O 3的分解,保存于棕色瓶中,放置10天后过滤,再标定.放置长时间后,再用前应重新标定。
2、K 2Cr 2O 7标准溶液的配制准确称取基准试剂K 2Cr2O 7 0.26—0.28g 于小烧杯中,加入少量蒸馏水溶解后,移入200ml 容量瓶中,用蒸馏水稀释至刻度,摇匀.3、0.1 mol·L-1Na2S2O3标准溶液的标定用移液管吸取上述标准溶液20. 00ml 于250ml 碘瓶中,加8ml 6 mol·L HCl,5-8ml 20%KI 溶液,盖上表面皿,在暗处放5分钟后,加100ml 水,立即以用待标定的Na2S2O3溶液滴定至淡黄色,再加入2ml 0.5%淀粉溶液, 继续滴至溶液呈亮绿色为终点.平行滴定3次。