常见感染致病菌耐药机制及防治对策
- 格式:pdf
- 大小:115.16 KB
- 文档页数:5

细菌的耐药机理与应对措施细菌是一类微生物,它们广泛分布在自然界中,有些细菌可以对抗药物,从而造成药物耐受性。
这就带来了医学上非常严重的问题,因为耐药细菌的存在使得某些疾病的治疗变得非常困难。
如果我们想要解决这个问题,就需要了解细菌的耐药机理以及应对措施。
一、细菌的耐药机理耐药是由细菌表达出来的一种属性,细菌可以通过多种方式对于抗生素产生耐受性。
其中比较常见的方式有:1. 基因变异细菌具有遗传变异能力,这种变异可能导致某些基因的表达发生改变,这对细菌来说可能是一种保命的机制。
某些细菌在不断进化过程中,可能会获得顽强的耐药性,这就是基因变异所带来的结果。
2. 分享基因信息细菌学中有一个重要的概念,叫做共生。
大多数情况下,细菌会形成群体,通过信息传递等方式进行合作。
在一个细菌群体内,如果某些细菌获得了耐药基因,那么它们就会与其他细菌分享这些信息,以便于整个群体获得更好的生存机会。
3. 改变细胞壁结构除了遗传变异和分享基因信息之外,细菌还可以通过改变细胞壁结构的方式来获取耐药性。
这种方式的主要原理是通过减少细胞膜自由流动性,从而获得对于抗生素的耐受性。
二、应对细菌耐药的措施细菌的耐药性对于医学是一个严重的挑战,但是我们可以通过一系列措施来应对这个问题。
下面列举了一些主要的措施:1. 优化使用抗生素抗生素的滥用是导致细菌耐药的一个主要因素。
因此,在应对细菌的耐药性问题时,我们需要优化抗生素的使用方式,仅当确实需要使用时才使用抗生素,并且要严格遵守使用规范。
2. 加强感染控制细菌感染是产生抗生素耐药性的另一个重要原因。
如果我们能够加强感染的控制,尽可能减少细菌感染,那么就可以减缓细菌抗药性的扩散速度。
3. 使用新型抗生素传统的抗生素已经开始失效,因此我们需要寻找新的抗生素。
现代生物科技的发展已经让我们可以更加深入地研究细菌的生物学特性,从而开发出具有高效抗菌作用和低毒副作用的新型抗生素。
4. 加强科学研究对细菌进行深入的科学研究,研发出更好的治疗方法和药物,是解决细菌耐药性问题的有效方法之一。

耐药菌的管理及防护措施
管理耐药菌的主要措施包括:
1.加强监测:建立和加强耐药菌的监测体系,定期进行细菌培养和药敏试验,及时监测和识别
耐药菌的类型和分布情况。
2.合理使用抗生素:医务人员应根据患者具体情况合理使用抗生素,并遵循抗生素使用指南,
避免滥用和不必要的使用,防止耐药菌的产生。
3.加强感染控制和预防:医疗机构应加强感染控制措施,包括洗手、消毒和隔离措施等,降低
耐药菌的交叉感染风险。
4.培训和教育:加强医务人员和患者的培训和教育,提高对耐药菌的认识和防护意识,推广正
确的使用抗生素和感染控制措施。
预防耐药菌感染的具体措施包括:
1.个人防护:保持良好的个人卫生习惯,经常洗手,并避免接触已感染或潜在感染的人或物品。
2.正确使用抗生素:使用抗生素时需按照医生的建议和处方使用,并完成整个疗程,切勿滥用
或过量使用。
3.避免交叉感染:在医疗机构和公共场所,遵守相关的感染控制措施,如洗手、消毒、使用口
罩等,避免与患者或病原体接触。
4.保持环境清洁:保持环境的清洁和卫生,定期清洁和消毒常接触的物品表面,如手机、键盘等。
5.接种疫苗:按照相关的疫苗接种建议,接种预防感染的疫苗,以提高抵抗力。
6.促进研究和开发新的抗生素:加强对耐药菌的研究,推动开发新的抗生素和抗菌药物,以应
对不断出现的耐药菌株。
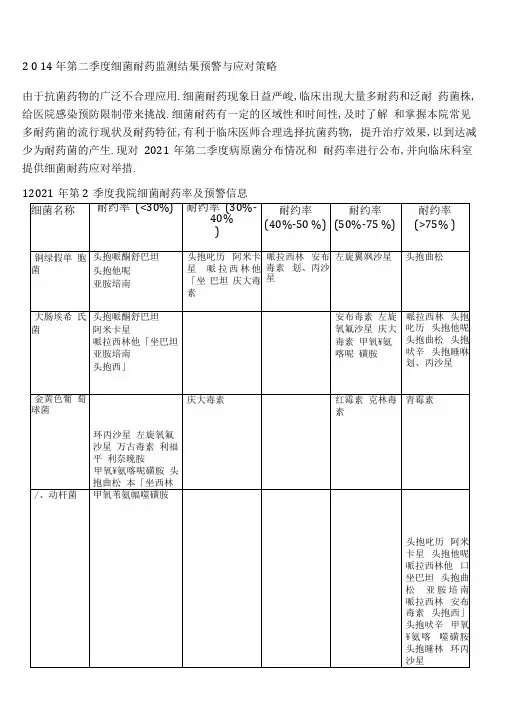
2 0 14 年第二季度细菌耐药监测结果预警与应对策略由于抗菌药物的广泛不合理应用.细菌耐药现象日益严峻,临床出现大量多耐药和泛耐药菌株,给医院感染预防限制带来挑战.细菌耐药有一定的区域性和时间性,及时了解和掌握本院常见多耐药菌的流行现状及耐药特征,有利于临床医师合理选择抗菌药物, 提升治疗效果,以到达减少为耐药菌的产生.现对2021年第二季度病原菌分布情况和耐药率进行公布,并向临床科室提供细菌耐药应对举措.12021年第2季度我院细菌耐药率及预警信息细菌名称耐约率(<30%)耐约率(30%-40%)耐约率(40%-50 %)耐约率(50%-75 %)耐约率(>75% )铜绿假单胞菌头抱哌酮舒巴坦头抱他呢亚胺培南头抱叱历阿米卡星哌拉西林他「坐巴坦庆大毒素哌拉西林安布毒素划、丙沙星左旋翼飒沙星头抱曲松大肠埃希氏菌头抱哌酮舒巴坦阿米卡星哌拉西林他「坐巴坦亚胺培南头抱西」安布毒素左旋氧氟沙星庆大毒素甲氧¥氨喀呢磺胺哌拉西林头抱叱历头抱他呢头抱曲松头抱吠辛头抱睡咻划、丙沙星金黄色葡萄球菌环丙沙星左旋氧氟沙星万古毒素利福平利奈晚胺甲氧¥氨喀呢磺胺头抱曲松本「坐西林庆大毒素红霉素克林毒素青霉素/、动杆菌甲氧苇氨幅噬磺胺头抱叱历阿米卡星头抱他呢哌拉西林他口坐巴坦头抱曲松亚胺培南哌拉西林安布毒素头抱西」头抱吠辛甲氧¥氨喀噬磺胺头抱睡林环丙沙星左旋氧氟沙星庆大毒素肺炎克'番伯菌头抱哌酮舒巴坦阿米卡星哌拉西林他「坐巴坦亚胺培南划、丙沙星左旋氧氟沙星头抱西」庆大毒素安布毒素头抱叱历头抱他呢头抱曲松头抱吠辛头抱睡咻甲氧平氮喀噬磺胺哌拉西林肺炎链球菌头抱叱历左旋氧氟沙星青霉素万古毒素头抱曲松头抱吠辛红霉素克林毒素甲氧¥氨喀呢磺胺表皮葡锢球菌万古霉素利福平利奈晚胺左旋氧氟沙星环丙沙星克林毒素甲氧平氮喀呢磺胺红霉素本「坐西林头抱曲松庆大毒素卡他布兰汉菌头抱哌酮舒巴坦哌拉西林他「坐巴坦左旋氧氟沙星头抱叱历头抱曲松头抱吠辛头抱西」头抱睡林甲氧平氮喀呢磺胺庆大毒素青霉素屎肠球菌万古霉素利奈晚胺红霉素青霉素左旋氧氟沙星利福平环丙沙星流感嗜血杆菌头抱叱历头抱哌酮舒巴坦头抱曲松左旋氧氟沙星利福平克林毒素红毒素头抱吠辛庆大毒素甲氧平氮喀呢磺胺青霉素备注:耐药率超过30%的抗菌药物,提示“预警抗菌药物〞;耐药率超过40%的抗菌药物,提示“慎用抗菌药物〞;耐药率超过50%的抗菌药物,提示“参照药敏试验结果用药〞;耐药率超过75%的抗菌药物,提示“暂停该类抗菌药物的临床应用〞.2细菌产生耐药性机制2.1铜绿假单胞菌耐药机制铜绿假单胞菌对生存环境和营养条件要求很低,在自然界分布广泛,甚至在医院内环境经常可见,其具有多药耐药性及耐药机制:〔1〕该菌能够产生破坏抗菌药物活性的多种灭活酶、钝化酶和修饰酶.〔2〕基因突变,作用靶位变异.〔3〕细胞膜通透性降低.〔4〕主动泵出机制将进入的药物排到体外.〔5〕产生生物膜,阻隔白细胞、多种抗体及抗菌药物进入细菌细胞内吞噬细菌.由于铜绿假单胞菌复杂的耐药机制导致其感染具有难治性和迁延性.2.2大肠埃希氏菌耐药机制大肠埃希菌是G-杆菌中别离率较高的时机致病菌,可引起人体所有部位的感染并且呈多重耐药性.(1)&内酰胺酶的产生①大肠埃希菌对B -内酰胺类抗菌药物耐药主要是由超广谱B -内酰胺酶〔ESBLs〕引起的, 对头霉素类及碳青霉烯类药物敏感. ESBLs可分为五大类:TEM型、SHV型、CTX-M 型、OXA 型和其他型,大肠埃希菌ESBLs酶以TEM型最常见.TEM型ESBLs呈酸性, 可水解头抱他咤、头抱曝历.SHV型ESBLs呈碱性,有水解头抱嚷吩的航基. CTX-M 型ESBLs呈碱性,对头抱曝肠水解水平强于头抱他咤.OXA型ESBLs呈弱酸性或弱碱性,主要水解底物是苯嘎西林,OXA型酶主要见于铜绿假单胞菌中,在大肠埃希菌中的别离率较低.②AmpC&内酰胺酶AmpC酶主要作用于头抱菌素类抗菌药物,且不能被克拉维酸抑制. 它是水解酶,与&内酰胺环竣基局部共价结合,在水分子作用下导致&内酰胺环开环,破坏&内酰胺类抗菌药物抗菌活性.③对酶抑制剂药的耐药的 &内酰胺酶对酶抑制剂药的耐药的 &内酰胺酶〔IRT〕主要有TEM 系列衍变而来,又称为耐酶抑制剂TEM系列酶.〔2〕药物作用靶位的改变〔3〕主动外排〔4〕外膜通透性的下降2.3肺炎克雷伯杆菌耐药机制肺炎克雷伯杆菌属于阴性杆菌,通常存在于人类肠道、呼吸道,是除大肠埃希氏菌外导致医源性感染的最重要的条件致病菌.由于抗菌药物的大量使用,在选择性压力下多药耐药肺炎克雷伯杆菌〔KPN〕菌株不断出现,耐药率日益上升,KPN耐药机制包括:〔1〕产抗菌药物灭活酶①&内酰胺酶包括产超广谱 &内酰胺酶〔ESBLs〕、AmpC酶、耐酶抑制剂&内酰胺酶、碳青霉烯酶〔KPC酶〕及金属&内酰胺酶〔MBLs〕等.ESBLs是耐药KPN产生的最主要的一类酶,由质粒介导,产ESBLsKPN对青霉素类、头抱菌素类及单环类药物耐药,但对头霉素类和碳青霉烯类及酶抑制剂敏感.KPN中AmpC酶由质粒介导,AmpC酶使KPN对临床上广谱&内酰胺类药物耐药, 且不能被&内酰胺酶抑制剂克拉维酸、舒巴坦抑制,但对碳青霉烯类敏感.产耐酶抑制剂&内酰胺酶菌株对青霉素类及青霉素与 &内酰胺酶抑制剂克拉维酸、舒巴坦的复合制剂均不敏感,可被他噪巴坦抑制.碳青霉烯酶〔KPC酶〕不能被EDTA抑制,由质粒介导.产KPC酶KPN对广谱头抱菌素类、单环类及碳青霉烯类耐药.2021年外国学者Eleman等发现2例携带KPC酶的泛耐药KPN甚至对多粘菌素和替加环素耐药.金属&内酰胺酶〔MBLs〕能被EDTA抑制,包括IMP、VIM、NDM-1等类型,前两者最常见且分布广泛.产MBLsKPN对头抱菌素类、单环类以及碳青霉烯类耐药.由于其具有较强耐药性和传播性,被媒体称为“超级细菌〞.②氨基糖昔修饰酶〔AMEs〕 KPN对氨基糖昔类耐药的主要机制是产AMEs,该酶可修饰抗菌药物分子中某些保持抗菌活性所必需的基团,使其与作用靶位核糖体的亲和力大为降低而导致耐药.修饰酶包括N-乙酰转移酶〔AAC〕、腺昔转移酶〔ANT〕、磷酸转移酶〔APH〕等.多药耐药KPNAMEs阳性率高达86.9%.〔2〕抗菌药物渗透障碍①细菌生物被摸〔BF〕形成BF是细菌适应环境形成的一种保护性生存方式,是细菌吸附于生物医学材料或机体黏膜外表,分泌多糖蛋白复合物后缠绕并聚集不同细菌隐藏其内部而形成的膜状物.由于BF具有屏障作用,其内部细菌得以被保护,从而逃脱免疫和抗菌药物的杀伤作用,其内部细菌得以被保护,从而逃脱免疫和抗菌药物的杀伤作用, 使其失效.BF菌的特殊结构和生理特性使菌体内抗菌药物浓度显着降低,而低于致死量的抗菌药物更易诱导细菌产生 &内酰胺酶而导致耐药.外膜孔蛋白的改变革兰阴性菌细胞外膜上存在由许多微孔蛋白组成的孔道,溶质可通过孔道进入外周间隙.假设微孔蛋白改变或缺失,那么抗菌药物难以渗入细菌细胞内,导致耐药.孔蛋白的改变能提升细菌耐药性,与灭活酶并存时的耐药程度较灭活酶单独作用时高,可降低KPN 对碳青霉烯类药物的敏感性.〔3〕主动外排机制主动外排以ATP供能,主动将渗入细菌细胞内的抗菌药物泵出胞外, 外排底物包括&内酰胺类、大环内酯类、唾诺酮类等抗菌药物.〔4〕抗菌药物作用靶位改变①DNA旋转酶和拓扑异构酶构象变异DNA旋转酶和拓扑异构酶构象发生变化,使抗菌药物不能与酶-DNA复合物结合,不能阻止细菌DNA的合成.引起KPN对曜诺酮类耐药.另一种机制是细菌产生由质粒介导的耐药基因qnr,其编码蛋白与拓扑异构酶IV特异性结合,从而减少了唾诺酮类药物的作用靶点,导致细菌耐药.②16srRNA甲基化酶细菌通过产16srRNA基因甲基化酶使药物作用靶位(16srDNA ) 甲基化,导致甲基化的16srDNA与氨基糖昔类药物的亲和力下降而耐药.产16srRNA 甲基化酶的细菌对氨基糖甘类泛耐药.(5)基因盒-整合子系统与细菌耐药性的获得和传播相关的基因元件,即整合子.它是能捕获外源基因使其转变为功能性基因的移动性DNA分子.常位于染色体、质粒或转座子上,并能在其间移动.I、II和田类整合子为耐药整合子.KPN中的整合子多为I、出类,II类整合子携带率降低.整合子可以在菌种间流动,在KPN多药耐药性的介导及传递中具有重要意义,促进KPN不断出现新的耐药方式,对临床治疗提出了严峻挑战.2.4鲍曼不动杆菌耐药机制鲍曼不动杆菌广泛分布于外界环境,主要存在水和土壤中,易在潮湿环境中生存, 如浴盆、肥皂盒等处.该菌粘附力极强,易在各类医用材料上粘附,成为潜在贮菌源. 此外,该菌还存在于健康人皮肤、咽部,也存在于结膜、唾液、胃肠道及阴道分泌物中. 感染源可以是患者自身(内源性感染),亦可以是鲍曼不动杆菌感染者或带菌者,尤其是双手带菌的医务人员.(1)产生抗菌药物灭活酶:①&内酰胺酶:最主要的是D组的OXA-23酶,局部菌株还携带超广谱&内酰胺酶(ESBLs)、头抱菌素酶(AmpC)和B类的金属&内酰胺酶;②氨基糖甘类修饰酶:由于各种修饰酶的底物不同,可导致一种和几种氨基糖甘类抗生素耐药.(2)药物作用靶位改变:拓扑异构酶gyrA、parC基因突变导致的唾诺酮类抗菌药物耐药;armA等16SrRNA甲基化酶导致几乎所有氨基糖甘类抗生素耐药.(3)药物到达作用靶位量的减少:包括外膜孔蛋白通透性的下降及外排泵的过度表达. 鲍曼不动杆菌基因组显示,其富含外排泵基因,外排泵高表达在鲍曼不动杆菌多重耐药中发挥重要作用.鲍曼不动杆菌能泵出的药物包括(3内酰胺类,氨基糖甘类,红霉素,氯霉素,四环素类,氟唾诺酮类,甲氧节咤.主动外排机制在鲍曼不动杆菌对碳青酶烯类耐药的机制中也有一定的作用.鲍曼不动杆菌的耐药相当复杂,其本身具有的多重耐药机制造成它的多重耐药性,从其他菌株获得耐药基因并能表达,抗菌药物的强大选择压力,是造成它对药物耐药性不断上升的主要原因.2.5金黄色葡萄球菌耐药机制(1)青霉素耐药的金黄色葡萄球菌:产生 &内酰胺酶,水解青霉素中有效基团.(2)甲氧西林耐药金黄色葡萄球菌(MRSA):获得MeeA基团,编码产生PBP2a, 对&内酰胺类抗菌药物敏感性减低.〔3〕万古霉素耐药的金黄色葡萄球菌〔VRSA〕:获得万古霉素耐药肠球菌的耐药基因, 使万古霉素失去作用位点;或是细胞壁增厚,使万古霉素不能到达作用靶位.2.6肺炎链球菌耐药机制〔1〕伊内酰胺类抗生素的耐药机制①青霉素结合蛋白〔PBPS〕的改变;②非青霉素结合蛋白因素:非PBPs基因相关的肺炎链球菌耐药菌株都是感受态缺陷菌株.在哌拉西林耐药菌株中存在一个非PBPs的耐药基因cpoA〔糖基转移酶〕,其变异使肺炎链球菌在〔3 -内酰胺类抗菌药物破坏了细胞壁肽聚糖合成的情况下仍能生存,从而导致耐药;murM基因变异与肺炎链球菌青霉素高水平耐药及头抱菌素耐药相关;肺炎链球菌获得性TEM基因可能是其对〔3-内酰胺类药物耐药的原因之一.〔2〕肺炎链球菌对大环内酯类的耐药①erm基因介导核糖体靶位修饰:耐药肺炎链球菌可合成Erm酶〔erm基因编码〕,将核糖体23SrRNA的2058位的腺喋吟残基N26位二甲基化,从而使大环内酯类抗生素与核糖体作用位点的亲和力下降,可引起大环内酯类抗生素高水平耐药;②mef基因介导的主动外排机制:大环内脂类外排基因〔mef〕编码的产物是一种外排泵,能以大环内脂类抗生素为底物,通过消耗能量将药物排出菌体外,从而降低细菌对药物的敏感性.MefA外排泵的特异性底物是十四元环和十五元环大环内酯类,mef基因介导的耐药都发生在M型耐药细菌,且一般是低水平耐药〔1〜32止g/mL〕临床上可以通过增加大环内脂类抗生素的剂量来克服此耐药;③50S核糖体突变:50S核糖体中23SrRNA任一位点的突变都会引起大环内酯类抗菌药物与核糖体结合亲和力的改变,从而导致肺炎链球菌的耐药,突变的核糖体数量与耐药水平呈正相关.〔3〕肺炎链球菌对唾诺酮类药物的耐药机制:肺炎链球菌对氟曜诺酮类药物耐药主要由两个机制介导:一是DNA促旋酶及拓扑异构酶IV唾诺酮耐药决定区域〔QRDR〕染色体变异;二是外排泵作用增加.3应对举措3.1铜绿假单胞菌〔PAE〕耐药应对举措3.1.1抗菌药物不能盲目使用,应根据药敏试验的结果选择应用.3.1.2铜绿假单胞菌〔PAE〕对碳青霉烯类抗菌药物美罗培南、亚胺培南耐药率最低,其次对含酶抑制剂的复合抗菌药物头抱哌酮/舒巴坦、哌拉西林/他嘎巴坦耐药率较低,对头抱他咤耐药率也较低,临床应从其中选择敏感性强且性价比高的药物来治疗PAE感染;虽然PAE对阿米卡星和氯霉素耐药率较低,但由于前者的肾毒性和后者对造血系统的抑制作用,临床医师很少选择应用.3.2大肠埃希菌〔ECO〕耐药应对举措3.2.1氟唾诺类药物已不适用于对大肠埃希菌感染的经验治疗,用药需慎重.3.2.2对头抱毗肠与碳青霉烯类药物的使用应严格掌握适应症,碳青霉烯类药物仅适用于大肠埃希菌所致的严重感染.3.2.3氨基糖甘类药物与〔3内酰胺酶抑制药是治疗大肠埃希菌感染较好的选择.3.3肺炎克雷伯杆菌〔KPN〕耐药的治疗策略3.3.1轻、中度感染:首选复方〔3 -内酰胺类/ %内酰胺酶抑制剂.次选氨基糖昔类与头霉素类抗菌药物联合治疗.3.3.2对上述治疗效果不佳者,可选用碳青霉烯类抗菌药物.3.3.3对严重的产ESBLs肠杆菌科细菌感染者,首选碳青霉烯类抗菌药物或联合治疗方案. 3.4针对鲍曼不动杆菌耐药的治疗策略3.4.1碳青霉烯类抗生素可通过细菌外膜上有通透性功能的孔蛋白,进入胞质间隙后与靶蛋白PBP结合,通过干扰细胞壁的合成从而杀菌,因其对大多数&内酰胺酶具有高度稳定性,所以在临床治疗中能取得较好的疗效,故临床医生可将碳青霉烯类抗生素作为经验治疗鲍曼不动杆菌引起的感染的一线药物,同时应高度注意微生物实验室的实验结果,结合药敏结果合理的调整使用有效抗菌药物.3.4.2舒巴坦可以抑制细菌产生的多种 &内酰胺酶和多数超广谱 &内酰胺酶的同时,它还可以直接作用于细菌的青霉素结合蛋白PBP2,从而显示出它对不动杆菌的独特杀菌作用.3.4.3由于外膜通透性下降及主动外排机制也是细菌的耐药机制,这使得联合用药治疗成为可能.多西环素和粘菌素联合可能是最正确选择,但临床可操作性及真正疗效报道甚少. 我们在选择联合用药方案时,一方面要考虑到药物的MIC值,另一方面应尽可能了解当地的主要耐药表型,便于针对不同的耐药机制,合理联合用药.3.4.4对于泛耐药鲍曼不动杆菌,也不一定就是无计可施,分析目前的泛耐药鲍曼不动杆菌,发现在全耐药中含舒巴坦的制剂有相当的比例为中介,选用相对大剂量的舒巴坦〔4〜6g/d〕有效,这说明,如果有中介药物,加大其剂量对泛耐药鲍曼不动杆菌也是有望取得疗效的.另一方面是新近研发的新型四环素类 -替加环素,因其可以克服所有的泵出机制,虽然应用的经验不多,却可以作为一种很具有潜力的新药.3.5金黄色葡萄球菌耐药应对策略3.5.1在MRSA高度流行的医院或科室,对疑似重度MRSA感染患者,首先经验性选择抗MRSA药物治疗,再根据药敏结果调整到相应敏感的药物.3.5.2不同器官的MRSA感染,疾病的严重程度不同,选择的药物、剂量、疗程、给药途径有较大差异:①皮肤感染:社区获得性MRSA所致的脓疱病,建议局部应用夫西地酸或莫匹罗星进行治疗.周围无蜂窝组织炎的小脓肿在切开引流后一般不需要抗菌药物治疗.②皮肤溃疡并感染:皮肤MRSA定植较感染更为常见,单纯的皮肤溃疡只需局部应用夫西地酸或莫匹罗星治疗.并发蜂窝组织炎、邻近部位骨髓炎或菌血症的患者,或糖尿病患者足部溃疡部位有MRSA定植的患者,应考虑针对MRSA进行全身治疗.③蜂窝组织炎/外科伤口感染:轻症感染建议应用多西环素和克林霉素治疗.多西环素和克林霉素耐药菌株的感染,应选择糖肽类或利耐噪胺,无磺胺过敏者也可选择复方新诺明;对于较严重的感染或者有菌血症高度风险的患者,建议应用静脉输注糖肽类、利耐噪胺或达托霉素治疗.如果考虑存在混合感染〔例如糖尿病足感染〕,且MRSA为主要病原体, 可以考虑单独应用替加环素治疗;有关联合治疗的临床试验极少,且联合治疗有增加药物毒性的风险,不建议任何联合治疗方案.利福平联合夫西地酸治疗皮肤软组织感染的不良反响明显,不建议这种联合.插管部位的感染:对伴有明显硬结、蜂窝组织炎或菌血症的静脉输注部位的严重感染,推荐静脉应用糖肽类或利耐噪胺治疗,轻症感染可以口服药物治疗.③对于单纯的泌尿系感染,建议根据体外药敏结果来选用味喃妥因、甲氧节胺喀咤、复方新诺明等口服药物治疗.对于复杂的泌尿系感染,建议用糖肽类或达托霉素治疗.④MRSA骨和关节感染应以外科综合治疗为根底.建议静脉应用糖肽类单独治疗或联合经静脉应用利福平或夫西地酸钠作为首选方案.急性假体MRSA感染,早期〔病症出现2d内〕手术对保存假体很重要.对于慢性假体感染,应进行外科清创、取出假体.没有证据说明任何单药或联合用药更具优势.⑤应用糖肽类或利耐噪胺治疗MRSA菌血症,疗程至少14d.并发感染性心内膜炎或具有发生感染性心内膜炎高危因素者应延长疗程至6周.利耐噪胺疗程一般不超过4周, 如需延长疗程需注意其不良反响.达托霉素可以作为万古霉素的替代选择.⑥应用糖肽类或利耐噪胺治疗MRSA引起的肺部感染;不伴肺炎的慢性化脓性肺病或支气管扩张症患者,抗MRSA治疗的临床意义尚不明确;利耐噪胺有良好肺组织穿透力, 可用于此类患者的治疗.⑦对MRSA引起的深部眼睛感染和中枢神经系统感染, 建议应用万古霉素单独或联合利福平治疗,根据药敏也可选用利耐噪胺或复方新诺明;对静脉治疗无效的MRSA脑膜炎, 可以考虑万古霉素鞘内注射;庆大霉素、夫西地酸钠或氯霉素可以用于敏感细菌引起的眼睛浅部感染.⑧外科手术感染的预防性用药:对有MRSA定植史或感染史且未去除者,或有MRSA 带菌的高危风险者,在接受外科手术时需接受糖肽类预防感染.如估计患者有重新出现MRSA带菌的可能或患者来自MRSA高流行的机构,建议使用糖肽类治疗;对无MRSA 定植的患者,建议应用氨基糖甘类预防葡萄球菌感染.3.6肺炎链球菌耐药应对策略3.6.1一般PISP 〔中介水平耐药〕仍可选用青霉素治疗,但应加大剂量;PRSP所致的下呼吸道感染可选用阿莫西林500mg/克拉维酸钾125mg 〔675mg〕配方的方案治疗.3.6.2奎奴普丁30/达福普丁70,该药为复合制剂,属链阳菌素类抗菌药,协同抗菌活性增强为单药的8〜16倍,用于PISR PRSP 〔耐青霉素肺炎链球菌〕、MRSP 〔耐红霉素肺炎链球菌〕感染治疗.3.6.3利奈噪胺,该药为恶噪烷酮类新型化学合成抗菌药,对PISR PRSP均有高度抗菌活性.特点为有静脉与口服制剂,口服吸收完全,与静脉给药相比,其绝对生物利用度达100%,适合于序贯疗法.由于作用部位和方式独特,〔选择性结合于50s亚单位核糖体、抑制细菌蛋白质合成〕,不易与其他抑制细菌蛋白质合成的抗菌药发生交叉耐药, 体外也不易诱导产生耐药性,此为该药的优点.3.6.4用药动学/药效学参数标准抗菌药的使用行为PRSP/MRSP别离率不断上升,与头抱菌素与大环内酯类抗菌药的大量使用以及治疗方案不合理有很大关系.如头抱曲松钠对PRSP本有很强抗药作用,但单剂量治疗,使治疗后的血药浓度虽高于抗敏感的肺炎链球菌但低于抗耐药肺炎链球菌的浓度,助长了耐药的增长.而MRSP那么主要是广泛应用大环内酯类抗菌药所致.4.结语对免疫力低下的住院患者采取支持疗法,增强患者抵御感染的水平;早期诊断,快速进入手术,缩短住院时间,减少医院内交叉感染的时机;围手术期合理使用抗菌药物, 以免造成新的耐药菌株出现;严格执行消毒隔离制度和无菌技术,定时通风、净化室内空气;医护人员在接触患者时应戴工作帽、口罩、鞋套,标准洗手方法;医疗操作应做到准确细致,可减少组织损伤;外科患者手术前备皮手法应轻柔细致,保护患者皮肤的自身免疫屏障;重视引流管的清洁,及时冲洗和更换引流管;严格执行家属探视制度, 减少家属逗留时间等.我院应继续增强抗菌药物治理,各个部门增强合作,标准抗菌药物使用,杜绝滥用抗菌药物.增强医务人员对院内感染的熟悉和防控,增强对医院的工作人员培训,标准操作,减少耐药菌的传播流行.另外,还应监测医院的细菌感染谱及耐药情况.通过各方面的综合举措,相信在对耐多药细菌的防治会获得更多的经验和更新的进展. 药剂科医院感染科微生物室2021年07月。


细菌耐药机制及其应对策略在现代医学的发展进程中,抗生素的发现和应用无疑是一项伟大的成就。
然而,随着时间的推移,细菌耐药问题逐渐凸显,成为全球公共卫生领域面临的严峻挑战之一。
了解细菌耐药机制并制定有效的应对策略,对于保障人类健康和生命安全具有至关重要的意义。
一、细菌耐药机制1、产生灭活酶细菌可以产生多种灭活酶,如β内酰胺酶、氨基糖苷类修饰酶、氯霉素乙酰转移酶等,这些酶能够直接破坏或修饰抗生素的化学结构,使其失去抗菌活性。
2、改变抗菌药物作用靶点细菌可以通过改变自身细胞内抗菌药物作用的靶点,从而降低对抗生素的敏感性。
例如,某些细菌可以改变青霉素结合蛋白的结构,导致β内酰胺类抗生素无法与之有效结合;还有的细菌可以改变核糖体的结构,使氨基糖苷类抗生素无法发挥作用。
3、降低细胞膜通透性细菌的细胞膜具有选择性通透作用,能够控制物质的进出。
一些细菌可以通过改变细胞膜的通透性,减少抗生素的摄入,从而产生耐药性。
例如,革兰氏阴性菌的外膜屏障可以阻止某些抗生素进入细胞内。
4、主动外排系统许多细菌具有主动外排系统,可以将进入细胞内的抗生素泵出细胞外,从而降低细胞内药物浓度,产生耐药性。
这种外排系统通常由一系列的外排蛋白组成,能够识别并排出多种不同类型的抗生素。
5、形成生物被膜细菌可以形成生物被膜,这是一种由细菌及其分泌的多糖、蛋白质等物质组成的复杂结构。
生物被膜可以阻止抗生素的渗透,同时为细菌提供一个相对稳定的生存环境,使其更易产生耐药性。
二、细菌耐药的影响1、治疗难度增加细菌耐药使得原本有效的抗生素疗效降低甚至失效,导致感染性疾病的治疗变得更加困难。
医生可能需要使用更高剂量、更强效的抗生素,或者联合使用多种抗生素,这不仅增加了治疗成本,还可能带来更多的副作用。
2、医疗费用上升由于治疗耐药菌感染需要使用更昂贵的抗生素或更复杂的治疗方案,患者的医疗费用大幅增加。
这给个人和社会带来了沉重的经济负担。
3、威胁公共卫生安全耐药菌的传播可能引发大规模的感染暴发,尤其是在医院、养老院等人员密集的场所。

耐药菌感染的预防与护理随着抗生素的广泛应用,耐药菌感染已成为全球性的医疗难题。
耐药菌感染指的是细菌对抗生素产生耐药性,使得常规抗生素无法有效治疗感染。
耐药菌感染不仅增加了治疗的难度和费用,还可能导致治疗失败和并发症的发生。
因此,预防耐药菌感染至关重要。
本文将就耐药菌感染的预防与护理进行探讨,希望能为大家提供一些参考和帮助。
一、耐药菌感染的常见途径耐药菌感染的传播途径多种多样,主要包括:空气传播、飞沫传播、接触传播、水源传播等。
其中,医院是耐药菌感染的高发地之一,患者在医院接受治疗时易受到感染。
此外,长期使用抗生素、不规范使用抗生素、个人卫生不良等也是导致耐药菌感染的重要原因。
二、预防耐药菌感染的措施1. 合理使用抗生素:医生在开具抗生素处方时应根据患者的病情和细菌培养结果选择合适的抗生素,避免滥用和不当使用抗生素。
2. 加强个人卫生:保持良好的个人卫生习惯,勤洗手、定期洗澡、保持环境清洁等,可以有效减少细菌的传播。
3. 避免接触耐药菌:尽量避免接触感染者的分泌物和排泄物,减少感染的机会。
4. 定期体检:定期进行健康体检,及时发现潜在的感染,有针对性地进行治疗,避免感染加重。
5. 加强环境消毒:保持室内外环境的清洁,定期对医疗器械、床单、衣物等进行消毒,减少细菌滋生的机会。
三、耐药菌感染的护理1. 隔离患者:对已经感染耐药菌的患者进行隔离,避免细菌的传播,保护他人的健康。
2. 严格执行医嘱:患者在接受治疗时应严格按照医嘱服药,不得擅自更改药物剂量和使用方法。
3. 注意个人卫生:患者应保持良好的个人卫生习惯,勤洗手、勤换衣、保持环境清洁,减少细菌的滋生。
4. 饮食调理:患者在饮食上应避免生冷油腻食物,多食用富含维生素和蛋白质的食物,增强身体的免疫力。
5. 定期复查:患者在治疗期间应定期复查病情,及时调整治疗方案,确保疗效。
通过以上的预防与护理措施,可以有效降低耐药菌感染的风险,保障患者的健康。
希望大家能够重视耐药菌感染的预防工作,共同维护良好的医疗环境,减少感染的发生。

常见多重耐药菌的耐药机制及防治对策摘要】细菌基因突变是导致细菌耐药性的主要原因,使用一种抗菌药物存在对其他药物耐药性共选择的可能。
本文首先介绍常见革兰阴性杆菌以及结核分枝杆菌等耐药机制,之后阐述了耐药菌耐药机制的预防措施。
【关键词】细菌耐药机制防治对策【中图分类号】R446.5 【文献标识码】A 【文章编号】2095-1752(2013)07-0119-021 前言细菌基因突变是导致细菌耐药性的主要原因。
某种细菌对抗菌药物的耐药性产生机制有多种,质粒交换、整合子以及转座子等对于细菌单药耐药性以及多重耐药等均具有一定的激化作用。
细菌耐药性随着免疫抑制剂应用范围的越来越广以及抗菌类药物的越来越多而呈现出上升趋势。
对常见耐药菌多重耐药机制进行深入分析,并及时采取有针对性的防治对策具有重要的意义。
2 常见多重耐药菌耐药机制分析2.1常见革兰阴性杆菌耐药机制G-杆菌耐药性产生途径是:利用灭活酶可以实现对结合靶位的改变,并使外膜通透性降低,从而出现外排以及生物被膜等机制。
(1)ECO:其所产生的ESBLs以及整合子等机制在一定程度上对于多重耐药性的产生具有促进作用。
连续使用抗菌药物或者是耐药基因出现转移的情况下,诸如TEM等多重BLA活性将会产生,其中可能包含诸如OXA或者SHV型BLA,进而导致多重耐药性的出现。
临床实践研究证实,滥用喹诺酮类药物与耐药率较高之间存在一定联系。
通过AMEs,rpsl发生突变会阻碍链霉素与核糖体的结合,卡那霉素活性通过mdfA基因编码多药转运蛋白酶实现输出,进而对氨基糖苷类药物产生耐药性;对利福平耐药性主要原因是rpoB发生基因突变。
(2)PAE,其对结构相异的抗菌药物产生耐药性的主要原因是:经典高通道蛋白缺失以及外膜通透性不强,除此之外,还存在以下耐药机制:灭活酶的产生;靶位发生变化;外膜发生外排以及外膜蛋白变异缺失等是导致对喹诺酮类、四环素以及氯霉素等药物耐药性的原因。
(3)SMA,其受到抗菌药物选择压力影响,生存空间较大,使用头孢他啶或者是亚胺培南等药物均有可能导致其出现。

病原菌抗药性形成机制及防治对策概述:随着抗生素的广泛应用,病原菌抗药性问题逐渐凸显。
病原菌的抗药性使得常规的治疗方法变得无效,甚至出现了多重耐药菌株。
本文将深入探讨病原菌抗药性形成的机制,并提出相应的防治对策。
一、病原菌抗药性形成机制1. 自然选择自然选择是病原菌抗药性形成的主要因素之一。
当抗生素暴露于病原菌时,对其有抗药性的菌株能够在环境中存活并繁殖,而对抗生素敏感的菌株则会被杀灭。
长期暴露于抗生素的压力下,病原菌菌株逐渐演化出耐药性。
2. 基因转移基因转移是病原菌抗药性形成的另一个重要机制。
通过质粒、转座子、整合子等基因载体的介导,病原菌可以从其他菌株中获取抗药性基因。
这些基因可以编码破坏抗生素的酶、调节外膜通道等,从而使菌株对抗生素产生抗药性。
3. 突变突变是导致病原菌抗药性形成的另一个重要因素。
病原菌在复制过程中可能发生错误,导致基因突变。
这些突变可能会使菌株产生抗药性。
当病原菌面临抗生素选择压力时,这些突变可能会使菌株适应抗生素的存在,并获得抗药性。
二、病原菌抗药性防治对策1. 合理使用抗生素减少抗生素的滥用是防治病原菌抗药性的关键措施之一。
医务人员应根据患者的具体情况合理选择使用抗生素,并且严格按照药物使用引导原则进行用药,包括用药方式、剂量和疗程等。
此外,教育患者正确使用抗生素,避免滥用和过量使用,也是预防抗药性的重要手段之一。
2. 加强环境卫生管理病原菌通过环境中的传播也是导致抗药性形成的重要途径之一。
加强医疗机构、社区和公共场所的环境卫生管理,如定期消毒、清洁和垃圾处理等,能够有效减少病原菌的传播和感染机会,从而减少抗药菌株的产生。
3. 发展新型抗生素由于病原菌对抗生素的抗药性不断增强,开发新型抗生素对付抗药性菌株变得至关重要。
科研机构和制药公司需要加强抗生素的研发,寻找新的抗生素分子结构和机制,对抗目前已存在的耐药性机制,从而提供有效的解决方案。
4. 多学科合作病原菌抗药性是一个复杂的问题,需要医学、生物学、化学等多个学科的专家共同合作。

细菌耐药性的分子机制与防治措施细菌耐药性是指细菌对抗生素及其他药物的抵抗力,是当今公共卫生领域的一大难题。
随着抗生素的广泛使用和滥用,细菌耐药性不断加剧。
很多病菌如金葡菌、大肠杆菌等已经产生了多重耐药,甚至无药可治。
下面我们来探讨一下细菌耐药性的分子机制和防治措施。
一、分子机制1.基因水平的变异细菌在繁殖过程中,由于DNA复制和修复过程中出现的错误或环境压力等原因,导致其基因序列发生变异,从而产生新的基因。
一些突变体表现出对抗生素的耐药性,并能通过基因水平的传递来将这种耐药性传递给后代。
这种基因水平的耐药性是细菌耐药性的一种重要机制。
2.质粒介导的传递质粒是细菌细胞外面积为常染色体的小环状DNA分子。
质粒可以携带多种抗生素耐药基因,通过与宿主菌的染色体结合,形成可移植的耐药质粒,传递耐药性。
3.核糖体保护蛋白的合成核糖体是细胞内生产蛋白质的重要组成部分。
抗生素可以通过影响细菌细胞的核糖体的正常功能,使细菌无法维持其正常生理功能并死亡。
然而,一些细菌通过合成核糖体保护蛋白来避免抗生素对核糖体的干扰,从而保持其存活和繁殖的能力。
4.多药泵的表达多药泵是一种可将化学物质从细胞内向外排出的蛋白质,它在细菌耐药性的形成中起到了重要的作用。
多药泵可以通过从细胞内排放抗生素来降低抗生素在细菌细胞内的浓度,从而减少抗生素的杀菌效果。
多药泵表达的增加是细菌对多种抗生素产生耐药的重要机制之一。
二、防治措施1.抗生素合理应用抗生素是用来治疗感染性疾病的药物,而不是预防疾病。
我们应该严格按照医师开具的用药指示,不要滥用抗生素,避免抗生素的滥用和过度使用。
2.控制感染预防是细菌耐药性最重要、最经济的策略之一。
通过控制感染,可以降低细菌耐药性的发生率。
我们应该保持手卫生,妥善贮藏食物,保持清洁卫生等措施来减少感染的风险。
3.开展监测和调查实时监测耐药菌株的变化,对于制定和调整治疗策略具有重要意义。
建立相关数据库,可及时收集和传递有关耐药性新信息,及时生产有力、有效的抗生素。


医院感染的病原菌及耐药性分析医院感染是指患者在接受医疗、就诊或住院治疗期间,在医疗机构内被病原微生物感染。
这种感染对患者的健康和生命安全构成了严重威胁。
近年来,医院感染引起了人们的广泛关注,因为很多病原菌已经对常用抗生素产生了耐药性,加剧了治疗难度和风险。
本文将分析医院感染的常见病原菌及其耐药性情况。
1. 革兰阳性菌革兰阳性菌是最常见的医院感染病原菌之一,包括金黄色葡萄球菌(MRSA)、肠球菌(VRE)和耐甲氧西林链球菌(PRSP)等。
这些菌株通常存在于人体皮肤和黏膜表面,感染途径多为空气飞沫、接触传播和手卫生不当。
这些菌株的主要特点是易产生耐药性,对多种抗生素呈现不同程度的耐药性。
2. 革兰阴性菌革兰阴性菌包括大肠杆菌、铜绿假单胞菌和肺炎克雷伯菌等,它们是医院感染中的重要致病菌。
这些菌株通过接触传播、污染食物和水源、医疗器械的使用等途径传播。
革兰阴性菌除了耐药性强外,还有一定的细胞外酶活性,能够分解抗生素,加速耐药性的发展。
3. 真菌感染除了细菌感染外,医院感染中的真菌感染也逐渐增多。
常见的真菌病原包括白色念珠菌和曲霉菌。
真菌感染往往发生在免疫功能低下或长期接受抗生素治疗的患者身上。
与细菌不同,真菌具有更强的耐药性,常规抗生素对其效果较差。
面对医院感染病原菌及其耐药性的问题,我们应该采取以下措施:1.严格执行手卫生手卫生是防止医院感染最关键的环节之一。
医务人员和访客在进入病房前后、接触患者前后都应注意洗手,避免病原菌通过手的传播进入患者体内。
2.加强医疗器械的消毒和灭菌医疗器械在使用前需进行消毒和灭菌处理,以杀死潜在的致病菌。
医疗机构应建立完善的器械消毒灭菌制度,并加强对医务人员的培训和督导。
3.合理使用抗生素医务人员应根据患者具体情况合理使用抗生素,避免滥用和过度使用。
此外,医院应建立抗生素使用监测机制,及时了解抗生素的使用情况和耐药性的发展。
4.加强环境卫生管理医院病房和公共区域的清洁和消毒工作尤为重要。
细菌耐药机制及其防治策略细菌耐药是指细菌对抗生素或其他抗菌药物产生耐受能力的现象,这是导致感染疾病治疗失败并增加死亡率的重要原因之一。
细菌耐药机制的深入研究对于制定有效的防治策略至关重要。
本文将介绍一些常见的细菌耐药机制及其防治策略。
1. 靶点突变细菌耐药的一个常见机制是通过突变改变细菌体内的靶点,从而使抗生素无法与该靶点结合,失去杀菌或抑制菌体生长的效果。
例如,青霉素类抗生素通过抑制细菌细胞壁合成来杀死细菌,但耐药菌株中的靶点PBP(penicillin-binding protein)经过突变,使抗生素无法与其结合,此时细菌就会产生抗药性。
防治此类耐药机制的策略之一是开发新型抗生素,能够突破细菌的耐药能力。
2. 药物降解或排出细菌耐药的另一个机制是通过产生酶或蛋白质,将抗生素降解为无效的物质,或利用外排泵将药物从细菌内排出。
酶介导的耐药机制包括β-内酰胺酶产生的青霉素酶和氨基糖苷酶等。
外排泵耐药机制涉及到多种外排泵蛋白,如药物外排泵AcrAB-TolC。
在防治此类耐药机制时,可以研究抗药酶或外排泵的结构,设计能够抑制它们活性的抗生素辅助药物。
3. 建立保护性结构有些细菌通过改变其细胞壁或膜结构,形成保护性的屏障,使抗生素难以穿透到细胞内。
例如,肺炎克雷伯杆菌(Pseudomonas aeruginosa)通过形成毒素外泌体、产生胞外粘胶等方式,建立了多种保护性结构,使其对抗生素的敏感性降低。
针对这种耐药机制,可以研究并开发穿透细菌保护结构的新型抗生素。
4. 氨基酸替代细菌通过改变特定蛋白质的氨基酸序列,降低了抗生素与该蛋白的结合亲和力,从而减少了抗生素的杀菌效果。
这种机制常发生在青霉素和大环内酯类抗生素的目标蛋白上。
对策之一是通过合成化学手段设计和合成新型抗生素结构,能够绕过耐药菌株已经产生的氨基酸替代。
为应对细菌耐药带来的严重威胁,研究人员和医学界制定了一系列细菌耐药的防治策略。
1. 合理使用抗生素抗生素在医学领域的发现和广泛应用,对细菌耐药问题起到了推波助澜的作用。
耐药菌的发生机制与防治策略随着抗生素的广泛使用,耐药菌已成为全球性的公共卫生问题。
耐药菌指的是对一种或多种抗生素具有抗药性的细菌。
这些细菌能够通过自身基因突变或者从其他细菌中获得抗药基因,逐渐形成对抗生素的耐受性。
本文将探讨耐药菌的发生机制以及防治策略。
一、耐药菌的发生机制(一)基因突变耐药菌的发生主要是由基因突变引起的。
细菌细胞的遗传物质DNA有可能发生突变,继而使细菌细胞产生抗性属性。
这种变异可以是自然产生或是由于外界环境等原因诱发。
一旦细菌突变,其后代就将遗传得到这种抗性属性。
(二)耐药基因转移耐药细菌可以通过水、空气、食物以及人与动物等传染方式感染到人体内,进而导致感染性疾病。
除了自身基因突变外,耐药细菌还可以通过耐药基因转移方式获得耐药性。
不同种类的细菌,甚至是跨越物种界的细菌,都可以通过共享性质相似的质粒或转座子来进行耐药基因交换。
这也是细菌抵御多种抗生素的原因之一。
(三)滥用抗生素抗生素是治疗感染性疾病的有效药物。
但是过度使用抗生素、不规范用药等因素,也会加速耐药细菌的产生。
这是因为在使用抗生素的过程中,细菌会逐渐适应药物,从而产生耐药性。
一旦耐药菌形成,就会对抗生素失去响应,也就难以控制感染。
二、耐药菌的防治策略(一)正确使用抗生素为了遏制耐药菌的形成,正确使用抗生素是最基本的措施。
不只是在个人治疗上,而是全社会的药物使用习惯都需要进行调整。
在临床应用中,医生应遵守抗生素使用规范,根据病情和感染程度开具抗生素处方。
同时,患者也必须遵守医生的建议,按时按量服药,并且不可过早停药。
(二)增强细菌感染控制细菌感染控制是防止耐药菌快速扩散的必要措施。
对于感染部位进行严密的消毒处理是必不可少的。
另外,在公共场合、医院等公共环境中采取良好的卫生保洁措施,也可以有效地控制病原菌的传播和感染。
(三)开发新的抗菌药物目前已经发现的抗菌药物已经不能对抗多数的耐药菌,因此,发展新的抗菌药物是治疗耐药菌的重要手段之一。
常见细菌耐药趋势及控制方法细菌耐药是指细菌对抗生素产生抵抗力,使抗生素失去对其杀菌或抑制作用的能力。
细菌耐药是一个严重的全球性健康问题,现在已经成为世界各国面临的主要挑战之一、下面将从细菌耐药的趋势及控制方法两个方面进行具体阐述。
一、细菌耐药的趋势:1.医院感染细菌耐药:由于抗生素的滥用和不当使用,医院感染细菌逐渐耐药,包括金黄色葡萄球菌(MRSA)、肠杆菌等。
这些抗生素耐药细菌传播性强,易造成多重耐药。
2.农业使用抗生素引发细菌耐药:在畜牧业和渔业中,大量使用抗生素作为预防疾病和促进生长的手段,使得细菌对抗生素产生抵抗力,从农产食物中传入人类体内,进一步加剧细菌耐药问题。
3.生活环境中细菌耐药:由于洁具、医疗设备等缺乏清洁,细菌在这些环境中滋生,逐渐对抗生素产生耐药性,给居住环境带来潜在风险。
二、细菌耐药的控制方法:1.加强监管和合理使用抗生素:政府应加强对抗生素的使用和销售监管,限制非法售卖抗生素,加强临床用药合理使用管理,禁止非医疗机构使用抗生素等。
医生应根据病患的具体情况,合理使用抗生素,避免滥用和过度使用。
2.提高公众对抗生素的认识:公众应加强对抗生素的正确认识,明白抗生素对病毒性感染无效,不应滥用抗生素。
同时,提高公众对个人卫生的重视,如勤洗手、咳嗽时使用纸巾或手肘遮挡等,有助于减少细菌传播。
3.加强卫生条件和环境清扫:加强医疗机构、公共场所和家庭的卫生条件,防止细菌滋生和传播,减少细菌暴露的机会。
定期清洁卫生设施和用具,如洗手间、医疗器械等,有利于控制细菌的生长。
4.开发新型抗生素和疫苗:科学家应加大对新型抗生素和疫苗的研发力度,开发对抗多种细菌耐药的药物和疫苗,以应对细菌耐药的挑战。
5.加强国际合作和信息共享:各国应加强国际合作,分享细菌耐药情报和研究成果,共同应对细菌耐药的威胁。
通过国际合作,可以更好地掌握细菌耐药的动态信息,制定应对策略和控制措施。
总结起来,细菌耐药是一个严重的全球性健康问题,必须引起政府、医生和公众的高度重视。
耐药菌的形成原因及其防治策略分析随着抗生素的广泛使用,耐药菌的问题越来越严重,给人类健康带来了极大的威胁。
那么,耐药菌的形成原因是什么?又该怎样防治耐药菌呢?一、耐药菌的形成原因1.滥用抗生素抗生素的使用十分普遍,但遗憾的是许多医生和患者对药物的理解并不够深入,导致了大量的滥用行为。
一次感染可能需要多个抗生素的联合治疗,但滥用抗生素会使细菌逐渐适应和产生抗药性,形成耐药菌。
2.医疗操作医疗过程中,细菌不断面临着抗生素的攻击,而细菌在适应环境的过程中选择了产生耐药突变,在这种情况下细菌会在特定环境中保存抗生素抵抗性,形成耐药菌。
3.环境污染加速了耐药菌的形成的环境也是不容忽视的,例如日常耳熟能详的抗菌洗手液。
许多抗菌洗手液中含有对病原菌有用的成分,但是如果长时间使用时会杀死人体细菌而使细菌产生适应环境的耐药性,致使耐药菌的产生。
二、耐药菌的防治策略1.合理使用抗生素合理使用抗生素就是使用足够、但等效的抗生素,不能过量或过短。
合理的使用抗生素就能够减少抗生素对细菌的攻击,使得细菌在不良环境中面临更大的压力,从而减少细菌的抗药性。
2.生态环境卫生控制保持生态环境卫生,是减少耐药菌的生长和培养的最有效方法,需要注意的是地球是一个生态系统,耐药菌和人们平时所不注意的细菌都处于统一的生态环境中,生态卫生控制需要统一进行管理。
3.扩大预防接种范围预防接种是预防重大传染病的有效手段。
目前已有若干种疫苗能预防重要的耐药菌感染,对于人们进行预防接种,可以有效遏制耐药菌的生长。
4.推广健康的生活方式根据调查显示,生活不良习惯也会导致耐药菌的产生。
生活不良习惯如:不良的饮食结构、缺乏运动、过度压力,等等。
改变这些不良生活习惯可以使得身体更加健康,从而减少耐药菌的产生。
结语总之,防治耐药菌的关键在于人类自己。
我们应该遏制滥用抗生素,减少医疗操作对细菌的攻击,保持生态环境、卫生和卫生习惯,从而减少耐药菌的产生。
只有在提高人类卫生素质的同时,才能有效控制耐药菌对健康的危害。