体心立方晶格与面心立方晶格
- 格式:doc
- 大小:89.00 KB
- 文档页数:5

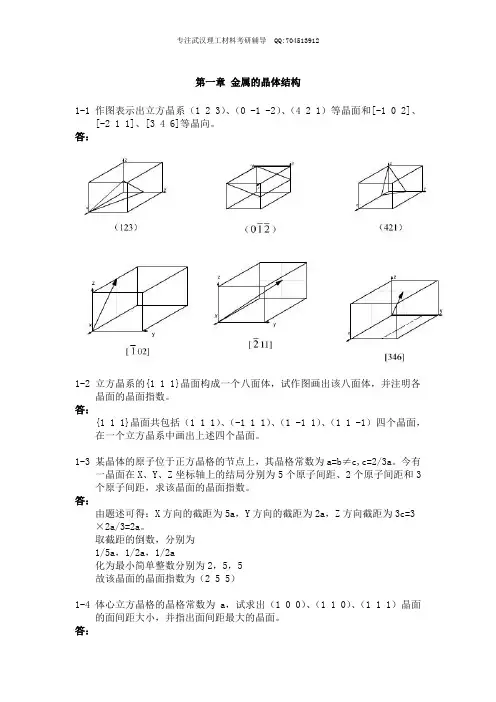
第一章金属的晶体结构1-1 作图表示出立方晶系(1 2 3)、(0 -1 -2)、(4 2 1)等晶面和[-1 0 2]、[-2 1 1]、[3 4 6]等晶向。
答:1-2 立方晶系的{1 1 1}晶面构成一个八面体,试作图画出该八面体,并注明各晶面的晶面指数。
答:{1 1 1}晶面共包括(1 1 1)、(-1 1 1)、(1 -1 1)、(1 1 -1)四个晶面,在一个立方晶系中画出上述四个晶面。
1-3 某晶体的原子位于正方晶格的节点上,其晶格常数为a=b≠c,c=2/3a。
今有一晶面在X、Y、Z坐标轴上的结局分别为5个原子间距、2个原子间距和3个原子间距,求该晶面的晶面指数。
答:由题述可得:X方向的截距为5a,Y方向的截距为2a,Z方向截距为3c=3×2a/3=2a。
取截距的倒数,分别为1/5a,1/2a,1/2a化为最小简单整数分别为2,5,5故该晶面的晶面指数为(2 5 5)1-4 体心立方晶格的晶格常数为a,试求出(1 0 0)、(1 1 0)、(1 1 1)晶面的面间距大小,并指出面间距最大的晶面。
答:H==a/2(1 0 0)==√2a/2H(1 1 0)==√3a/6H(1 1 1)面间距最大的晶面为(1 1 0)1-5 面心立方晶格的晶格常数为a,试求出(1 0 0)、(1 1 0)、(1 1 1)晶面的面间距大小,并指出面间距最大的晶面。
答:==a/2H(1 0 0)H==√2a/4(1 1 0)==√3a/3H(1 1 1)面间距最大的晶面为(1 1 1)注意:体心立方晶格和面心立方晶格晶面间距的计算方法是:1、体心立方晶格晶面间距:当指数和为奇数是H=,当指数和为偶数时H=2、面心立方晶格晶面间距:当指数不全为奇数是H=,当指数全为奇数是H=。
1-6 试从面心立方晶格中绘出体心正方晶胞,并求出它的晶格常数。
答:1-7 证明理想密排六方晶胞中的轴比c/a=1.633。
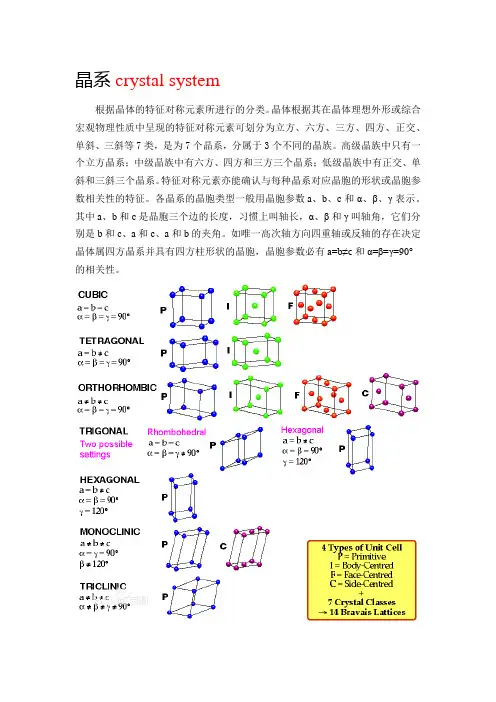



《固体物理学》部分习题解答1.3 证明:体心立方晶格的倒格子是面心立方;面心立方晶格的倒格子是体心立方。
解由倒格子定义体心立方格子原胞基矢倒格子基矢同理可见由为基矢构成的格子为面心立方格子面心立方格子原胞基矢倒格子基矢同理可见由为基矢构成的格子为体心立方格子1.4 证明倒格子原胞的体积为,其中为正格子原胞体积证倒格子基矢倒格子体积1.5证明:倒格子矢量垂直于密勒指数为的晶面系。
证:容易证明与晶面系正交。
1.6如果基矢构成简单正交系证明晶面族的面间距为说明面指数简单的晶面,其面密度较大,容易解理证简单正交系倒格子基矢倒格子矢量晶面族的面间距面指数越简单的晶面,其晶面的间距越大晶面上格点的密度越大,这样的晶面越容易解理1.9 指出立方晶格(111)面与(100)面,(111)面与(110)面的交线的晶向解(111)面与(100)面的交线的AB-AB平移,A与O重合。
B点位矢(111)与(100)面的交线的晶向——晶向指数(111)面与(110)面的交线的AB——将AB平移,A与原点O重合,B点位矢(111)面与(110)面的交线的晶向――晶向指数2.1.证明两种一价离子组成的一维晶格的马德隆常数为.证设想一个由正负两种离子相间排列的无限长的离子键,取任一负离子作参考离子(这样马德隆常数中的正负号可以这样取,即遇正离子取正号,遇负离子取负号),用r表示相邻离子间的距离,于是有前边的因子2是因为存在着两个相等距离的离子,一个在参考离子左面,一个在其右面,故对一边求和后要乘2,马德隆常数为当X=1时,有2.3 若一晶体的相互作用能可以表示为求1)平衡间距2)结合能W(单个原子的)3)体弹性模量4)若取,计算值。
解1)晶体内能平衡条件2) 单个原子的结合能3) 体弹性模量晶体的体积——A为常数,N为原胞数目晶体内能体弹性模量由平衡条件体弹性模量()4)2.6.用林纳德—琼斯(Lennard—Jones)势计算Ne在bcc(球心立方)和fcc(面心立方)结构中的结合能之比值.解2.7.对于,从气体的测量得到Lennard—Jones势参数为计算结合成面心立方固体分子氢时的结合能(以KJ/mol单位),每个氢分子可当做球形来处理.结合能的实验值为0.751kJ/mo1,试与计算值比较.解以为基团,组成fcc结构的晶体,如略去动能,分子间按Lennard—Jones势相互作用,则晶体的总相互作用能为:因此,计算得到的晶体的结合能为2.55KJ/mol,远大于实验观察值0.75lKJ/mo1.对于的晶体,量子修正是很重要的,我们计算中没有考虑零点能的量子修正,这正是造成理论和实验值之间巨大差别的原因.3.1.已知一维单原子链,其中第个格波,在第个格点引起的位移为,,为任意个相位因子,并已知在较高温度下每个格波的平均能量为,具体计算每个原子的平方平均位移。

固体物理(黄昆)第一章总结(总5页)页内文档均可自由编辑,此页仅为封面第一章晶体结构1.晶格实例1.1面心立方(fcc)配位数12 格点等价格点数4 致密度0.74原胞基矢:()()()123222aa j kaa k iaa i j=+=+=+原胞体积3123()/4Ωa a a a=⋅⨯=NaCl: 两组面心立方格子平行穿套而成的复式格子基元= Na+ + Cl-具有面心立方:简单格子(Al、Cu、Ag; Ar Kr Xe Ne)、复式格子(Cao MgS 碱卤族等)1.2简单立方(SC)配位数6 格点等价格点数1 致密度0.52CsCl两组简单立方格子穿套而成的复式结构基元= Cs+ + Cl-钙钛矿结构:CaTiO3五个简单立方穿套而成基元:Ca、Ti、OI、OII、OIII (OI、OII、OIII 的化学环境各不相同,氧八面体) 典型晶体:BaTiO3、PbZrO3、LiNbO3、LiTaO3氯化铯型结构: CsCl, CsBr, CsI, TlCl, TlBr, TlI 等1.3体心立方(bcc)配位数8 格点等价格点数2 致密度0.68原胞基矢:123()2()2()2aa i j kaa i j kaa i j k=-++=-+=+-原胞体积:3123()/2Ωa a a a=⋅⨯=体心立方晶体: 碱金属、W、Mo、Nb、V、Fe等1.4六角密堆(hcp)配位数12 两种格点原子数6 基元数3 致密度0.74典型晶体举例:He, Be, Mg, Ti, Zn, Cd, Co, Y, Lu 等1.5金刚石结构最近邻原子数4 次近邻原子数12 致密度0.34晶体结构=布拉维格子(面心立方)+ 基元(A+B)*将金刚石结构中的基元置换成一对硫离子和锌离子,则为两个面心立方复合而成的复式结构,典型晶体:SiC, ZnSe, AlAs, GaP, GaAs 等2.晶体的周期性结构2.1基本概念晶体:1. 化学性质相同 2. 几何环境相同 基元:晶体结构中最小的重复单元布拉维点阵(布拉维格子): 112233R n a n a n a =++ 晶体结构 = 布拉维格子+基元原胞:由基矢1a 、2a 、3a 确定的平行六面体,是体积最小的周期性结构单元,原胞只包含一个格点晶胞:同时计及周期性及对称性的尽可能小的重复单元,原胞实际上是体积最小的晶胞2.2维格纳-赛茨原胞(WS 原胞)1. 作某个格点与其它格点的连接矢量2. 作所有这些连接矢量的垂直平分面3. 这些垂直平分面围起的凸多面体就是维格纳-赛茨原胞3. 晶向、晶面及其标志 晶列(向)指数:[l m n]晶面指数(米勒指数):( h k l )米勒指数是以晶胞基矢为基准,而面指数则以原胞基矢为基准标定4. 布里渊区倒格子空间中的维格纳-赛茨(WS )原胞,即所谓的第一布里渊区,布里渊区包含了所有能在晶体上发生布拉格反射的波的波矢22h h k G G ⋅=4.1简单立方的倒格矢(简单立方——简单立方)基矢123a aia aj a ak ⎧=⎪=⎨⎪=⎩ 倒格矢123(2π/a)(2π/a)(2π/a)b i b j b k ⎧=⎪=⎨⎪=⎩4.2体心立方晶格的倒格子(体心立方——面心立方)基矢1231()21()21()2a a i j k a a i j k a a i j k ⎧=-++⎪⎪⎪=-+⎨⎪⎪=+-⎪⎩ 倒格矢1232π()2π()2π()b j k a b k i a b i j a ⎧=+⎪⎪⎪=+⎨⎪⎪=+⎪⎩倒格矢可以表示为:1122332331122π[()()()]h G h b h b h b h h i h h j h h k a=++=+++++ 其中(h1 h2 h3)是米勒指数,h G 垂直于米勒指数,其第一布里渊区是一个正十二面体4.3面心立方晶格的倒格子(面心立方——体心立方)基矢1231()21()21()2a a j k a a k i a a i j ⎧=+⎪⎪⎪=+⎨⎪⎪=+⎪⎩ 倒格矢1232π()2π()2π()b i j k a b i j k a b i j k a ⎧=-++⎪⎪⎪=-+⎨⎪⎪=+-⎪⎩第一布里渊区为截角八面体即5. 晶体的宏观对称性xx xy xz x x y yx yy yz y z zx zy zz z D E D E D E εεεεεεεεε⎛⎫⎛⎫⎛⎫⎪ ⎪ ⎪= ⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎝⎭⎝⎭⎝⎭5.1对于所有立方对称的晶体中,介电常数是一个对角张量:0 (,,,)x y z αβαβεεδαβ==该结论适用于一切具有二阶张量形式的宏观性质 (如电导率、热导率)5.2六角对称的晶体中,若坐标轴选取在六角轴的方向和与它垂直的平面内,则介电常数有如下形式// 0 00 00 0 εεε⊥⊥⎛⎫ ⎪ ⎪ ⎪⎝⎭ ,//////D E ε=, D E ε⊥⊥⊥=,六角对称的晶体有双折射现象5.3对称操作(正交变换:旋转、中心反演、镜面反映) 1. 旋转绕 z 轴旋转 q 角的正交矩阵cos sin 0sin cos 0 0 0 1θθθθ-⎛⎫ ⎪⎪ ⎪⎝⎭,中心反演的正交矩阵1 0 0 0 1 0 0 0 1-⎛⎫⎪- ⎪ ⎪-⎝⎭由于cost = (1 - m)/2 所以 m = -1 0 1 2 3,所以t = 0 2π/6 2π/4 2π/3 2π/2,没有所谓的5度轴和7度轴。



金属中常见的晶格类型有哪三种;1、体心立方晶格2、面心立方晶格3、密排立方晶格金属有铬、钨、钼、钒、及&铁属于(体心立方晶格)金属有铜、铝、银、金、镍、y铁属于(面心立方晶格)金属有铍、镁、锌、钛等属于(密排立方晶格)金属的晶体缺陷:按照缺陷的几何特征,一般分为以下三类:1.空位和间隙原子(点缺陷)2.位错(线缺陷)3.晶界和亚晶界(面缺陷)一般来说,在常温下细晶粒金属比粗晶粒金属具有较高的强度、硬度、塑性和韧性。
工业中常用以下方法细化晶粒1.增加过2.变质处3.附加振动4.降低浇注速度1.铁素体(F)碳溶入&铁中的间隙固溶体称为铁素体,2.奥氏体(A)碳溶入y铁中的间隙固溶体称为奥氏体,3.渗碳体(Fe3C)铁与碳组成的金属化合物称为.渗碳体,第四章铁碳合金相图根据相图中S点碳钢可以分为以下几类1.共析钢(含碳量小于0.0218%)的铁碳合金,其室温组织为铁素体。
2亚共析钢(含碳量等于0.0218%到2.11%)的铁碳合金,其室温组织为珠光体+铁素体。
3过共析钢(含碳量等于0.77%到2.11%)的铁碳合金,其室温组织为+二次渗碳第五章钢的热处理一般加热时的临界点用Ac1、Ac3、Accm来表示;冷却时的临界点用Ar1、Ar3、Arcm来表示。
共析碳钢的过冷奥氏体在三个不同的温度转变,可发生三种不同的转变:珠光体型转变、贝氏体型转变、马氏体型转变。
珠光体型转变有区别起见,又分为珠光体、索氏体、和托氏体三单晶体的塑性变形的方式有两种:滑移和孪生(孪晶),而滑移是单晶体塑性变形的主要方式。
多晶体的塑性变形的方式有两种:晶内变形和晶间变形。
二、填空题1.珠光体是由铁素体和渗碳体组成的机械混合物共析组织)。
2.莱氏体是由奥氏体和渗碳体组成的机械混合物(共晶组织)。
3.奥氏体在1148℃时碳的质量分数可达2.11%,在727℃时碳的质量分数为0.77%。
4. 根据室温组织的不同,钢可分为亚共析钢、共析钢和过共析钢。

固体物理习题.1 如果将等体积球分别排列成下列结构,设x表示刚球所占体积与总体积之比,证明:结构 简单立方 体心立方 面心立方 六角密排 金刚石 证明: (1)简单立方:设晶格常数为,球半径为,则,如右图所示,晶胞内包含一个原子,(2)体心立方:在简单立方的体心增加一球,则立方单元内包含二个原子,(3)面心立方:在简单立方的六个面心上分别增加一个球,则立方单元内包含4个原子,(4)六角密排:如左图所示晶胞内包含6个原子,,晶胞的高用表示,则晶胞的体积=(5)金刚石:在面心立方结构的四条互不相邻的体对角线中心分别加一原子,则原胞内包含8个原子,且1.2试证六方密排堆积中证: 由上题可知 ,则1.3证明:体心立方晶格的倒格子是面心立方,面心立方的倒格子是体心立方。
证明:根据题根据,则计算可得倒格子基矢(需有运算过程):与体心立方基矢相比这正好是以为晶格常数的体心立方格子的基矢。
同理可证体心立方晶格的倒格子是晶格常数为的面心立方格子。
1.4证明:倒格子原胞体积为,其中为正格子原胞体积。
证:有正格子基矢与倒格子基矢之间的关系:则倒格子体积。
1.5证明倒格子矢量垂直于密勒指数为的晶面系。
证:根据密勒指数的定义,晶面在基矢上的截距分别为,作矢量显然这三个矢量互不平行,均落在晶面上,且有同理,故倒格矢垂直于的晶面系。
1.6对于简单立方晶格,证明密勒指数为的晶面系,面间距满足,其中为立方边长。
证:由上题可知,倒格矢垂直于密勒指数为的晶面系,对于简单立方,两两垂直,则面间距而,所以。
1.7写出体心立方和面心立方晶格结构的金属中,最近邻和次近邻的原子数。
若立方边长为,写出最近邻和次近邻的原子间距。
解:最近邻次近邻原子数原子间距原子数原子间距体心立方 8 6面心立方 12 61.8画出体心立方和面心立方晶格结构的金属在(100),(110),(111)面上的原子排列。
答:略1.9指出立方晶格(111)面和(100)面,(111)面和(110)面的交线的晶向。
体心立方、面心立方晶格主要晶面的原子排列和密度体心立方、面心立方晶格主要晶面的原子排列和密度第1章小结体心立方晶格(胞): 晶格常数a 、90 °晶胞原子数为2个,1.三种常见金属的晶体结构 原子半径: 5面心立方晶格(胞): 晶格常数a 、90 °晶胞原子数为4个, 致密度为68%,最大空隙半径 「四=0.29「原子,配位数为8原子半径:厂.,致密度为74% ,最大空隙半径r八=0.414 r原子,配位数为12。
密排六方晶格(胞):晶格常数a、c、90 ° 120 °晶胞原子数为6个,1r原子半径:匕致密度为74%,最大空隙半径r八=0.414 r原子,配位数为12。
2 .晶面与晶向可用晶面指数与晶向指数来表达。
不同晶面、不同晶向上的原子排列情况不同。
体心立方晶格的最密面为{110},最密方向为<111>。
面心立方晶格的最密面为{111}最密方向为<110>。
密排六方晶格的最密面为{0001},最密方向为^刀“‘。
3 .实际金属中含有点缺陷(空位、间隙原子、异类原子)、线缺陷(位错)、面缺陷(晶界、亚晶界)三类晶体缺陷,位错密度增加,材料强度增加。
晶界越多,晶粒越细,金属的强度越高,同时塑性越好(即细晶强化)。
4 .合金中有两类基本相:固溶体和金属化合物。
固溶强化是金属强化的一种重要形式。
细小弥散分布的金属化合物可产生弥散强化或第二相强化。
材料的微观组成和微观形貌称组织,材料的组织取决于化学成分和工艺过程。
5.金属材料的性能特点是:强度高,韧性好,塑性变形能力强,综合机械性能好,通过热处理可以大幅度改变机械性能。
金属材料导电、导热性好。
不同的金属材料耐蚀性相差很大,钛、不锈钢耐蚀性好,碳钢、铸铁耐蚀性差。
6.高分子材料结构由大分子链组成,大分子链之间的相互作用力为分子键,分子链的原子之间、链节之间的相互作用力为共价键。
高分子材料的大分子链结构与聚集态及其性能密切相关。
体心立方晶体结构
体心立方晶体结构是晶体学中一种非常常见的晶体类型。
它的结
构特点是晶格点为体心,即每个晶体内部存在一个原子,且每个原子
周围都有其他原子,形成一个立方体的体中心。
在体心立方晶体结构中,原子的堆积方式有两个。
一个是直接堆
积方式,即将每个原子直接堆积在体心的晶格点上。
另一个是间接堆
积方式,即将每个原子堆积在体心和每个面心上。
在体心立方晶体结构中,原子之间的距离是非常均匀的,这种均
匀的结构使得该晶体具有很高的密度和强度。
同时,由于晶格点的体
心位置,每个晶胞内有更多的原子,因此具有更高的原子密度。
这种
高密度的结构使得体心立方晶体结构非常适合用于金属合金、半导体、半金属等材料的制备。
此外,体心立方晶体结构的另一个特点是具有很高的对称性。
由
于每个晶胞内存在一个原子及其对称相等的相邻原子,因此整个结构
表现出完全的立方对称性。
这种对称性使得体心立方晶体结构的研究
更具有指导意义。
总之,体心立方晶体结构是一种具有均匀结构、高密度、高强度
和高对称性的晶体。
它的研究对于制备金属合金、半导体、半金属等
材料具有重要的指导意义,同时在晶体学等领域也有广泛应用。
机械工程材料1.室温下,金属晶粒越细,则强度越高、塑性越高;2.因为体心立方晶格与面心立方晶格具有相同数量的滑移系,所以两种晶体的塑性变形能力完全相同;3.间隙固溶体一定是无限固溶体;4.铁素体的本质是碳在a-Fe中的间隙相;5.在铁碳合金平衡结晶过程中,只有碳质量分数为4.3%的铁碳合金才能发生共晶反应;6.高合金钢既具有良好的淬透性,也具有良好的淬硬性;7.钢的淬透性高,则其淬透层的深度也越大;8.T8钢比T12和40钢有更好的淬透性;9.灰铸铁可以经过热处理改变基体组织和石墨形态;10.齿轮渗碳用钢常采用低碳钢;是非题1.√ 2.× 3.× 4.√ 5.× 6.× 7.√8.√ 9.× 10.√1.金属结晶时,冷却速度越快,其实际结晶温度将a.越高; b.越低; c.越接近理论结晶温度2.α-Fe是实际原子数为 ;a.2; b.4; c.63.固溶体的晶体结构 ;a.与溶剂相同; b.与溶质相同; c.为其他晶型4.间隙相的性能特点是 ;a.熔点高、硬度低; b.硬度高、熔点低;c.硬度高、熔点高5. 金属的加工硬化现象将导致 ;a. 强度降低,塑性提高;b. 强度提高,塑性降低; c.强度降低,塑性降低6.用下述三种方法制成齿轮, 种方法较为理想;a. 用厚钢板切出圆饼,再加工成齿轮;b. 由粗钢棒切下圆饼,再加工成齿轮;c. 由圆棒锻成圆饼,再加工成齿轮7. 钢中含硫量过高的最大危害是造成 ;a. 热脆;b. 冷脆;c. 氢脆8.奥氏体是 ;a.碳在γ-Fe中的间隙固溶体 b.碳在α-Fe中的间隙固溶体;c. 碳在α-Fe中的无限固溶体9.珠光体是一种 ;a.单相固溶体; b.两相混和物; c.Fe与C的化合物10.铁素体的机械性能特点是 ;a.强度高、塑性好、硬度低; b.强度低、塑性差、硬度低;c. 强度低、塑性好、硬度低11. 奥氏体向珠光体的转变是 ;a.扩散型转变; b.非扩散型转变; c.半扩散型转变12. 钢经调质处理后获得的组织是 ;a,回火马氏体; b.回火屈氏体; c.回火索氏体13. 共析钢的过冷奥氏体在550℃~350℃的温度区间等温转变时,所形成的组织是 ;a.索氏体 b.下贝氏体; c.上贝氏体14. 若合金元素能使C曲线右移,钢的淬透性将 ;a.降低; b.提高; c.不改变15. 淬硬性好的钢 ;a.具有高的合金元素含量; b.具有高的碳含量;c.具有低的碳含量16. 钢的回火处理是在 ;a.退火后进行; b.正火后进行; c.淬火后进行17.渗碳钢后性能最好;a. 直接淬火;b. 一次淬火;c. 二次淬火18. 量具钢加工工艺中,在切削加工之后淬火处理之前可能的热处理工序为;a. 退火;b. 调质;c. 回火19. 灰口铸铁铸件薄壁处出现白口组织,造成切削加工困难采取的热处理措施为 ;a. 高温退火;b. 调质;c. 回火20.在下列牌号中属于球墨铸铁的是 ;a. HT100;b. KT30-6;c. QT40-7选择2.a 3.a 4.c1.晶粒大小对金属性能有何影响如何细化晶粒2.什么是热处理常见的热处理方法有几种其目的是什么5已知某轴的材料为45钢,其生产工艺路线为:下料→锻造→预备热处理→切削加工→最终热处理→精加工→装配请说明各道热处理工序的名称及作用;7. 为什么一般机器的支架、机床的床身常用灰口铸铁制造一:名词解释1.过冷度:理想结晶温度与实际结晶温度的差值;2.变质处理:向液体中加入固态元素或化合物作为非均质形核的核心,从而提高了形核率,细化了晶粒;3.再结晶:当变形金属加热到某一温度,破碎拉长的晶粒长大为等轴晶粒;4.马氏体:C在α-Fe中形成的过饱和间隙固溶体;5.球化退火:过共析钢加热到不完全奥氏体化退火,使渗碳体由片状转为球状,提高了塑性和切削加工能力;三:四:简答1.解:晶粒越细,强度、硬度、塑性和韧性越大;细化晶粒采取提高过冷度、变质处理、振动处理;2.解:把固态金属材料通过一定的加热,保温和冷却以获得所需组织、结构和性能的工艺称热处理;常见的热处理方法有退火、正火、淬火和回火;退火的目的:降低钢的硬度,提高塑性;细化晶粒,消除因铸、锻、焊引起的组织缺陷,均匀钢的组织和成分;消除钢中的内应力,以防止变形和开裂;正火的目的:细化晶粒,获得比较均匀的组织和性能;对低碳钢可提高硬度,改善切削加工性;对过共析钢可抑制网状渗碳体析出为球化退火作准备;淬火的目的:使钢件获得所需的马氏体组织,提高工件的硬度,强度和耐磨性;回火的目的:主要是消除钢件在淬火时所产生的应力;稳定组织,使工件尺寸和性能稳定;提高钢的塑韧性;4.解:马氏体分解;残余奥氏体转变;碳化物转变;碳化物聚集长大及α回复与再结晶;5.解:预备热处理:完全退火,作用是细化晶粒,消除内应力,降低硬度,提高塑性;最终热处理:淬火+高温回火,作用是获得良好的综合机械性能;7.解:铸铁的铸造性能良好;铸铁具有良好的切削加工性能;铸铁具有优良的减磨性;铸铁具有优良的消震性;铸铁具有低的缺口敏感性;所以一般机器的支架、机床的床身常用灰口铸铁制造;一、填空题1、金属中常见的三种晶体结构分别是体心立方、、 ,室温下铁α-Fe的晶体结构属于 ;2、根据使用性能确定淬火后零件的回火温度,T12锉刀采用温回火,60钢弹簧采用温回火,45钢车床主轴采用温回火;3、冷变形后的金属在加热的过程中,随着温度的升高和加热时间的延长,其组织和性能一般要经历三个阶段的变化,它们依次是、、 ;4、所有的固态物质就其原子或分子排列的规则性来分类,可分为两大类,其中把内部原子或分子呈周期性规则排列的物质称为 ,否则称为 ;5、按钢中含碳量高低,可将其分为、、和 ;6、某些原子半径很小的非金属元素溶入固态溶剂金属内,便形成_ __固溶体;溶质原子置换了溶剂晶格中的部分溶剂原子便形成_________固溶体;7、通常高碳钢奥氏体化后经快速冷却淬火所得到的组织为____ ____和少量的残余奥氏体;8、所有的固态物质就其原子或分子排列的规则性来分类,可分为两大类,其中把内部原子或分子呈周期性规则排列的物质称为 ,否则称为 ;9、钢材加热时奥氏体的形成包括四个过程,依次为、残余Fe3C的溶解及奥氏体的均匀化;10、按钢中合金元素含量高低,可将合金钢分为、、 ;11.晶体缺陷有、、和 ;12.固溶体按溶质原子在晶格位置分为、 ;13.铸造时常选用接近共晶成分、单相固溶体的合金;14.疲劳断裂的特点有、、 ;15.正火和退火的主要区别是 ;16. 淬火发生变形和开裂的原因是 ;17.40Cr,GCr15,20CrMo,60Si2Mn中适合制造轴类零件的钢为 ;18.用T12钢制造车刀,在切削加工前进行的预备热处理为、 ;19.灰口铸铁铸件薄壁处出现白口组织,造成切削加工困难采取的热处理措施为 ;20.在牌号HT100、KT30-6、QT40-7中属于球墨铸铁的是 ;二、选择题1、固溶体的性能特点是 ;A、韧性高、硬度低B、硬度高、韧性低C、硬度高、韧性高2、为细化晶粒,可采用 ;A、快速浇注B、加变质剂C、以砂型代金属型3、钢中含磷量过高的最大危害是造成 ;A、热脆B、冷脆C、氢脆4、铁碳合金的基本组织中,强度最大的是 ;A、莱氏体B、铁素体C、珠光体5、金属的加工硬化现象将导致: ;A、强度降低,塑性提高B、强度提高,塑性降低C、强度降低,塑性降低6、20钢的室温组织是: ;A、铁素体B、珠光体C、铁素体+珠光体7、共析钢的过冷奥氏体在350℃~230℃的温度区间等温转变时,所形成的组织是 ;A、索氏体B、下贝氏体C、上贝氏体8、45钢淬火后测量硬度宜采用的硬度计是 ;A、HRAB、HRBC、HRC9、不完全退火主要适用于 ;A、亚共析钢B、共析钢C、过共析钢10、工业上所用的铸铁绝大部分是属于: ;A、白口铸铁B、麻口铸铁C、灰口铸铁11、碳在γ-Fe中形成的间隙固溶体,叫做 ;A、铁素体B、奥氏体C、马氏体D、贝氏体12、含碳%的Fe-C合金,从奥氏体相区冷却到727℃时,生成珠光体的过程叫做 ;A、共析转变B、奥氏体转变C、共晶转变D、马氏体转变13、合金元素含量低于5%的合金钢,叫做 ;A、低合金钢B、低碳钢C、高合金钢D、中合金钢14、晶界、亚晶界是实际晶体材料的晶体缺陷中的 ;A、点缺陷B、线缺陷C、面缺陷D、体缺陷15、9SiCr中碳的质量分数含碳量约为 ;A、%B、%C、9%D、%16、从铁碳合金相图中可知,亚共析钢所得到的室温平衡组织为 ;A、珠光体B、铁素体+珠光体C、低温莱氏体D、铁素体17、金属结晶时,冷却速度越快,其过冷度将 ;A、越大B、越小C、等于零D、变化不确定18、GCr15钢中的Cr的平君含量为 ;A、15%B、%C、%19、汽车、拖拉机的齿轮要求表面高耐磨性,中心有良好的强韧性,常常选用渗碳钢,下列可以作为生产该类零件的材料是 ;A、20CrMnMoB、65MnC、Cr12MoVD、T820、为了减少金属铸锭、铸件或锻坯的化学成分和组织的不均匀性,一般所采用的退火工艺是 ;A、再结晶退火B、去应力退火C、扩散退火D、球化退火三、判断题1、同种钢材在相同的加热条件下加热后保温、淬火,其中水淬比油淬的淬透性好,小件比大件的淬透性好;2、65Mn是合金调质结构钢;3、从C曲线中分析可知,共析钢的过冷奥氏体在A1~550℃的范围内发生珠光体类型的组织转变;4、共晶反应就是在某一恒定温度时,从一定浓度成分的液相中同时结晶析出两种不同浓度成分的固相;5、T12钢与45钢均属于中碳钢;6、过共析钢中,网状渗碳体的存在使钢的强度和塑性均上升;7、正火是将钢件加热至完全奥氏体化后空冷的热处理工艺;8、铁碳相图中塑性最好的区域是莱氏体区;9、间隙固溶体一定是无限固溶体;10、回火索氏体的综合力学性能明显优于奥氏体等温冷却直接所得到的片层状索氏体的综合力学性能;11、晶粒度级数数值越大,晶粒越细;12、金属铸件可以通过再结晶退火来细化晶粒;13、当原始组织为片状珠光体的钢加热奥氏体化时,细片状珠光体的奥氏体化速度要比粗片状珠光体的奥氏体化速度快;14、在退火状态接近平衡组织45钢比20钢的塑性和强度都高;15、马氏体是碳在的a-Fe中的过饱和固溶体;当奥氏体向马氏体转变时,体积要收缩;16、当共析成分的奥氏体在冷却发生珠光体转变时,温度越低,其转变产物组织越粗;17、经退火后再高温回火的钢,能得到回火索氏体组织,具有良好的综合机械性能;18、表面淬火既能改变钢的表面组织,也能改善心部的组织和性能;19、合金元素Mn、Ni可以扩大奥氏体区;20、高速钢需要反复锻造是因为硬度高不易成形;四、简答题1、淬火后为什么一定要进行回火才可使用按回火温度的高低可将回火分为哪三类各自的所对应的回火组织是什么2、影响金属结晶过程的主要因素是什么3、金属的塑性变形对金属的组织与性能有何影响4、正火和退火的主要区别是什么5、分析高速钢中合金元素的作用;6、现要求用20钢采取渗碳方法制造齿轮,其加工路线为:锻造→预备热处理→切削加工→最终热处理→喷丸→精磨;试写出各热处理工艺名称,并解释其目的和所获得的细微组织;一、填空题每空1分,共20分1.机械设计时常用和两种强度指标;2.若退火亚共析钢试样中先共析铁素体占%,珠光体%,则此钢的含碳量为 ;3.屈强比是与之比;4.一般工程结构用金属是晶体,在各个方向上的性能 ,这就是实际金属的现象;5.实际金属存在、和三种缺陷;实际晶体的强度比理想晶体的强度高,低得多;6.根据组成合金的各组元之间的相互作用不同,合金的结构可分为两大类:和 ;固溶体的晶格结构同 ,其强度硬度比纯金属的 ;7.共析钢加热至Ac1时将发生向的转变,其形成过程包括四个阶段;8.把两个45钢的退火态小试样分别加热到Ac1~Ac3之间和Ac3以上温度水冷淬火,所得到的组织前者为 ,后者为 ;二、判断改错题对打√,错打“×”并改错,每小题1分,共10分1.随奥氏体中碳含量的增高,马氏体转变后,其中片状马氏体减少,板条状马氏体增多;2.回火屈氏体、回火索氏体和过冷奥氏体分解时形成的屈氏体、索氏体,只是形成过程不同,但组织形态和性能则是相同的;3.退火工件常用HRC标出其硬度,淬火工件常用HBS标出其硬度;4.马氏体是碳在α-Fe中所形成的过饱和固溶体;当发生奥氏体向马氏体的转变时,体积发生膨胀;5.表面淬火既能改变工件表面的化学成分,也能改善其心部组织与性能;6.化学热处理既能改变工件表面的化学成分,也能改善其心部组织与性能;7.高碳钢淬火时,将获得高硬度的马氏体,但由于奥氏体向马氏体转变的终止温度在0℃以下,故钢淬火后的组织中保留有少量的残余奥氏体;8.为了消除加工硬化便于进一步加工,常对冷加工后的金属进行完全退火;9.片状珠光体的机械性能主要决定于珠光体的含碳量;10.由于钢回火的加热温度在A1以下,所以淬火钢在回火时没有组织变化;三、选择题每小题1分,共10分1.钢在淬火后所得的组织是A.淬火马氏体B.回火索氏体C.回火屈氏体D.索氏体2.在淬火钢中,当含碳量增加到%以后,随含碳量的增加,硬度增加缓慢,这是因为A. 随含碳量的增加,残余奥氏体的量增多B. 随含碳量的增加,片状马氏体的量增多C. 随含碳量的增加,淬火内应力增大D. 随含碳量的增加,非马氏体的量减少3.若钢中加入的合金元素能使C曲线左移,则将使钢的淬透性A.提高B.降低C.不改变D.对小试样堤高,对大试样则降低4.下列钢铁材料中切削性能较好的是A.工业纯铁钢 C.白口铸铁钢5.钢锭中的疏松可以能过下面哪种方法改善A.完全退火B.足够变形量的锻轧C.扩散退火D.正火6.正火T8钢与完全退火T8钢相比A.前者珠光体更细密,故强度要低些B. 前者珠光体更细密,故强度要高些C.前者珠光体更粗大,故强度要低些D. 前者珠光体更粗大,故强度要高些7.退火亚共析钢,随含碳量的增加、σb值减小,δ、a K值增加 B. HBS、σb值增加,δ、a K值减小C. HBS、σb值增加,δ、a K值增加D. HBS、σb值减小,δ、a K值减小8.碳含量为Wc=%的铁碳合金具有良好的A. 可锻性B. 切削加工性能C. 可焊性D. 铸造性能9.建筑用钢筋宜选用A. 高碳钢B.中碳钢C. 低碳钢D.工具钢10.下述退火态钢中强度最高的是钢钢钢钢四、简答题30分1.某厂仓库有20钢、45钢、T12钢和白口铸铁,大小和形状都一样,根据所学知识,可用哪些简单方法把它们迅速区分开请说明理由;5分2. 60钢经正常淬火后得到什么组织经退火后得到什么组织60钢淬火后分别在200℃、400℃、600℃回火又得到什么组织5分五、综合分析题10分用一根冷拉钢丝绳吊装一大型工件进入热处理炉,并随工件一起加热到1000℃保温,当出炉后再次吊装工件时,钢丝绳发生断裂,试分析其原因;一、填空题每空1分,共20分1. 抗拉强度σb,屈服强度σs或σ2. 约%3. 屈服强度,抗拉强度4. 多,相同,各向同性5.点缺陷,线缺陷,面缺陷,低6. 固溶体,金属化合物,溶剂,高7. 珠光体,奥氏体8. 马氏体+铁素体+残余奥氏体,马氏体+残余奥氏体二、判断改错题对打√,错打“×”并改错,每小题1分,共10分1. ×,片状马氏体增多,板条马氏体减少;2. ×,组织形态和性能也不同;3. ×,退火工件硬度用HBS标出,淬火工件硬度用HRC标出;4.√;5.×,表面淬火只能改变工件表面的组织与性能;;6.√;7.√;8. ×,进行再结晶退火;9×,取决于珠光体的片间距;10. ×,尽管钢回火的加热温度在A1以下,但是淬火钢在回火时仍有组织变化;三、选择题每小题1分,共10分1. A四、简答题30分1.5分答:方法一:硬度测试;硬度值大小顺序是:白口铸铁>T12钢>45钢>20钢; 因为铁碳合金的硬度随含碳量的增加而升高;四种铁碳合金的含碳量是:白口铸铁大于%C > T12钢%C>45钢%>20钢%C;方法二:分别制备四种材料的金相试样,在金相显微镜上进行显微组织观察;亚共析钢组织为F+P,且亚共析钢中随含碳量增加铁素体减少,珠光体增多;过共析钢组织为P+Fe3CⅡ,且当Wc>%时,Fe3CⅡ沿晶界呈网状分布;白口铸铁的组织中有莱氏体;所以,组织为F+P而铁素体少的为20钢、珠光体多的为45钢;组织中有Fe3CⅡ沿晶界呈网状分布的T12钢,有莱氏体组织存在的是白口铸铁;2.5分答:60钢淬火后组织为马氏体;1分退火组织为珠光体+铁素体;1分200℃回火后组织为回火马氏体;1分400℃回火后为回火屈氏体;1分600℃回火后为回火索氏体;1分五、10分答:冷拉钢丝绳是利用加工硬化效应提高其强度的,在这种状态下的钢丝中晶体缺陷密度增大,强度增加,处于加工硬化状态;在1000℃时保温,钢丝将发生回复、再结晶和晶粒长大过程,组织和结构恢复到软化状态;在这一系列变化中,冷拉钢丝的加工硬化效果将消失,强度下降,在再次起吊时,钢丝将被拉长,发生塑性变形,横截面积减小,强度将比保温前低,所以发生断裂;一、名词解释共15分,每小题3分二、1. 奥氏体A 2.回复3.固溶体4.自然时效5.加工硬化三、四、二、填空题共20分,每空1 分五、1.石墨为片状的灰口铸铁称为铸铁,石墨为团絮状的灰口铸铁称为__ 铸铁,石墨为球状的灰口铸铁称为铸铁;其中铸铁的韧性最高,因而可以锻造;六、2. 陶瓷材料中的气相是指,在程中形成的,它了陶瓷的强度;七、3.根据采用的渗碳剂的不同,将渗碳分为__________、__________和__________三种;八、4.工程中常用的特殊性能钢有_________、_________、_________等;九、5.金属的断裂形式有__________和__________两种;十、6.金属元素在钢中形成的碳化物可分为_________、_________两类;十一、7.常见的金属晶体结构有____________、____________和____________三种;二、填空题十二、1、普通灰口;可锻;球墨;十三、2、气孔;烧结;降低;十四、3、固体渗碳气体渗碳十五、4、不锈钢耐热钢耐磨刚十六、5、延性断裂十七、6、合金渗碳体特殊碳化物十八、7、体心立方晶格密排六方晶格十九、二十、二十一、三、选择题共25分,每小题1分二十二、钢钢锭在1000℃左右轧制,有时会发生开裂,最可能的原因是二十三、 A.温度过低; B.温度过高;C.钢锭含磷量过高; D.钢锭含硫量过高二十四、2.下列碳钢中,淬透性最高的是二十五、钢;钢;钢;钢二十六、在1Cr18Ni9Ti钢中的主要作用是二十七、A.提高淬透性; B.固溶强化;C.扩大Fe-Fe3C相图中的γ相区; D.细化晶粒;二十八、钢锻造后,在机械加工之前应进行二十九、A.完全退火;B.球化退火;C.去应力退火;D.再结晶退火三十、5.下列材料中,最适合制造机床床身的是三十一、钢;钢;;三十二、6.下列材料中,最适合制造气轮机叶片的是三十三、钢;钢;钢;钢三十四、7.下列材料中,最适合制造飞机蒙皮的是三十五、;旧牌号LD5;;旧牌号LY12三十六、8.下列材料中,最适合制造盛放氢氟酸容器的是三十七、;; C.聚四氟乙烯;三十八、9.下列材料中,最适合制造汽车板弹簧的是三十九、;;;四十、10.下列材料中,最适合制造汽车火花塞绝缘体的是四十一、; B.聚苯乙烯;C.聚丙烯;D.饱和聚酯四十二、11.铜只有通过冷加工并经随后加热才能使晶粒细化,而铁则不需冷加工,只四十三、需加热到一定温度即使晶粒细化,其原因是四十四、A.铁总是存在加工硬化,而铜没有;B.铜有加工硬化现象,而铁没有;四十五、C.铁在固态下有同素异构转变;而铜没有 D.铁和铜的再结晶温度不同四十六、12.常用不锈钢有铁素体不锈钢、奥氏体不锈钢、马氏体不锈钢和四十七、A.铁素体-奥氏体不锈钢;B.马氏体-奥氏体不锈钢;C.莱氏体不锈钢; D.贝氏体不锈钢四十八、13.以下哪种铸铁的断口呈灰黑色四十九、A.马口铁;B.白口铸铁;C.麻口铸铁;D.灰铸铁五十、14.用于制造渗碳零件的钢称为;五十一、 A.结构钢;B.合金钢; C.渗碳钢;D.工具钢五十二、15.马氏体组织有两种形态;五十三、 A.板条、树状;B.板条、针状;C.树状、针状; D.索状、树状五十四、16.实际生产中,金属冷却时;五十五、A.理论结晶温度总是低于实际结晶温度;B.理论结晶温度总是等于实际结晶温度;五十六、C.理论结晶温度总是大于实际结晶温度; D.实际结晶温度和理论结晶温度没有关系五十七、17.零件渗碳后,一般需经过才能达到表面硬度高而且耐磨的目的;五十八、A.淬火+低温回火; B.正火;C.调质; D.淬火+高温回火五十九、曲线右移使淬火临界冷却速度,淬透性;六十、 A.减小、增大; B.减小、减小; C.增大、减小;D.增大、增大六十一、19.机械制造中,T10钢常用来制造;六十二、 A.容器; B.刀具;C.轴承;D.齿轮六十三、20.钢经表面淬火后将获得;六十四、 A.一定深度的马氏体; B.全部马氏体; C.下贝氏体; D.上贝氏体六十五、钢的含铬量是:六十六、六十七、22.铅在常温下的变形属:六十八、A.冷变形; B.弹性变形;C.热变形; D.既有冷变形也有热变形六十九、23、黄铜是以为主加元素的铜合金;七十、A.铅 B.铁C.锡D.锌七十一、24、在Fe-Fe3C和图中,奥氏体冷却到ES线时开始析出;七十二、A.铁素体 B.珠光体C.二次渗碳体D.莱氏体七十三、25、从金属学的观点来看,冷加工和热加工是以温度为界限区分的;七十四、A.结晶B.再结晶C.相变℃三、选择题七十五、; ; ; ; ; ; ; ; ; ; ;; ; ; ; ; ; ;七十六、七十七、七十八、四、判断题共10 分,每小题1 分七十九、1.回火托氏体和托氏体皆由铁素体和渗碳体两个相构成,因而其性能相同;八十、2.冷却速度越快,钢的淬透性越高;八十一、3.钢的淬透性越高,产生焊接裂纹的倾向越大;八十二、4.铝合金也可以象钢那样通过淬火明显提高其硬度;八十三、5.所有强化金属的手段,都在提高强度的同时降低了韧性;八十四、6.可锻铸铁中的团絮状石墨是浇注球墨铸铁时石墨球化不良的结果;八十五、7.一定加热温度下,奥氏体晶粒长大倾向小的钢称为本质细晶粒钢;八十六、8.所谓过量弹性变形,是指零件发生了塑性变形;八十七、9.铝极易氧化,故铝制品的抗氧化失效能力极差;八十八、10.弹簧钢淬火后采用中温回火是想提高钢的弹性模量;四、判断题1.×;2.×;3.√;4.×;5.×;6.×;7.√;9.×;10.×;五、简答题共30分,每题10分1.简述奥氏体晶粒对钢在室温下组织和性能的影响;2.简述回火的目的;3.何谓碳钢中的铁素体、渗碳体、珠光体他们的力学性能各有何特点五、简答题1、答:奥氏体晶粒细小时,冷却后转变产物的组织也细小,其强度与塑性韧性都较高,冷脆转变温度也较低;反之,粗大的奥氏体晶粒,冷却转变后仍获得粗晶粒组织,使钢的力学性能特别是冲击韧性降低,甚至在淬火时发生变形、开裂;2、答:回火的目的是:1降低零件脆性,消除或降低内应力;2获得所要求的力学性能;3稳定尺寸;4改善加工性;3、答:铁素体——碳在α-Fe中的间隙固溶体,软而韧;渗碳体——碳与铁形成的间隙化合物,硬而脆;珠光体——铁素体与渗碳体形成的层片状交替排列的机械混合物,良好的综合力学性能;参考答案一、名词解释1.奥氏体A:C在γ-Fe中的间隙固溶体,常用A或γ表示,是一种硬度较低而塑性较高的固溶体;3.固溶体:组成合金的组元,在固态时相互溶解,所形成的单一均匀的物质;4.自然时效:自然时效是指经过冷、热加工或热处理的金属材料,于室温下发生性能随时间而变化的现象;5.加工硬化:金属材料随着冷塑变形程度的增大,强度和硬度逐渐升高,塑性和韧性逐渐降低的现象称为加工硬化或冷作硬化;一、名词解释:⒈调质:对钢材作淬火+高温回火处理,称为调质处理;⒉碳素钢:含碳量≤%的铁碳合金;⒊SPCD:表示冲压用冷轧碳素钢薄板及钢带,相当于中国08Al13237优质碳素结构钢;二、填空题:10×2=20分⒈按腐蚀过程特点,金属腐蚀可分为化学腐蚀_和电化学腐蚀___;2.常用力学性能判据有_强度____、__韧性_、_延展性_和_弹性模量_;。
铁元素的晶格类型
铁元素是一种常见的过渡金属元素,其晶体结构与其他过渡金属元素有所不同。
铁元素的晶格类型主要有两种:面心立方晶格和体心立方晶格。
面心立方晶格是指每个原子都位于正方形面的中心,所有原子的排列方式呈现出一种六方对称的结构。
这种晶格类型在高温下稳定,但在室温下则不太稳定。
体心立方晶格则是指每个原子都位于正方形的顶点和立方体的
中心,所有原子的排列方式呈现出一种立方体对称的结构。
这种晶格类型在室温下是最稳定的铁晶体结构。
此外,铁元素还可以形成一些其他的晶格类型,比如六方密堆积和六方紧密堆积等,但这些结构都比较不稳定,只在一些特殊的条件下才会出现。
- 1 -。
体心立方、面心立方晶格主要晶面的原子排列和密度
体心立方晶格面心立方晶格
晶面指数晶面原子
排列示意图
晶面原子密度
(原子数/面积)
晶面原子
排列示意图
晶面原子密度
(原子数/面积)
{100} {110} {111}
体心立方、面心立方晶格主要晶向的原子排列和密度
体心立方晶格面心立方晶格
晶向指数晶向原子
排列示意图
晶向原子密度
(原子数/长度)
晶向原子
排列示意图
晶向原子密度
(原子数/长度)
<100>
<110>
<111>
第1章小结
1.三种常见金属的晶体结构
体心立方晶格(胞):晶格常数a、90°,晶胞原子数为2个,原子半径:,
致密度为68%,最大空隙半径r四=0.29r原子,配位数为8面心立方晶格(胞):晶格常数a、90°,晶胞原子数为4个,
原子半径:
,
致密度为74%,最大空隙半径r八=0.414r原子,配位数为12。
密排六方晶格(胞):晶格常数a、c、90°、120°,晶胞原子数为6个,
原子半径:,
致密度为74%,最大空隙半径r八=0.414r原子,配位数为12。
2.晶面与晶向可用晶面指数与晶向指数来表达。
不同晶面、不同晶向上的原子排列情况不同。
体心立方晶格的最密面为{110},最密方向为<111>。
面心立方晶格的最密面为{111},最密方向为<110>。
密排六方晶格的最密面为{0001},最密方向为。
3.实际金属中含有点缺陷(空位、间隙原子、异类原子)、线缺陷(位错)、面缺陷(晶界、亚晶界)三类晶体缺陷,位错密度增加,材料强度增加。
晶界越多,晶粒越细,金属的强度越高,同时塑性越好(即细晶强化)。
4.合金中有两类基本相:固溶体和金属化合物。
固溶强化是金属强化的一种重要形式。
细小弥散分布的金属化合物可产生弥散强化或第二相强化。
材料的微观组成和微观形貌称组织,材料的组织取决于化学成分和工艺过程。
5.金属材料的性能特点是:强度高,韧性好,塑性变形能力强,综合机械性能好,通过热处理可以大幅度改变机械性能。
金属材料导电、导热性好。
不同的金属材料耐蚀性相差很大,钛、不锈钢耐蚀性好,碳钢、铸铁耐蚀性差。
6.高分子材料结构由大分子链组成,大分子链之间的相互作用力为分子键,分子链的原子之间、链节之间的相互作用力为共价键。
高分子材料的大分子链结构与聚集态及其性能密切相关。
高分子的聚集态结构分无定形和晶态两种。
线型非晶态高聚物在不同温度下表现三种物理状态:玻璃态、高弹态、粘流态。
高分子材料的性能特点:高聚物轻,其特有的机械性能是高弹性和粘弹性。
由于可以处于不同的力学状态,高分子材料可以是硬脆、强硬、强韧、柔韧或软弱的,机械性能不高,刚度小,强度不高,韧性较低。
高分子材料耐磨、减摩性能好,绝缘、绝热、绝声,耐蚀性能好,但耐热性不高,存在老化问题。
7. 陶瓷材料的生产过程包括原料的制备、坯料的成形和制品的烧结三大步骤。
典型陶瓷的组织由晶体相、玻璃相和气相组成。
晶体相是陶瓷的主要组成,决定材料的基本性能。
普通陶瓷的晶体相主要是硅酸盐,特种陶瓷的晶体相为氧化物、碳化物、氮化物、硼化物和硅化物,金属陶瓷则还有金属。
玻璃相为非均质的酸性和碱性氧化物的非晶态固体,起粘结剂作用。
气相是陶瓷组织中残留的孔洞,极大地破坏材料的机械性能。
陶瓷的性能特点是:具有不可燃烧性、高耐热性、高化学稳定性、不老化性、高的硬度和良好的抗压能力,但脆性很高,温度急变抗力很低,抗拉、抗弯性能差,不易加工。