溶血性链球菌的检验
- 格式:ppt
- 大小:745.50 KB
- 文档页数:14



链球菌属的特性及其检验作者:陆德胜来源:《中国当代医药》2010年第31期[摘要] 目的:总结链球菌属的特性及其检验技术,结合临床经验,进一步提高细菌分离及鉴定水平。
方法:采用显微镜检查、分离培养、细菌生化反应、血清学试验等进行分离和鉴定。
结果:根据菌体形态、菌落形态、溶血特征将链球菌分为甲型溶血性链球菌、乙型溶血性链球菌、丙型链球菌;按链球菌细胞壁中多糖抗原不同,可分成A、B、C、D等20个群。
结论:链球菌是临床常见的致病菌,正确掌握检验方法,科学地分离和鉴定,有助于临床做出合理的诊治决策。
[关键词] 链球菌属;特性;分离培养;生化反应;血清学试验[中图分类号] R446.5[文献标识码] B [文章编号] 1674-4721(2010)11(a)-080-02链球菌属细菌广泛分布于自然界、人及动物肠道和鼻咽部,大多数不致病。
其中A、B群及肺炎链球菌是本属的3种重要致病菌,可引起各种化脓性炎症、医源性伤口感染、新生儿败血症、细菌性心内膜炎以及风湿热、肾小球肾炎等超敏反应性疾病[1]。
另外草绿色链球菌为条件致病菌。
因此,本属细菌的鉴定、药敏试验是微生物检验工作的重要内容之一,临床上常见的标本包括咽拭子、痰液、分泌物、穿刺液、尿液、脑脊液和血液。
现将本属的特性及其检验总结如下:1 资料与方法1.1一般资料本院微生物实验室2009年共接收咽拭子样本299例、痰液样本1 319例、分泌物817例、穿刺液239例、尿液704例、脑脊液54例和血液培养815例,合计4 247例。
其中门诊患者样本239例,住院患者样本4 008例。
细菌培养阳性结果1 475例,阳性率为34.73%。
其中链球菌属阳性83例,占5.63%。
1.2 检验方法根据不同疾病采集不同标本。
1.2.1 显微镜检查咽拭子、痰液、脓液、穿刺液、脑脊液等标本可直接涂片革兰染色,镜检见链状排列革兰阳性球菌可初步报告,及时供临床参考。
1.2.2 分离培养血液标本需要先增菌培养,脓液、咽拭可直接接种血琼脂平板。


【GB/T 4789.11—1994】食品卫生微生物学检验溶血性链球菌检验1 主题内容与适用范围本标准规定了食品中溶血性链球菌的检验方法。
本标准适用于食品和食物中毒样品中溶血性链球菌的检验。
2 引用标准GB 4789.28 食品卫生微生物学检验染色法、培养基和试剂3 设备和材料3.1 温箱:36±1℃。
3.2 水浴:36±1℃。
3.3 显微镜。
3.4 离心机。
3.5 试管架。
3.6 灭菌平皿。
3.7 灭菌小试管。
3.8 载玻片。
3.9 灭菌吸管:1mL、10mL。
3.10 灭菌镊子。
3.11 均质器。
3.12 酒精灯。
3.13 接种环。
4 培养基和试剂4.1 葡萄糖肉浸液肉汤:按GB 4789.28中4.1规定,在肉浸液肉汤内加入1%葡萄糖。
4.2 肉浸液肉汤:按GB 4789.28中4.1规定。
4.3 匹克氏肉汤:按GB 4789.28中4.62规定。
4.4 血琼脂平板:按GB 4789.28中4.6规定。
4.5 人血浆。
4.6 0.25%氯化钙。
4.7 灭菌生理盐水。
4.8 杆菌肽药敏纸片(含0.04单位)。
5 检验程序(图略)6 操作步骤6.1 样品处理称取25g固体检样;称取25mL液体检样,加入225mL灭菌生理盐水,研成匀浆制成混悬液。
6.2 一般培养将上述混悬液吸取5mL,接种于50mL葡萄糖肉浸液肉汤;或直接划线接种于血平板,如检样污染严重,可同时按上述量接种匹克氏肉汤,经36±1℃培养24h,接种血平板,置36±1℃培养24h,挑起乙型溶血圆形突起的细小菌落,在血平板上分纯,然后观察溶血情况及革兰氏染色,并进行链激酶试验及杆菌肽敏感试验。
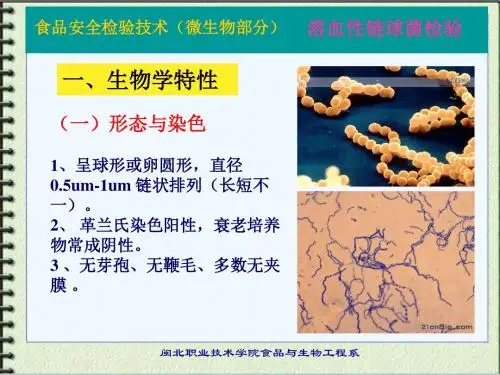
6.3 形态与染色本菌呈球形或卵圆形,直径0.5~1μm,链状排列,链长短不一,短者4~8个细胞组成,长者20~30个,链的长短常与细菌的种类及生长环境有关;液体培养中易呈长链;在固体培养基中常呈短链,不形成芽孢,无鞭毛,不能运动。



链球菌属及其检验「微生物检验」链球菌属(Streptococcus)细菌,呈链状排列的革兰阳性球菌,个别种成双排列。
广泛分布于自然界、人及动物肠道和健康人鼻咽部,大多数不致病,致病菌可引起各种化脓性炎症、猩红热、新生儿败血症、细菌性心内膜炎以及风湿热、肾小球肾炎等超敏反应性疾病。
下面是yjbys店铺为大家带来的关于链球菌属细菌的知识,欢迎阅读。
⒈分类链球菌的分类方法尚未统一。
常用下列两种方法。
⑴根据溶血现象:分为3类。
①甲型溶血性链球菌(α-hemolytic streptococcus):菌落周围有1~2mm宽的草绿色溶血环,称甲型溶血或α溶血,该类菌又称草绿色链球菌,为条件致病菌。
②乙型溶血性链球菌(β-hemolytic streptococcus):菌落周围有2~4mm宽的透明溶血环,称乙型溶血或β溶血,该类菌又称溶血性链球菌,致病性强,常引起人和动物多种疾病。
③丙型链球菌(γ-streptococcus):菌落周围无溶血环,因而又称不溶血性链球菌,一般不致病。
⑵根据抗原结构:按链球菌细胞壁中多糖抗原不同,可分成A、B、C、D …等20个群。
同群链球菌间,因表面蛋白质抗原不同又分若干型。
如A群根据其M抗原不同,可分成约100个型;B群分4个型。
对人致病的链球菌菌株,主要是 A群,多数呈现乙型溶血。
⒉细菌特性⑴链球菌① 形态染色球形或椭圆形,直径0.5~1.0μm,链状排列,链的长短与细菌的种类和生长环境有关,在液体培养基中形成的链较长。
无芽胞,无鞭毛。
多数菌株在培养早期(2~4h)形成透明质酸的荚膜。
革兰染色阳性。
②分离培养要求较高,培养基中需加入血液或血清、葡萄糖、氨基酸、维生素等物质。
多数菌株兼性厌氧,少数为专性厌氧。
在液体培养基中呈沉淀生长,在血平板上,37℃18~24h后可形成灰白色、圆形、凸起、光滑、直径为0.5mm~0.75mm的细小菌落,菌落周围出现不同类型的溶血环。
③生化反应触酶阴性、一般不分解菊糖,不被胆汁溶解,这两特性可用来鉴别甲型溶血性链球菌和肺炎链球菌。

抗链球菌溶血素“O"试验参考范围:免疫比浊法:0~200 u/ml临床评价:1.链球菌溶血素“O”(ASO)是A群链球菌的代谢产物之一,它是一种具有酶活性的蛋白质,能溶解红细胞,也能破坏白细胞和血小板。
溶血素“O”具有很强的抗原性,机体受A群链球菌感染后可产生溶血素“O”抗体,这种抗体可以抑制溶血素“O”的溶血作用。
通过测定血清中ASO水平,有利于A群链球菌感染的诊断。
2.当ASO试验呈阳性反应,且抗体滴度有逐步增高趋势时,即具有诊断参考价值。
主要见于A群链球菌感染后引起的变态反应性疾病,如风湿热、急性肾小球肾炎等,还可见于A群链球菌感染所致的上呼吸道炎症(咽炎或扁桃体炎)。
85%~90%的患者感染后2周左右到病愈后数月至年余血清中均可测到ASO。
应用ELISA可检测患者血清中的IgM型和IgG 型ASO特异性抗体,IgM-ASO多见于感染的急性期,IgG-ASO见于恢复期。
抗体效价逐步下降时为疾病缓解期,抗体恒定在高效价水平多为非活动期。
3.咽拭培养直接分离病原菌是诊断A群链球菌感染的可靠方法,急性风湿热发作时阳性率可高达70%~90%。
进行多项链球菌抗体试验,可提高对A群链球菌感染诊断的准确率。
这些试验包括抗链球菌激酶(ASK),抗脱氧核糖核酸酶B(ADNase B),抗链球菌二磷酸吡啶核苷酸酶(ADPNase)和抗透明质酸酶(AH)等,其中ASK试验是新近链球菌感染的一个非常敏感的指标。
其它实验室检查还有红细胞沉降率,血清C-反应蛋白试验,血清补体C3、C4成分测定等,上述项目联合应用对A群链球菌感染所致疾病有一定辅助诊断意义。
4.影响本试验结果的因素(1)单一次试验结果对诊断意义不大。
(2)链球菌溶血素“O”在Ph6.5环境中活性最强,偏酸或偏碱都可影响其活性。
(3)在溶血抑制法中,血清溶血、黄疸、高胆固醇或血清保存过久污染长菌者,皆可致试验结果偏高,胆固醇有抑制溶血素活性的作用。

溶血性链球菌检验操作规程溶血性链球菌(英文简称:S. pyogenes)是一种常见的革兰氏阳性球菌,通常引起咽峡炎、皮肤感染和淋巴结炎等疾病。
准确的检测和鉴定溶血性链球菌对于诊断和治疗这些疾病至关重要。
下面是关于溶血性链球菌检验的操作规程。
一、检验前准备1. 检验人员需佩戴好防护用具,如实验手套、隔离眼镜和口罩。
2. 准备好所需的检验试剂和材料,包括培养基、琼脂培养基、草莓牛血琼脂、货架刀等。
3. 仔细核对标本的标签和信息,确保和病人信息一致。
二、标本采集和处理1. 从患者口咽部或其他可疑感染部位采集标本,如咽拭子或分泌物样本。
2. 将标本稀释或切碎,使其与培养基充分混合。
3. 使用棉签或货架刀,将混合好的标本涂抹在琼脂培养基上。
三、培养和鉴定1. 将含有标本的琼脂培养基置于37℃恒温箱中培养18-24小时。
2. 观察培养基上是否有溶血环形形成,表明有溶血性链球菌的存在。
3. 将溶血环形的菌落或单个菌落划取到草莓牛血琼脂上。
4. 再次置于37℃恒温箱中培养18-24小时。
5. 观察草莓牛血琼脂上生长的菌落形态和特征。
6. 进一步进行革兰染色,观察菌形和细胞特征。
四、药敏试验对已鉴定的溶血性链球菌,可以进行药敏试验以确定对何种抗生素敏感。
1. 用细菌悬浮液调整到0.5~0.6麦克法尔兰(McFarland)标准。
2. 使用含有不同抗生素的纸片置于琼脂平板上。
3. 用择菌钳将纸片粘贴于琼脂平板上。
4. 将准备的溶血性链球菌悬液均匀涂抹在琼脂平板上。
5. 将琼脂平板置于37℃恒温箱中培养18-24小时。
6. 观察菌落的生长和抗生素纸片周围的抑制圈,根据直径大小判断菌株的抗药性。
五、结果判定和记录根据溶血环形、菌落形态、革兰染色和药敏试验的结果,判定溶血性链球菌的存在和鉴定结果,并将结果准确记录在检验报告中。
操作规程中的注意事项:1. 检验过程中应严格遵守无菌操作,避免交叉感染。
2. 确保检验室设备和培养基的质量,以及培养温度和时间的准确控制。
一、编制目的为规范本单位β型溶血性链球菌的检测编制本作业指导书。
二、适用范围本指导书适用于食品中β型溶血性链球菌的测定。
三、编制依据GB/T 4789.11-2014《食品安全国家标准食品微生物学检验β型溶血性链球菌检验》四、设备和材料除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:a)恒温培养箱:36℃±1℃;b)冰箱:2℃~5℃;c)厌氧培养装置;d)天平:感量0.1g;e)均质器与配套均质袋;f)显微镜:10×~100×;g)无菌吸管:1ml(具0.01ml刻度)、10ml(具0.1ml刻度)或微量移液器及吸头h) 三角烧瓶;i)无菌培养皿:直径90mm;j)pH计或pH比色管或精密pH试纸;k)水浴装置:36℃±1℃;l)微生物生化鉴定系统。
五、培养基和试剂5.1.改良胰蛋白胨大豆肉汤5.2 哥伦比亚CNA血琼脂5.3 哥伦比亚血琼脂5.4 革兰氏染色液5.5 胰蛋白胨大豆肉汤5.6 草酸钾血浆5.7 0.25%氯化钙(CaCl2)溶液5.8 3%过氧化氢(H2O2)溶液5.9生化鉴定试剂盒或生化鉴定卡六、检验程序溶血性链球菌检验程序见图1图1溶血性链球菌检验程序七、操作步骤7.1样品处理及增菌以无菌操作取样25g(ml),加入装有灭菌225mlmTSB的均质杯,用旋转刀片式均质器以8000r/min~10000 r/min均质;或加入装有225ml mTSB的均质袋中,用拍击式均质器连续均质1min~2min,液体样品振荡混匀即可。
于36℃±1℃,厌氧培养18h~24h。
7.2 分离将增菌液划线接种于哥伦比亚CNA血琼脂,36℃±1℃,厌氧培养18h~24h,观察菌落形态。
溶血性链球在哥伦比亚CNA血琼脂平板上的典型菌落形态为直径约2mm~3mm,灰白色、半透明、光滑、表面凸起、圆形、边缘整齐,并产生β型溶血。
7.3 鉴定7.3.1分纯培养挑取5个(如小于5个则全选)可疑菌落分别接种哥伦比亚血琼脂平板和TSB增菌液,36℃±1℃,培养18h~24h。