烃类选择性氧化01
- 格式:ppt
- 大小:5.17 MB
- 文档页数:5


第七节选择性催化氧化一、烃类晶格氧选择性催化氧化概念烃类的选择性催化氧化,在工业上一般以氧气或空气为氧化剂,催化剂多为可变价过渡金属复合氧化物。
就反应机理而言,大多符合Redox机理,它包括两个主要的过程:①气相的烃分子与高价态金属氧化物催化剂表面上的晶格氧(或吸附氧)作用,烃分子被氧化为目的产物,晶格氧参与反应后,催化剂的金属氧化物被还原为较低价态;②气相氧将低价金属氧化物氧化到初始高价态,补充晶格氧,完成Redox循环。
按Mars和Van Krevenlen提出的Redox模型,选择氧化反应:C n H m+O2→C n H m-2+H2O (1)可写成两个基元反应:C n H m+2OM→C n H m -2O+H2O+2M (2)2M+O2→2OM (3)式中,M——低价态的活性位;OM——有晶格氧的活性位。
但是总反应(1)的速率,实际上是受两个基元反应(2)和(3)中速率较慢的反应所控制。
在通常情况下,催化剂被烃分子还原的反应(2)是慢步骤。
烃类催化氧化反应动力学的研究结果表明,副反应对氧气的反应级数比主反应对氧气的反应级数高,所以提高氧分压通常不能有效增加反应(1)的速率,反而会导致选择性下降。
这是因为提高气相氧分压,一方面会增加与气相氧出于平衡的可逆吸附氧物种(如O2-、O22-、或O-)的表面浓度,这种高活性的可逆吸附氧物种,一般认为主要参与非选择性氧化反应;另一方面对于高温(>900K)的烃类氧化过程表面催化反应外,还伴随有气相自由基反应发生,气相氧的存在也会加快气相深度氧化反应,导致选择性下降。
为了避免气相氧对烃类分子的深度氧化,提高目的产物的选择性,人们在不断改进催化剂性能的同时,尝试了采用催化剂晶格氧作为氧源的反应新工艺。
该工艺按Redox 模型将烃分子与氧气或空气分开进行反应,以便从根本上排除气相深度氧化反应。
目前有两种反应工艺可用于烃类晶格氧选择氧化,一种是膜反应器,另一种是循环流化床。




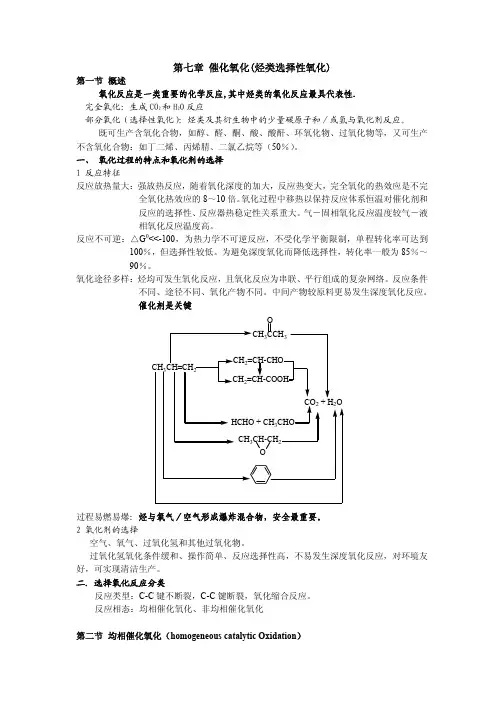




第七章烃类选择性氧化第一节概述 1第二节均相催化氧化(自学)第三节非均相催化氧化(自学)第四节乙烯环氧化制环氧乙烷4第五节丙烯氨氧化制丙烯腈 5主要内容:了解氧化反应的特点、环氧乙烷和丙烯腈的性质、用途、生产方法、操作条件、工艺流程等。
掌握乙烯直接氧化法生产环氧乙烷的主副反应、催化剂、工艺流程、操作参数,掌握丙烯氨氧化法生产丙烯腈的主副反应、催化剂、工艺流程、操作参数等。
授课方式:重点采用课堂讲授,利用启发式、提问式与讲解式相结合的方法,并将理论与实际化工厂相结合进行讲解,同时选部分内容让学生自学。
重点和难点:氧化反应的特点、环氧乙烷和丙烯腈的生产方法、操作条件、工艺流程、主副反应、催化剂、工艺流程、操作参数等。
第一节概述烃类氧化可分为完全氧化(生成二氧化碳和水)和部分氧化(生成淳、醛、酮、酸、酐、环氧化物等)两种。
部分氧化又称选择性氧化。
一、氧化过程的特点和氧化剂的选择1 氧化反应的特征(1)反应放热量很大。
完全氧化放出的热量是部分氧化的8-10倍。
(2)反应不可逆。
氧化反应的ΔGӨ远远小于0,热力学不可逆,不受化学平衡限制。
(3)氧化途径复杂多样。
(4)过程易燃易爆。
2 氧化剂的选择常见的氧化剂有空气、氧气、过氧化氢和其他过氧化物等。
最常用的是空气和氧气。
二、烃类选择性氧化过程的分类按反应类型分:(1)碳链不发生断裂的氧化反应。
(2)碳链发生断裂的氧化反应。
(3)氧化缩合反应。
按反应相态分:均相催化氧化和非均相催化氧化三、作用物结构与氧化难易程度(1)碳氢化合物的C-H键(按键能大小)易被氧化顺序:叔C-H键>仲C-H键>伯C-H键。
(2)具有C=C、C=O双键时,α位(紧挨官能团的碳原子上的氢)的C-H 键键能小,易被氧化。
(3)醛类中,C=O碳原子上的氢易被氧化。
(4)烷基苯,α位(紧挨芳环的碳原子上的氢)的C-H键键能小,易被氧化。
(5)芳环稳定,不易被氧化。
第二节均相催化氧化(自学)第三节非均相催化氧化(自学)第四节乙烯环氧化制环氧乙烷一、环氧乙烷的性质与用途环氧乙烷(简称EO)是最简单最重要的环氧化物,在常温下为气体,沸点10.4 ℃,可与水、醇、醚及大多数有机溶剂以任意比例混合,在空气中的爆炸限(体积分数)为2.6%~100%,有毒。