多组分系统(第一部分
- 格式:pptx
- 大小:1.64 MB
- 文档页数:17




第三章 多组分系统热力学§ 引言基本概念 1、多组分系统两种或两种以上的物质(或称为组分)所形成的系统称为多组分系统。
多组分系统可以是均相的,也可以是多相的。
它(如:多组分单相系统)的热力学性质,则不仅由系统的温度、压力所决定,还与系统的相的组成有关。
2、混合物(mixture )多组分均匀系统中,各组分均可选用相同的方法处理,有相同的标准态,遵守相同的经验定律,这种系统称为混合物。
混合物有气相、液相和固相之分。
3、溶液(solution )含有一种以上组分的液体相或固体相称之为溶液。
溶液有液态溶液和固态溶液之分,但没有气态溶液。
4、溶剂(solvent )和溶质(solute )如果组成溶液的物质有不同的状态,通常将液态物质称为溶剂,气态或固态物质称为溶质。
如果都具有相同状态,则把含量多的一种称为溶剂,含量少的称为溶质。
溶剂和溶质要用不同方法处理,他们的标准态、化学势的表示式不同,服从不同的经验定律。
溶质有电解质和非电解质之分,本章主要讨论非电介质所形成的溶液。
如果在溶液中含溶质很少,这种溶液称为稀溶液,常用符号“∞”表示。
多种气体混合在一起,因混合非常均匀,称为气态混合物,而不作为气态溶液处理。
多组分系统的组成表示法 1、B 的质量浓度B def(B)m Vρ 即用B 的质量m B 除以混合物的体积V 。
B ρ的单位是: kg ·m —3。
2、B 的质量分数BAAdef(B)m w m ∑ 即B 的质量m B 与混合物的质量之比。
w B 的单位为1。
3、B 的浓度B Bdefn c V即B 的物质的量与混合物体积V 的比值。
c B 常用单位是mol ·L —1。
4、B 的摩尔分数B BAAdefn x n ∑ B 的物质的量与混合物总的物质的量之比称为溶质B 的摩尔分数,又称为物质的量分数。
摩尔分数的单位为1。
气态混合物中摩尔分数常用y B 表示。





多组分系统热力学
多组分系统热力学是研究多个组分构成的系统的热力学行为的科学。
在多组分系统中,各个组分之间可能会相互作用,从而影响整个系统的热力学性质。
多组分系统热力学的研究内容包括:
1.热力学第一定律:能量守恒定律,即在一个封闭系统中,能量不
能被创造或消除,只能从一种形式转化为另一种形式。
2.热力学第二定律:熵增定律,即在一个封闭系统中,熵(即系统
的混乱程度)只能增加,不能减少。
这意味着,系统总是朝着熵增的方向演化,而不是熵减的方向。
3.相平衡:研究在给定的温度和压力下,不同物质之间是如何平衡
的。
4.化学平衡:研究在给定的温度和压力下,化学反应是如何平衡的。
5.热力学第三定律:绝对零度不能达到原理,即任何物质在绝对零
度下的熵均为零。
这些定律和原理对于理解多组分系统的热力学行为非常重要。
在化学工程、材料科学、生物工程等领域中,多组分系统热力学被广泛应用于研究复杂系统的热力学性质和行为。
第四章 多组分系统热力学 主要内容1.混合物和溶液(1)多组分系统的分类含一个以上组分的系统称为多组分系统。
多组分系统可以是均相(单相)的,也可以是非均相(多相)的。
将多组分均相系统区分为混合物和溶液,并以不同的方法加以研究:(Ⅰ)混合物:各组分均选用同样的标准态和方法处理;(Ⅱ)溶液:组分要区分为溶剂及溶质,对溶剂及溶质则选用不同的标准态和方法加以研究。
(2)混合物及溶液的分类混合物有气态混合物液态混合物和固态混合物;溶液亦有气态溶液液态溶液和固态溶液。
按溶液中溶质的导电性能来区分,溶液又分为电解质溶液和非电解质溶液(分子溶液)。
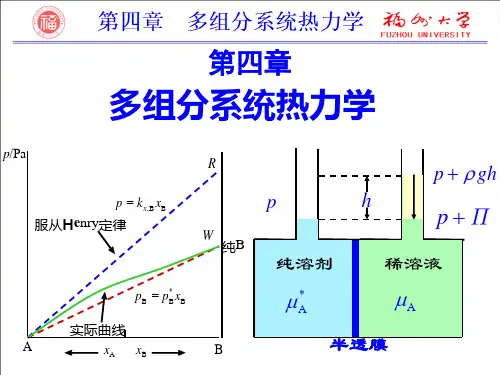
2.拉乌尔定律与亨利定律拉乌尔定律与亨利定律是稀溶液中两个重要的经验规律。
(1)拉乌尔定律平衡时,稀溶液中溶剂A 在气相中的蒸气分压A p 等于纯溶剂在同一温度下的饱和蒸气压与该溶液中溶剂的摩尔分数A x 的乘积。
这就是拉乌尔定律。
用数学式表达拉乌尔定律为 A *A Ax p p = (2)亨利定律一定温度下,微溶气体B 在溶剂A 中的溶解度B x 与该气体在气相中的分压B p 成正比。
也可表述为:一定温度下,稀溶液中挥发性溶质B 在平衡气相中的分压力B p 与该溶质B 在平衡液相中的摩尔分数B x 成正比。
这就是亨利定律。
用数学式表达亨利定律为: B B ,B x k p x =B ,x k 、B ,b k 为以不同组成标度表示的亨利系数,其单位分别为Pa ,Pa·kg·mol -1。
应用亨利定律时,要注意其不同表达式所对应的亨利系数及其单位。
还要注意亨利定律适用于稀溶液中的溶质分子同气相同种分子相平衡,即亨利定律适用于稀溶液中的溶质在液相及气相中具有相同分子形态的场合。
3.偏摩尔量(1)偏摩尔量的定义设X 代表V ,U ,H,S ,A ,G 这些广度性质,则对多组份系统(混合物或溶液)即 X =f (T ,p ,n A ,n B ,…)定义 ()B C C,,,B B def ≠⎪⎪⎭⎫ ⎝⎛∂∂n p T n X X式中,X B称为广度性质X (X=V ,U ,H ,S ,A ,G 等)的偏摩尔量,它们分别为只有系统的广延量才具有偏摩尔量,偏摩尔量是强度量。
5第五章多组分系统多组分系统:两种或两种以上的组分组成的系统,组成(组元):组成系统的化学物质——构成系统的化学物质总数组分,独立组成数(独立组元数)例,O2,CO,CO2气体混合,CO+O2->CO2三者平衡有一定数量关系,三者中仅有两组元为独立组分为二,组成为三多组分系统:包括溶液,混合气体,合金(溶体:多组元均匀系)溶液:液态溶体混合气体:气态溶体合金:金属固态溶体和金:非金属固态溶体广义溶液:多组分的均匀系(不仅是指液体,气体也可以)从纯物质热力学到多组分系统热力学的过渡是以偏摩尔量和化学势为基础的。
5-1内能与化学成分的关系1.内能的试验测定法假设,一均匀系,包含r种不同的化学组分,其中质量分别为:M1,M2,……Mr摩尔数分别为:n1,n2,……nr分子量分别为:μ1,μ2……μr有(以上参量关系式为)MI=μInI(I=1,2,……r)记Ni为可独立变动的摩尔数.以θ,P,n1,n2,…,nr为描写均匀系的平衡态的独立变量.其中,θ为任一温标所定的温度.容积V=V(θ,P,n1,n2,…,nr)任意地变动θ,P,n1,n2,…,nr,都可直接测得V由于内能U---不可直接测得.故应用等压过程P不变,有:Q=△H其中,H=H(θ,P,n1,n2,…,nr)其值可由实验测定∴由U=H-PV可求解内能U.上述焓的确定-----由实验法测得.∵H=H(ni)增加某一组元数量,即将一定数量的化学能物质加入到均匀系,以增加某组元的数量,然后用绝热法或等温法测量物质的吸热量.其中,绝热法指:物系与外界绝热,测量过程中的温度改变.等温法指:对物系供给热量,或取出热量,维持温度不变.以下分别详细介绍绝热法和等文法:1)绝热法:假定:第i组元,数量为n’摩尔加入均匀系,过程中为等压,无化学反应.∴H=cont.初温为θ,终温为θ’第I种化学纯物质的焓为H’.H’与n’成正比即H’=n’h’h’=h’(θ,p)初始的总焓,H(θ,p,n1,n2,…,nr)+H’终态的总焓,H(θ’,p,n1,n2,…,ni+n’,…,nr)∵总焓不变∴两者相等(其中两者指初始的总焓和终态的总焓).若,Cp以(已)在各种情况下求得,则H(θ’,p,n1,n2,..,ni+n’,…,nr)-H(θ,p,n1,…,ni+n’,…,nr)=Cp(,p,n1,n2,...,nin',...,nr)d.'H(θ,p,n1,…,ni+n’,…,nr)=H(θ’,p,n1,n2,…,ni+n’,…,nr)-'Cp(,p,n1,n2,...,nin',...,nr)d即H(θ,p,n1,n2,…,ni+n’,…,nr)=H(θ,p,n1,n2,…,nr)+H’-Cp(,p,n1,n2,...,nin',...,nr)d.'方程确定了H~ni的关系对全部r种组元作一连串实验,可确定H与化学成分的关系.2)等温法:θ保持不变,测量物质放出的热量Q.该热量相当于公式的Cp(,p,n1,n2,...,nin',...,nr)d'∴H(θ,p,n1,n2,…,ni+n’,…,nr)=H(θ,p,n1,n2,…,nr’)+H’-Q2.广延量与偏摩尔物质.广延量与总质量成正比设:有一均匀系,其θ,p不变,ni→ni(i=1,2,…,r)总质量M’=M.(ni’=ni,i=1,2,3,…,r)有:V’=VU’=U∴V’=V(θ,p,n1,n2,…,nr)=V(θ,p,n1,…,nr)U’=U(θ,p,n1,n2,…,nr)=U(θ,p,n1,…,nr)即V’,U’作为θ,p,ni’的函数,与V,U作为θ,p,ni的函数相同,此为广延量的数学性质.------一阶齐次函数.以下给出一阶齐次函数的数学定义:已知:f(某1,某2,…,某r)=m(某1,某2,…,某r)称f为某1,某2,…,某r的m阶齐次函数,举例来说,强度量为零阶齐次函数.若函数中包含广延量与强度量,应将强度量看作参数项.以下给出Euler定理的数学定义:假设:函数f对各变量某1,某2,…,某r有连续的偏微商,则,m阶齐次函数有:136i某if某imf.-----------------Euler定理.Euler定理应用:将此定理用到V,U,ni相当于某i,m=1(一次齐次函数).Vnivni1rU.p.niUni1r.p.Vni.p.vi------------组元i的偏摩尔容积Uni.p.ui------------组元i的偏摩尔内能其它偏摩尔变量:hi=riHni.p.,CPi=Cpnir.p.,CVi=Cvni.p.偏摩尔变量符合ripivHnhCi1pnCC1nCivi1化学成分,用各组元的某i表示.某i=rninn=ni某1i1---------r种摩尔百分比中,仅(r-1)种为独立(组分r-1,.组成r个)平均摩尔内能umUnVn其他平均摩尔能:vm5-2基本方程,hmHn1多组分的热力系函数确定简单可压缩封闭系的热力状态,需要独立热力参数2个,相应于一种做功形式和热量交换.例U=U(,v)定成分,定质量系统,U取决于,v,若有物质加入系统(开口系)U↗∴dU与加入物质dn有关,又与加入物质的种类有关.∴uu(,v,n1,n2,,nr)∴确定变成分,多组分系统的热力状态,需独立热力参数及组分变量(组分多少,浓度多少,——也是独立变量)137组元数量的表示:摩尔数u1,u2——nr,在含r个组分的均相系中,状态由r+2个参数确定。
练习1.以下说法对吗?为什么?(1)溶液的化学势等于溶液中各组分化学势之和。
(2)对于纯组分,化学势等于其吉布斯自由能。
(3)等温、等压下,纯物质的量越多,其化学势越大。
提示答案:〔(1) 不对,溶液无化学势,(2) 应等于摩尔吉布斯自由能,(3) 不对,化学势是强度量,与量无关。
)2.指出下列各量哪些是偏摩尔数量,哪些是化学势。
提示答案:〔(1)(3)(6)是偏摩尔量,(4)(5)(7)是化学势〕3.下列说法对吗?为什么?(1)温度、压力没有偏摩尔量。
(2)偏摩尔吉布斯自由能是化学势,因此,凡属化学势均有集合公式。
(3)体系无限稀释时,溶质B 的偏摩尔体积为零。
提示答案:〔(1) 对,因为温度、压力是强度性质,(2) 不对,集合公式只适合于偏摩尔量,(3) 不对,偏摩尔体积不为零。
〕4.某不法之徒想制造假酒以获取暴利。
他造假酒的过程是:往空瓶里分别注入按一定酒精含量计算出的乙醇和水,两者体积加和为500cm3,随后封口、混合均匀并贴上商标。
后来,当这些假酒被查封后,工商局的检验人员用最简单的科学方法证明这酒是假的。
请你用所学的知识说明工商人员所用的方法及其科学依据。
提示答案:(混合后,总体积不等于 500ml)5.25℃,101325Pa 时NaCl(B) 溶于1kg H2O(A) 中所成溶液的V与n B的关系如下:V=〔1001.38+16.6253(n B/mol)+1.7738(n B/mol)3/2+0.1194(n B/mol)2〕cm3(1)求H2O 和NaCl 的偏摩尔体积与n B的关系;(2)求n B=0.5mol 时H2O 和NaCl 的偏摩尔体积;(3)求无限稀释时H2O 和NaCl 的偏摩尔体积。
提示答案:6.化学势和有什么不同?若标准压力不是选择而是另一个压力值,则值是否不同?值又如何?提示答案:(与T、p有关,只与温度有关,p不同,不同,但不变。
)7.温度不同的两种理想气体在绝热恒容条件下混合,其过程熵变。