第三章 化学反应速率和化学平衡答案
- 格式:doc
- 大小:231.18 KB
- 文档页数:6

高中化学《化学反应速率与化学平衡》练习题(附答案解析)学校:___________姓名:___________班级:___________一、单选题1.对于在恒容密闭容器中进行的反应()()()()22C s +H O g CO g +H g ,下列说法错误的是 ( )A .其他条件不变,充入少量He ,则反应速率增大B .若()()2正逆v CO =v H O ,则反应达到平衡状态C .其他条件不变,增加C(s)的质量,反应速率不变D .若混合气体的质量不再改变,则反应达到平衡状态 2.下列反应中,熵减小的是( ) A .2HI (g)=H 2 (g)+I 2 (g)B .NH 4NO 3爆炸:2NH 4NO 3 (s)=2N 2 (g)+4H 2O (g)+O 2 (g)C .2O 3 (g)=3O 2 (g)D .4NH 3 (g)+5O 2 (g)=4NO (g)+6H 2O (1)3.aA(g)+bB(g)⇌cC(g)+dD(g) ΔH=Q ,同时符合两图中各曲线规律的是( )A .a+b>c+d T 1>T 2 Q>0B .a+b>c+d T 1>T 2 Q<0C .a+b>c+d T 1<T 2 Q<0D .a+b <c+d T 1<T 2 Q<04.某对于平衡体系xA(g)+yB(g)mC(g)+nD(g),其他条件不变增大压强,C 的百分含量减少,则下列关系中正确的是( ) A .x +m<n B .x +y<m +n C .m +n>xD .m +n<y +x5.已知某反应中各物质的浓度数据如下: ()()-1-1mA g +nB g qC g /mol L 3.6 2.4 2.42s /mol L 2.41.64.0⋅⋅()起始浓度末浓度则m:n:q等于()A.3:2:2 B.3:2:3 C.3:2:4 D.3:2:56.化学知识和技术发展离不开伟大化学家,下列人物与其贡献不匹配的是()A.侯德榜——工业制备烧碱B.勒夏特列——化学平衡的移动C.李比希——元素定量分析D.盖斯——反应热的计算7.现有下列两个图象:下列反应中符合上述图象的是()A.N2(g)+3H2(g)2NH3(g) ΔH<0B.2SO3(g)2SO2(g)+O2(g) ΔH>0C.4NH3(g)+5O2(g)4NO(g)+6H2O(g) ΔH<0D.H2S(g)H2(g)+S(s) ΔH>0,10min 8.将1mol X和3mol Y在2L的恒容密闭容器中混合,一定条件下发生反应X(s)3Y(g)2Z(g)时测得Y的物质的量为2.4mol,下列说法正确的是()A.10min内,X的平均反应速率为0.01mol/(L·min)B.第10min时,Z的浓度为0.4mol/LC.10min时,X的转化率为20%D.反应时,向容器中通入He,容器内压强增大,反应速率加快9.下列说法正确的是()A.活化分子间的碰撞一定能发生化学反应B.增大浓度时,化学反应速率加快,主要原因是反应物活化分子百分数增大,单位时间内有效碰撞次数增多C.△H<0的反应均是自发反应D.反应NH4HCO3(s)═NH3(g)+H2O(g)+CO2(g)△H=+185.57kJ•mol-1能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向10.下图是可逆反应X 2+3Y 22Z 在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述不正确的是( )A .t 1、t 2时,用不同物质表示正、逆反应速率有2v(X 2)=v(Z)B .t 2时,反应已达到了一定限度C .t 2~t 3,反应不再发生D .t 2~t 3,各物质的浓度不再发生变化 11.已知298K 时,2SO 2(g)+O 2(g)2SO 3(g);△H=-197kJ ·mol -1。

第三章 化学反应速率和化学平衡习题3-1 什么是反应的速率常数?它的大小与浓度、温度、催化剂等因素有什么关系? 答:反应的速率大都可以表示为与反应物浓度方次的乘积成正比:υ=k·c α(A)·c β(B),式中比例常数k 就是速率常数。
速率常数在数值上等于反应物浓度均为1 mol·L -1时的反应速率。
k 的大小与反应物浓度无关,改变温度或使用催化剂会使速率常数k 的数值发生变化。
习题 3-2 什么是活化能?答:Arrhenius 总结了大量实验事实,提出一个经验公式:速率常数k 的对数与1/T 有线形关系:C TRE k a +⋅-=1ln 式中E a 就是活化能,它表示活化分子具有的最低能量与反应分子平均能量之差。
习题3-3 什么是催化剂?其特点有哪些?答:某些物质可以改变化学反应的速率,它们就是催化剂。
催化剂参与反应,改变反应历程,降低反应活化能。
催化剂不改变反应体系的热力学状态,使用催化剂同样影响正、逆反应的速率。
不影响化学平衡,只能缩短达到平衡的时间。
习题3-4 NOCl 分解反应为2NOCl→2NO+Cl 2实验测得NOCl 的浓度与时间的关系如下:t/s0 10 20 30 40 50 c (NOCl )/mol·L -12.001.420.990.710.560.48求各时间段内反应的平均速率;用作图法求t =25s 时的瞬时速率。
解:t=0-10s 时,1042.100.2-=∆∆=t c υ= 0.058mol·L -1·s -1 t=10-20s 时,102099.042.1--=∆∆=t c υ= 0.043mol·L -1·s -1 t=20-30s 时,203071.099.0--=∆∆=t c υ= 0.028mol·L -1·s -1 t=30-40s 时,304056.071.0--=∆∆=t c υ= 0.015mol·L -1·s -1 t=40-50s 时,405048.056.0--=∆∆=t c υ= 0.008mol·L -1·s -1 作图法略。

化学反应速率及化学平衡试题及答案化学反应速率及化学平衡试题及答案化学反应速率和化学平衡测试题1.反应,在不同情况下测得反应速率,其中反应速率最快的是A.υ(D)=0.4 mol / ?L·s? B.υ(C)=0.5 mol / ?L·s?C.υ(B)=0.6 mol / ?L·s? D.υ(A)=0.15 mol / ?L·s?2.某化学反应其△H== —122 kJ/mol,?S== 231 J/(mol·K),则此反应在下列哪种情况下可自发进行A.在任何温度下都能自发进行 B.在任何温度下都不能自发进行C.仅在高温下自发进行 D.仅在低温下自发进行3.可逆反应N2+3H22NH3的正逆反应速率可用各反应物或生成物浓度的变化来表示。
下列关系中能说明反应已达到平衡状态的是A.υ正(N2)=υ逆(NH3) B.3υ正(N2)=υ正(H2) C.2υ正(H2)=3υ逆(NH3) D.υ正(N2)=3υ逆(H2)4.下列说法正确的是A.增大压强,活化分子百分数增大,化学反应速率一定增大B.升高温度,活化分子百分数增大,化学反应速率可能增大C.加入反应物,使活化分子百分数增大,化学反应速率增大D.一般使用催化剂可以降低反应的活化能,增大活化分子百分数,增大化学反应速率5.在2L密闭容器中加入4molA和6molB,发生以下反应:4A(g)+6B(g) 4C(g) +5D(g)。
若经5s后,剩下的A是2.5mol,则B的反应速率是A.0.45 mol / ?L·s?B.0.15 mol / ?L·s?C.0.225 mol / ?L·s? D.0.9 mol / ?L·s?6.有一处于平衡状态的反应:X(s)+3Y(g) 2Z(g),ΔH<0。
为了使平衡向生成Z的方向移动,应选择的条件是①高温②低温③高压④低压⑤加催化剂⑥分离出ZA.①③⑤ B.②③⑤ C.②③⑥ D.②④⑥7.同质量的锌与盐酸反应,欲使反应速率增大,选用的反应条件正确的组合是反应条件:①锌粒②锌片③锌粉④5%盐酸⑤10%盐酸⑥15%盐酸⑦加热⑧用冷水冷却⑨不断振荡⑩迅速混合后静置A.③⑥⑦⑨ B.③⑤⑦⑨C.①④⑧⑩8.某温度下,在固定容积的密闭容器中,可逆反应达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1。


第三章 化学反应速率总章目标:1:了解化学反应速度的概念及反应速度的实验测定 2:了解基元反应、复杂反应、反应级数、反应分子数的概念 3:掌握浓度、温度及催化剂对反应温度的影响4:了解速率方程的实验测定和阿累尼乌斯公式的有关计算 5:初步了解活化能的概念及其于反应速度的关系。
各小节目标:第一节:反应速率的定义1:掌握表示化学反应速率的两个概念。
2:学会用平均速率和瞬时速率来表示化学反应速率。
○1平均速率:2121c c r tt -=-- ○2瞬时速率:某一时刻的化学反应速率。
第二节:反应速率与反应浓度的关系○1掌握反应级数的概念,学会建立简单的速率方程。
○2掌握速率常数k 的概念及意义,可以由速率常数的单位来确定反应级数。
第三节:反应机理○1了解什么是基元反应。
○2学会从微观角度角度建立速率方程探讨反应机理。
第四节:反应物浓度与时间的关系○1熟练掌握零级、一级、二级、三级反应中反应物浓度与时间的关系。
○2学会计算零级、一级反应的半衰期,了解二级、三级反应的半衰期。
第五节:反应速率理论的简介了解解释基元反应速率方程的碰撞理论和解释阿仑尼乌斯方程的过渡态理论。
第六节:温度对化学反应速率的影响○1掌握阿仑尼乌斯公式的三种表达方式及计算○1aE RTk Ae-=○2ln ln Eak A RT =-+○3ln lg 2.303a E k A RT=-+,○2熟悉温度对化学反应速率的影响。
○3学会计算不同温度下的速率常数的关系212112lg ()2.303a E k T T k R TT -=。
第七节:催化剂与催化反应简介简单了解催化剂对化学反应速率的影响原理。
Ⅱ 习题一 选择题1.下列说法正确的是( )A.反应速率常数的大小即反应速率的大小B.反应级数和反应分子数是同义词C.反应级数越大,反应速率越大D.从反应的速率常数的单位可以推测该反应的反应级数2.关于催化剂的下列说法中,正确的是( )(《无机化学例题与习题》吉大版)A 不能改变反应的△G , △H, △S, △UB 不能改变反应的△G ,但能改变△H ,△S, △UC 不能改变反应的△G ,△H ,但能改变△S, △UD 不能改变反应的△G ,△H, △U ,但能改变△S3.对任意化学反应,其含义是( )A.表明它是二级反应B.表明它是双分子反应C.表明反应物与产物间的计量关系D.表明它是基元反应4.二级反应速度常数的量纲是( )(《无机化学例题与习题》吉大版)A. s -1B. mol ∙dm -3 C . mol ∙dm -3 ∙ s -1 D . mol -1∙dm 3∙ s -15.某化学反应进行1h ,反应完成50%,进行2h ,反应完成100%,则此反应是( )A.零级反应B.一级反应C.二级反应D.三级反应6.升高同等温度,反应速度增大幅度大的是( )(《无机化学例题与习题》吉大版)A.活化能小的反应B.双分子反应C. 多分子反应 D .活化能大的反应7.对于反应2D+E→2F,若反应机理为:(快)(快)(慢)则反应的速度方程为()A.v=kC D2C EB.v=kC D C EC.v=kC D3/2C E D .v=kC D1/2C E8.某一级反应的速率常数为9.5×10-2min-1,则此反应的半衰期为()(《无机化学例题与习题》吉大版)A.3.65 minB.7.29 minC.0.27 minD.0.55 min9.反应W产物的速度常数为8L2mol-2s-1,若浓度消耗一半时的速度为8L2mol-2s-1,则起始浓度为()A.8mol/LB.4mol/LC.16mol/L D .2mol/L10.温度升高导致反应速率明显增加的主要原因是()(《无机化学例题与习题》吉大版)A .分子碰撞几率增加 B.反应物压力增大C .活化分子数增加D .活化能降低11.有反应X+Y=Z。

第1页共24页2023年高考化学总复习:化学反应速率与化学
平衡
注意事项
1.全卷满分100分。
考试用时90分钟。
2.可能用到的相对原子质量:H 1C 12O 16N 14Zn 65。
一、选择题(本题共15小题,每小题3分,共45分)
1.关节炎首次发作一般在寒冷季节,原因是关节滑液中形成了尿酸钠晶体(NaUr ),易诱发关节疼痛,其化学机理是①HUr (aq )+H 2O (l
)Ur -(aq )+H 3O +(aq )、②Ur -(aq )+Na +(aq
)NaUr (s )ΔH 。
下列叙述不正
确的是()
A.降低温度,反应②平衡正向移动
B.反应②正向吸热
C.降低关节滑液中HUr 及Na +含量是治疗方法之一
D.关节保暖可以缓解疼痛,原理是平衡②逆向移动
2.已知当ΔH -T ·ΔS <0时化学反应能自发进行。
下列化学反应肯定能自发进行的是(
)A.N 2(g )+3H 2(g
)
2NH 3(g )B.2K (s )+2H 2O (l
)
2K +(aq )+2OH -(aq )+H 2↑C.2Mg (s )+O 2(g
)
2MgO (s )D.CaCO 3(s
)CaO (s )+CO 2(g )。

化学反应速率化学平衡问题讨论题型一:根据化学计量数之比,计算反应速率【例1】反应4NH 3(g)+5O 2(g) 4NO(g)+6H 2O(g)在10L 密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol ,则此反应的平均速率)(X v (反应物的消耗速率或产物的生成速率)可表示为( )A .)mol/(L 0.010)(NH 3s v ⋅=B .)mol/(L 0.001)(O 2s v ⋅=C .)mol/(L 0.001(NO)s v ⋅=D .)mol/(L 0.045O)(H 2s v ⋅=【点拨】 正确答案是C 。
【规律总结】遇到这一类题目,一定要充分利用化学反应中各物质的反应速率之比等于它们的化学计量数之比这一规律进行计算。
题型二:以图象形式给出条件,计算反应速率【例2】某温度时,在2L 容器中,X 、Y 、Z 三种物质的物质的量随时间变化的曲线如图所示。
由图中数据分析:该反应的化学方程式为_________________。
反应开始至2min ,用Z 表示的平均反应速率为____________。
【点拨】由图可知,X 、Y 的物质的量随反应的进行而减小,Z 的物质的量随反应的进行而增大,则X 和Y 为反应物,Z 为生成物。
∵mol 0.3mol 0.7mol 1.0(X)=-=∆nmol 10.mol 90.mol 1.0(Y )=-=∆nmol 20.mol 0mol 2.0(Z)=-=∆n∴反应方程式为:3X+Y =2Z 。
min)mol/(L 0.05min2L 2mol 0.2)(⋅=÷=Z v 题型三:根据已知的浓度、温度等条件,比较反应速率的大小【例3】把下列四种X 溶液分别加入四个盛有10mL 2mol/L 盐酸的烧杯中,均加水稀释到50mL,此时,X和盐酸缓慢地进行反应,其中反应最快的是()A.10℃20mL 3mol/L的X溶液B.20℃30mL 2mol/L的X溶液C.20℃10mL 4mol/L的X溶液D.10℃10mL 2mol/L的X溶液本题若没有看清楚题目实质,仅仅从选项的表面看X浓度的大小及反应温度的高低来判断反应速率的快慢,则会错选C。

化学反应速率化学反应速率就是化学反应进行的快慢程度(平均反应速率),用单位时间内反应物或生成物的物质的量来表示。
在容积不变的反应容器中,通常用单位时间内反应物浓度的减少或生成物浓度的增加来表示。
影响化学反应速率的外界条件因素内因:反应物的性质是决定反应速率的主要因素。
外界条件:温度、溶液浓度、气体压强、催化剂、固体的表面积、反应物状态、潮湿的空气、形成原电池。
1.浓度的影响:增加反应物的浓度可以加快化学反应速率;降低反应物的浓度,可以减慢化学反应速率。
2.温度的影响:升高温度,不论吸热反应还是放热反应,也不论是正反应速率还是逆反应速率都增大。
即升高体系的温度可以加快化学反应速率;降低体系的温度,可以减慢化学反应速率。
3.催化剂的影响:使用正催化剂可以加快化学反应速率;使用负催化剂,可以减慢化学反应速率。
4.压强的影响:(仅适用于有气体参加的反应)增加体系的压强,可以加快化学反应速率;降低体系的压强,可以减慢化学反应速率。
压强对反应速率的影响,是通过改变气体的浓度实现的。
有以下几种情况:①恒温时:压缩反应体系的体积导致引起压强增大,进而导致引起反应物浓度增大,从而引起反应速率加快。
②恒温时,对于恒容密闭容器:a. 充入气体反应物导致引起气体反应物浓度增大(压强也增大),从而引起反应速率加快。
b. 充入“惰性”气体导致引起气体总压强增大,但气体反应物的浓度没有改变,从而反应速率不变。
③恒温恒压时:充入“惰性”气体导致引起反应体系的体积增大,进而引起气体反应物浓度减小,从而引起反应速率减小。
5.其他因素的影响:光波、电磁波、超声波、溶剂等也能影响化学反应速率。
说明:(1)纯液体和固体浓度视为常数,它们的量的改变不会影响化学反应速率。
但颗粒的大小导致接触面积的大小发生变化,故影响反应速率。
(2)固体、液体物质,由于压强改变时对它们的体积影响很小,因而压强对它们浓度的影响可看作不变,压强对无气体参加的化学反应的速率无影响。
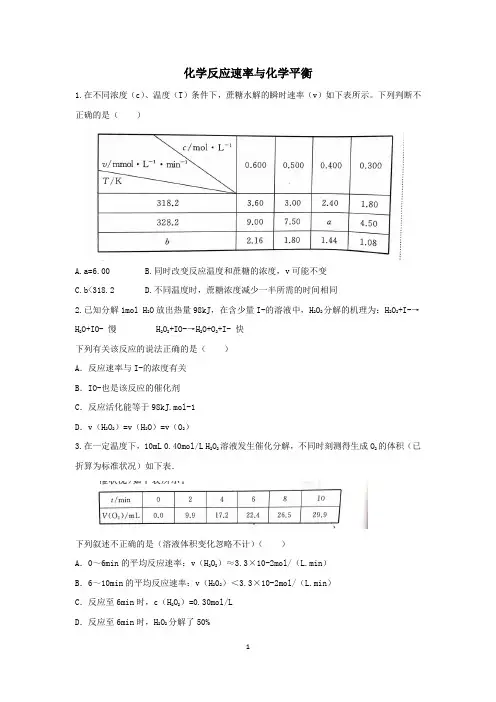
化学反应速率与化学平衡1.在不同浓度(c)、温度(T)条件下,蔗糖水解的瞬时速率(v)如下表所示。
下列判断不正确的是()A.a=6.00B.同时改变反应温度和蔗糖的浓度,v可能不变C.b<318.2D.不同温度时,蔗糖浓度减少一半所需的时间相同2.已知分解1mol H2O放出热量98kJ,在含少量I-的溶液中,H2O2分解的机理为:H2O2+I-→H2O+IO- 慢 H2O2+IO-→H2O+O2+I- 快下列有关该反应的说法正确的是()A.反应速率与I-的浓度有关B.IO-也是该反应的催化剂C.反应活化能等于98kJ.mol-1D.v(H2O2)=v(H2O)=v(O2)3.在一定温度下,10mL 0.40mol/L H2O2溶液发生催化分解,不同时刻测得生成O2的体积(已折算为标准状况)如下表.下列叙述不正确的是(溶液体积变化忽略不计)()A.0~6min的平均反应速率:v(H2O2)≈3.3×10-2mol/(L.min)B.6~10min的平均反应速率:v(H202)<3.3×10-2mol/(L.min)C.反应至6min时,c(H2O2)=0.30mol/LD.反应至6min时,H2O2分解了50%4.NaHSO4溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率。
将浓度均为0.020 mol·L-1 NaHSO3溶液(含少量淀粉)10.0 mL、KIO3(过量)酸性溶液40.0 mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如右图。
据图分析,下列判断不正确的是()A.40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反B.图中b、c两点对应的NaHSO3反应速率相等C.图中a点对应的NaHSO3反应速率为5.0 ×10-5mol·L-1·s-1D.温度高于40℃时,淀粉不宜用作该实验的指示剂5.在一密闭容器中充入1mol H2和 1 mol I2,压强为p(Pa),并在一定温度下使其发生反应,H 2(g)+ I2(g)2HI(g),下列说法正确的是()A. 保持容器容积不变,向其中加入1molH2,化学反应速率不变B. 保持容器容积不变,向其中加入1molAr,化学反应速率增大C. 保持容器内气体压强不变,向其中加入1molAr,化学反应速率不变D. 保持容器内气体压强不变,向其中加入1molH2(g)和1molI2(g),化学反应速率不变6.为了研究CaCO3与盐酸反应的反应速率,某同学测定反应中生成的CO2体积随反应时间的变化的情况如下图所示。

第3章 化学平衡和化学反应速率【3-1】写出下列反应的标准平衡常数表达式 (1) 2N 2O 5(g)+4NO 2(g)O 2(g)(2) SiCl 4(l)2H 2O(g)+SiO 2(s)+4HCl(3) CaCO 3(s)CaO(s)CO 2(g)+(4) ZnS(s)+2H +(aq)Zn 2+(aq)+H 2S(g)解:(1)222542(/)(/)(/)N O O NO p p p p Kp p θθθθ=(2)4242(/)(/)(/)H C l S iC l HOp p Kc c p p θθθθ=(3)2/C O Kp p θθ=(4)222(/)(/)(/)H SZ nHcc p p Kcc θθθθ++=【3-2】尿素22()C O N H (s )的△f G ⊙=-197.15kJ·mol -1,其他物质△f G ⊙的查附录二。
求下列反应在298K 时的K ⊙:23C O +2g )N H ((g )222 H O +C O (g )()N H (s )解:∆r G θ = -197.15 + (-228.6) – 2⨯(-16.5) – (-394.4) = 1.65 (kJ/mol)1.65⨯103 = -8.314⨯298lnK θ, K θ = 0.514【3-3】 673K 时,将0.025molCOCl 2(g)充入1.0L 容器中,当建立下列平衡时:COCl 2(g)CO(g)+Cl 2(g)有16% COCl 2解离。
求此时的K ⊙。
解:042.0p/RT )16.01(025.0)p /()RT 16.0025.0(K22=-⨯⨯=θθθ[p θ = 101.3 kPa, R = 8.314 J/(mol·K)]【3-4】 298K 时,向1.00L 烧瓶中充入足量的N 2O 4,使起始压力为100kPa ,一部分N 2O 4分解为NO 2,达平衡时总压力为116kPa ,计算如下反应的K ⊙:N 2O 4(g) 2NO 2(g)。
高考化学化学反应速率与化学平衡的综合复习含详细答案一、化学反应速率与化学平衡1.为了证明化学反应有一定的限度,进行了如下探究活动:步骤1:取8mL0.11mol L -⋅的KI 溶液于试管,滴加0.11mol L -⋅的FeCl 3溶液5~6滴,振荡; 请写出步骤1中发生的离子反应方程式:_________________ 步骤2:在上述试管中加入2mLCCl 4,充分振荡、静置;步骤3:取上述步骤2静置分层后的上层水溶液少量于试管,滴加0.11mol L -⋅的KSCN 溶液5~6滴,振荡,未见溶液呈血红色。
探究的目的是通过检验Fe 3+,来验证是否有Fe 3+残留,从而证明化学反应有一定的限度。
针对实验现象,同学们提出了下列两种猜想: 猜想一:KI 溶液过量,Fe 3+完全转化为Fe 2+,溶液无Fe 3+猜想二:Fe 3+大部分转化为Fe 2+,使生成Fe (SCN )3浓度极小,肉眼无法观察其颜色为了验证猜想,在查阅资料后,获得下列信息:信息一:乙醚比水轻且微溶于水,Fe (SCN )3在乙醚中的溶解度比在水中大。
信息二:Fe 3+可与46[()]Fe CN -反应生成蓝色沉淀,用K 4[Fe (CN )6]溶液检验Fe 3+的灵敏度比用KSCN 更高。
结合新信息,请你完成以下实验:各取少许步骤2静置分层后的上层水溶液于试管A 、B 中,请将相关的实验操作、预期现象和结论填入下表空白处:【答案】322222Fe I Fe I +-++=+ 若液体分层,上层液体呈血红色。
则“猜想一”不成立 在试管B 中滴加5-6滴K 4[Fe (CN )6]溶液,振荡【解析】 【分析】 【详解】(1) KI 溶液与FeCl 3溶液离子反应方程式322222FeI Fe I +-++=+;(2)①由信息信息一可得:取萃取后的上层清液滴加2-3滴K 4[Fe (CN )6]溶液,产生蓝色沉淀,由信息二可得:往探究活动III 溶液中加入乙醚,充分振荡,乙醚层呈血红色,实验操作预期现象结论若液体分层,上层液体呈血红色。
高一化学化学反应速率和化学平衡试题答案及解析1. T ℃时在2L 容积不变的密闭容器中使X(g)与Y(g)发生反应生成Z(g)。
反应过程中X 、Y 、Z 的 浓度变化如图1所示;若保持其他条件不变,温度分别为T 1和T 2时,Y 的体积百分含量与时间的关系如图2所示。
则下列结论错误的是A .容器中发生的反应可表示为:3X(g)+Y(g)2Z(g)B .反应进行前3min 内,用X 表示的反应速率v(X)=0.1mol/(L·min)C .若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂D .保持其他条件不变,升高温度,化学平衡向逆反应方向移动【答案】D【解析】 A .根据图示1可知:XY 是反应物,Z 是生成物,它们的物质的量的比等于3:2:1,由于最终各种物质都存在,所以该反应是可逆反应。
故容器中发生的反应可表示为:3X(g)+Y(g)2Z(g),正确;B .反应进行前3min 内,用X 表示的反应速率v(X)=(2.0—1.4)mol÷2L÷3min= 0.1mol/(L·min),正确;C .由图3可知:各种物质在2min 时就达到了平衡,但是物质的平衡浓度不变,所以平衡未发生移动。
因为该反应是反应前后气体体积不等的可逆反应,则改变的条件是使用催化剂,正确;D .根据图2可知:T 2>T 1.升高温度,Y 的平衡含量降低,即平衡向正反应方向移动。
根据平衡移动原理:升高温度化学平衡向吸热反应方向移动,所以正反应方向是吸热反应。
错误。
【考点】考查图像法在确定化学反应的速率、平衡移动、物质的转化率的应用的知识。
2. 据图回答下列问题:Ⅰ、(1)若烧杯中溶液为稀硫酸,则观察到的现象是______________________ 负极反应式为:_________________________________________________。
习题三(1)(2)一、选择题(将正确答案序号填在括号内)1.反应2SO 2(g)+O 2(g)=2SO 3(g)的反应速率可以表示为( )d.2.反应A+2B →C ,若 ,则 是多少? (单位为mol·1-1·s -1)( )a.2.6×10-2b.5.2×10-2c.1.3×10-2d.6.5×10-2 3.质量作用定律只适用于( )a.可逆反应b.不可逆反应c.基元反应d.复杂反应4.基元反应:A (g )+2B(g)=C(g)+D(g),A 和B 的初始分压分别为60.78kPa ,81.04kPa ,当Pc=20.2kPa 时,反应速率相对于初始速率是( )a.61b.241c.161d.4815.温度一定时,有A 和B 两种气体反应,设c(A)增加一倍,则反应速率增加了100%,c(B )增加一倍,反应速率增加了300%,该反应速率方程式为( )a.V=kc(A)c(B)b.V=kc 2(A)c(B)c.V=kc(A)c 2(B)d.以上都不是6.对于一个化学反应,下列哪种情况下速率越大( )a.越负θm r H ∆ b.越负θm r G ∆ c.越正θm r S ∆ d.活化能Ea 越小7.反应A+B →3D ,正、逆反应的活化能分别为mkJ.mol -1,nkJ.mol -1,则反应的()1-⋅∆mol kJ H 为( )a.m-nb.n-mc.m-3nd.3n-m8.在300K 时鲜牛奶大约4小时变酸,便在277K 时的冰箱中可保持48小时,则对于牛奶变酸的反应活化能(kJ·mol -1)是( )a.-74.66b.74.66c.5.75d.-5.75 9.改变速率常数k 的因素是( )a.减少生成物浓度b.增加体系总压力c.增加反应物浓度d.升温和加入催化剂 10.对于0>∆m r G 的反应,使用催化剂可以使( )a.V 正大大加速b.V 正减速c.无影响d.V 正、V 逆加速11.反应A(g)+B(g)→C(g)的反应速率常数k 的单位为( )a.s -1b.L ·mol -1·s -1()dtSO dc V a 22.=()dtO dc V c 2.=()dtSO dc V b 221.=()121106.2--⋅⨯=-mol dtA dc ()dtB dc -()dtB dc -c.L 2·mol -2·s -1d.不能确定12.在503K 时反应2HI (g )=H 2(g)+I 2(g)的活化能为184.1kJ·mol -1,当某种催化剂存在时,其活化能为104.6kJ·mol -1,加入催化剂后,该反应速率约增加倍数为( )a.1.1×103b.1.8×106c.1.8×108d.1.3×10513.生物化学工作者常将37℃时的速率常数与27℃时的速率常数之比称Q 10,若某反应 Q 10为2.5,则它的活化能(kJmol -1)为( )a.105b.54c.26d.7114.反应A(g)+B(g)=C(g)的速率方程是V=kc 2(A)C(B),若使密闭反应容器体积增大一倍,则反应速率为原来的( )倍。
1.了解化学反应速率的概念、化学反应速率的定量表示方法。
2.了解催化剂在生产、生活和科学研究领域中的重要作用。
3.了解化学反应的可逆性。
4.了解化学平衡建立的过程。
理解化学平衡常数的含义,能够利用化学平衡常数进行简单的计算。
5.理解外界条件(浓度、温度、压强、催化剂等)对反应速率和化学平衡的影响,认识其一般规律。
6.了解化学反应速率和化学平衡的调控在生活、生产和科学研究领域中的重要作用。
平衡理论作为一个相对独立的知识体系是高考中的必考考点,而化学平衡又是三大平衡体系(化学平衡、电离平衡、沉淀溶解平衡)之首,在高考中占有相当重要的地位。
这类题目难度较大,具有良好的区分度,选拔功能强。
知识点一、物质状态和浓度对反应速率的影响1.对于有固体参加的化学反应而言,由于在一定条件下,固体的浓度是固定的,所以固体物质在化学反应中浓度不改变,因此在表示化学反应速率时,不能用固体物质。
但因为固体物质的反应是在其表面进行的,故与其表面积有关,当固体颗粒变小时,会增大表面积,加快反应速率。
2.对于有气体参加的反应而言,改变压强,对化学反应速率产生影响的根本原因是引起浓度改变所致。
所以,在讨论压强对反应速率的影响时,应区分引起压强改变的原因,这种改变对反应体系的浓度产生何种影响,由此判断出对反应速率产生何种影响。
对于气体反应体系,有以下几种情况:(1)恒温时:高中化学复习《化学反应速率与化学平衡》知识点解析与练习题含答案增加压强体积缩小浓度增大反应速率加快。
(2)恒容时:①充入气体反应物浓度增大总压增大速率加快②充入“惰气”总压增大,但各分压不变,即各物质的浓度不变,反应速率不变。
(3)恒压时:充入:“惰气”体积增大各反应物浓度减少反应速率减慢。
知识点二、外界条件对化学反应速率的影响活化分子浓度影响因素分子总数活化分子百分数活化分子总数(单位体积活化分子数)增大浓度增加不变增加增加增大压强不变不变不变增加升高温度不变增加增加增加正催化剂不变增加增加增加知识点三、化学反应速率的图象图象也是一种表达事物的语言符号,化学反应速率图象是将化学反应速率变化的状况在直角坐标系中以图的形式表达的结果,是化学反应速率变化规律的反映。
第三章 化学反应速率和化学平衡习题3-1 什么是反应的速率常数?它的大小与浓度、温度、催化剂等因素有什么关系? 答:反应的速率大都可以表示为与反应物浓度方次的乘积成正比:υ=k·c α(A)·c β(B),式中比例常数k 就是速率常数。
速率常数在数值上等于反应物浓度均为1 mol·L -1时的反应速率。
k 的大小与反应物浓度无关,改变温度或使用催化剂会使速率常数k 的数值发生变化。
习题 3-2 什么是活化能?答:Arrhenius 总结了大量实验事实,提出一个经验公式:速率常数k 的对数与1/T 有线形关系:C TRE k a +⋅-=1ln 式中E a 就是活化能,它表示活化分子具有的最低能量与反应分子平均能量之差。
习题3-3 什么是催化剂?其特点有哪些?答:某些物质可以改变化学反应的速率,它们就是催化剂。
催化剂参与反应,改变反应历程,降低反应活化能。
催化剂不改变反应体系的热力学状态,使用催化剂同样影响正、逆反应的速率。
不影响化学平衡,只能缩短达到平衡的时间。
习题3-4 NOCl 分解反应为2NOCl→2NO+Cl 2实验测得NOCl 的浓度与时间的关系如下:t/s0 10 20 30 40 50 c (NOCl )/mol·L -12.001.420.990.710.560.48求各时间段内反应的平均速率;用作图法求t =25s 时的瞬时速率。
解:t=0-10s 时,1042.100.2-=∆∆=t c υ= 0.058mol·L -1·s -1 t=10-20s 时,102099.042.1--=∆∆=t c = 0.043mol·L -1·s -1t=20-30s 时,203071.099.0--=∆∆=t c υ= 0.028mol·L -1·s -1t=30-40s 时,304056.071.0--=∆∆=t c υ= 0.015mol·L -1·s -1t=40-50s 时,405048.056.0--=∆∆=t c = 0.008mol·L -1·s -1 作图法略。
习题3-5 660K 时反应2NO + O 2→2NO 2 ,NO 和O 2的初始浓度c (NO )和c (O 2)及反应的初始速率υ的实验数据:(2)求出反应的级数和速率常数;(3)求c (NO )= c (O 2)= 0.15mol·L -1时的反应速率。
解: (1) 设反应的速率方程为υ = k·c α(NO)·c β(O 2),将数据代入得: 0.030= k ⨯ 0.10 ⨯ 0.10 ①0.060 = k ⨯ 0.10 ⨯ 0.20 ② 0.240 = k ⨯ 0.20 ⨯ 0.20 ③②/① 得 β =1 ③/② 得 α =2∴ 反应的速率方程为υ= kc 2(NO)c (O 2)(2) 反应的级数为α+β =3 速率常数k = 30.0 (mol·L -1)-2·s -1 (3) υ = 0.101 mol·L -1·s -1习题3-6 某反应25℃时速率常数为1.3×10-3s -1,35℃时为3.6×10-3s -1。
根据van’t Hoff 规则,估算该反应55℃时的速率常数。
解: k (35℃)/k (25℃) = γ = 2.77 k (55℃)/k (35℃)= γ 2k (55℃)= γ 2⨯ k (35℃) =2.772⨯3.6⨯10-3 = 27.6⨯10-3s -1习题3-7 求反应C 2H 5Br→C 2H 4+HBr 在700K 时的速率常数。
已知该反应活化能为225 kJ·mol -1,650K 时k =2.0×10-3s -1。
解:设700K (T 2)时的速率常数为k 2, 650K (T 1)时的速率常数为k 1。
根据Arrhenius 公式⎪⎪⎭⎫ ⎝⎛-=1212a 12303.21g T T T T R E k k 122332109.3650700314.8303.2)650700(10225100.2lg ---⨯=⨯⨯⨯-⨯=⨯S k k习题3-8 反应C 2H 4+H 2→C 2H 6 在300K 时k 1 = 1.3×10-3mol·L -1·s -1,400K 时k 2 = 4.5×10-3 mol·L -1·s -1,求该反应的活化能E a 。
解:根据Arrhenius 公式1-a a 332112a 12mol kJ 4.12400300314.8303.2)300400(103.1105.4lg 303.2)(lg⋅=⨯⨯⨯-=⨯⨯⋅⋅-=--E E T T R T T E k k习题3-9 某反应活化能为180kJ·mol -1,800K 时反应速率常数为k 1,求k 2=2k 1时的反应温度。
解:2231112800314.8303.2)800(101802lg 2lg lg T T k k k k ⨯⨯-⨯=== k 2 = 2k 1时的反应温度T 2 = 821K习题3-10 写出下列反应的标准平衡常数表示式223422232N (g) +3H (g) = 2NH (g)CH (g) + 2O (g) = CO (g) + 2H O(l)CaCO (s) = CaO(s) + CO (g)解: (1)()()()3θ2θ2θ3θ/)H (/)N (/)NH (p p p p p p K ⋅=(2)()()()2θ2θ42θ2θ/)O (/)CH (/)CO (p p p p p p K⋅=(3)θ2θ/)CO (p p K =习题3-11 已知在某温度时(1)2CO 2(g) ᆖ2CO(g) + O 2(g) θ1K = A(2)SnO 2(s) +2CO(g) ᆖSn(s) + 2CO 2(g) θ2K= B,则同一温度下的反应(3)SnO 2(s) 〓 Sn(s) + O 2(g)的θ3K 应为多少?解: (3)=(1)+(2)θ3K =θ1K ·θ2K = AB习题3-12 在1273K 时反应:FeO (s )+ CO (g )ᆖFe (s )+ CO 2(g )的K θ = 0.5,若CO 和CO 2的初始分压分别为500 kPa 和100 kPa ,问:(1)反应物CO 及产物CO 2的平衡分压为多少?(2)平衡时CO 的转化率是多少?(3)若增加FeO 的量,对平衡有没有影响?解 : (1) FeO(s) + CO(g) ᆖFe(s) + CO 2(g)起始时刻p/Pa 500 100平衡时刻p/Pa 500-x 100+x5.0500100)CO ()CO (θθ2θ=-+==xx p p p p K x = 100kPaCO 的平衡分压为400 kPa , CO 2的平衡分压为200 kPa . (2) 平衡时CO 的转化率α =%100500)400500(⨯- = 20%(3) 增加FeO 的量,对平衡有没有影响。
习题3-13 在585K 和总压为100 kPa 时,有56.4%NOCl (g )按下式分解:2NOCl (g )〓 2NO (g )+ Cl 2(g )若未分解时NOCl 的量为1mol 。
计算(1)平衡时各组分的物质的量;(2)各组分的平衡分压;(3)该温度时的K θ。
解:(1) 2NOCl (g )ᆖNO (g )+Cl 2(g )未分解时各组分的物质的量n/mol 1 0 0 平衡时各组分的物质的量n/mol 0.436 0.546 0.28222kPa)Cl (44kPa 1001.2820.564)NO (34kPa 1001.2820.436)NOCl ()2(2==⨯==⨯=p p p()()()()()()368.0100/34100/22100/44)NOCl ()Cl ()NO ()3(22θθ22θθ==⋅=p p p p p p K习题3-14 反应Hb·O 2(aq )+CO (g )ᆖHb·CO (aq )+O 2(g )在298K 时θK = 210,设空气中O 2的分压为21kPa ,计算使血液中10%红血球(Hb·O 2)变为Hb·CO 所需CO 的分压。
解: Hb·O 2(aq )+ CO (g )ᆖHb·CO (aq )+ O 2(g )()[][]()[][]()[][]()[][][]()210CO 910211/CO)(/O Hb 9.0/)O (/O Hb 1.0/CO)(/O Hb /)O (/CO Hb 3θθ2θ2θ2θθ2θ2θθ=⨯⨯=⋅⋅⋅⋅=⋅⋅⋅⋅=p p p c c p p c c p p c c p p c c K∴ 使血液中10%红血球(Hb·O 2)变为Hb·CO 所需CO 的分压p (CO) = 11.11 kPa习题3-15 计算反应CO+3H 2ᆖCH 4+H 2O 在298K 和500K 时的K θ值(注意:298K 和500K 时水的聚集状态不同,利用θm f H ∆,θm S 计算)。
解: 298K 时 CO (g ) + 3H 2 (g) ᆖ CH 4(g) + H 2O(l)θmf H ∆/ kJ·mol -1-110.53 0 -74.81 -285.84 θmS / J·K -1·mol -1 197.56 130.57 186.15 69.94 θmr H ∆ = -250.12 kJ·mol -1 θmr S ∆ = -133.18 J·K -1·mol -1 θmr G ∆ = θm r H ∆θm r S T ∆-= -150.83 kJ·mol -1θmr G ∆ = -RT ln K θ= -8.314⨯298ln K θ K θ (298K)= 2.75 ⨯ 1026500K 时 CO (g ) + 3H 2 (g) ᆖ CH 4 (g) + H 2O (g)θm f H ∆/ kJ·mol -1 -110.53 0 -74.81 -241.82θm S / J·K -1·mol -1 197.56 130.57 186.15 188.72θm r H ∆ = -206.1 kJ·mol -1θm r S ∆ =-214.4 J·K -1·mol -1θm r G ∆ = θmr H ∆θm r S T ∆-= -98.9 kJ·mol -1θm r G ∆= -RT ln K θ= -8.314⨯500ln K θK θ (500K) = 2.15 ⨯ 1010习题3-16 反应H 2(g )+I 2(g )ᆖ2HI (g )在713K 时K θ = 49,若698K 时的K θ = 54.3(1)上述反应θm r H ∆为多少?(698~713K 温度范围内),上述反应是吸热反应,还是放热反应?(2)计算713K 时反应的θm r G ∆。