金属及其化合物的转化关系图
- 格式:doc
- 大小:18.00 KB
- 文档页数:1



元素化合物及其价类二维图引子:元素化合物的知识给人的感觉就是“繁、乱、杂、难”,我们认为以物质的类别为横坐标,以某元素的化合价为纵坐标,在二维平面内,绘制含有某元素的物质的转化图像,既能体现“元素观”也能体现“分类观”和转化观,进而实现对元素化合物知识的系统化,有助于建立系统的知识体系,明确学习要点,形成化学基本观念。
思路点拨分析物质的通性分析氧化性和还原性元素的最高价态只有氧化性,元素的中间价态既有氧化性又有还原性,元素的最低价态只有还原性。
分析离子反应离子反应发生的条件包括生成沉淀、弱电解质或气体的复分解反应,也包括因氧化还原反应的导致的离子反应,还包括相互促进的彻底水解、沉淀的转化、络合反应等。
一、钠元素及其化合物1.价类二维图2.核心物质的性质3.重要化学方程式的书写0101钠和氧气在加热条件下的反应(化) 2Na +O 2=====△Na 2O 20102钠和氯气在加热条件下的反应(化) 2Na+Cl 2=====△2NaCl0103过氧化钠和水反应(化)2Na2O2+2H2O===4NaOH+O2↑0104过氧化钠和二氧化碳反应(化)2Na2O2+2CO2===2Na2CO3+O20105钠和水反应(离)2Na+2H2O===2Na++2OH-+H2↑0106氢氧化钠与过量二氧化碳反应(离)OH-+CO2===HCO3-0107钠和乙醇反应(化)2CH3CH2OH+2Na→2CH3CH2ONa+H2↑0108过量钠与氯化铝溶液反应,先后可能发生的三个反应(化)2Na+2H2O===2NaOH+H2↑AlCl3+3NaOH===Al(OH)3↓+3NaCl Al(OH)3+NaOH===Na[Al(OH)4]二、氯元素及其化合物1.价类二维图2.核心物质的性质3.重要化学方程式的书写0201向氯化亚铁溶液中滴加氯水(化) 2FeCl 2+Cl 2=2FeCl 30202铁在氯气中燃烧(化)2Fe+3Cl 22FeCl 30203氯气的尾气吸收(离) Cl 2+2OH -===ClO -+Cl -+H 2O 0204漂白粉的制备(化)2Ca(OH)2+2Cl 2===CaCl 2+Ca(ClO)2+2H 2O 0205漂白粉的失效(2 化)Ca(ClO)2+CO 2+H 2O===CaCO 3↓+2HClO 2HClO2HCl+O 2↑0206氯气的实验室制备(离)4H ++2Cl -+MnO 2=====△Mn 2++Cl 2↑+2H 2O0207将等物质的量的二氧化硫和氯气通入水中(离) SO 2+Cl 2+2H 2O===SO 2-4+2Cl -+4H +0208工业上盐酸的制备(化)Cl2+H22HCl0209氯离子检验(证明存在)过程中一定会发生的离子方程式(离)Cl-+Ag+===AgCl↓三、铁元素及其化合物1.价类二维图2.核心物质的性质3.重要化学方程式的书写0301铁在高温条件下与水蒸气反应(化)3Fe+4H 2O Fe 3O 4+H 2↑0302铁与硫化合(化) Fe+S =====△FeS0303铁与非氧化性强酸反应(离) Fe+2H +=== Fe 2++H 2↑0304铁和硫酸铜溶液反应(离) Fe+ Cu 2+=== Fe 2++ Cu0305铁和氯化铁溶液反应(离) Fe +2Fe 3+===3Fe 2+0306向氯化亚铁溶液中通入氯气(离) 2Fe 2++Cl 2===2Fe 3++2Cl -0307向硝酸亚铁溶液中滴加稀硫酸(离) 3Fe 2++NO 3-+4H +===3Fe 3++NO ↑+2H 2O0308向硫酸亚铁溶液(酸性)中滴加过氧化氢溶液(离)2Fe2++H2O2+2H+===2Fe3++2H2O0309向硫酸铁溶液中通入二氧化硫气体(离)2Fe2++SO2+2H2O===2Fe3++SO42-+4H+0310氢氧化亚铁露置在空气中(化)4Fe(OH)2+O2+2H2O===4Fe(OH)3四、碳元素及其化合物1.价类二维图2.核心物质的性质3.重要化学方程式的书写0401碳和浓硫酸在加热条件下反应(化)C+2H2SO4(浓)CO2↑+2SO2↑+2H2O0402碳和水在高温条件下反应(化)C+H2O CO+H20403向次氯酸钠溶液中通入过量二氧化碳(离)ClO-+CO2+ H2O=HCO3-+HClO0404实验室制备二氧化碳(离)CaCO3 + 2H+ = Ca2++CO2↑+ H2O0405可溶性碳酸盐与强酸反应(离)CO32- + 2H+=CO2↑+ H2O0406碳酸氢钠溶液与氢氧化钠溶液反应(离)HCO3-+OH-=CO32- + H2O0407向碳酸氢钠溶液中滴加盐酸(离)HCO3-+H+=CO2↑+ H2O0408向可溶性碳酸盐溶液中加入氯化钡溶液(离)CO32- +Ba2+=BaCO3↓0409向氢氧化钡溶液中通入少量二氧化碳气体(离)Ba2++2OH-+CO2 =BaCO3↓+H2O0410加热碳酸氢钠固体(化)2NaHCO3Na2CO3+CO2↑+ H2O五、氮元素及其化合物1.价类二维图2.核心物质的性质3.重要化学方程式的书写 0501工业制氨气(化)N 2+3H 22NH 30502实验室制氨气(化)2NH 4Cl +Ca(OH)2=====△CaCl 2+2NH 3↑+2H 2O 0503铜与稀硝酸反应(离)3Cu +2NO -3+8H +===3Cu 2++2NO ↑+4H 2O 0504碳与浓硝酸的反应(化)C +4HNO 3(浓) =====△CO 2↑+4NO 2↑+2H 2O 0505氨的催化氧化(化) 4NH 3+5O 2=====催化剂△4NO +6H 2O 0506氯化铝溶液与氨水的反应(离)Al 3++3NH 3·H 20=A1(OH)3↓+3NH 4+0507氯化铵和氢氧化钠溶液在加热条件下反应(离) NH 4++OH -=====△NH 3↑+H 20 0508碳酸铵的受热分解(化)(NH 4)2CO 3=====△2NH 3↑+CO 2↑+H 20六、硫元素及其化合物 1.价类二维图2.核心物质的性质3.重要化学方程式的书写 0601铜与硫的化合(化) 2Cu+S =====△Cu 2S0602硫与浓硫酸的反应(化) S+2H 2SO 4(浓)=====△3SO 2↑+2H 2O 0603硫化氢和二氧化硫的反应(化) 2H 2S +SO 2===3S ↓+2H 2O 0604二氧化硫尾气的吸收(化) 2NaOH+SO 2=Na 2SO 3+H 2O0605二氧化硫的催化氧化(工业制备硫酸)(化) 2SO 2↑+O 2=====催化剂△2SO 3 0606将二氧化硫通入到溴水中(化) SO 2+Br 2+2H 2O===H 2SO 4+2HBr 0607浓硫酸和碳反应(化)C +2H 2SO 4(浓)=====△CO 2↑+2SO 2↑+2H 2O 0608浓硫酸和铜反应(化)Cu +2H 2SO 4(浓)=====△CuSO 4+SO 2↑+2H 2O七、镁元素及其化合物 1.价类二维图2.核心物质的性质3.重要化学方程式的书写0701镁与空气中燃烧时可能发生的反应(3 化)2Mg+ O22MgO 3Mg+N2Mg3N22Mg+ CO22MgO+C 0702工业上镁的炼制(化)MgCl2Mg+Cl2↑0703氢氧化镁与盐酸反应(离)Mg(OH)2+2H+===Mg2++2H2O0704氯碱工业(化)2NaCl+2H2O2NaOH+Cl2↑+H2↑0705向溴化钠溶液中滴加氯水(离)2Br-+Cl2===2Cl-+Br20706向碘化钾溶液中滴加溴水(离)2I-+Br2===2Br-+I2八、硅元素及其化合物1.价类二维图2.核心物质的性质3.重要化学方程式的书写0801硅与氧气在加热条件下的反应(化) Si+O 2=====△SiO 20802不能用带玻璃塞的试剂瓶保存碱性溶液的原因(化) SiO 2+2NaOH===Na 2SiO 3+H 2O 0803玻璃刻蚀过程中发生的反应(化) SiO 2+4HF===SiF 4↑+2H 2O 0804工业上硅的制备(化)SiO 2+2C Si+2CO0805玻璃制备过程发生的反应(2 化)Na 2CO 3+SiO 2Na 2SiO 3+CO 2↑ CaCO 3+SiO 2CaSiO 3+CO 2↑0806能证明碳酸酸性比硅酸酸性强的反应(化) Na 2CO 3+CO 2+H 2O===H 2SiO 3↓+Na 2CO 3 0807硅酸的受热分解(化) H 2SiO 3=====△SiO 2+H 2O 九、铝元素及其化合物 1.价类二维图2.核心物质的性质3.重要化学方程式的书写0901铝与氢氧化钠溶液反应(离)2Al+2OH-+2H2O===2AlO-2+3H2↑0902铝与四氧化三铁在高温条件下的反应(化)8Al+3Fe3O44Al2O3+9Fe0903氧化铝与氢氧化钠溶液反应(离)Al 2O 3+2OH -===2AlO -2+H 2O 或Al 2O 3+2OH -+3H 2O===2[Al(OH)4]- 0904实验室中氢氧化铝的制备(离) Al 3++3NH 3·H 2O===Al(OH)3↓+3NH +40905氯化铝溶液与过量氢氧化钠溶液反应(离) Al 3++4OH -===[Al(OH)4]-0906向四羟基合铝酸钠溶液中通入过量二氧化碳气体(离) [Al(OH)4]-+CO 2===Al(OH)3↓+HCO 3- 0907氢氧化铝的受热分解(化) 2Al(OH)3=====△Al 2O 3+3H 2O 0908工业上铝的冶炼(化)2Al 2O 34Al+3O 2↑十、铜元素及其化合物 1.价类二维图2.核心物质的性质3.重要化学方程式的书写 1001铜与浓硫酸的反应(化)Cu +2H 2SO 4(浓)=====△CuSO 4+SO 2↑+2H 2O 1002铜与稀硝酸的反应(化)3Cu +8HNO 3===3Cu(NO 3)2+2NO ↑+4H 2O 1003氧化铜溶于盐酸中(离) CuO+2H +===Cu 2++H 2O1004铜与氯化铁溶液反应(离) Cu+2Fe 3+===Cu 2++2Fe 2+1005氧化铜高温条件下分解(化)4CuO2Cu 2O+O 2↑1006气体中少量水的检验过程中发生反应(化) CuSO 4+5H 2O ===CuSO 4?5H 2O1007铜在潮湿空气中被腐蚀生成铜绿(化) 2Cu+O 2+CO 2+H 2O ===Cu 2(OH)2CO 3。
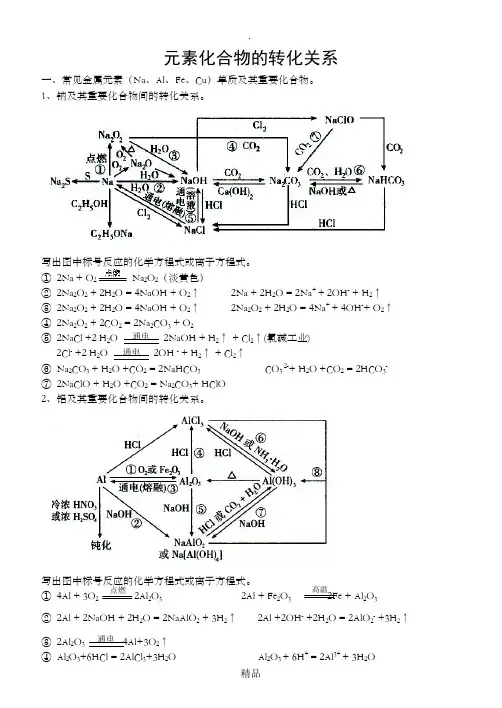
元素化合物的转化关系一、常见金属元素(Na 、Al 、Fe 、Cu )单质及其重要化合物。
1、钠及其重要化合物间的转化关系。
写出图中标号反应的化学方程式或离子方程式。
① 2Na + O 2 Na 2O 2(淡黄色)② 2Na 2O 2 + 2H 2O = 4NaOH + O 2↑ 2Na + 2H 2O = 2Na + + 2OH - + H 2↑ ③ 2Na 2O 2 + 2H 2O = 4NaOH + O 2↑ 2Na 2O 2 + 2H 2O = 4Na + + 4OH -+ O 2↑ ④ 2Na 2O 2 + 2CO 2 = 2Na 2CO 3 + O 2⑤ 2NaCl +2 H 2O 2NaOH + H 2↑ + Cl 2↑(氯碱工业)2Cl - +2 H 2O 2OH - + H 2↑ + Cl 2↑⑥ Na 2CO 3 + H 2O +CO 2 = 2NaHCO 3 CO 3 2-+ H 2O +CO 2 = 2HCO 3- ⑦ 2NaClO + H 2O +CO 2 = Na 2CO 3+ HClO2、铝及其重要化合物间的转化关系。
写出图中标号反应的化学方程式或离子方程式。
① 4Al + 3O 2 2Al 2O 3 2Al + Fe 2O 3 2Fe + Al 2O 3 ② 2Al + 2NaOH + 2H 2O = 2NaAlO 2 + 3H 2↑ 2Al +2OH - +2H 2O = 2AlO 2- +3H 2↑③ 2Al 2O 3 4Al+3O 2↑④ Al 2O 3+6HCl = 2AlCl 3+3H 2O Al 2O 3 + 6H + = 2Al 3+ + 3H 2O通电 通电 通电 点燃 高温⑤ Al 2O 3 + 2NaOH = 2NaAlO 2 +H 2O Al 2O 3 + 2OH - = 2AlO 2- + H 2O ⑥ AlCl 3 +3NH 3·H 2O = Al(OH)3↓+ 3NH 4Cl Al 3+ + 3 NH 3·H 2O = Al(OH)3↓+ 3NH 4+ AlCl 3 +3Na OH = Al(OH)3↓+ 3NaCl Al 3+ + 3OH - = Al(OH)3↓ ⑦ Al(OH)3 + NaOH =NaAlO 2 +2 H 2O Al(OH)3 + OH - = AlO 2- +2H 2O ⑧ Al 3+ +3 AlO 2- +6H 2O = 4Al(OH)3↓3、铁及其重要化合物间的转化关系。
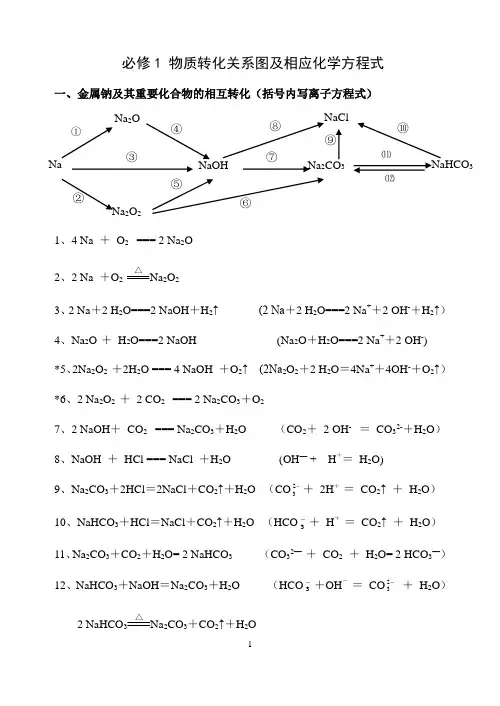
必修1 物质转化关系图及相应化学方程式一、金属钠及其重要化合物的相互转化(括号内写离子方程式)1、4 Na + O 2 === 2 Na 2O2、2 Na +O 2△Na 2O 23、2 Na +2 H 2O===2 NaOH +H 2↑ (2 Na +2 H 2O===2 Na ++2 OH -+H 2↑)4、Na 2O + H 2O===2 NaOH (Na 2O +H 2O===2 Na ++2 OH -) *5、2Na 2O 2 +2H 2O === 4 NaOH +O 2↑ (2Na 2O 2+2 H 2O =4Na ++4OH -+O 2↑) *6、2 Na 2O 2 + 2 CO 2 === 2 Na 2CO 3+O 27、2 NaOH + CO 2 === Na 2CO 3+H 2O (CO 2+ 2 OH - = CO 32-+H 2O ) 8、NaOH + HCl === NaCl +H 2O (OH — + H += H 2O)9、Na 2CO 3+2HCl =2NaCl +CO 2↑+H 2O (CO -23+ 2H + = CO 2↑ + H 2O )10、NaHCO 3+HCl =NaCl +CO 2↑+H 2O (HCO -3+ H + = CO 2↑ + H 2O )11、Na 2CO 3+CO 2+H 2O= 2 NaHCO 3 (CO 32— + CO 2 + H 2O= 2 HCO 3—)12、NaHCO 3+NaOH =Na 2CO 3+H 2O (HCO -3+OH - = CO -23 + H 2O )2 NaHCO 3△Na 2CO 3+CO 2↑+H 2ONa 2O Na ①NaCl NaHCO 3Na 23Na 2O 2 ② ③ ④ ⑤ ⑥⑦ ⑧ ⑨⑩ ⑾ ⑿二、非金属氯及其化合物的相互转化(括号内写离子方程式)1、H 2 + Cl 2点燃2HCl 2、2Na + Cl 2 点燃2NaCl3、Cu + Cl 2 点燃CuCl 24、2Fe + 3Cl 2点燃2FeCl 35、HCl +AgNO 3 = AgCl↓+HNO 3 (Cl -+Ag +=Ag Cl↓)6、NaCl +AgNO 3 = AgCl↓+NaNO 3 (Cl -+Ag +=AgCl↓)7、CuCl 2+2AgNO 3 = 2AgCl↓+Cu(NO 3)2 (Cl -+Ag +=AgCl↓)8、FeCl 3+3AgNO 3 = 3AgCl↓+Fe(NO 3)3 (Cl -+Ag +=AgCl↓)9、Cl 2 + 2NaOH = NaCl + NaClO + H 2O (Cl 2 + 2OH - = Cl - + ClO - + H 2O) 10、2Cl 2 + 2Ca(OH)2 = CaCl 2+ Ca(ClO)2 +2 H 2O(Cl 2 + 2OH - = Cl - + ClO - + H 2O)11、Cl 2 + H 2O = HCl + HClO (Cl 2 + H 2O = H ++Cl -+ HClO) 12、NaClO +HCl = NaCl + HClO (ClO - +H += HClO)2NaClO+H 2O+CO 2= Na 2CO 3+ 2HClO (2ClO -+H 2O+CO 2= CO 32-+ 2HClO) 13、Ca(ClO) 2+2HCl = CaCl 2 + 2HClO (ClO - +H += HClO)Ca(ClO)2+H 2O+CO 2=CaCO 3↓+2HClO (Ca 2++2ClO -+H 2O+CO 2=CaCO+ 2HClO)14、2HClO 2HCl+O 2↑NaCl 23AgCl⑤ ⑥ ⑦ ⑧光照三、金属铝及其重要化合物的相互转化(括号内写离子方程式)1.4Al +3O 2点燃2Al 2O 3 2.2 Al (OH )3△Al 2O 3 +3H 2O3.2Al +6HCl==2AlCl 3+3H 2↑ ( 2Al +6H +==2 Al 3++3H 2↑) 4.2Al +2NaOH +2H 2O==2NaAlO 2+3H 2↑ (2 Al +2OH -+2H 2O =2AlO 2-+3 H 2↑)5.Al 2O 3+6HCl =2AlCl 3+3H 2O ( Al 2O 3+6H +=2Al 3++3H 2O ) 6. Al 2O 3+2NaOH =2Na AlO 2+H 2O (Al 2O 3+2OH -=2 AlO 2-+H 2O )7、Al (OH )3+3HCl =AlCl 3+3H 2O ( Al (OH )3+3H + = Al 3++3H 2O )8、Al (OH )3+NaOH =NaAlO 2+2H 2O ( Al (OH )3+OH - = AlO 2-+2H 2O )9、实验制取Al (OH )3: AlCl 3+3NH 3·H 2O = Al (OH )3↓+3NH 4Cl (Al 3++3 NH 3·H 2O = Al (OH )3 ↓+ 3NH 4+ )AlAl (OH )3NaAlO 2Al 2O 3AlCl 3①②③④ ⑤ ⑥⑦ ⑧四、金属铁及其化合物的相互转化(括号内写离子方程式)1、3Fe +2O2 点燃Fe3O42、Fe+2HCl=FeCl2+H2↑(Fe+2H+=Fe2++H2↑)Fe+CuCl2=FeCl2+Cu (Fe+Cu2+=Fe2++Cu)3、FeO+2HCl=FeCl2+H2O(FeO+2H+=Fe2++H2O)4、Fe2O3+6HCl=2 FeCl3+3H2O (Fe2O3+6H+=2Fe2++3H2O)5、FeCl2+2NaOH =Fe(OH)2↓+2NaCl (Fe2++2OH-=Fe(OH) 2)↓6、Fe(OH)2 + 2HCl=FeCl2+2H2O(Fe(OH)2+2H+=Fe2++2H2O)7、FeCl3+3NaOH =Fe(OH)3↓+3NaCl ( Fe3++3OH-=Fe(OH) 3↓)8、Fe(OH) 3+3HCl=FeCl3+3H2O (Fe(OH) 3+3H+=Fe3++3H2O)9、2FeCl2+Cl2=2FeCl3 (2Fe2++Cl2=2 Fe3++2Cl—)10、属于化合反应的:Fe+2FeCl3 =3FeCl2(Fe +2 Fe3+=3 Fe2+) 印刷腐蚀电路板:Cu+2FeCl3 =CuCl2+2FeCl2 (Cu+2 Fe3+=Cu2++2 Fe2+)11、2 Fe(OH)3△Fe2O3+3H2O12、白色沉淀,然后迅速变为灰绿色,最后变为红褐色4 Fe(OH)2+ O2 + 2 H2O ═ 4 Fe(OH) 3①Fe3O4②23⑾⑿。




金属及其化合物之间的相互转化(尽量写出下列转化的化学方程式或离子方程式) (1)钠及其化合物(2)镁、铝及其化合物(3)铁、铜、银及其化合物Na Na 2S NaOH Na 2CO 3 NaHCO 3 CO 2 H 2O ①△②OH -CO 2 Ca(OH)2 H 2O SNa 2O 2 H 2O O 2点燃 CO 2C 2H 5ONa NaCl C 2H 5OH 电解水溶液HCl △ Mg MgOMgCO 3 Mg(OH)2 MgCl 2MgSO 4 H 2SO 4 H 2SO 4 H 2SO 4 电解 沸水HClNaOH Ca(OH)2H 2O 煅烧 ①O 2点燃 ②CO 2点燃 Cl 2 Fe FeO H 2SO 4 Cl 2 FeFeCl 2 FeS FeSO 4 Fe 2O 3 FeCl 3Fe(SCN)3 Fe(OH)3 Fe(OH)2 Fe 3O 4 H 2SO 4 H 2SO 4H 2SO 4 HCl NaOH HCl NaOH C O 2 Al H 2O C O 2 AlCO O 2 O 2 H 2O△S △ KSCN Al Al 2O 3 NaAlO 2AlCl 3 Al(OH)3 ①O 2点燃②Fe 2O 3高温电解 NaOH NaOHNaOH NaOH 、NH 3·H 2O HCl HCl HClHCl 、CO 2 △H 2SO 4 △ NaOHFeFe HNO 3Cu H 2SO 4△HNO 3 CuO Cu(OH)2Cu 2OCu(NO 3)2CuSO 4Cu 2S CuSH 2S浓H 2SO 4S 点燃O 2 △CO △ HNO 3 高温 RCHO 水浴加热 AgOHNa 2SS △FeAgAgNO 3Ag 2SAg(NH 3)2OHRCHO 水浴加热Ag 2CO 3AgI AgBr AgClH 2SHNO 3 HNO 3 NH 3·H 2O NH 3·H 2OHCl硅及其化合物之间的相互转化关系氯气及其化合物相互转化关系Cl2PCl 3、PClO 2②点燃NaClAgClNaOH光照3硫及其化合物相互转化关系H3Na SO 4223H 22SO 4O ,燃烧2NaOHO 2BaCl 2H 2O2氮及其化合物相互转化关系NH 4N NO 3243N 23·H 2ONH 4+ OH +H 2,催化剂高温 高压O 2 , 放电2O 2浓H 2SO 4△①浓酸,Cu ②见光或△③C点燃2O。

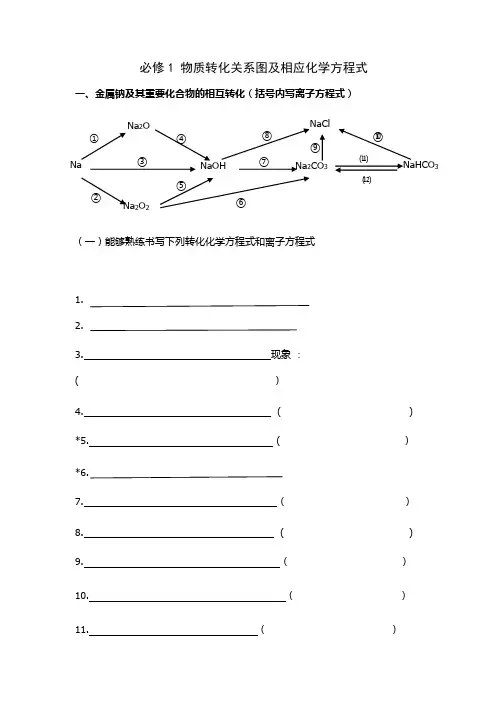
必修1 物质转化关系图及相应化学方程式一、金属钠及其重要化合物的相互转化(括号内写离子方程式)(一)能够熟练书写下列转化化学方程式和离子方程式1. 2.3. 现象 : ( )4. ( ) *5. ( ) *6.7. ( ) 8. ( ) 9. ( ) 10. ( ) 11. ( )Na 2O Na ①NaCl NaHCO 3Na 2CO 3NaOH Na 2O 2②③④⑤⑥⑦⑧ ⑨ ⑩⑾⑿[NaHCO 3固体](二) 熟记下列物质的颜色状态Na: Na 2O: Na 2O 2: NaHCO 3: Na 2CO 3:(三) 熟记下列信息溶解度: NaHCO 3 Na 2CO 3溶液碱性强弱: NaHCO 3 Na 2CO 3 俗名: NaHCO 3: Na 2CO 3: Na 的保存: Na 2O 2的用途:二、金属铝及其重要化合物的相互转化(括号内写离子方程式)1. 2.3. ( )AlAl (OH )3NaAlO 2Al 2O 3AlCl 3 ①② ③ ④ ⑤ ⑥ ⑦ ⑧5. ( ) 6. ( ) 7. ( ) 8. ( ) 9.实验制取Al (OH )3:( ) 10.Al 2O 3的用途:三、金属铁及其化合物的相互转化(括号内写离子方程式)1.2. ( )3. ( )4. ( )5. ( )①Fe 3O 4②23⑿7. ( )8. ( )9. ( )10.属于化合反应的 ( )印刷腐蚀电路板的 ( )11.12.白色沉淀,然后迅速变为灰绿色,最后变为红褐色13.离子颜色:Fe2+ Fe3+四、非金属氯及其化合物的相互转化(括号内写离子方程式)1.2.3.4. NaCl23AgCl⑤⑥⑦⑧6. ( )7. ( )8. ()9. ()10. ()11. ()12. ()13. ()()14.五、非金属硫及其化合物转化关系1.2.3.9.10111213182021六、氮及其化合物相互转化。
第3课时 利用“价态二维图〞认识铁及其化合物的关系(提升课时)铁及其化合物的关系1.铁及其化合物的“价—类〞二维图:2.铁及其化合物之间的主要转化关系:3.从物质分类的角度理解铁及其化合物的性质(1)Fe 2O 3、FeO 都是碱性氧化物,能与酸反响生成盐和水。
Fe 2O 3+6H +===2Fe 3++3H 2O ;FeO +2H +===H 2O +Fe 2+。
(2)FeSO 4和FeCl 3都属于盐类,能和碱反响生成Fe(OH)2及Fe(OH)3。
Fe 2++2OH -===Fe(OH)2↓;Fe 3++3OH -===Fe(OH)3↓。
(3)Fe(OH)2和Fe(OH)3均属于碱,能与酸反响生成盐和水。
Fe(OH)2+2H +===Fe 2++2H 2O ;Fe(OH)3+3H +===Fe 3++3H 2O 。
4.从化合价的角度理解铁及其化合物的氧化性和复原性:(1)Fe 单质中铁元素化合价为0价,仅具有复原性Fe +Cu 2+===Fe 2++CuFe +2H +===H 2↑+Fe 2+2Fe +3Cl 2=====△ 2FeCl 33Fe +4H 2O(g)=====高温 Fe 3O 4+4H 2(2)Fe 2O 3 中的铁元素为高价态,具有氧化性,因而可用复原剂将其复原为铁单质。
例:3CO +Fe 2O 3=====高温 2Fe +3CO 2。
(3)Fe 2+化合价可以升高到+3价,表现为复原性,也可以降低到0价,表现为氧化性。
(4)Fe 3+是铁元素的高价态,可以被复原剂复原为+2或0价,具有氧化性。
(5)Fe(OH)2具有复原性,能被氧化为Fe(OH)3:4Fe(OH)2+O 2+2H 2O===4Fe(OH)3。
【典例】如图为铁及其化合物的“价-类〞二维图。
(1)填写二维图缺失的类别①______________和化学式②____________。
(2)某同学利用以下试剂研究FeCl3性质,进行了如下预测:①Cl2②Fe ③NaOH ④H2SO4⑤AgNO3从物质类别上看,FeCl3属于________,可能与_______发生反响(填序号);从化合价角度看,Fe3+具有________性,可能与_________发生反响(填序号)。