身边的化学物质
- 格式:ppt
- 大小:1.23 MB
- 文档页数:64

主题三身边的化学物质知识点一空气1.空气的成分按体积分数计算,大约是氮气占78%、氧气占21%、稀有气体占0.94、二氧化碳占0.03,其他气体和杂质占0.03。
因此空气是混合物。
2.通过实验测定了空气组成的科学家是( ) A.门捷列夫,B.达尔文,C.拉瓦锡3.空气中氧气含量的测定(见图1-3-1):实验步骤如下:先用弹簧夹夹住乳胶管,再点燃红磷,伸入瓶中,并塞上瓶塞,打开弹簧夹(1)红磷燃烧时可观察到的主要现象是冒白烟,产生黄色火焰,待红磷熄灭并冷却后,打开弹簧夹,可观察到的现象是水倒吸入集气瓶,约占瓶内空气体积的1/5,说明空气中的氧气被消耗了,约占空气体积的1/5。
图1-3-1(2)实验完毕后,发现某同学所做实验的广口瓶中水面上升明显小于瓶内空气体积的1/5,产生问题的原因可能是红磷量不足、没等冷却就打开了弹簧夹。
某同学所做实验的广口瓶中水面上升明显大于瓶内空气体积的1/5,产生问题的原因可能是红磷点着后没有迅速伸入集气瓶中、点燃红磷前没有夹好弹簧夹。
(3)通过该实验可推出氮气的性质有氮气不燃烧,不支持燃烧,不与水反应,难溶于水。
(4)此实验中能否用铁、铝代替红磷?不能,原因:铁、铝不能在空气中燃烧。
此实验中能否用碳、硫代替红磷?不能,原因:碳、硫燃烧后会生成新的气体。
(5)此实验中,瓶底预先放水的作用是吸收热量和白烟。
(6)此实验中选用红磷做可燃物的原因是红磷能在空气中燃烧;红磷燃烧后的产物是固态;红磷不能与氮气反应。
4.氧气的物理性质:通常情况下,氧气是一种无色无味的气体,在标准状况下,氧气的密度比空气大,不易溶于水。
5.氧气的化学性质:(1)氧气是一种化学性质比较活泼的气体。
(2)氧气具有助燃性,能支持燃烧。
6.氧气用途:供给呼吸:医疗急救、登山、潜水等助燃性:物质燃烧时作助燃剂、气割、气焊等。
7.二氧化碳的物理性质:通常状况下,二氧化碳是无色无味的气体,密度比空气大,能溶于水。
降温条件下,会变为固体,称作“干冰”。

身边的化学物质复习课【学习目标】1.通过复习二氧化碳、氧气的性质、用途和实验室制法,掌握一般气体的实验室制法和常见气体的性质、用途。
2.通过复习有关“水”的一系列知识,引导学生认识以发展的眼光看待与水相关的知识以及水的用途。
3.通过复习,我们要关注生活中的化学、关注身边的化学物质并主动探究,学会保护我们的环境,并用所学的知识解决生产、生活中的问题。
【重难点】1、氧气的物理性质和化学性质。
2、二氧化碳的化学性质和水的组成。
3、氧气和二氧化碳的实验室制取。
4、水资源的保护和利用。
【教学过程】一、自主学习1、在通常情况下,氧气是一种、的气体,在0℃,1.01×105Pa下,密度为g.L-1,液态氧为色,固态氧为的状固体,溶于水。
2、在通常情况下,二氧化碳是一种、的气体,固态的二氧化碳常被称为,常用于、、。
3、氧气的检验方法:4、二氧化碳的检验方法:二、合作探究(一)O2和CO21、O2和CO2的性质和用途O2CO2物理性质化学性质用途功与过讨论:1、铝、铁是“同门”两兄弟,为何“自我保护能力”却截然不同呢?到底谁惹的祸呢?2、空气中的二氧化碳能不能更少,能不能更多?2、O2和CO2的实验室制取O2CO2原料反应原理仪器装置收集方法(二)水1.水的电解实验。
如右图所示,通直流电后,电极上出现气泡,一段时间后停止通电,试管1和试管2中所收集到的气体的体积比约为。
试管1中的气体能使带火星的木条,说明是;试管2中的气体能够,火焰呈色,说明是;该实验说明水是由元素组成。
写出该反应的文字表达式式。
2.水的净化(1)蒸馏:获取较纯净水的最好方法(2)过滤①过滤操作中有哪些注意事项?一贴:二低:三靠:。
②玻璃棒的作用是。
③过滤后的滤液仍浑浊的原因有哪些?(3)自来水的生产过程:3.借助水完成实验检查装置气密性。
如何检查装置的气密性?4.鉴别硬水和软水是。
5.水的保护和利用:水质污染的原因,:。
如何防止水污染:。


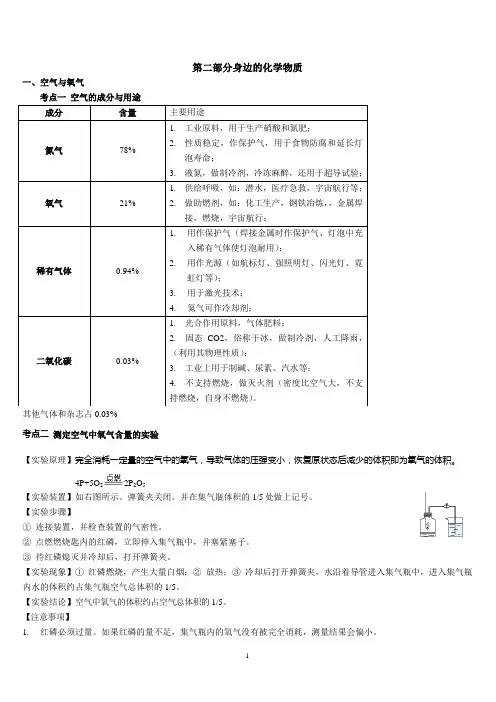
第二部分身边的化学物质一、空气与氧气考点一 空气的成分与用途其他气体和杂志占0.03%考点二 测定空气中氧气含量的实验【实验原理】完全消耗一定量的空气中的氧气,导致气体的压强变小,恢复原状态后减少的体积即为氧气的体积。
4P+5O 22P 2O 5【实验装置】如右图所示。
弹簧夹关闭。
并在集气瓶体积的1/5处做上记号。
【实验步骤】① 连接装置,并检查装置的气密性。
② 点燃燃烧匙内的红磷,立即伸入集气瓶中,并塞紧塞子。
③ 待红磷熄灭并冷却后,打开弹簧夹。
【实验现象】① 红磷燃烧,产生大量白烟;② 放热;③ 冷却后打开弹簧夹,水沿着导管进入集气瓶中,进入集气瓶内水的体积约占集气瓶空气总体积的1/5。
【实验结论】空气中氧气的体积约占空气总体积的1/5。
【注意事项】1. 红磷必须过量。
如果红磷的量不足,集气瓶内的氧气没有被完全消耗,测量结果会偏小。
2.装置气密性要好。
如果装置的气密性不好,集气瓶外的空气进入集气瓶,测量结果会偏小。
3.导管中要注满水。
否则当红磷燃烧并冷却后,进入的水会有一部分残留在试管中,导致测量结果偏小。
4.冷却后再打开弹簧夹,否则测量结果偏小。
5.如果弹簧夹未夹紧,或者塞塞子的动作太慢,测量结果会偏大。
考点三空气污染和防治1.空气污染的污染物是有害气体和烟尘。
污染源包括煤、石油等化石燃料燃烧产生的二氧化硫、二氧化氮、一氧化碳(三大有害气体),还包括工业废气等方面。
2.计入空气污染指数的项目为:二氧化硫、一氧化碳、二氧化氮、可吸入颗粒物和臭氧等。
3.空气污染的危害:造成世界三大环境问题(温室效应、臭氧层破坏、酸雨)、损害人体健康、破坏生态平衡、影响作物生长、破坏生态平衡等。
4.防治空气污染:加强大气质量监测;改善环境状况;减少使用化石燃料;使用清洁能源;积极植树、造林、种草;禁止露天焚烧垃圾等。
考点四氧气的性质1.物理性质氧气通常是无色、无味的气体,密度比空气大,不易溶于水,液态、固态时呈淡蓝色。

身边的化学物质(第1课时)一、知识梳理1.通常状况下,氧气是一种无气无味的气体,密度比空气密度略大,因而可用向收集,_______溶于水,因此,也可用排水法法收集2.铁在氧气中燃烧的现象是反应方程式为.做该实验时要在细铁丝末端系上一根火柴梗的目的是.氧气瓶底铺少量的纱子或加少量水的目的是.3.镁条在空气中燃烧的最能说明发生了化学变化的现象是, 反应方程式为.4.红磷在空气中燃烧的反应方程式为是该反应产生大量的而不是雾。
.5.硫在空气中燃烧产生的火焰是色,在氧气中燃烧燃烧产生的火焰是色6.分别写出氢气、一氧化碳、甲烷在氧气中燃烧的反应方程式这三种物质都是无色气体,鉴别它们可以根据它们的不同。
7.氧气的化学性质比较活泼,许多物质会与氧气发生反应,物质与氧气发生的缓慢的氧化反应叫缓慢氧化, 如生活中的。
8.举出氧气的两个重要用途9.工业上制取O2是用的分离液态空气法,其原理是根据氧气和氮气的不同.该过程属于____________变化。
10.写出用高锰酸钾和过氧化氢制氧气的反应方程式____________________________ _________________________________11.现有下图所示的实验装置,请回答问题:(1)在加入药品之前应对实验装置进行。
(2)若选用A装置制备气体时应考滤的因素是。
(3)可用于实验室用高锰酸钾制备和收集O2的一套装置是(填字母,下同)。
⑷写出实验室用过氧化氢溶液和二氧化锰制取氧气的发生装置是,并据此选择上图中组装一套制取于燥氧气的装置,收集氧气时,验满的方法是。
⑸写出实验室用用金属锌和稀硫酸制取氢气的化学方程式__________________________.制备和收集较纯净的氢气的一套装置是(填字母)。
二、牛刀小试1.(1)要证实“氢气的密度比空气小”,这属于氢气的_____(填“物理”或“化学”)性质,请设计一种简单的实验方案,简述该方案的操作方法和有关的现象________________________ 。

通常情况下,氧气是一种无色无味的气体,密度稍大于空气,氧气不易溶于水。
液态氧气呈淡蓝色液体,固态氧气呈淡蓝色雪花状固体。
2.氧气的化学性质:比较活泼的气体,能与许多物质发生化学反应。
例如:⑴木炭在氧气中的燃烧:化学方程式:C+O2点燃CO2实验现象:剧烈燃烧,发白光,放大量热,生成使澄清石灰水变浑浊的气体。
⑵蜡烛的燃烧:文字表达式:石蜡+氧气点燃→二氧化碳+水;实验现象:剧烈燃烧,发白光,瓶内壁有水雾出现,生成使澄清石灰水变浑浊的气体。
⑶铁丝在氧气中燃烧:化学方程式:3Fe+2O2点燃Fe3O4实验现象:剧烈燃烧,火星四射..固体。
....,放出大量热,生成黑色※铁丝在氧气中燃烧实验的注意事项:(如图甲)①铁丝绕成螺旋状的目的是增大铁丝与氧气的接触面积及受热面积;②铁丝一端系根火柴的目的是引燃(预热);③等火柴即将燃尽时,再放入集气瓶内,防止:火柴燃烧消耗过多氧气;④集气瓶内放少量水或铺一层细沙的目的是:防止灼热的生成物溅落瓶底,使集气瓶炸裂。
⑷硫在氧气中燃烧:(如图乙)化学方程式:S+O2点燃SO2实验现象:剧烈燃烧,产生明亮的蓝紫色火焰,放大量热,生成有刺激性气味的气体。
注意点:该实验集气瓶内装少量水或氢氧化钠溶液,用于吸收生成的二氧化硫气体,减少大气污染。
3.氧化反应:⑴定义:物质与氧气的反应都是氧化反应。
⑵种类:①剧烈氧化反应,如:物质的燃烧。
②缓慢氧化反应,如:金属生锈,食物腐败,新陈代谢,有机肥的腐熟等。
4.氧气的用途:⑴供给呼吸;如:宇航、潜水、登山、急救等。
⑵支持燃烧;(即助燃性)如:富氧炼钢、氧炔焰焊接金属、火箭助燃剂等。
自然界中氧气的获得途径:绿色植物的光合作用;●工业上制氧气:根据氮气和氧气的沸点不同,分离液态空气法制取氧气;(物理变化)●实验室制取氧气的方法:一、加热高锰酸钾制氧气1.药品:高锰酸钾(化学式:KMnO4,紫黑色晶体颗粒。
)2.反应原理:文字表达式:高锰酸钾加热→锰酸钾+二氧化锰+氧气;化学方程式:2KMnO4△K2MnO4+MnO2+O2↑3.实验装置仪器名称:①铁架台,②试管,③酒精灯,④集气瓶,⑤水槽。

化学就在我们身边,今天给大家整理了50例生活中的化学现象及解释。
一起看看吧,涨知识啦~1.在山区常见粗脖子病〔甲状腺肿大〕,呆小病〔克汀病〕,医生建议多吃海带,进行食物疗法。
上述病患者的病因是人体缺一种元素:碘。
2.用来制取包装香烟、糖果的金属箔〔金属纸〕的金属是:铝。
3.黄金的熔点是1064.4℃,比它熔点高的金属很多。
其中比黄金熔点高约3倍,通常用来制白炽灯泡灯丝的金属是:钨。
4.有位妇女将6.10克的一个旧金戒指给金银匠加工成一对耳环。
她怕工匠偷金或掺假,一直守在旁边不离开。
她见工匠将戒指加热、捶打,并放人一种液体中,这样屡次加工,一对美丽的耳环加工完毕了。
事隔数日,将这对耳环用天平称量,只有5.20克。
那么工匠偷金时所用的液体是:王水。
5.黑白相片上的黑色物质是:银。
6.很多化学元素在人们生命活动中起着重要作用,缺少它们,人将会生病。
例如儿童常患的软骨病是由于缺少:钙元素。
7.在石英管中充入某种气体制成的灯,通电时能发出比萤光灯强亿万倍的强光,因此有“人造小太阳〞之称。
这种灯中充入的气体是:氙气。
8.在紧闭门窗的房间里生火取暖或使用热水器洗澡,常产生一种无色、无味并易与人体血红蛋白〔Hb〕结合而引起中毒的气体是:CO。
9.地球大气圈的被破坏,则形成臭氧层空洞,致使作为人们抵御太阳紫外线损害的臭氧层受到损坏,引起皮肤癌等疾病的发生,并破坏了自然界的生态平衡。
造成臭氧层空洞的主要原因是:冷冻机里氟里昂泄漏。
10.医用消毒酒精的浓度是:75%。
11.医院输液常用的生理盐水,所含氯化钠与血液中含氯化钠的浓度大体上相等。
生理盐水中NaCl的质量分数是:0.9%。
12.发令枪中的“X纸〞〔火子〕打清脆,产生的白烟是:五氧化二磷。
13.萘卫生球放在衣柜里变小,这是因为:萘在室温下缓慢升华。
14.人被蚊子叮咬后皮肤发痒或红肿,简单的处理方法是:擦稀氨水或碳酸氢钠溶液。
15.因为某气体A在大气层中过量累积,使地球红外辐射不能透过大气,从而造成大气温度升高,产生了“温室效应〞。



精心整理《第二章身旁的化学物质 》知识重点一、氧气(一)、氧气的物理性质1、色、味、态:往常状况下,是无色无味的气体;2、密度:标准状况下,密度为 1.429g/L ,略大于空气 。
(可用向上排空气法)3、溶解性:氧气 不易溶于 水。
(可用排水法采集),4、三态变化:降温后,氧气能够变为淡蓝色的液体,甚至淡蓝色雪花状固体。
(二)、氧气的化学性质(1)与非金属的反响 1、木炭(黑色)与氧气反响实验现象 :在空气中焚烧发出红光;在氧气中:①强烈焚烧,发出白光②放出热量③ 产生使澄清石灰水变污浊的气体文字表达式 :碳 +氧气 点燃二氧化碳点燃CO 2符号表达式 : C+O 2 2、硫(淡黄色)与氧气反响实验现象 :在空气中发出轻微的淡蓝色火焰; 在氧气中①强烈焚烧, 发出光亮的蓝紫色火焰②放出热量③产生有刺激性气味的气体(瓶底放水汲取,防备污染空气)点燃文字表达式 :硫 +氧气 二氧化硫点燃符号表达式 : S+O 2 SO 2 3、磷与氧气反响实验现象: 磷在氧气中焚烧比在空气中焚烧更旺,放出热量,产生大批的白烟点燃文字表达式 :磷 +氧气 五氧化二磷点燃符号表达式 : P+O 2 P 2O 54、蜡烛与氧气反响实验现象 :在空气中焚烧产生黄色火焰,放热,稍有黑烟。
在氧气中强烈焚烧,发出白光,集气瓶内壁出现水珠,有使澄清石灰水变污浊的无色无味气体产生。
(2)与金属反响1、铁丝(银白色) [铁粉:黑色 ]与氧气反响实验现象 :在空气中不可以焚烧;在氧气中①强烈焚烧,火星四射②放出热量③生成黑色固体( Fe 3O 4)注意:集气瓶里要早先装少许水或细沙, 防备高温熔融物溅落瓶底,使其炸裂 。
点燃文字表达式 :铁 +氧气 四氧化三铁点燃符号表达式 : Fe+O 2 Fe 3O 4注意:(1)细铁丝绕成 螺旋状 且在尾端系上火柴梗: 集中热量,提升局部温度 ,有益于铁丝连续焚烧(2)火柴梗的作用: 引燃2、镁带(银白色)在空气中焚烧实验现象 :强烈焚烧,发出刺眼的白光,放出热量,生成白色粉末状固体。
第9讲身边的化学物质--空气、氧气、碳和二氧化碳经典精讲重难点突破题一:关于空气中氧气含量的测定:Ⅰ.某化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,改进了教材中的实验,设计出了如图1所示的实验装置。
实验步骤如下:①如图1所示,连接仪器,检查装置的气密性良好。
②在集气瓶里装进适量a 体积的水,燃烧匙里放一块白磷,在酒精灯上把玻璃棒下端加热后,立刻将集气瓶上的三孔胶塞塞紧。
③迅速将预热过的玻璃棒按下与白磷接触,观察到白磷燃烧,产生大量白烟。
④待白磷燃烧完毕,将集气瓶稍加振荡,白烟消失。
⑤待集气瓶完全冷却至室温,打开止水夹,量出集气瓶中水的体积为b,整个集气瓶的体积为c。
⑥根据a、b、c三个数据,计算出空气中氧气的体积分数。
根据以上实验信息,回答下列有关问题:(1)为了充分消耗容器中的氧气,药品中白磷的用量应保证_____________。
(2)若实验非常成功,请写出a、b、c三个数据应满足的一个等量关系式____________________。
(3)小组成员小张对“实验前向集气瓶内装入适量a体积的水”不理解。
咨询组长小明后,他终于明白加入水的作用,其一是_______________;其二是___________________。
Ⅱ.该小组的同学们通过查阅资料得知,四硫化钠(Na2S4)固体可替代白磷测定空气中氧气的体积分数,反应原理为:2Na2S4+O2+2H2O=8S↓+ 4NaOH。
【实验过程】①将足量的四硫化钠固体和水放入试管中,迅速塞紧橡胶塞,充分振荡,测量液面至橡胶塞下沿的距离,记录数据h1(如图2所示)。
②将该试管插入水中(如图3所示),在水中取下橡胶塞,观察到____________,塞紧橡胶塞。
将试管取出,倒过来,测量液面至橡胶塞下沿的距离,记录数据h2,理论上h1:h2 = _________。
【实验结论】根据第1次实验数据,计算空气中氧气的体积分数为_______%(结果精确到0.1%)。
身边的化学物质讲学稿一、地球周围的空气1、空气的成分空气是由多种气体组成的物,空气中主要含有的气体为和,另外还有等气体。
可燃物之所以能在空气中燃烧,就是因为空气中有的存在,温室效应是由于空气中含量的增多而导致的。
2、O2的化学性质①O2可以和很多种物质发生化学反应。
如C、S、P、Fe、Al、CO、H2、CH4、C2H5OH等物质的燃烧都是由于它们和O2反应的结果,记住它们与氧气反应的现象,请写出其中三种物质燃烧的化学方程式。
结论:象上述反应,都是物质与氧发生的化学反应称为反应,在上面几个反应中,O2都是剂,具有性。
②由于许多物质可以在空气中燃烧,显现不同的现象:在军事上可以利用的燃烧来制照明弹,利用的燃烧来制烟幕弹,做铝与氧气反应时,要在集气瓶瓶底放点水或者沙子,目的是,在氧气中燃烧会生成有刺激性气味的气体,测空气中氧气的含量时,是用在空气中燃烧实现的,点燃前需要验纯的是,最清洁的燃料是,天然气的主要成分是,是可再生的能源,将它加入汽油中,可减少汽车尾气对空气的污染。
③如何检验CO、H2、CH4三种气体?二、水的组成、净化和保护1、回忆电解水的实验,填写下面空格(1)电解水的化学方程式:(2)实验现象:①②(3)实验结论:①②2、按照单一操作过滤、静置沉淀、吸附沉淀、蒸馏四种净化水的效果由低到高的顺序为3、含有较多的钙镁化合物的水叫水,含有较少或者不含钙镁化合物的水叫水,我们可以用来区别它们,现象是。
生活中常用的方法降低水的硬度,实验室常用的方法获取水以降低水的硬度。
三、碳和碳的化合物1、碳元素组成的单质有许多种,如、和就是碳的单质。
不同的碳单质具有不同的物理性质,所以有不同的用途:金刚石由于,所以可以用来切割玻璃;石墨由于,所以可以用在干电池中作为电极,活性炭由于具有性,所以可用于防毒面具中吸附毒气。
金刚石和石墨物理性质的不同,是由于两者导致的。
2、碳单质的化学性质①在常温下,碳的化学性质;②在点燃或者高温条件下,碳具有性和性,请分别用化学方程式表示碳的化学性质:、。
身边de 化学物质一、性质活泼de 氧气1.氧气在自然界de 循环产生:植物de 光合作用消耗:动植物de 呼吸作用,燃料de 燃烧,缓慢氧化作用2.氧气de 性质(1)物理性质通常情况下,氧气是一种无色无味de 气体。
当温度下降,氧气可以转变为淡蓝色de 液氧,甚至淡蓝色de 固态氧。
在通常情况下,氧气不易溶于水,所以氧气能够用排水法收集;在标准状态下,氧气de 密度略大于空气,所以氧气可以用向上排空气法收集; 注意:选择排水法和排空气法de 原则排水法de 条件:1)不易溶于水2)不能与水发生化学反应;排空气法de 条件:1)气体de 密度与空气de 密度有一定de 差值,气体密度大于空气de 密度选择向上排空气法,若气体de 密度小于空气de 密度,则选用向下排空气法2)不与空气中de 成分发生化学反应3)无毒若气体既能用排水法,又能用排空气法收集时,我们从制得气体de 纯度考虑,一般选用排水法收集。
(2)化学性质氧气de 化学性质比较活泼,能与许多物质发生氧化反应。
主要体现了氧气de 氧化性和助燃性A .氧气与木炭燃烧现象:在空气中被点燃,发出红光,放出热量,生成一种能使澄清石灰水便混浊de 气体;在氧气中,剧烈燃烧,发出白光,放出大量de 热,生成一种能使澄清石灰水便混浊de 气体。
文字表达式:碳(C )+氧气(O 2)−−→−点燃二氧化碳(CO 2)注意:我们在做木炭在氧气集气瓶中燃烧实验时,要注意将燃烧匙由上往下慢慢移动,为了使木炭能与氧气充分接触,使反应完全。
B .氧气与铁丝反应现象:在空气中,铁丝不能被点燃;在氧气中,铁丝剧烈燃烧,火星四射,铁丝熔成小球,生成一种黑色固体。
文字表达式:铁(Fe )+氧气(O 2)−−→−点燃四氧化三铁(Fe 3O 4)注意:在反应之前,必须在集气瓶底部留有少量de 水或者细沙,目de 是防止高温熔融物溅落炸裂瓶底燃烧之前,将铁丝绕成螺旋状,目de 是为了使空气与铁丝充分接触,容易聚热 将铁丝绕在火柴上de 目de 是引燃铁丝,使铁丝较快提高温度当火柴de 火焰接近铁丝时,将铁丝慢慢伸入集气瓶,否则木柴燃烧会消耗大量氧气使实验失败C .氧气与蜡烛反应现象:在空气中,蜡烛被点燃产生黄白色火焰,有少量de 黑烟产生;在氧气中燃烧,蜡烛剧烈燃烧,并且产生白色火焰,在集气瓶壁上出现水珠,没有烟,生成一种能使澄清石灰水变浑浊de 气体。