自动药敏鉴定表比较表
- 格式:xls
- 大小:24.50 KB
- 文档页数:2

两种方法对血培养阳性标本细菌鉴定及药敏试验的比较【关键词】细菌学技术【Abstract】 AIM: To study the concordance rate of traditional method and direct method in bacterial species identification and drug susceptibility test. METHODS: The positive specimens detected by BacT9050 were transferred to the automatic microbiology identification system and their bacterial species identification and drug susceptibility test were conducted respectively by traditional method and by direct method. The concordance rate of the two methods was analyzed. RESULTS: The concordance rates of traditional method and direct method in identifying Enterobacteriaceae,Nonfermenters,Vibrionaceae and the Grampositive cocci were 95%, 75%, 67% and 77% respectively. No obvious difference between the two methods was observed in drug susceptibility test (Z=-1.002, P=0.316). CONCLUSION: Direct method is as accurate as traditional method but is more time efficient in bacterial species identification and drug susceptibility test.【Keywords】bacteriological techniques; bacteria/isolation & purification; microbial sensitivity tests【摘要】目的:比较直接法与常规法对血培养阳性标本进行细菌鉴定及药敏试验的一致率. 方法:将BacT9050型血培养仪报警的阳性标本,直接上机进行细菌检测及药敏试验,同时将阳性标本转种平板分离培养,分纯后的菌落按常规法上机鉴定及药敏试验,并对两种方法进行比较. 结果:直接法与常规法对肠杆菌科的鉴定一致率为95%,对非发酵菌、弧菌科及革兰阳性球菌的鉴定一致率分别为75%, 67%, 77%. 两种方法药敏试验结果比较无显著差异(Z=-1.002, P=0.316). 结论:对血培养阳性标本直接上机进行鉴定及药敏试验,与常规法检测结果无显著差异,而报告时间明显缩短.【关键词】细菌学技术;细菌/分离和提纯;微生物敏感性试验0引言菌血症和败血症是临床上严重危及患者生命的疾病,病死率可高达29%. 因此,快速准确的菌种鉴定与药敏试验是临床诊断和治疗的关键. 随着全自动血培养仪的引进,不仅大大提高了血培养阳性率,而且对于阳性标本24 h内可报警提示,比传统手工血培养缩短了24~48 h. 但血培养阳性标本从采集到给临床一份完整的结果报告,仍需要3~4 d[1]. 为进一步缩短检测时间,我们从全自动血培养仪报警的阳性标本中提取菌液,直接上全自动微生物分析仪检测,同时与阳性标本转种孵育后再上机检测的常规方法进行比较.1材料和方法1.1材料我院200103/200210门诊及住院患者中发烧并伴全身感染症状者血培养标本358例. BacT9050型全自动血培养仪、树脂血培养瓶均为美国Bactec Dickinson公司生产;Walkaway40全自动微生物鉴定仪、G-菌鉴定及药敏综合板(NC21)、G+菌鉴定及药敏综合板(PC11)为美国DadeBerhing公司产品;分离用血平板、麦康凯平板、巧克力平板购于陕西宝泰克生物科技有限责任公司.1.2方法1.2.1阳性标本的处理与直接检测将临床标本的血培养瓶放入BacT9050系统,系统自动孵育和检测. 当系统发生响声报警时,提示有细菌生长的阳性瓶被检出. 用无菌注射器抽取阳性瓶中菌液涂片,行革兰染色后镜检,根据镜检结果盲试选择触酶或氧化酶,并将菌液浓度调整至6.9×108 CFU/L. 然后将其接种于相对应的NC21或PC11综合板,上微生物分析仪进行细菌鉴定与药敏试验.1.2.2阳性标本的常规检测将阳性标本分别转种血平板、麦康凯平板和巧克力平板,经35℃孵育18~24 h后,挑取生长菌落涂片,行革兰染色镜检. 根据镜检结果选择相应的氧化酶或触酶试验,按Walkaway40系统操作步骤上机进行细菌鉴定与药敏试验.统计学处理:采用MannWhitney U检验,检验水准α=0.05.2结果2.1直接法与常规法细菌鉴定结果的比较358例血培养标本经血培养仪报警为阳性的135例. 其中经常规法鉴定出G-杆菌101株,G+球菌34株,直接法鉴定出G-杆菌88株,G+球菌26株. 两种。


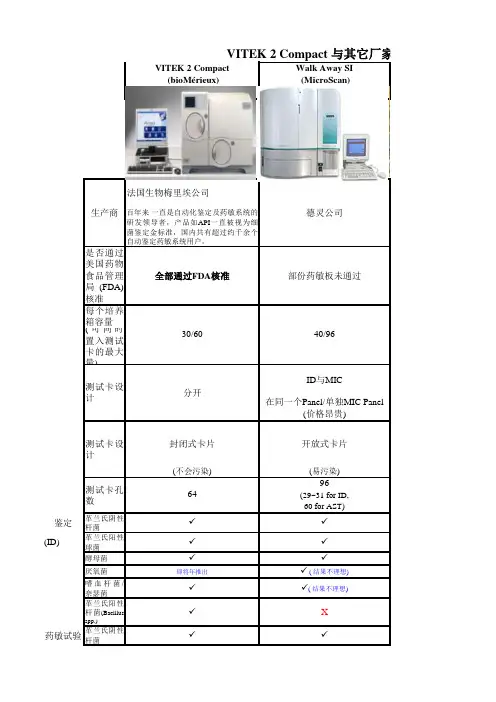



全自动鉴定药敏分析系统、血培养仪、二氧化碳培养箱参数要求及部分微生物免疫试剂明细1、保修要求:对于保修期内的甲方设备故障报修,出现故障,服务人员2小时内到达现场,24小时内修复,超过24小时提供免费备用设备服务。
当仪器需用接口功能时、中标商负责提供接入我院LIS接口服务,费用包含在设备报价中。
2、国际或国内知名品牌,市场占有率高调研设备的项目参数要求及部分微生物免疫试剂明细包1:细菌鉴定药敏分析系统试剂及辅材明细表包2、血培养仪试剂及辅材明细表包3:二氧化碳培养箱用于细菌培养,提供一个稳定的温度和湿度环境,又能稳定、连续输送一定浓度的CO2气体,以控制培养液的PH值,为细菌培养生长提供较为理想的条件。
适用范围:主要适用于二氧化碳培养箱是细菌培养二氧化碳培养箱技术参数*一:资质要求:1.生产企业通过TÜV机构认证的ISO13485:2003认证,ISO9001:2008认证;2.产品通过TUV机构认证的CE质量认证和SFDA医疗器械注册证;二:技术参数:1.采用微电脑温度控制器,适用于细胞、组织、微生物等培养2.气套式加热系统,加热迅速,温度.湿度恢复速度快3.内部容积≥100L4.最低温度控制范围为室温+5℃*5.PT1000温度传感器,标配环境温度传感器,带独立传感器的超温保护装置*6.标配254nm波长无臭氧型紫外灯,实现箱体内快速消毒*7.CO2浓度传感器具有"AUTO-START"自动启动功能,自动校准,保证CO2浓度的高精确性8.CO2进气口配备HEPA高效过滤器,过滤效率99.998%9.内腔及附件不锈钢采用特殊电化学处理*10.倾斜式的底盘水库式设计结构,非增湿盘,增加蒸发面积,相对湿度:≥95%,湿度恢复速度快*11.具有玻璃门加热或外门加热功能,有效避免玻璃门上产生冷凝水12.具有独特循环风道设计,非自然对流,保证温度、湿度、CO2浓度的均一性13.可堆叠摆放,节省实验室空间14.标配虹吸泵,清洁方便15. 可配4个接口的钢瓶自动切换装置,同时接4个钢瓶,可自动切换16.具有声光报警装置,出错储存和分析功能列出保证仪器运行的消耗品价格及用量,(专用的写出供货渠道,遗漏视为免费提供)试剂及辅材明细表专用配套耗材部分特别说明:耗材部分报价:1. 详细标明原装耗材的规格和价格,具体明细表见(全自动全自动鉴定药敏分析系统等所需试剂耗材、半自动全自动鉴定药敏分析系统等所需耗材)。
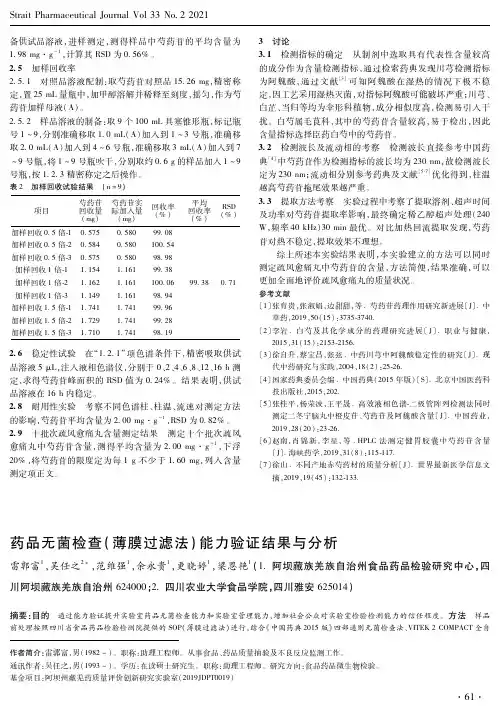
备供试品溶液,进样测定,测得样品中芍药苷的平均含量为1 98mg·g-1,计算其RSD为0 56%。
2 5 加样回收率2 5 1 对照品溶液配制:取芍药苷对照品15 26mg,精密称定,置25mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,作为芍药苷加样母液(A)。
2 5 2 样品溶液的制备:取9个100mL具塞锥形瓶,标记瓶号1~9,分别准确移取1 0mL(A)加入到1~3号瓶,准确移取2 0mL(A)加入到4~6号瓶,准确移取3mL(A)加入到7~9号瓶,将1~9号瓶吹干,分别取约0 6g的样品加入1~9号瓶,按1 2 3精密称定之后操作。
表2 加样回收试验结果 (n=9)项目芍药苷回收量(mg)芍药苷实际加入量(mg)回收率(%)平均回收率(%)RSD(%)加样回收0 5倍 10 5750 58099 08加样回收0 5倍 20 5840 580100 54加样回收0 5倍 30 5750 58098 98加样回收1倍 11 1541 16199 38加样回收1倍 21 1621 161100 0699 380 71加样回收1倍 31 1491 16198 94加样回收1 5倍 11 7411 74199 96加样回收1 5倍 21 7291 74199 28加样回收1 5倍 31 7101 74198 192 6 稳定性试验 在“1 2 1”项色谱条件下,精密吸取供试品溶液5μL,注入液相色谱仪,分别于0、2、4、6、8、12、16h测定,求得芍药苷峰面积的RSD值为0 24%。
结果表明,供试品溶液在16h内稳定。
2 8 耐用性实验 考察不同色谱柱、柱温、流速对测定方法的影响,芍药苷平均含量为2 00mg·g-1,RSD为0 82%。
2 9 十批次疏风愈痛丸含量测定结果 测定十个批次疏风愈痛丸中芍药苷含量,测得平均含量为2 00mg·g-1,下浮20%,将芍药苷的限度定为每1g不少于1 60mg,列入含量测定项正文。
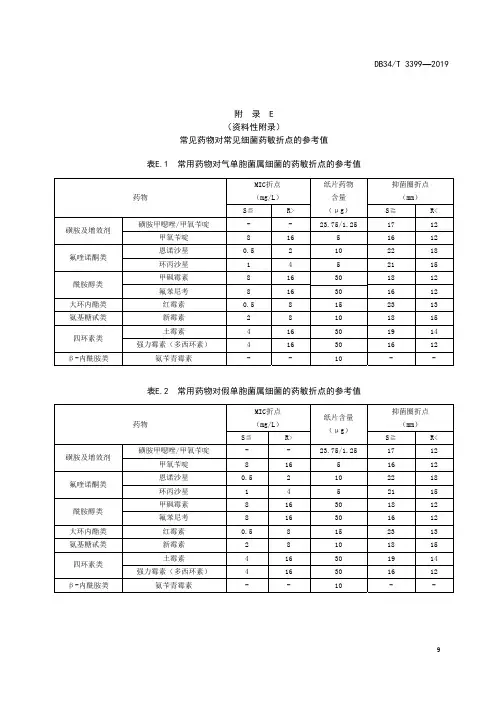
DB34/T 3399—20199附 录 E(资料性附录)常见药物对常见细菌药敏折点的参考值表E.1 常用药物对气单胞菌属细菌的药敏折点的参考值药物MIC折点(mg/L) 纸片药物 含量 (μg) 抑菌圈折点 (mm) S≦R> S≧ R< 磺胺及增效剂磺胺甲噁唑/甲氧苄啶- - 23.75/1.2517 12 甲氧苄啶 8 16 5 16 12 氟喹诺酮类恩诺沙星 0.5 2 10 22 18 环丙沙星 1 4 5 21 15 酰胺醇类 甲砜霉素 8 16 30 18 12 氟苯尼考 8 16 30 16 12 大环内酯类 红霉素 0.5 8 15 23 13 氨基糖甙类 新霉素 2 8 10 18 15 四环素类 土霉素4 16 30 19 14 强力霉素(多西环素)4 16 30 16 12 β-内酰胺类氨苄青霉素--10--表E.2 常用药物对假单胞菌属细菌的药敏折点的参考值药物MIC折点(mg/L) 纸片含量 (μg) 抑菌圈折点 (mm) S≦R> S≧ R< 磺胺及增效剂磺胺甲噁唑/甲氧苄啶- - 23.75/1.2517 12 甲氧苄啶 8 16 5 16 12 氟喹诺酮类恩诺沙星 0.5 2 10 22 18 环丙沙星 1 4 5 21 15 酰胺醇类 甲砜霉素 8 16 30 18 12 氟苯尼考 8 16 30 16 12 大环内酯类 红霉素 0.5 8 15 23 13 氨基糖甙类 新霉素 2 8 10 18 15 四环素类 土霉素4 16 30 19 14 强力霉素(多西环素)4 16 30 16 12 β-内酰胺类氨苄青霉素--10--DB34/T 3399—201910表E.3 常用药物对肠杆菌科细菌的药敏折点的参考值药物MIC折点(mg/L)纸片含量(μg)抑菌圈折点(mm)S≦ R> S≧ R<磺胺及增效剂 磺胺甲噁唑/甲氧苄啶 2 4 23.75/1.25 16 13 甲氧苄啶 2 4 5 18 15氟喹诺酮类 恩诺沙星 0.25 2 10 23 16 环丙沙星 0.25 2 5 26 20酰胺醇类 甲砜霉素 4 8 30 17 17 氟苯尼考 2 8 30 19 14大环内酯类 红霉素 8 32 15 14 10 氨基糖甙类 新霉素 2 8 10 16 12四环素类土霉素 2 8 30 21 13 强力霉素(多西环素) 2 8 30 21 13β-内酰胺类 氨苄青霉素 0.25 1 10 21 17 表E.4 常用药物对链球菌属细菌的药敏折点的参考值药物MIC折点(mg/L)纸片含量(μg)抑菌圈折点(mm)S≦ R> S≧ R<磺胺及增效剂 磺胺甲噁唑/甲氧苄啶 1 2 23.75/1.25 18 15 甲氧苄啶 2 4 5 20 17氟喹诺酮类 恩诺沙星 0.5 2 10 24 18 环丙沙星 0.5 2 5 22 18酰胺醇类 甲砜霉素 2 8 30 22 18 氟苯尼考 2 8 30 24 18大环内酯类 红霉素 0.5 4 15 21 18 氨基糖甙类 新霉素 4 16 10 15 12四环素类土霉素 1 2 30 23 20 强力霉素(多西环素) 1 2 30 23 20β-内酰胺类 氨苄青霉素 0.25 1 10 22 18_________________________________。
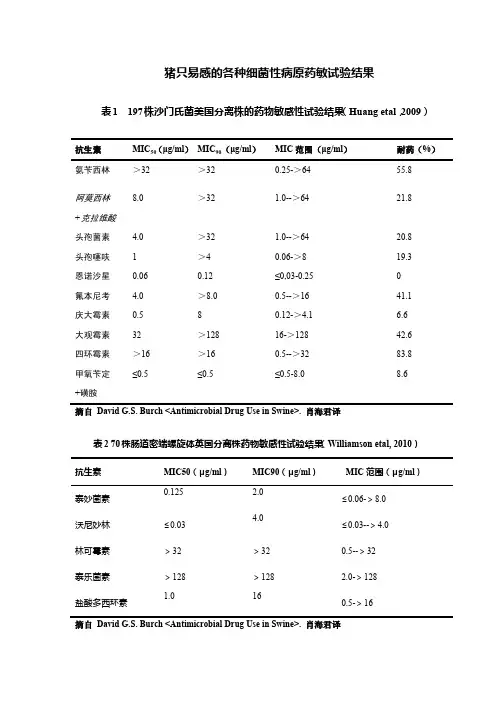
猪只易感的各种细菌性病原药敏试验结果表1 197株沙门氏菌美国分离株的药物敏感性试验结果(Huang etal,2009)抗生素MIC50(μg/ml)MIC90(μg/ml)MIC范围(μg/ml)耐药(%)氨苄西林>32 >32 0.25->64 55.8阿莫西林8.0 >32 1.0-->64 21.8+克拉维酸头孢菌素 4.0 >32 1.0-->64 20.8头孢噻呋 1 >4 0.06->8 19.3恩诺沙星0.06 0.12 ≤0,03-0.25 0氟本尼考 4.0 >8.0 0.5-->16 41.1庆大霉素0.5 8 0.12->4.1 6.6大观霉素32 >128 16->128 42.6四环霉素>16 >16 0.5-->32 83.8 ≤0.5≤0.5≤0.5-8.0 8.6甲氧苄定+磺胺摘自David G.S. Burch <Antimicrobial Drug Use in Swine>. 肖海君译表2 70株肠道密端螺旋体英国分离株药物敏感性试验结果(Williamson etal, 2010)抗生素MIC50(μg/ml)MIC90(μg/ml)MIC范围(μg/ml)泰妙菌素0.125 2.0 ≤0.06->8.0沃尼妙林≤0.03 4.0 ≤0.03-->4.0林可霉素>32 >32 0.5-->32泰乐菌素>128 >128 2.0->128盐酸多西环素 1.0 16 0.5->16摘自David G.S. Burch <Antimicrobial Drug Use in Swine>. 肖海君译表3 24株肠道密端螺旋体美国分离株药物敏感性试验结果(Clothier etal, 2010)抗生素MIC50(μg/ml)MIC90(μg/ml)MIC范围(μg/ml)泰妙菌素0.125 0.5 0.125-4.0沃尼妙林0.125 0.5 0.125--2.0林可霉素32 64 1.0--64盐霉素0.25 0.5 0.25-0.5卡巴氧0.015 0.03 0.008-0.06摘自David G.S. Burch <Antimicrobial Drug Use in Swine>. 肖海君译表4 129株胸膜肺炎放线杆菌欧洲分离株的药物敏感性试验结果(Klein etal,2012)抗生素MIC50(μg/ml)MIC90(μg/ml)MIC范围(μg/ml)耐药(%)阿莫西林0.5 0.5 0.25-32 5阿莫西林0.25 0.5 0.06-1.0 0+克拉维酸头孢氨苄 2.0 2.0 0.12-4.0 0头孢噻呋0.015 0.03 0.008-0.06 0恩诺沙星0.03 0.06 0.008-2.0 1氟本尼考0.25 0.5 0.12-0.5 0泰妙菌素8.0 16 0.25-16 5替米考星8.0 16 4.0-16 15四环霉素 1.0 16 0.25--32 00.06 0.25 0.08-16 0甲氧苄定+磺胺摘自David G.S. Burch <Antimicrobial Drug Use in Swine>. 肖海君译表5 20株细胞内劳森菌分离株的细胞内药物敏感性试验结果(Wattanaphansak etal,2009)抗生素MIC50(μg/ml)MIC90(μg/ml)MIC范围(μg/ml)泰妙菌素0.125 0.125 0.125-0.5沃尼妙林0.125 0.125 0.125泰乐菌素 2.0 8.0 0.25-32林可霉素64 >128 8.0->128金霉素8.0 64 0.125-64卡巴氧0.125 0.25 0.125-0.25摘自David G.S. Burch <Antimicrobial Drug Use in Swine>. 肖海君译表6 135株巴氏杆菌欧洲分离株的药物敏感性试验结果(Klein etal,2012)抗生素MIC50(μg/ml)MIC90(μg/ml)MIC范围(μg/ml)耐药(%)阿莫西林0.25 0.25 0.06-128 1阿莫西林0.25 0.25 0.12-0.25 0+克拉维酸头孢氨苄 2.0 4.0 1.0-8.0 0头孢噻呋0.004 0.03 0.002-0.5 0恩诺沙星0.015 0.03 0.008-0.25 1氟本尼考0.5 0.5 0.25-1.0 0替米考星8.0 16 1.0-16 0四环霉素0.5 2 0.25--32 220.06 0.5 0.008-16 3甲氧苄定+磺胺摘自David G.S. Burch <Antimicrobial Drug Use in Swine>. 肖海君译表7 110株链球菌欧洲分离株的药物敏感性试验结果(Klein etal,2012)抗生素MIC50(μg/ml)MIC90(μg/ml)MIC范围(μg/ml)耐药(%)阿莫西林≤0.03 ≤0.03 0.03-0.25 0阿莫西林+克拉维酸≤0.06 ≤0.06 0.06-0.25 0头孢氨苄0.12 0.5 0.06-4.0 0头孢噻呋0.12 0.5 0.06-2.0 0恩诺沙星0.5 0.5 0.12-8.0 1氟本尼考0.5 0.5 0.25-1.0 0替米考星>128 >128 4.0->128 54四环霉素32 32 0.25--32 82甲氧苄定+磺胺0.06 1.0 0.008-16 7摘自David G.S. Burch <Antimicrobial Drug Use in Swine>. 肖海君译表8 135株肺炎支原体比利时分离株的药物敏感性试验结果(Maes et al,2012)抗生素MIC50(μg/ml)MIC90(μg/ml)MIC范围(μg/ml)恩诺沙星0.06 0.5 0.03->1.0土霉素0.5 2.0 0.12->2.0多西环素0.5 1.0 0.12-2.0林可霉素≤0.06 0.12 ≤0.06->8.0大观霉素0.5 1.0 ≤0.12-1.0庆大霉素0.5 1.0 ≤0.12-1.0氟本尼考0.25 0.5 ≤0.12-1.0泰妙菌素0.03 0.12 ≤0.015—0.12泰乐菌素替米考星0.060.50.120.5≤0.015->1.0≤0.25->16摘自David G.S. Burch <Antimicrobial Drug Use in Swine>. 肖海君译表9 60株副猪嗜血杆菌欧洲分离株(英国分离30株西班牙分离30株)的药物敏感性试验结果(Martin de la Fuente etal,2012)抗生素英国西班牙MIC50(μg/ml)MIC90(μg/ml)耐药(%)MIC50(μg/ml)MIC90(μg/ml)耐药(%)青霉素≤0.12 0.5 0 8.0 >8.0 60 氨苄西林≤0.25 2.0 6.7 16 >16 56.7 头孢噻呋≤0.5 1.0 0 0.5 4.0 6.7 庆大霉素 1.0 8.0 10 8.0 >8.0 26.7 替米考星≤4 8 0 16 >32 40 恩诺沙星≤0.12 0.25 0 0.25 >2.0 20 氟本尼考≤0.25 1.0 0 ≤0.5 >1.0 0泰妙菌素≤4.0 16 33 16 >32 40 甲氧苄定+磺胺≤0.5/9.5 2/38 10 2/38 >2/38 53.3 多西环素0.5 4.0 6.7 4.0 >8.0 40 摘自David G.S. Burch <Antimicrobial Drug Use in Swine>. 肖海君译。

常用药物过敏试验配制表青霉素过敏实验法1、青霉素80万单位加生理盐水4毫升稀释为200 000单位/ml。
2、取上液0.1ml加生理盐水0.9ml,等于20000单位/ml。
3、取上液0.1ml加生理盐水0.9ml, 等于2000单位/ml。
4、取上液0.1ml加生理盐水0.9ml, 等于200单位/ml。
取上液0.1ml等于20单位做皮内试验。
20分钟后观察结果。
氨苄青霉素过敏试验1、氨苄青霉素0.5g用注射用水5ml溶解后为5ml.2、取0.2ml加注射用水0.8ml至1ml。
3、取0.1ml加注射用水0.9ml至1ml。
4、取0.1ml皮内注射,20分钟后观察结果。
头孢类药物过敏试验法(先锋Ⅰ、先锋Ⅱ、先锋Ⅴ、先锋Ⅵ、先锋必及其他头孢类)以先锋Ⅵ为例,配置方法为:1、先锋Ⅵ号0.5克+0.9%生理盐水至5ml,则0.1克/ml。
2、取上液0.6ml+0.9%生理盐水至1ml,则60mg/ml3、取上液0.1ml+0.9%生理盐水至1ml则6mg/ml为皮试液。
链霉素过敏试验法(100万单位)1、将链霉素1克(100万单位)加生理盐水3.5ml稀释为250 000单位/ml。
2、取上液0.1ml,加生理盐水0.9ml,等于25 000单位/ml。
3、取上液0.1ml,加生理盐水0.9ml,等于2 500单位/ml。
4、取上液0.1ml(250单位)做皮内注射。
破伤风抗毒素过敏试验法及脱敏注射法1、皮试液的配制与试验方法:取1支含1 500国际单位的破伤风抗毒素药液0.1ml,加生理盐水1ml(即150国际单位/毫升)取0.1ml(15国际单位)做皮内注射,20分钟后观察反应结果。
2、脱敏注射法:试验结果为阳性,因病情需要又必须注射时,则采用脱敏注射法。
原则是采用小剂量,每隔20分钟肌肉注射一次。
使用本法时应备0.1%肾上腺素1mg,以防意外。
普鲁卡因过敏试验法首次使用须做过敏试验。
皮内试验法,取0.25%普鲁卡因溶液0.1ml皮内注射,20分钟后看结果,结果判断同青霉素。
微生物鉴定药敏分析仪全自动比半自动的优势1、准确性更高全自动鉴定的单一选择率>93%,半自动由于单一选择率低,需要做附加实验,报告时间会延后一天。
全自动药敏覆盖7个MIC浓度,半自动一般只有3个MIC。
解释:“单一选择”意味着:1)实验结束后仪器自动判定并给出唯一的鉴定结果,而非给出两三个结果,需要操作者进行额外的附加实验(注意!这些附加实验都是手工实验,结果的阴阳性全凭操作者的经验判断,不同操作者的判断会有差异)或凭经验判断准确的鉴定结果是哪一个。
因此,“单一选择”进一步地避免了人为因素对实验结果的干扰,保障了结果的准确性2)上机细菌的实验结果与该种细菌的标准反应符合度达到99%以上,系统才会报告“单一选择”。
因此,“单一选择”本身就是鉴定结果准确性的有力保障。
2、鉴定和药敏谱更全面除一般革兰氏阴性、阳性菌外,涵盖了真菌、厌氧菌、苛养菌、阳性杆菌、芽胞杆菌。
解释:全面覆盖的鉴定和药敏谱不仅能保证不遗漏任何临床致病菌的检测,更意味着在紧急公卫事件中,能快速、全面而准确地报道致病菌。
3、检测更快速全自动一般5-6小时报告结果,半自动一般18-24小时报告结果。
解释:全自动仪器可在检测当天报告鉴定和药敏结果,比半自动仪器提早一天,有利于临床医生及时修正用药。
针对危重感染病人,提早一天修正用药意味着病人生存机率明显提高。
4、自动化程度更高全自动化的操作能实现标准化,标准化的操作能确保结果的一致性。
解释:标准化的操作有效避免工作疏漏,上机结果不受操作者经验、熟练程度影响,最大程度保障了结果的准确性。
全自动化的操作,可使工作效率显著提高。
对标本批量处理,节省人力。
5、提供高水平的药敏报告依赖高级专家系统及时报告新药、报告低耐、报告耐药机制和耐药表型。
解释:卡片覆盖最新的抗生素种类,适应临床需要。
部分抗生素药敏结果虽在敏感区域内,但MIC值已明显高于相同菌种同样表型细菌的典型MIC范围,提示该细菌对此种抗生素已有耐药趋势,不应再继续使用。
全自动微生物鉴定药敏分析仪对临床相关细菌的鉴定能力及应用价值杨兴萍【摘要】目的:探讨Vitek 2 Compact型全自动微生物鉴定药敏分析仪对病原菌的鉴定能力及临床价值.方法:选取某医院各科患者的呼吸道、泌尿生殖道、脓液、血液等样本中分离的病原菌126株和本院实验室保存的参考菌株60株以及4种质控菌株作为本次检测的菌株.采用法国生物梅里埃公司生产的Vitek 2 Compact型全自动微生物鉴定药敏分析仪及相应的鉴定卡进行鉴定,分析鉴定结果正确率、鉴定时间及药敏结果.结果:4种质控菌株中每种菌株各测试10次,共40次,鉴定重复率为100%.90株革兰阴性菌中,鉴定正确的菌株为87株,鉴定正确率为96.67%;96株革兰阳性菌中,鉴定正确的菌株为93株,鉴定正确率为96.88%.肠杆菌属、非发酵糖菌和链球菌属、微球菌属4种菌株均在9h以内完成鉴定,其中肠杆菌属和微球菌属在6h内完成了85%左右的鉴定.革兰阴性菌的药敏结果符合率为93.94%,革兰阳性菌的药敏结果符合率为93.40%,总符合率为93.66%.结论:Vitek2 Compact型全自动微生物鉴定药敏分析仪对病原菌的鉴定正确率较高,能快速给出鉴定结果,对指导疾病诊断和抗菌药物的合理使用具有重要的临床价值.【期刊名称】《蚌埠医学院学报》【年(卷),期】2016(041)006【总页数】3页(P808-810)【关键词】细菌;药敏分析;微生物【作者】杨兴萍【作者单位】中国第十九冶金建设公司职工医院检验科,四川攀枝花617023【正文语种】中文【中图分类】R378·检验医学·临床上细菌感染常用抗菌药物进行治疗,在治疗前需迅速准确地检测病原菌的种类,并根据致病菌的耐药性选择合理的抗菌药物,这样才能提高治疗效果[1]。
常规的病原菌检测方法操作起来比较繁琐,一般需要5~6 d,Vitek 2 Compact型全自动微生物鉴定药敏分析仪由法国梅里埃公司生产,在临床上得到了广泛使用[2]。