◆ 全书优质试题随意编辑 ◆ 课堂教学流程完美展示 ◆ 独家研发错题组卷系统
目目标标导典典例例透透析析
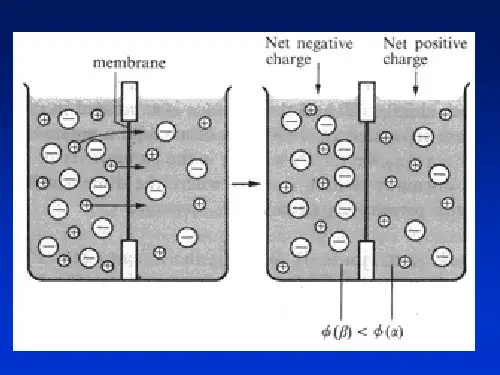
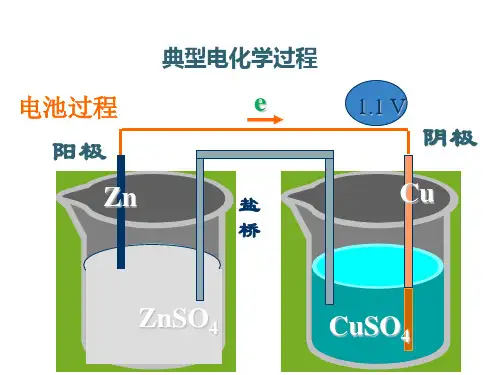
二、原电池的工作原理和正负极的判断 1.原电池的工作原理
◆ 全书优质试题随意编辑 ◆ 课堂教学流程完美展示 ◆ 独家研发错题组卷系统
目目标标导导航航
2.原电池正负极的一般判断
Zn2++Cu
目目标标导导航航
知识梳理
重重难难聚聚焦焦
典典例例透透析析
一二
2.原电池形成的条件 (1)两个活泼性不同的电极: 相对活泼的金属作负极; 较不活泼的金属或非金属作正极。 (2)电解质溶液。 (3)形成闭合回路。 (4)能自发地发生氧化还原反应。 ◆ 全书优质试题随意编辑 ◆ 课堂教学流程完美展示 ◆ 独家研发错题组卷系统 思考感悟 盐桥的作用是什么? 提示:(1)连接两个半电池构成闭合回路。(2)保持盐桥两边电解 质溶液呈电中性。
目目标标导导航航
知识梳理
重重难难聚聚焦焦
典典例例透透析析
知识点1 知识点2 知识点3
原电池的判断 【例题1】 下图中能组成原电池产生较大电流的是 ( )
◆ 全书优质试题随意编辑 ◆ 课堂教学流程完美展示 ◆ 独家研发错题组卷系统
解析:A、D两项中电极与电解质溶液之间不发生反应,不能构成 原电池;B项符合原电池的三个构成条件,且Zn能与H2SO4溶液反应, 两电极发生的反应分别是Zn-2e- Zn2+,2H++2e- H2↑;C项中 酒精不是电解质,故不是原电池。
如本例中可用FeCl 溶液作电解质溶液。 ◆ 全书优质试题3随意编辑 ◆ 课堂教学流程完美展示 ◆ 独家研发错题组卷系统 (4)构成闭合回路:将电极用导线连接,使之构成闭合回路。 特别提醒设计原电池时,若氧化还原反应方程式中无明确的电解 质溶液,可用水作电解质,但为了增强其导电性,通常加入强碱或强 酸。如燃料电池,水中一般要加入KOH或H2SO4。