各种细胞转染方法比较
- 格式:docx
- 大小:12.19 KB
- 文档页数:2

细胞转染实验总结引言细胞转染是生物学研究中常用的实验技术,用于将外源DNA、RNA或蛋白质引入到目标细胞中。
通过细胞转染,可以实现基因表达、基因敲除、蛋白质定位等多种研究目的。
本文总结了细胞转染实验的基本原理、常用方法和注意事项。
基本原理细胞转染实验的基本原理是通过物理或化学方法将外源DNA、RNA或蛋白质传递到目标细胞内。
细胞内的转染物质可以在细胞内进行表达、干扰或定位,从而实现对目标细胞功能的研究。
常见的细胞转染方法包括:1.电穿孔法:通过应用电流使细胞膜发生临时孔洞,从而使转染物质进入细胞内。
2.化学转染法:利用聚合物、脂质体等化学物质,将目标物质载体化,并与细胞膜结合,实现内源化学转染。
3.病毒载体介导转染法:利用病毒(如腺病毒、逆转录病毒等)作为载体,传递目标物质到细胞内。
常用方法1. 电穿孔法电穿孔法是细胞转染中常用的物理方法之一。
通过应用高电压或脉冲电场,可以使细胞膜发生临时性孔洞,从而使外源DNA、RNA或蛋白质进入细胞内。
常用的电穿孔方法包括:•电转染:将转染物质与细胞悬浮液混合后施加电脉冲,使细胞膜发生孔洞并吸收转染物质。
•静电转染:将转染物质与带正电荷的载体(如聚乙烯亚胺)混合后,与带负电荷的细胞膜相互吸引,从而将转染物质导入细胞内。
2. 化学转染法化学转染法是一种通过化学物质介导的细胞转染方法。
常用的化学转染法有:•使用聚合物:聚合物(如聚乙烯亚胺、聚合丙烯酸等)能与转染物质结合成复合物,使其稳定且易于细胞摄取。
•脂质体转染:脂质体是由磷脂、胆固醇等成分构成的脂质双层结构,可以包裹转染物质形成脂质体-转染物复合物,通过与细胞膜融合实现内源转染。
3. 病毒载体介导转染法病毒载体介导转染法是细胞转染中较常用的方法之一。
常见的病毒载体包括:•腺病毒:腺病毒是一种双链DNA病毒,可以携带大片段的外源DNA,并有效地传递到目标细胞内。
•逆转录病毒:逆转录病毒(如 lentivirus、retrovirus等)可以将外源RNA逆转录成DNA,然后整合到宿主细胞基因组中。
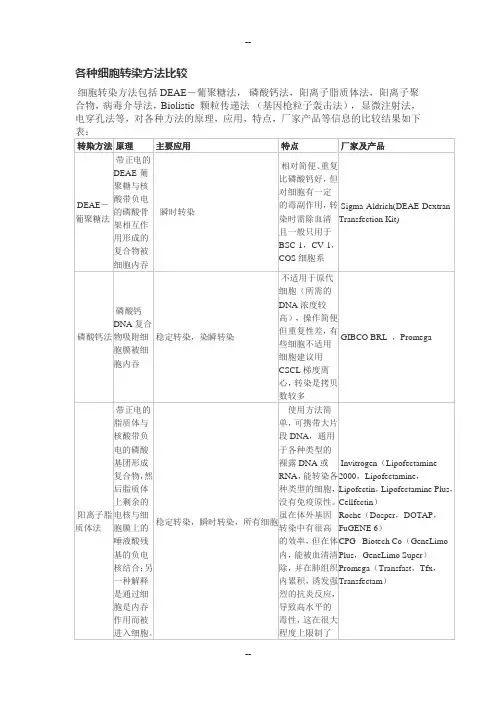

细胞转染的原理操作步骤以及小技巧细胞转染是一种将外源DNA、RNA、蛋白质等分子导入到细胞内的实验技术。
这种技术可以用来研究基因功能、发现新的信号通路和治疗基因疾病等。
下面将介绍细胞转染的原理、操作步骤以及一些小技巧。
一、细胞转染的原理:细胞转染主要通过三种方法实现:物理法、化学法和生物学法。
1.物理法:通过高压、电穿孔、微射流等方式,使细胞膜发生瞬时破裂,从而使DNA、RNA等外源分子进入细胞。
常用的物理法有电穿孔法和基因枪法。
2.化学法:通过化学物质,如聚吡咯、脂质体等,使外源分子与细胞膜结合,从而实现转染。
常用的化学法有聚乙烯亚胺(PEI)法、磷酸钙共沉淀法等。
3.生物学法:通过利用病毒载体将外源基因导入目标细胞,实现基因的转移。
常用的生物学法有腺相关病毒(AAV)转染、逆转录病毒(RETRO)转染等。
二、细胞转染的操作步骤:1.细胞的预处理:根据细胞类型和实验要求,将细胞培养至合适的状态。
通常细胞应处于快速生长期,但还未达到接触抑制的阶段。
对于一些特定的细胞,如悬浮细胞,可能需要将其转接至适当的培养基中。
2.外源分子的准备:将外源DNA、RNA等转染载体制备好。
如将DNA克隆并纯化至高质量的质粒DNA,或将RNA合成或纯化。
根据实验要求选择合适的转染载体。
3.转染方法的选择:根据实验要求选择合适的转染方法,如物理法、化学法或生物学法。
一般情况下,物理法适用于悬浮细胞,化学法适用于贴壁细胞,而生物学法适用于大多数细胞类型。
4.细胞转染操作:a.物理法:i.电穿孔法:将细胞悬浮于含有外源分子的缓冲液中,然后通过电穿孔仪的电极或电穿孔板进行电穿孔。
ii. 基因枪法:使用基因枪将外源分子直接“枪”入目标细胞中。
b.化学法:i.PEI法:将PEI与外源DNA或RNA按一定比例混合,在适当条件下形成复合物,然后添加至目标细胞中。
ii. 磷酸钙共沉淀法:将外源DNA与磷酸钙按比例混合,并静置形成磷酸钙- DNA沉淀,然后加入至目标细胞中。


稳定转染VS瞬时转染展开全文生物通报道:转染是将外源遗传物质导入真核细胞的过程,是细胞和分子生物学研究的重要工具,可用于研究基因表达对细胞生理水平的影响。
不论是质粒、DNA还是各种RNA(mRNA、siRNA或microRNA),要将这些外源核酸转入细胞并不容易,它们必须穿过细胞膜这层屏障才能进入细胞质。
转染方法可分为物理转染和化学转染,物理转染方法包括电穿孔、显微注射和基因枪等,化学转染可使用磷酸钙共沉淀、DEAE-Dx或基于阳离子脂质的转染试剂。
上述方法都可以解决转染面临的主要挑战,即让带负电荷的核酸分子穿过带负电的细胞膜。
物理转染方法一般是在细胞膜上打洞来克服静电排斥,使核酸插入。
而化学转染中,一般是利用带正电的转染试剂将带负电的核酸包裹起来。
这些方法都可以实现转染,可谓条条大路通罗马,那么究竟是选瞬时转染好还是选稳定转染好呢?瞬时转染的细胞中,外源基因得以表达但它们并不会整合到细胞的基因组中,也就不会被复制。
细胞中瞬时转染的外源基因表达时间有限,通常仅持续几天,直到外源基因在细胞分裂过程中因各种因素丢失为止我们如何区分细胞是否转染成功了呢?在转染质粒中往往都含有一个报告基因,来指示细胞中目标基因是否存在,这样的报告基因一般可以在转染后一两天内检测到。
稳定转染可以在瞬时转染的基础上建立,只不过需要一个重要的偶发过程:在少数转染细胞中,外源基因能够整合到细胞的基因组中。
外源基因成为细胞基因组的一部分从而得以复制,这就是稳定转染细胞的标志。
稳定转染细胞的子代细胞也同样表达外源基因,由此形成稳定转染的细胞系。
在建立上述稳定转染细胞系时,我们需要使用选择性标记来区分瞬时转染与稳定转染。
将这些选择性标记与基因共表达,我们就可以筛选出外源基因已成功整合到基因组的细胞,同时剔除瞬时转染的细胞。
将外源基因与抗生素抗性基因共转染(如新霉素抗性基因neo)是一种常用方法,随后可用相应抗生素(如geneticin或G418)对转染后的细胞进行筛选。

各种转染方法比较不同的实验室转染方法选择会依赖于多个相关因素,如目标细胞类型、转染效率、细胞毒性、需求的表达时间、实验的规模和预算等。
以下是一些常见的转染方法的比较:1. 离子交换法(Calcium phosphate transfection)离子交换法是最早开发和使用的转染方法之一、它使用磷酸钙和DNA或RNA的复合物在细胞表面形成凝析沉淀物。
该方法简单、经济且较为普遍,适用于许多细胞类型。
然而,它的转染效率较低,存在较多的细胞毒性。
2. 迷走转染法(Lipofection)迷走转染法是当前最常用的转染技术之一,通过磷脂体(例如Lipofectamine)与质粒DNA形成复合物。
该方法转染效率高,而且适用于许多类型的细胞,包括哺乳动物和非哺乳动物。
然而,迷走转染法存在一些限制,如细胞毒性、稳定性较差,和细胞特异性。
3. 电穿孔法(Electroporation)电穿孔法是通过应用电场使细胞膜暂时性孔化来实现转染效果。
它可以用于转染各种类型的细胞,包括哺乳动物、鸟类和植物。
电穿孔法的转染效率高,但存在一定的细胞毒性和细胞损伤风险。
此外,电穿孔设备的成本较高,需要专门训练的技术人员来操作。
4. 病毒载体转染法(Viral vector transfection)病毒载体转染法使用经修饰的病毒作为转染载体,可实现高效的基因传递和表达。
常用的病毒载体包括腺病毒、衣壳病毒和逆转录病毒。
这些病毒对于不同类型的细胞具有不同的亲和力和转染效率。
然而,病毒载体转染法的主要限制是细胞对病毒的感染能力,以及在临床应用中可能引发的安全性问题。
5. 直接注射法(Direct microinjection)直接注射法是一种机械刺伤细胞膜直接将DNA注入细胞的方法。
这种方法对于特定的细胞类型具有高效转染的能力,如哺乳动物受精卵和干细胞。
它可以实现精确控制和单细胞水平的转染,但需要昂贵的设备和专业技能。
总结起来,转染方法的选择应根据实验的具体需求来进行。
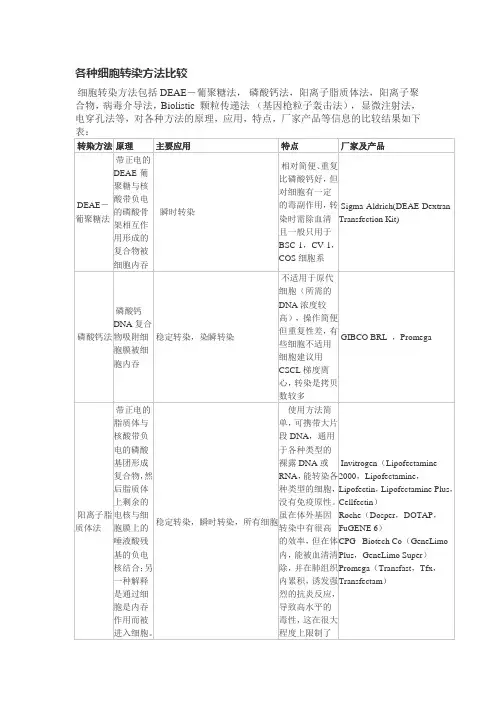

各种转染方法比较转染是将外源DNA或RNA导入体细胞的一种常用技术,用于研究基因功能、疾病机制、基因治疗等领域。
常用的转染方法包括化学法、电穿孔法、病毒载体介导转染和生物矢量直接注射法等。
下面将对这些转染方法进行详细比较。
1.化学法:化学法是最简单、最常用的转染方法之一,主要通过化学试剂与DNA或RNA形成复合物,进而被细胞摄取。
常用的化学试剂有钙磷酸盐、聚乙烯亚胺(PEI)、脂质体、高分子聚合物等。
化学法的优势在于易操作、适用于不同细胞类型,且无需特殊设备。
但其转染效率相对较低,引起细胞毒性的风险较高。
2.电穿孔法:电穿孔法又称为电转染法,通过利用电场作用使细胞膜发生瞬时通透性,使外源DNA或RNA进入细胞。
这种方法可使用电脉冲仪或特殊转染设备进行操作,适用于多种细胞类型。
相比于化学法,电穿孔法的转染效率更高,但对细胞的毒性稍高。
3.病毒载体介导转染:病毒载体介导转染是一种高效的转染方法,常用的病毒载体有腺病毒(Adenovirus)、腺相关病毒(Adeno-associated virus,AAV)、逆转录病毒(Retrovirus)和慢病毒(Lentivirus)等。
这些病毒载体不仅能将外源DNA或RNA导入细胞,还能使其在细胞内稳定表达。
病毒载体介导转染的优势在于高转染效率、稳定表达,适用于许多细胞类型。
然而,为了避免潜在的致病性和免疫反应,需要选择无毒性、无致病性的病毒载体。
4.生物矢量直接注射法:生物矢量直接注射法是将外源DNA或RNA直接注射到体内,让其进入目标细胞。
这种方法适用于许多动物模型研究,如小鼠、斑马鱼等。
生物矢量直接注射法的优势在于转染效率高、实验操作简单,但对于人体病理研究等实验要求较高的场景,其应用范围较窄。
根据以上比较,选择适合自己研究需求和细胞类型的转染方法非常重要。
需要考虑的因素包括转染效率、细胞毒性、操作难度、成本等。
在实际应用中,有时也可结合多种方法,例如将化学法与电穿孔法相结合,能够提高转染效率。


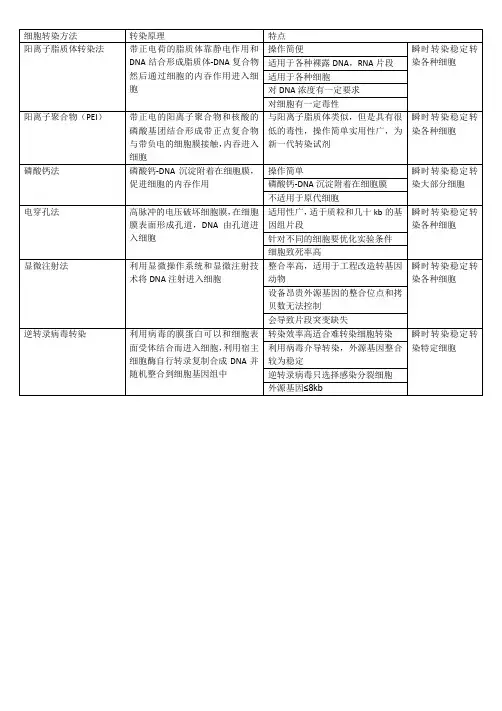
几种转染方法的比较
目前,基因转染技术已经发展为分子生物学、生物工程和基因治疗等
领域的重要实用工具,它可以极大地提高研究的效率和准确度,是许多重
要的基础实验的重要手段。
基因转染,就是把DNA片段植入受体细胞,使
其形成完整的外源基因,从而使其编码的蛋白质可以表达出来。
其中,质
粒转染(经典CaCl2转染)、电穿孔转染、膜融合转染、磁珠转染、膜膜
转染、管状细胞转染(cylinder-mediated gene transfer)、病毒转染
和小肠转染等转染方法,是目前比较常用的基因转染方法。
一、质粒转染
质粒转染是将外源DNA片段载体在质粒上,用极低的浓度CaCl2诱导
细胞膜的瞬时通透性,使外源基因可以通过通透的细胞膜进入细胞,这是
质粒转染的原理,也是最常用的一种质粒转染方法。
质粒转染的优点:
(1)操作简单,易于大批量高效率的实验。
(2)操作条件宽松,不受受体细胞类型的限制,可以适应多种宿主
细胞。
(3)转染效率高,可以达到百分之九十以上。
(4)可以通过有效的筛选系统,有效控制外源DNA的插入和表达量。
质粒转染的缺点:
(1)转染过程对细胞毒性较大,转染效率有限。
转染步骤及经验(精华)一、基础理论转染是将外源性基因导入细胞内的一种专门技术。
分类:物理介导方法:电穿孔法、显微注射和基因枪;化学介导方法:如经典的磷酸钙共沉淀法、脂质体转染方法、和多种阳离子物质介导的技术;生物介导方法:有较为原始的原生质体转染,和现在比较多见的各种病毒介导的转染技术。
理想细胞转染方法,应该具有转染效率高、细胞毒性小等优点。
病毒介导的转染技术,是目前转染效率最高的方法,同时具有细胞毒性很低的优势。
但是,病毒转染方法的准备程序复杂,常常对细胞类型有很强的选择性,在一般实验室中很难普及。
其它物理和化学介导的转染方法,则各有其特点。
需要指出的一点,无论采用哪种转染技术,要获得最优的转染结果,可能都需要对转染条件进行优化。
影响转染效率的因素很多,从细胞类型、细胞培养条件和细胞生长状态到转染方法的操作细节(见后文)。
二、转染操作流程(以常用的6孔板为例)(1) 细胞培养:取6孔培养板,以3x104/cm2密度铺板,37℃5%CO2培养箱中培养至70%~90%汇合。
(不同细胞略有不同,根据实验室优化的条件进行,汇合过分,转染后不利筛选细胞)。
(2) 转染液制备:在EP管中制备以下两液(为转染每一个孔细胞所用的量)A液:用不含血清培养基稀释1-10μg DNA,终量100μL,B液:用不含血清培养基稀释对应量的转染试剂,终量100μL;轻轻混合A、B液(1:1混匀),室温中置15分钟,稍后会出现微浊现象,但并不妨碍转染。
(3) 转染准备:用2mL不含血清培养液漂洗两次,再加入2mL不含血清及PS的培养液。
(4) 转染:把A/B复合物缓缓加入培养液中(缓慢滴加),轻轻摇匀,37℃温箱置6~8小时,吸除无血清转染液,换入正常培养液继续培养。
三、转染注意事项1. 血清A. DNA-阳离子脂质体复合物形成时不能含血清,因为血清会影响复合物的形成。
B.一般细胞对无血清培养可以耐受几个小时没问题,转染用的培养液可以含血清也可以不加,但血清一度曾被认为会降低转染效率,转染培养基中加入血清需要对条件进行优化。
细胞转染的方法和基本原理细胞转染是生物学研究中常用的实验技术,用于将外源DNA、RNA或蛋白质引入到靶细胞中。
本文将介绍细胞转染的方法和基本原理。
一、细胞转染的方法1. 化学法转染:化学法转染是最常用的细胞转染方法之一。
通过利用化学物质如聚乙烯亚胺(PEI)或脂质体等,将外源DNA或RNA 包裹成复合物,与细胞膜结合后进入细胞。
这种方法操作简单、成本低廉,适用于多种细胞类型。
但转染效率较低,对细胞有一定毒性。
2. 病毒载体转染:病毒载体转染是一种高效的细胞转染方法。
病毒载体可以将外源基因嵌入病毒基因组中,然后通过感染细胞的方式将基因导入细胞内。
常用的病毒载体有腺病毒、逆转录病毒等。
这种方法转染效率高,适用于多种细胞类型,但需要特殊设备和技术,同时也有一定的生物安全风险。
3. 电穿孔法转染:电穿孔法利用高压脉冲作用于细胞膜,破坏细胞膜结构,从而使外源DNA或RNA进入细胞。
这种方法操作简单,转染效率较高,但对细胞有一定的毒性,并且只适用于某些特定的细胞类型。
4. 基因枪法转染:基因枪法是一种生理穿孔法,通过利用高压气体或火药驱动基因枪,将外源DNA或RNA以微粒形式直接射入细胞。
这种方法适用于多种细胞类型,转染效率较高,但需要特殊设备和技术,并且对细胞有一定的毒性。
二、细胞转染的基本原理细胞转染的基本原理是通过一定的方法将外源DNA、RNA或蛋白质引入靶细胞,使其在细胞内表达或功能发挥。
转染后的细胞可以用于研究基因功能、蛋白质表达及相互作用等。
细胞转染的基本原理可以分为三个步骤:吸附、内化和表达。
1. 吸附:在化学法转染中,外源DNA或RNA会与载体相结合形成复合物,通过静电作用与细胞膜结合。
在病毒载体转染中,病毒载体会与细胞膜表面的受体结合。
吸附是转染的第一步,直接影响转染效率。
2. 内化:吸附后,外源DNA、RNA或蛋白质需要进入细胞内部。
在化学法转染中,复合物通过细胞膜的内吞作用或直接渗透进入细胞质。
细胞转染方法根据不同的试验目的,外源DNA导入哺乳细胞有两种类型:瞬时转染和稳定转染。
瞬时转染是指外源基因进入受体细胞后,存在于游离的载体上,不整合到细胞的染色体上,在外源基因导入细胞1-4天后收获细胞进行分析;稳定转染需要外源基因整合到细胞的染色体上,从而得到稳定的转染细胞株。
下面介绍几种转染方法:DEAE-葡聚糖:这是早在1965年出现的转染方法。
带正电的DEAE-葡聚糖或polybrene(多聚季胺)多聚体可以结合带负电的DNA分子,使得DNA复合物结合在带负电的细胞表面。
通过使用DMSO或甘油获得的渗透休克,也可能是细胞内吞作用使得DNA复合体进入细胞。
DEAE-葡聚糖仅限于瞬时转染,可重复性好,转染时要除掉血清。
磷酸钙共沉淀转染:最早在1973年开始采用。
氯化钙+DNA+磷酸缓冲液按一定的比例混和,形成极小的磷酸钙-DNA复合物沉淀黏附在细胞膜表面,借助内吞作用进入细胞质。
沉淀颗粒的大小和质量对于转染的成功至关重要,pH值、钙离子浓度、DNA浓度、沉淀反应时间、细胞孵育时间乃至各组分加入顺序和混合的方式都可能对结果产生影响,重复性不佳。
此法较易得到稳定转染,但转染原代细胞比较困难。
电穿孔法:通过短暂的高电场电脉冲处理细胞,沿细胞膜的电压差异会导致细胞膜的暂时穿孔。
DNA被认为是穿过孔扩散到细胞内的。
电脉冲和场强的优化对于成功的转染非常重要,因为过高的场强和过长的电脉冲时间会不可逆地伤害细胞膜而裂解细胞。
理论上说电穿孔法可用于各种细胞,且不需要另外采购特殊试剂,但需要昂贵的电转仪。
此法每次转染需要更多的细胞和DNA,因为细胞的死亡率高。
每种细胞电转的条件都需要进行多次优化。
脂质体法:中性脂质体是利用脂质膜包裹DNA,借助脂质膜将DNA 导入细胞膜内。
带正电的阳离子脂质体则不同,DNA并没有预先包埋在脂质体中,而是带负电的DNA自动结合到带正电的脂质体上,形成DNA-阳离子脂质体复合物,从而吸附到带负电的细胞膜表面,经过内吞被导入细胞。
细胞转染方法比较
细胞转染方法是指将外源基因转入细胞中的一种技术,是细胞基因学
研究的基础。
它具有非常重要的研究意义,可以将DNA、RNA或蛋白质引
入细胞,从而提高研究的准确性,发展基因治疗技术,还可以实现重组技术,在生物医药方面已经发挥了巨大的作用。
常用的细胞转染方法有电穿孔、热穿孔、化学转染、动力转染、质粒
载体转染等,下面就具体介绍这些方法的优缺点及适用条件。
一、电穿孔
电穿孔是将外源DNA用电压转染到细胞表面的一种方法,采用电穿孔
转染时,首先将目的基因与含有盐的溶液混合,然后在细胞上施加脉冲电压,使基因可以透过电穿孔进入细胞。
优点是转染效率高,可以较快地将
基因转染到细胞中,而不会造成细胞的死亡和损伤,并且不需要昂贵的设备。
缺点是转染的时间短,极易受环境条件的影响,转染率往往显著降低,另外,由于电压的作用,细胞表面可能受到副作用,效果不一定很理想。
二、热穿孔
热穿孔是通过改变细胞温度以及外源基因的溶液温度,使膜的稳定性
得到改变,有助于外源基因进入细胞。
优点是转染效率较高,能够获得比
较好的转染效果,且操作简单,易于掌握。
G418筛选稳定表达细胞系经验总结我做了稳定转染,从G418浓度确定到最后的单克隆化鉴定。
有自己的体会也有其他战友遇到的情况, 和大家分享. 没有总结好的地方,大家补充。
筛选之前确定G418浓度:1、由于每种细胞对G418的敏感性不同,而且不同的厂家生产的G418有效成分的比重不同,一般1g的粉剂中有效的G418含量大约为0.722g。
2、G418是新霉素的类似物,两者都是通过抑制核糖体的功能和蛋白质的合成而杀死细胞的。
但是新霉素对真核细胞无作用而G418对细菌和真核细胞都起作用。
neo就是编码3‘磷酸转移酶的基因,它表达的蛋白能够分解新霉素G418。
在进行转染时细胞膜受到影响,抗生素可能对细胞产生较大影响,加上G418有杀菌作用,所以有人主张转转染时不加其它抗生素。
3、汇合度对G418筛选结果的影响很大,一般筛选时汇合度不宜超过50%4,G418的活性不尽相同,所以在筛选之前,一定要确定G418的最佳筛选浓度。
具体如下:将细胞稀释到1000个细胞/ml,在100ug/ml~1mg/ml的G418浓度范围内进行筛选,选择出在10~14天内使细胞全部死亡的最低G418浓度来进行下一步的筛选试验。
一个具体试验:3x106个细胞电转后,分别接种1/4000,1/1000,1/300细胞到24孔板中,48h后加药筛选,此时1/300细胞孔内大约50%汇合度。
理论上1/4000孔内应有4%的汇合度。
筛选9天后,观察1/4000孔内有两三个克隆,按比例1/300孔内应该有几十个克隆,事实上,它们几乎全死光了,只有几个克隆。
加药时间和维持浓度1,由于基因转染到细胞内之后要一段时间才能表达出蛋白质。
所以筛选不能太早;但是也不能太晚,因为转染了外源基因的细胞代谢负荷较大,增值较慢,时间长了就会被没有外源基因转入的细胞所淹没,最终导致筛选不出阳性克隆,一般要在转染24小时之后才开始加G418筛选。
随着细胞的代谢G418的浓度和活性都会下降,所以每3~5天都要更换一次含有G418的筛选液。