高考化学一轮复习化学计量与化学计算
- 格式:doc
- 大小:309.00 KB
- 文档页数:6

专题02 化学计量和化学计算2021年化学高考题一、单选题1.(2021·山东高考真题)X 、Y 均为短周期金属元素,同温同压下,0.1molX 的单质与足量稀盐酸反应,生成H 2体积为V 1L ;0.1molY 的单质与足量稀硫酸反应,生成H 2体积为V 2L 。
下列说法错误的是A .X 、Y 生成H 2的物质的量之比一定为12V VB .X 、Y 消耗酸的物质的量之比一定为122V VC .产物中X 、Y 化合价之比一定为12V VD .由12V V 一定能确定产物中X 、Y 的化合价2.(2021·浙江高考真题)设A N 为阿伏加德罗常数的值,下列说法不正确...的是A .标准状况下,1821.12L O 中含有中子数为A NB .431g P (分子结构:)中的共价键数目为A 1.5NC .1100mL0.1mol L -⋅的NaOH 水溶液中含有氧原子数为A 0.01ND .18.9g 三肽63334C H N O (相对分子质量:189)中的肽键数目为A 0.2N3.(2021·全国高考真题)A N 为阿伏加德罗常数的值。
下列叙述正确的是A .18g 重水(2D O )中含有的质子数为A 10NB .3mol 的2NO 与2H O 完全反应时转移的电子数为A 4NC .32g 环状8S ()分子中含有的S-S 键数为A 1ND .1L pH=4的-12270.1mol L K Cr O ⋅溶液中2-27Cr O 离子数为A 0.1N4.(2021·广东)设A N 为阿伏加德罗常数的值。
下列说法正确的是A .31mol CHCl 含有C Cl -键的数目为A 3NB .1L1.0mol/L 的盐酸含有阴离子总数为A 2NC .11.2L NO 与211.2L O 混合后的分子数目为A ND .23g Na 与足量2H O 反应生成的2H 分子数目为A N5.(2021·河北高考真题)N A 是阿伏加德罗常数的值,下列说法错误的是A .22.4L(标准状况)氟气所含的质子数为18N AB .1mol 碘蒸气和1mol 氢气在密闭容器中充分反应,生成的碘化氢分子数小于2N AC .电解饱和食盐水时,若阴阳两极产生气体的总质量为73g ,则转移电子数为N AD .1L1mol•L -1溴化铵水溶液中NH 4+与H +离子数之和大于N A6.(2021·湖南高考真题)A N 为阿伏加德罗常数的值。

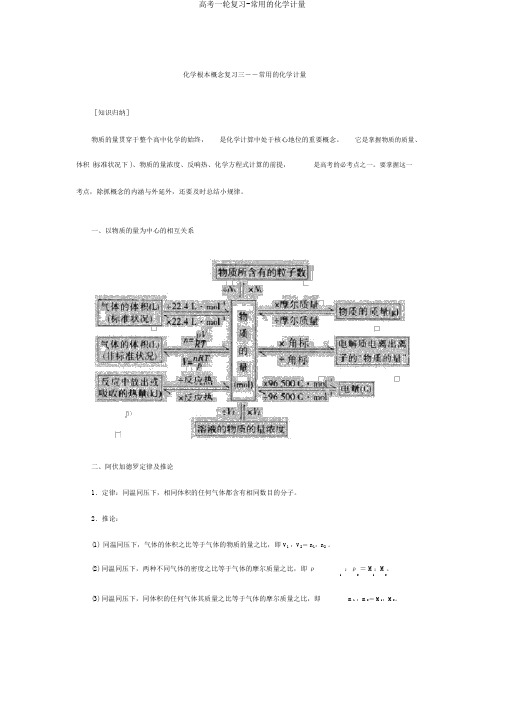
化学根本概念复习三――常用的化学计量[知识归纳]物质的量贯穿于整个高中化学的始终,是化学计算中处于核心地位的重要概念。
它是掌握物质的质量、体积 (标准状况下 )、物质的量浓度、反响热、化学方程式计算的前提,是高考的必考点之一。
要掌握这一考点,除抓概念的内涵与外延外,还要及时总结小规律。
一、以物质的量为中心的相互关系二、阿伏加德罗定律及推论1.定律:同温同压下,相同体积的任何气体都含有相同数目的分子。
2.推论:(1)同温同压下,气体的体积之比等于气体的物质的量之比,即V1:V2= n1:n2。
(2) 同温同压下,两种不同气体的密度之比等于气体的摩尔质量之比,即ρ1:ρ= M:M。
212(3) 同温同压下,同体积的任何气体其质量之比等于气体的摩尔质量之比,即m1:m2= M1:M2。
(4) 同温同下,同量任何气体的体之比等于其摩量倒数之比,即V1: V2=M2:M1。
(5) 同温同体下,气体的之比等于气体的物的量之比:P1: P2== n1:n2。
三、物的量与气体平均相分子量之的算1.(m 气体量,n 气体物的量) (此公式也适合非气物)2.混合气体的体分数或摩分数求平均相分子量。
其中 M A、M B、⋯⋯,分气体的相分子量;a%、b%、⋯⋯,分气体的体分数或摩分数。
3.其中ρ 气体在准状况下的密度。
4.其中 D 相对混合气体某已气体的相密度,M 气体的相分子量。
四、物的量度及有关算原理1.关于物的量度概念的算主要包括:(1)溶的量、溶液的体和物的量度之的算。
可运用公式:n= m/M ,c= n/V ,所以。
(2)气体溶的体(准状况下 )、溶的体和溶液的密度,算溶液中溶的物的量度。
先运用 n=V/22.4L ·mol —1,求出溶的物的量;再运用V 〔溶液〕= m/ρ求出溶液的体,其中m 气体和水的量和,即溶液的量,ρ 溶液的密度,V〔溶液〕的位L ;最后用物的量度公式算。
(3)算溶液中的离子度,要根据溶的离方程式,算出离子的物的量。

第8讲 化学计算的常用方法[课程标准] 1.进一步理解物质的量在化学计算中的“桥梁作用”。
2.了解化学计算的常用方法。
3.初步建立化学计算的思维模型。
方法一 关系式法的应用关系式是表示两种或多种物质之间量的关系的一种简化的式子。
在多步反应中,它可以把始态的反应物与终态的生成物之间量的关系表示出来,将多步计算简化为一步计算。
高考题量大、时间紧,对于涉及多步计算问题,如滴定试验的有关计算,奇异运用关系式法,可大大缩短答题时间。
BaCrO 4常用于制备颜料、陶瓷、玻璃、平安火柴等。
为了测定某铬酸钡样品中BaCrO 4的含量,进行如下试验:w g 样品――→过量HI 溶液盐酸I 2、Cr 3+、Ba 2+、Cl -――――――――――――――――――→V mL c mol ·L -1 Na 2S 2O 3标准液终点已知:杂质不参加反应;滴定反应为I 2+2S 2O 2-3 ===2I -+S 4O 2-6 。
(1)写出BaCrO 4与过量HI 溶液反应的离子方程式: _。
(2)BaCrO 4的摩尔质量为M g ·mol -1,则样品中BaCrO 4的质量分数为 %(用代数式表示)。
[解题导引]分析流程中的物质信息 ―→确定产物 ―→依据得失电子配平 ―→找出已知量和目标量 ―→找出关系式 ―→进行计算解析: 依据题示信息,BaCrO 4中+6价Cr 元素被还原成Cr 3+,HI 中I -被氧化成I 2,依据得失电子守恒配平离子方程式2BaCrO 4+6I -+16H +===2Ba 2++2Cr 3++3I 2+8H 2O ,由滴定反应知, 2BaCrO 4~3I 2~6Na 2S 2O 3,3n (BaCrO 4)=n (Na 2S 2O 3),则样品中BaCrO 4的质量分数为cVM 1 000×3w ×100%=cVM30w%。
答案: (1)2BaCrO 4+6I -+16H +===2Ba 2++2Cr 3++3I 2+8H 2O (2)cVM30w归纳总结学生用书第37页归纳总结对点练1.测定K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)中铁的含量。


第1课时 化学入门——化学常用计量知识点一 物质的量、摩尔质量1.物质的量、阿伏加德罗常数 (1)基本概念间的关系[提醒] “物质的量”的计量对象是微观粒子(如:分子、原子、离子、原子团、质子、中子、电子等),而不是宏观物质。
(2)“物质的量”的表示方法如:1 mol Fe 、1 mol O 2、1 mol Na +。
[提醒] 物质的量(n )、粒子数(N )、阿伏加德罗常数(N A )之间的关系:n =NN A。
2.摩尔质量(1)概念:单位物质的量的物质所具有的质量。
符号:M ,单位:g·mol -1。
(2)数值:当粒子的摩尔质量以g·mol -1为单位时,在数值上等于该粒子的相对分子(或原子)质量。
(3)关系:物质的量(n )、质量(m )与摩尔质量(M )之间的关系为n =m M 。
(4)计算方法①根据标准状况下气体的密度(ρ):M =ρ×22.4 L·mol -1。
如:标准状况下某气体的密度为1.429 g·L -1,则该气体的M =32_g·mol -1。
②根据气体的相对密度⎝⎛⎭⎫D =ρ1ρ2:M1M 2=D 。
如:某气体对甲烷的相对密度为4,则该气体的M =64_g·mol -1。
③根据物质的质量(m )和物质的量(n ):M =mn 。
如:0.5 mol 某气体的质量是22 g ,则该气体的M =44_g·mol -1。
④根据一定质量(m )的物质中粒子数目(N )和阿伏加德罗常数(N A ):M =N A · mN 。
如:45 g乳酸中含乳酸的分子数为3.01×1023,则乳酸的摩尔质量为90_g·mol -1。
[对点训练]1.判断正误(正确的打“√”,错误的打“×”)。
(1)0.012 kg 12C 中含有的碳原子数约为6.02×1023个(√) (2)7.8 g Na 2O 2中含有的阴离子数为0.2N A (×) (3)1 mol NaCl 和1 mol HCl 含有相同的粒子数目(×) (4)1 mol OH -的质量是17 g·mol -1(×)(5)22 g CO 2中含有的氧原子数为N A (√)(6)常温常压下,14 g 乙烯和丙烯的混合物中含有的氢原子数目为2N A (√) 2.在0.5 mol Na 2SO 4中含有的离子的个数和氧原子的质量分别是( ) A .1.5N A 2 mol B .1.5N A 32 g C .3.01×1023 4 molD .N A 64 g解析:选B 0.5 mol Na 2SO 4中含有的离子数为0.5×3N A =1.5N A ,含氧原子的物质的量为0.5 mol ×4=2 mol ,质量为2 mol ×16 g·mol -1=32 g 。
化学计量法和化学计算化学计量法和化学计算是化学领域中重要的计算方法和技巧,用于研究化学反应过程中物质的量和比例关系。
通过精确的计量和计算,可以帮助化学家预测反应的产率、计算摩尔量以及确定反应的平衡状态。
本文将介绍化学计量法和化学计算的基本概念和应用。
一、化学计量法的概念和原理化学计量法是通过化学反应中的物质的量关系,计算和推导出其他物质的量的方法。
其基本原理是以反应方程式中的化学计量关系为基础进行计算。
化学计量法的应用领域广泛,包括化学合成、分析化学以及确定元素的相对原子质量等。
在化学计量法中,常用的计量单位是摩尔。
摩尔是物质量的计量单位,用化学计量单位的摩尔质量表示。
化学计量法通过化学方程式中的化学计量关系以及已知物质的质量或化学计量关系推导未知物质的质量。
化学计量法的基本步骤包括确定所需计算的物质、编写反应方程式、确定已知和未知物质的质量以及根据化学计量关系计算出未知物质的质量。
例如,已知某化学反应中产生了1 mol的H2O,需要计算反应中产生的CO2的摩尔量,可以通过已知的化学计量关系计算出。
二、化学计算的应用化学计算在化学领域中具有广泛的应用,以下将介绍一些常见的应用。
1. 反应产率的计算反应产率是指化学反应中实际产生的物质在理论上可以产生的最大量之比。
通过化学计量法可以根据已知物质的质量和反应的化学计量关系计算反应产率。
2. 摩尔质量的计算摩尔质量是指物质1摩尔的质量,通常以g/mol表示。
通过已知物质的质量和化学计量关系,可以计算出未知物质的摩尔质量。
3. 反应平衡的计算在化学反应中,反应物和产物之间存在一定的比例关系,即反应平衡。
通过化学计算可以确定反应平衡时各个物质的摩尔量,并帮助化学家预测反应的方向和平衡常数。
4. 结晶水的计算结晶水是某些物质中结合的水分子,通过化学计量法可以计算出物质中结晶水的摩尔量。
例如,通过质量差异可以计算出固体物质中结晶水的摩尔量,进而确定物质的化学组成。
2019年高考化学一轮综合复习第一章化学计量在实验中的应用专题讲座一化学计算的常用方法练习编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(2019年高考化学一轮综合复习第一章化学计量在实验中的应用专题讲座一化学计算的常用方法练习)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为2019年高考化学一轮综合复习第一章化学计量在实验中的应用专题讲座一化学计算的常用方法练习的全部内容。
专题讲座一化学计算的常用方法方法一电解质溶液的计算法宝——电荷守恒法涉及溶液中离子浓度的计算时常需用到电荷守恒,首先找出溶液中所有阳离子和阴离子,再根据阳离子所带正电荷总数等于阴离子所带负电荷总数列等式。
如Al2(SO4)3、NH4NO3混合溶液的电荷守恒为3c(Al3+)+c(NH+,4)+c(H+)=2c(SO错误!)+c(NO错误!)+c(OH-)。
注意一般情况下,列电荷守恒等式时不能忽略H+、OH-,但在计算时,酸性溶液中常可忽略OH-,碱性溶液中常可忽略H+。
针对训练1.(2017·开封模拟)在硫酸钠和硫酸铝的混合溶液中,Al3+的物质的量浓度为0.2mol·L-1,SO错误!为0.4mol·L-1,溶液中Na+的物质的量浓度为( )A.0。
1mol·L-1B.0。
2mol·L-1C.0。
3mol·L-1D.0。
4mol·L-1答案B解析在任何溶液中,阳离子所带的正电荷总数等于阴离子所带的负电荷总数,则有3c(Al3+)+c(Na+)=2c(SO2-,4),解得c(Na+)=0。
化学计量与化学计算
1.已知N A 是阿伏加德罗常数的值,下列说法错误的是
A .3 g 3He 含有的中子数为1N A
B .1 L 0.1 mol·L −1磷酸钠溶液含有的34PO -
数目为0.1N A
C .1 mol K 2Cr 2O 7被还原为Cr 3+转移的电子数为6N A
D .48 g 正丁烷和10 g 异丁烷的混合物中共价键数目为13N A 【答案】B
【解析】A .3He 的中子数为3-2=1,则3g 3He 的中子数为=N A ,A 项正确; B .磷酸钠为强碱弱酸盐,磷酸根离子在水溶液中会发生水解,则1L 0.1mol/L 的磷酸钠溶液中磷
酸根离子的个数小于1L×
0.1mol/L×N A mol -1 =0.1N A ,B 项错误; C .重铬酸钾被还原为铬离子时,铬元素从+6降低到+3,
1mol 重铬酸钾转移的电子数为3mol×2×N A mol -1 =6N A ,C 项正确;
D .正丁烷与异丁烷的分子式相同,1个分子内所含共价键数目均为13个,则48g 正丁烷与10g 异丁烷所得的混合物中共价键数目为48g+10g 58g/mol ×13×N A mol -1 =13N A ,D 项正确; 答案选B 。
2.设N A 为阿伏加德罗常数值。
关于常温下pH=2的H 3PO 4溶液,下列说法正确的是
A .每升溶液中的H +数目为0.02N A
B .c (H +)= c (42H PO -)+2c (24HPO -)+3c (34PO -
)+ c (OH −)
C .加水稀释使电离度增大,溶液pH 减小
D .加入NaH 2PO 4固体,溶液酸性增强 【答案】B
【解析】A 、常温下pH =2,则溶液中氢离子浓度是0.01mol/L ,因此每升溶液中H +数目为0.01N A ,
A 错误;
B 、根据电荷守恒可知选项B 正确;
C 、加水稀释促进电离,电离度增大,但氢离子浓度减小,pH 增大,C 错误;
D 、加入NaH 2PO 4固体,H 2PO 4-浓度增大,抑制磷酸的电离,溶液的酸性减弱,D 错误;。