烯烃的命名和同分异构体
- 格式:ppt
- 大小:315.00 KB
- 文档页数:7



烯烃》总结1.烯烃:分子里含有键的一类链烃叫烯烃。
一般,我们所说的烯烃都是指分子中只含一个碳碳双键的不饱和烃,所以也叫单烯烃,还有二烯烃,如CH2=CH—CH=CH2(丁二烯)。
2.烯烃的通式:CH2(n>2,其中有个C-H键,个C=C双键,个n2nC-C单键。
注意:环烷烃的通式与烯烃的通式相同,故通式为CH2的烃不一定是烯烃,如下图中的环丁烷n2n的分子式也符合CH O3.烯烃的系统命名法:命名方法与烷烃相似,坚持最长、最近、最简、最小原则。
不同点是主链必须含有双键。
(1)选主链:选含C=C的最长的碳链,称某烯。
2)编号:从离双键最近(不是离取代基最近)的主链碳的一端开始编号,当主链两端的碳原子离双键等近时,要求从离简单取代基近的一端开始编号,且要求取代基位次和要小。
(3)命名:取代基编号-取代基一双键位置编号+某。
CH:-CI1—CH2-C=CH2例:a.右出L HL、CH$-f=CH-fH—b.匚印CHx:O4.烯烃的物理性质:(1)常温常压下,C个数为1-4的烯烃为气态,C个数为5-18的烯烃为液态,C个数为18以上的烯烃为固态。
(2)随碳原子数增多,熔沸点逐渐升高;碳原子数相同的烯烃,支链越多,熔沸点越低。
(3)碳原子数增多,密度逐渐增大。
5.烯烃的化学性质:(1)氧化反应:a. __________________________________________ 燃烧反应:Ob.在催化剂作用下被空气氧化生成醛:c.被氧化剂(如酸性KMnO4溶液、臭氧等)氧化:d.臭氧分解反应(常以信息题形式出现):O(2)易发生加成反应:可以和碳碳双键加成试剂有为H2、HCN、X2、HX、H2O等。
:-222-G——C-f一般用怖作加單的催化剂)6.烯烃的不对称加成:一般遵循马尔科夫尼科夫规则,简称马氏规则。
马氏规则:当不对称 烯烃与卤化氢发生加成反应时,通常氢加到氢多的不饱和碳原子上。
C^-C-C^-C^+甘出一如匾.CHi-CH^CHz-FHzO —7.1,3—丁二烯(CH 2=CH —CH=CH 2)的加成反应:二烯烃的通式为C n H 2n _^,其化学性质与烯烃相似,在加成反应时有多种情况:(1) ______________________________________________________________ 1,2—加成:CH 2=CH —CH=CH 2+Br 2_。

有机化合物的命名与结构一、有机化合物的命名:1.烷烃命名:选取最长碳链为主链,从离支链近的一端给主链上的碳原子进行编号,支链最多为主链,支链编号之和最小。
2.烯烃命名:选取含双键的最长碳链为主链,从离双键近的一端给主链上的碳原子进行编号,双键位置用字母表示。
3.炔烃命名:选取含三键的最长碳链为主链,从离三键近的一端给主链上的碳原子进行编号,三键位置用字母表示。
4.卤代烃命名:选取含卤素的最长碳链为主链,从离卤素近的一端给主链上的碳原子进行编号,卤素位置用字母表示。
5.醇命名:选取含羟基的最长碳链为主链,从离羟基近的一端给主链上的碳原子进行编号,羟基位置用字母表示。
6.醚命名:根据醚键的位置给主链上的碳原子进行编号,编号从距离醚键近的一端开始。
7.酮命名:选取含酮基的最长碳链为主链,从离酮基近的一端给主链上的碳原子进行编号,酮基位置用字母表示。
8.羧酸命名:选取含羧基的最长碳链为主链,从离羧基近的一端给主链上的碳原子进行编号,羧基位置用字母表示。
二、有机化合物的结构:1.烷烃结构:碳原子之间以单键相连,形成直链或分支链状结构。
2.烯烃结构:含有碳碳双键,双键两端的碳原子连接其他原子或基团。
3.炔烃结构:含有碳碳三键,三键两端的碳原子连接其他原子或基团。
4.卤代烃结构:含有卤素原子,卤素原子连接在碳原子上。
5.醇结构:含有羟基,羟基连接在碳原子上。
6.醚结构:含有醚键,醚键连接两个碳原子。
7.酮结构:含有酮基,酮基连接在碳原子上。
8.羧酸结构:含有羧基,羧基连接在碳原子上。
9.有机化合物的立体结构:包括顺式和反式结构,以及立体异构体等。
通过以上知识点,学生可以掌握有机化合物的命名方法和结构特点,为深入学习有机化学打下基础。
习题及方法:1.习题:将下列化合物命名:CH3-CH2-CH=CH-CH3方法:这是一个烯烃,选取含双键的最长碳链为主链,共有5个碳原子,双键在2号和3号碳原子之间,从离双键近的一端给主链上的碳原子进行编号,得到名称为2-戊烯。

第三章烯烃
一、写出烯烃C6H12的所有同分异构体,命名之,并指出那些有顺反异构体。
解:CH2=CHCH2CH2CH2CH3 CH3CH=CHCH2CH2CH3有顺反异构
CH3CH2CH=CHCH2CH3 有顺反异构
2,3-二甲基- 2,3-二甲基- 3,3-二甲基-
-1-丁烯-2-丁烯-丁烯
-1-丁烯
3-甲基-1-戊烯 3-甲基-2-戊烯有顺反异构
2-甲基-1-戊烯 2-甲基-2-戊烯 4-甲基-2-戊烯有顺反异构
4-甲基-1-戊烯
二、写出下列各基团或化合物的结构式:
1 ①乙烯基 CH2=CH- ② 丙烯基 CH3CH=CH- ③ 烯丙基CH2=CHCH2-
④异丙烯基
⑤4-甲基-顺-2-戊烯
⑥ (E)-3,4-二甲基-3-庚烯
⑦(Z)-3-甲基-4-异丙基-3-庚烯
三、命名下列化合物,如有顺反异构现象,写出顺反(或)Z-E名称:2-乙基-1-戊烯
(E)-3,4-二甲基-3-庚烯
(E)-2,4-二甲基-3-氯-3-己烯
(Z)-1-氟-2-氯-溴-1-碘乙烯
反-5-甲基-2-庚烯
(E)-3,4-二甲基-5-乙基-3-庚烯
(E)-3-甲基-4-异丙基-3-庚烯
(E)-3,4-二甲基-3-辛烯
四、(略)
五、2,4-庚二烯有否顺反异构现象,如有,写出它们的所有顺反异构体,并以顺反和Z,E两种命名法命名之。
解:
顺,顺-2-4-庚二烯(Z,Z)-2-4-庚二烯
顺,反-2-4-庚二烯(Z,E)-2-4-庚二烯
反,顺-2-4-庚二烯(E,Z)-2-4-庚二烯
反,反-2-4-庚二烯
(E,E)-2-4-庚二烯。


课时:2课时教学目标:1. 让学生掌握烯烃的结构、命名、同分异构体及化学性质。
2. 培养学生分析问题、解决问题的能力,提高学生的实验操作技能。
3. 增强学生的环保意识,关注有机化学在环境保护中的应用。
教学内容:1. 烯烃的结构与性质2. 烯烃的命名3. 烯烃的同分异构体4. 烯烃的化学性质教学重点:1. 烯烃的结构与性质2. 烯烃的化学性质教学难点:1. 烯烃的命名2. 烯烃的同分异构体教学过程:一、导入新课1. 回顾有机化学基础知识,引出烯烃的概念。
2. 简要介绍烯烃在有机合成和工业生产中的应用。
二、烯烃的结构与性质1. 讲解烯烃的结构特点,如碳碳双键、sp2杂化等。
2. 分析烯烃的性质,如不饱和性、亲电性等。
3. 结合实例,讲解烯烃的物理性质,如熔点、沸点、溶解性等。
三、烯烃的命名1. 介绍烯烃的命名原则,如主链选择、编号等。
2. 讲解烯烃的命名方法,如直链烯烃、支链烯烃等。
3. 通过实例,让学生掌握烯烃的命名技巧。
四、烯烃的同分异构体1. 讲解烯烃的同分异构体类型,如碳链异构、位置异构、顺反异构等。
2. 分析烯烃同分异构体的产生原因。
3. 通过实例,让学生掌握烯烃同分异构体的判断方法。
五、烯烃的化学性质1. 讲解烯烃的亲电加成反应,如卤化氢、水、卤化氢酸等。
2. 讲解烯烃的自由基加成反应,如卤化氢的加成反应。
3. 讲解烯烃的氧化反应,如高锰酸钾氧化、臭氧化反应等。
4. 讲解烯烃的聚合反应。
六、课堂小结1. 总结烯烃的结构、命名、同分异构体及化学性质。
2. 强调烯烃在有机合成和工业生产中的应用。
七、课后作业1. 完成课后习题,巩固所学知识。
2. 查阅资料,了解烯烃在环境保护中的应用。
教学反思:本节课通过讲解烯烃的结构、命名、同分异构体及化学性质,使学生掌握了烯烃的基本知识。
在教学过程中,注重理论联系实际,提高学生的实验操作技能。
同时,引导学生关注有机化学在环境保护中的应用,培养学生的环保意识。

烯烃的同分异构体引言烯烃是一类含有碳-碳双键的有机化合物。
由于双键的存在,烯烃分子可以发生同分异构,即同一分子式但结构不同的同分异构体形成。
同分异构体的存在增加了有机化学的复杂性和多样性,对于理解化学反应、性质以及应用具有重要意义。
本文将重点介绍烯烃的同分异构现象。
同分异构的定义和原因同分异构是指分子式相同但结构不同的化合物之间的关系。
在烯烃中,同分异构的主要原因是双键的位置和立体构型的不同。
烯烃中的双键可以出现在不同的碳原子上,即可以是1-烯烃或2-烯烃。
例如,对于丁烯(C4H8)来说,可以存在1-丁烯和2-丁烯两种同分异构体,它们的双键位置不同。
此外,烯烃还可以存在立体异构体。
这是由于在碳-碳双键周围存在自由旋转的限制,使得烯烃分子可以固定在不同的立体构型中。
比如,2-丁烯可以存在顺式异构体和反式异构体两种不同的立体构型。
同分异构体的举例1.丁烯的同分异构体:–1-丁烯:CH2=CHCH2CH3–2-丁烯:CH3CH=CHCH32.戊烯的同分异构体:–1-戊烯:CH2=CHCH2CH2CH3–2-戊烯:CH3CH=CHCH2CH3–3-戊烯:CH3CH2CH=CHCH33.辛烯的同分异构体:–1-辛烯:CH2=CH(CH2)6CH3–2-辛烯:CH3(CH2)4CH=CHCH3这些同分异构体的存在使得烯烃化合物具有不同的化学性质和反应活性。
例如,1-丁烯在水中容易发生加成反应,而2-丁烯则更容易发生异构反应。
同分异构体的应用同分异构体的存在对于有机化学的研究和应用具有重要意义。
首先,通过研究同分异构体的不同性质和反应行为,可以深入理解化学反应的机理和活性。
同一分子式但不同结构的同分异构体对于反应速率、选择性和产物分布等方面的影响提供了重要参考。
其次,同分异构体的存在使得有机合成有更多的选择。
在有机合成中,可以选择不同的同分异构体来合成目标化合物,从而达到更高的产率和选择性。
最后,同分异构体在天然产物领域有重要的应用。
第三节乙烯烯烃●教学目的:1、了解乙烯的物理性质和主要用途,掌握乙烯的化学性质和实验室制法。
2、使学生了解加成反应和聚合反应以及不饱和烃的概念。
3、使学生了解烯烃在组成、结构、主要化学性质上的共同点,以及物理性质随碳原子数的增加而变化的规律。
●教学重点:乙烯的化学性质。
●教学难点:乙烯的结构以及与化学性质的关系。
教学过程:[引入]何谓烷烃?其通式如何?它属于何类烃?(饱和链烃)与此相对应就应该有不饱和烃。
另外有机物之所以种类繁多,除了存在大量的同分异构现象,在有机物中碳原子除了可以形成C —C ,还可能形成或—C ≡C —,从而使得碳原子上的氢原子数少于饱和链烃里的氢原子数。
这样的烃叫做不饱和烃。
[板书]不饱和烃:烃分子里含有碳碳双键或碳碳三键,碳原子所结合的氢原子数少于饱和链烃里的氢原子数,这样的烃叫做不饱和烃。
[讲解] 根据烃分子中碳原子的连接方式不同,烃可以分为如下类别:饱和烃——烷烃链烃烯烃烃不饱和烃炔烃环烃[过渡]今天我们来学习最简单的烯烃——乙烯。
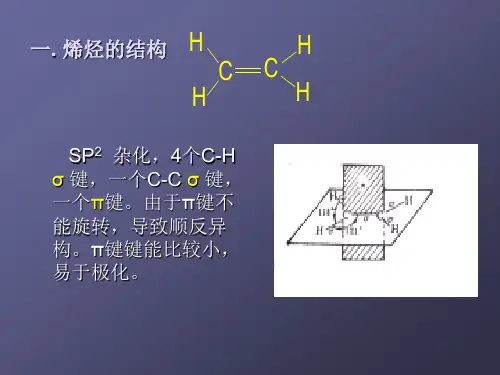
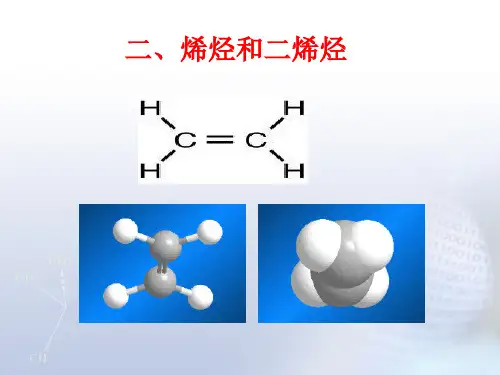
一、乙烯来源及用途 C C二、乙烯的分子组成和结构1、[设问]:(1)把乙烷C 2H 6中H 原子去掉两个就变成了乙烯C 2H 4,根据每个原子通过共用电子对达到饱和的原理,试推导C 2H 4中共价键是怎样组成的? 电子式:分子式:C 2H 4 最简式:CH 2 结构简式:CH 2=CH 2 结构式:(2)展示乙烯和乙烷的球棍模型,对比两者有何不同?2、[[设问](1)乙烯中C==C 双键可否认为是两个C —C 的加和?不能,因为C==C 键能小于C —C 单键键能的2倍,615<2×384=768 (2)通过键能大小来看,乙烯和乙烷哪个化学性质较活泼?C C H H H H乙烯为平面分子,键角为120°,“C==C”中有一个碳碳键等同于C—C,叫δ键,另一个碳碳键键能小于C—C,叫π键,π键稳定性较差。
因此乙烯的化学性质较为活泼,表现为“C==C”中有一个碳碳键易断裂........。
第三章 烯 烃不饱和烃是指分子中含有碳碳重键(碳碳双键或碳碳叁键)的碳氢化合物,分子中含有碳碳双键的烃称为烯烃,根据分子中所含双键的数目又可分为单烯烃、二烯烃和多烯烃;分子中含有碳碳叁键的烃称为炔烃。
碳碳双键和碳碳叁键分别是烯烃和炔烃的官能团。
3.1 烯烃的构造和命名与烷烃相似,含有四个和四个以上碳原子的烯烃都存在碳链异构,如:CH 2=CHCH 2CH 31-丁烯 异丁烯与烷烃不同的是,烯烃分子中存在双键,在碳骨架不变的情况下,双键在碳链中的位置不同,也可产生异构体,如下式中的1-丁烯和2-丁烯,这种异构现象称为官能团位置异构。
CH 2=CHCH 2CH 3 CH 3CH=CHCH 31-丁烯 2-丁烯碳链异构和官能团位置异构都是由于分子中原子之间的连接方式不同而产生的,所以都属于构造异构。
另外,含相同碳原子数目的单烯烃和单环烷烃也互为同分异构体,例如丙烯和环丙烷、丁烯与环丁烷和甲基环丙烷等,它们也属于构造异构体。
烯烃的系统命名法基本上与烷烃相似,其要点是:(1)首先选择含有双键的最长碳链作为主链,按主链中所含碳原子的数目命名为某烯。
主链碳原子数在十以内时用天干表示,如主链含有三个碳原子时,即叫做丙烯;在十以上时,用中文字十一、十二、……等表示,并在烯之前加上碳字,如十二碳烯。
(2)给主链编号时从距离双键最近的一端开始,侧链视为取代基,双键的位次须标明,用两个双键碳原子位次较小的一个表示,放在烯烃名称的前面。
(3)其它同烷烃的命名规则。
3,5 -二甲基-2-己烯 3,3-二甲基-1-戊烯 3-甲基-2-乙基-1-丁烯 3-甲基环己烯烯烃去掉一个氢原子后剩下的一价基团称为某烯基,烯基的编号自去掉氢原子的碳原子开始。
如:CH 2=CH- CH 3CH=CH- CH 2=CHCH 2-乙烯基 1-丙烯基(丙烯基) 2-丙烯基(烯丙基)3.2.烯烃的顺反异构与烷烃不同,由于双键不能自由旋转,所以当两个双键碳原子各连有两个不同的原子或基团时,可能产生两种不同的空间排列方式。