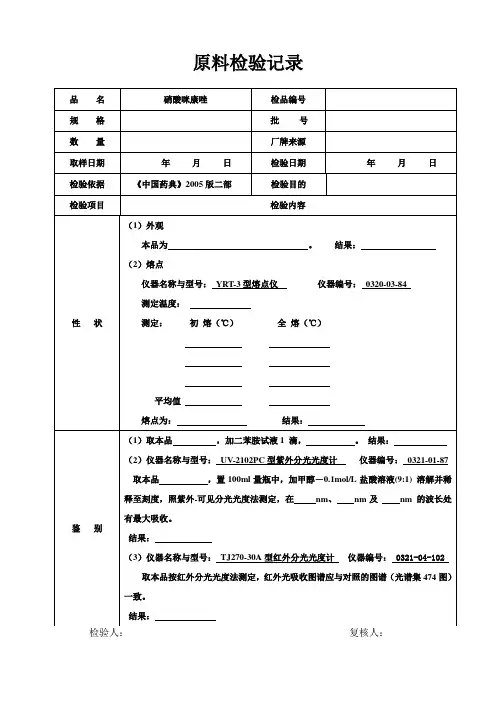
硝酸咪康唑乳膏成品检验标准操作规程
- 格式:doc
- 大小:36.50 KB
- 文档页数:3
目的:建立硝酸咪康唑软膏的生产工艺规程。
范围:硝酸咪康唑软膏的生产。
职责:生产管理部、质量管理部、车间主任、班长、工艺员、操作工、QA。
规程:1.品名、剂型与处方依据1.1通用名称:硝酸咪康唑软膏汉语拼音:Xiaosuan Mikangzuo Ruangao英文名:Miconazole Nitrate Ointment1.2 剂型:软膏剂1.3 处方与处方依据项的说明1.3.1批量产品的工艺处方(制成10000支量):硝酸咪康唑 2030g 二甲基亚砜 6000g 单硬酯酸甘油酯 8000g 十八醇 6000g 白凡士林 5000g 液体石蜡 8000g 平平加O 3500g甘油 10000g 乙醇 2000ml 羟苯乙酯 100g 玫瑰香精 100ml 纯化水 51.5kg1.3.2 处方依据项说明:药品的生产批文:批准时间:质量标准编号:2.工艺流程示意图:检验 →↓ →← 中间产品检验→← 成品检验3.生产工艺操作要求、工艺技术参数: 3.1配制:3.1.1配料操作工按照“软(乳)膏剂、凝胶剂配制岗位标准操作规程”SOP-MN/Z-(R )-001-00规定,在油相缸中加入处方量的单硬脂酸甘油脂、十八醇、白凡士林、液体石蜡加热至全熔,加入平平加O ,熔解保温至94℃左右。
3.1.2在水相缸中加入聚山梨酯—80、甘油、羟苯乙酯溶液(用乙醇溶解)、纯化水加热至沸腾,过滤、降温到95℃。
3.1.3先后将水相、油相抽入到真空乳化机内,以80~100次/分钟的速度搅拌至75℃时,加入硝酸咪康唑,加入玫瑰香精,搅拌至冷却即得。
3.2中间品检验:检验室按“中间产品取样操作规程”规定,抽取配制好的膏体进行中间产品的检验。
检验合格后,发放“中间产品合格证”。
3.3灌装、封尾:接到“中间产品合格证”后,车间按“软(乳)膏剂灌封岗位标准操作规程”SOP-MN/Z-(R )-002-00的要求,进入灌封工序。
封尾时随时抽检,注意剔除不合格品。


第7卷第11期 总第79期 二〇〇九年十一月•己丑年148[16] 王晶娟,张贵君,周群,等.聚类分析法在快速鉴别中药牵正散中的应用[J].计算机与应用化学,2007,24(8):1043-1046.[17] 刘名扬,赵景红,王洪艳,等.偏最小二乘-近红外透射光谱法用于秦皮中多组分测定的研究[J].检验检疫科学,2008,18(1):21-23.[18] 王天志,叶利明,陈聪,等.近红外漫反射光谱法测定川产黄柏中小檗碱含量[J].光谱学与光谱分析,2008,27(8):1527-1530.[19] 赵玉清,杨天鸣,罗源,等.近红外透射光谱法测定黄芪提取液中总皂苷含量[J].化学与生物工程,2009,26 (2):73-75.[20] 虞科,胡楚楚,程翼宇.近红外光谱法测定复方丹参滴丸中的3种有效成分[J].中国药学杂志, 2006, 41(3):226-229.[21] 李艳英,白雁,陈志红,等.近红外漫反射光谱法测定不同厂家一清颗粒的含量[J].药物分析杂志,2009,29(7):1126-1129.[22] 王宁,傅春华,周爱敏,等.近红外漫反射光谱法直接测定小儿消食片中总有机酸的含量[J].中国中药杂志,2007,32(15):1597-1598.[23] 翟海斌,李斌,刘雪松,等.红参醇提取液浓缩过程近红外光谱在线分析方法[J].中国药学杂志,2005,40(24):1897-1899.[24] 朱向荣,张卓勇,李娜,等.近红外光谱与组合的间隔偏最小二乘法测定清开灵四混液中总氮和栀子苷的含量[J].高等学校化学学报,2008,29(5): 906-911.[25] 陈雪英,李页瑞,陈勇,等.近红外光谱分析技术在赤芍提取过程质量监控中的应用研究[J].中国中药杂志,2009,34(11):1355-1358.[26] 严诗楷,罗国安,王义明,等.栀子药材提取工艺的近红外光谱实时控制方法研究[J].光谱学与光谱分析,2006,26(6):1026-1030.(本文校对:张文娟 收稿日期:2009-09-21)硝酸咪康唑乳膏薄层色谱鉴别方法的改进崔红彬 蒋俊春 孟建升 商丘市食品药品检验所(476000)摘要:目的 改进硝酸咪康唑乳膏的鉴别方法。

软膏剂、乳膏剂检验标准操作规范软膏剂(《中国药典》)2010年版二部附录IF)系指药物与油脂性基质混合制成均匀的半固体外用制剂。
分为溶液型软膏剂和混悬型软膏剂。
溶液型软膏剂为药物溶解(或共熔)于基质或基质组成中制成的软膏剂;混悬型软膏剂药物细粉均匀分散于基质中制成的软膏剂。
乳膏剂(《中国药典》2010年版第二附录IF)系指药物溶解或分散于乳状液型基质中形成均匀的半固体外用制剂。
所以基质可分为水包油型和油包水型。
软膏剂、乳膏剂所用基质应均匀、细腻、涂于皮肤或黏膜上应无刺激性。
对于软膏剂、乳膏剂的质量要求,除应无酸败、异臭、变色、变硬,以及药典品种项下规定的检验项目外,还应检查“粒度”、“装量”,以及“微生物限度”或“无菌”。
混悬型软膏剂还应检查“粒度”。
“粒度”检查法1 简述1.1 本法系根据力度和粒度分布测定法(《中国药典》2010年版二部附录IX E 第一法显微镜法)规定,适用于混悬型软膏剂的粒度检查。
1.2 软膏剂所用药物如不溶于基质者,在生产过程中应预先研成细粉,使均匀分散于基质中制成混悬型软膏剂。
因药物的颗粒过大,会影响其释放度,故药典规定检查项目。
2 仪器与用具同粒度和粒度分布测定法标准操作规范第一法显微镜法项下。
显微镜镜台测微尺和目镜测微尺(直尺式)盖、载玻片计数器3 操作方法3.1 目镜测微尺的标定用以确定使用同一显微镜及的特定倍数的物镜,目镜和镜筒长度时,目镜微测尺上每一格所代表的长度。
标定时,将镜台微测尺至于载物台上,对光调焦,并移动测微尺使物象于视野中央,取下目镜,旋下接目镜的目镜盖,将目镜测微尺放入目镜筒中部的光栏上,旋上目镜盖后反置镜筒上,此时在视野中可同时观察到镜台微测尺的像及目镜微测尺得分度小格,移动镜台微测尺和旋转目镜,使两种量尺的刻度平行,并使左边的0刻度重合,然后在寻找第二条重合刻度,记录两条刻度的读书,并根据比值计算出目镜微测尺没小格在该物镜条件下所相当的长度(um)。

软膏剂、乳膏剂检验标准操作规范软膏剂(《中国药典》)2010年版二部附录IF)系指药物与油脂性基质混合制成均匀的半固体外用制剂。
分为溶液型软膏剂和混悬型软膏剂。
溶液型软膏剂为药物溶解(或共熔)于基质或基质组成中制成的软膏剂;混悬型软膏剂药物细粉均匀分散于基质中制成的软膏剂。
乳膏剂(《中国药典》2010年版第二附录IF)系指药物溶解或分散于乳状液型基质中形成均匀的半固体外用制剂。
所以基质可分为水包油型和油包水型。
软膏剂、乳膏剂所用基质应均匀、细腻、涂于皮肤或黏膜上应无刺激性。
对于软膏剂、乳膏剂的质量要求,除应无酸败、异臭、变色、变硬,以及药典品种项下规定的检验项目外,还应检查“粒度”、“装量”,以及“微生物限度”或“无菌”。
混悬型软膏剂还应检查“粒度”。
“粒度”检查法1 简述1.1 本法系根据力度和粒度分布测定法(《中国药典》2010年版二部附录IX E 第一法显微镜法)规定,适用于混悬型软膏剂的粒度检查。
1.2 软膏剂所用药物如不溶于基质者,在生产过程中应预先研成细粉,使均匀分散于基质中制成混悬型软膏剂。
因药物的颗粒过大,会影响其释放度,故药典规定检查项目。
2 仪器与用具同粒度和粒度分布测定法标准操作规范第一法显微镜法项下。
显微镜镜台测微尺和目镜测微尺(直尺式)盖、载玻片计数器3 操作方法3.1 目镜测微尺的标定用以确定使用同一显微镜及的特定倍数的物镜,目镜和镜筒长度时,目镜微测尺上每一格所代表的长度。
标定时,将镜台微测尺至于载物台上,对光调焦,并移动测微尺使物象于视野中央,取下目镜,旋下接目镜的目镜盖,将目镜测微尺放入目镜筒中部的光栏上,旋上目镜盖后反置镜筒上,此时在视野中可同时观察到镜台微测尺的像及目镜微测尺得分度小格,移动镜台微测尺和旋转目镜,使两种量尺的刻度平行,并使左边的0刻度重合,然后在寻找第二条重合刻度,记录两条刻度的读书,并根据比值计算出目镜微测尺没小格在该物镜条件下所相当的长度(um)。

GMP质量体系克霉唑软膏中间产品检验操作规程一、目的与范围为了保证GMP质量体系克霉唑软膏中间产品的质量,规范中间产品检验操作流程,制定本规程。
二、检验项目1.外观检查:检查克霉唑软膏中间产品的颜色、气味、透明度等外观特征。
2.pH值检查:采用pH计测定克霉唑软膏中间产品的酸碱性。
3.含量检查:采用高效液相色谱法(HPLC)测定克霉唑软膏中间产品中克霉唑的含量。
4.菌落总数检查:采用菌落计数法检查克霉唑软膏中间产品的菌落总数。
5.重金属残留检查:采用原子吸收光谱法检测克霉唑软膏中间产品中重金属残留。
三、检验仪器和试剂1.pH计:精度为0.012.高效液相色谱仪(HPLC):设备型号为XX,柱型为XX,检测波长为XX,流动相为XX。
3.菌落计数器:精度为0.014.原子吸收光谱仪:设备型号为XX,检测波长为XX。
四、操作流程1.外观检查操作流程:(1)将克霉唑软膏中间产品取出,放置在干净的容器中。
(2)观察克霉唑软膏中间产品的颜色、气味、透明度等外观特征。
(3)记录观察结果,并与标准要求进行比对。
如有异常,将中间产品送往实验室进一步检验。
2.pH值检查操作流程:(1)取一定量的克霉唑软膏中间产品,放入pH计中。
(2)按照pH计的使用说明进行测量,记录测得的pH值。
(3)根据标准要求,判断pH值是否符合要求。
如不符合,将中间产品送往实验室进一步调整。
3.含量检查操作流程:(1)取一定量的克霉唑软膏中间产品,用适量的溶剂进行溶解。
(2)将溶解后的样品过滤,取得过滤液。
(3)使用HPLC进行测定,按照仪器的使用说明进行操作。
(4)根据标准要求,判断克霉唑的含量是否符合要求。
如不符合,将中间产品送往实验室进一步调整。
4.菌落总数检查操作流程:(1)取一定量的克霉唑软膏中间产品,用适量的溶剂进行稀释。
(2)将稀释后的样品分别均匀涂抹在琼脂培养基上。
(3)将涂抹好的琼脂培养基放置在恒温箱中进行培养。
(4)在培养结束后,使用菌落计数器进行菌落总数的检测。

目的:为检验药用软膏铝管规定一个标准的程序,以便获得准确的实验数据。
范围:适用于药用软膏铝管的检验。
职责:检验室主任、检验员。
规程:
1.产品组成:药用软膏铝管(以下简称铝管)由铝质管体和塑料官帽组成。
2.材料:铝管材料含铝量不低于99.7%的纯铝
3.内涂层的化学稳定性
用蘸取丙酮的脱脂棉轻擦内表面,内涂层应无脱落。
4.印刷质量
4.1印刷内容应清晰完整,位置正确。
印刷表面应平整光洁,并符合药品有关印刷的要求。
4.2印刷面应有足够的固化强度,用蘸乙醇的脱脂棉轻擦铝管印刷表面,应无脱色。
4.3清洁度
4.3.1铝管应清洁,管内应无加工残屑及其他异物。
4.3.2管帽与管嘴螺纹旋配后,应不产生金属碎屑。
4.4管帽配合
铝管的管帽与管嘴螺纹配合应适宜。
4.5 微生物检查
按下列方法检验,细菌、霉菌各不得超过5个/ml,金黄色葡萄球菌和绿脓杆菌不得检出。
4.5.1 提取液制备
取5支供试铝管(规格 16 ;管身长度 85mm ,向每支铝管内灌注无菌生理盐水15ml。
振荡5min后合并提取液备用。
4.5.2 按《中华人民共和国药典》2000年版二部规定进行检查。

HPLC法测定硝酸咪康唑栓中硝酸咪康唑的含量唐永红;宋愿智;李秋菲【摘要】目的建立硝酸咪康唑栓的HPLC含量测定方法.方法采用HPLC法,色谱条件:ODS柱(250 mm×4.6 mm,5 μm);甲醇-乙腈-5 g·L-1醋酸铵溶液(42.5∶42.5∶15)为流动相;流速1.0 mL·min-1;检测波长230 nm;进样量10 μL;柱温35 ℃.结果硝酸咪康唑进样量在0.499~2.994 mg·mL-1范围内,其峰面积值与进样质量浓度有良好的线性关系,r=0.999 1,回收率为100.7%,RSD为1.0%(n=3).结论经与紫外-可见分光光度法比较,该法重复性好,灵敏度高,结果准确,适用于硝酸咪康唑栓的含量测定.%Objective To establish an HPLC method for Miconazole Nitrate Suppositories. Method Chromatography conditions were as follows:ODS column (250 mm × 4. 6 mm,5μm) ;methanol-acetonitrile-5 g o L-1 ammonium acetate solution (42. 5 : 42. 5 : 15) as mobile phasejflow rate of 1. 0 mL o min-1 ;detection wavelength of 230 nm;injection volume 10 μL;column temperature 35 ℃. Results Within the miconazole nitrate injection amount of 0. 499-2. 994 mg o mL-1 ,the peak area values and sample concentration showed a good linear relationship,r = 0. 999 1. The recovery was 100. 7% with RSD of 1. 0% (n = 3). Conclusion Compared with the UV-visible spectrophotometry,the method has good reproducibility and high sensitivity. The method is accurate, and is suitable for the determination of Miconazole Nitrate Suppository.【期刊名称】《西北药学杂志》【年(卷),期】2012(027)005【总页数】3页(P433-435)【关键词】硝酸咪康唑栓;硝酸咪康唑;含量测定;HPLC【作者】唐永红;宋愿智;李秋菲【作者单位】西安泰科迈医药科技有限公司,西安,710077;陕西省食品药品检验所,西安,710061;陕西省食品药品检验所,西安,710061【正文语种】中文【中图分类】R927.2硝酸咪康唑栓为国家食品药品监督管理局国家药品标准新药转正标准第 46 册〔WS1-(X-423)-2003X〕收载品种,为抗真菌类药物,主要用于假丝酵母菌如白色假丝酵母菌等所致的皮肤感染和外阴阴道炎等症的治疗[1-2]。
![硝酸咪康唑乳膏及制备方法[发明专利]](https://uimg.taocdn.com/dc09a9b6ed3a87c24028915f804d2b160b4e8669.webp)
[19]中华人民共和国国家知识产权局[12]发明专利申请公布说明书[11]公开号CN 101474188A[43]公开日2009年7月8日[21]申请号200910010074.2[22]申请日2009.01.07[21]申请号200910010074.2[71]申请人张克斌地址134300吉林省白山市红旗街102-12号康家药房[72]发明人张克斌 [51]Int.CI.A61K 31/57 (2006.01)A61K 31/4174 (2006.01)A61K 9/06 (2006.01)A61P 31/10 (2006.01)权利要求书 1 页 说明书 3 页[54]发明名称硝酸咪康唑乳膏及制备方法[57]摘要一种硝酸咪康唑乳膏及制备方法由:配方硝酸咪康唑2g,丙酸氯佩他素0.5g,十八醇0.5g,液体石蜡4g,白凡士林2g,平平加O 0.5g,羟苯乙酯0.5g,无水乙醇3g,丙二醇0.5g。
充分均匀混合,搅拌15-25min的乳化质,缓慢冷却室温即可。
200910010074.2权 利 要 求 书第1/1页 1、一种硝酸咪康唑乳膏。
其特征是:配方硝酸咪康唑2g,丙酸氯佩他素0.5g,十八醇0.5g,液体石腊4g,白凡士林2g,平平加O 0.5g,羟苯乙脂0.5g,无水乙醇3g,丙二醇0.5g。
2、根据权利要求一所述的硝酸咪康唑乳膏及制备方法其特征是:将配方硝酸咪康唑2g,丙酸氯佩他素0.5g,十八醇0.5g,液体石腊4g,白凡士林2g,平平加O 0.5g,羟苯乙脂0.5g,无水乙醇3g,丙二醇0.5g。
充他均匀混合,搅拌15-25min的乳化质,缓慢冷却室温即可。
200910010074.2说 明 书第1/3页硝酸咪康唑乳膏及制备方法技术领域本发明涉及一种治疗灰指甲的药物,尤其是硝酸咪康唑乳膏及制备方法。
背景技术目前治疗灰指甲病的药物有亮灰甲,均有毒副作用大,有时达不到治疗目的。
发明内容本发明的目的是提供一种以硝酸咪康唑等9种西药,经科学配方的药物,治疗效果较明显。

硝酸咪康唑搽剂微生物限度检查法的建立硝酸咪康唑搽剂微生物限度检查法的建立【摘要】目的建立硝酸咪康唑搽剂微生物限度检查法。
方法测定硝酸咪康唑搽剂对大肠埃希菌等5种试验菌的回收率,对2个控制菌(铜绿假单胞菌、金黄色葡萄球菌)的检查方法进行验证。
结果用薄膜过滤法和0.1%吐温80-pH7.0氯化钠-蛋白胨缓冲液作冲洗剂检查本品的细菌总数、真菌及酵母菌计数,其试验菌回收率均达到70%以上。
同样用该方法检查本品的铜绿假单胞菌、金黄色葡萄球菌,其试验组呈阳性反应,阴性菌对照组呈阴性反应。
结论用薄膜过滤法联用0.1%吐温80-pH7.0氯化钠-蛋白胨缓冲液作冲洗剂可以消除硝酸咪康唑搽剂在试验条件下的抑菌作用,从而顺利检出该品种所污染的各种微生物。
【关键词】硝酸咪康唑搽剂;微生物限度检查;方法学验证微生物限度检查法是检查非规定制剂及原料、辅料受微生物污染程度的方法,检查项目包括细菌数、真菌数、酵母菌数及控制菌检查[1]。
但具有抑菌成分的药品由于其抑菌活性的干扰,常规检查结果不能真实地反映出药品中污染微生物的情况,必须先消除供试品中的抑菌活性,再根据《中国药典》规定的方法进行检查,并必须对所采取的检查方法进行验证,以确认抑菌活性的消除和检查方法的可靠性。
具有抑菌作用的药品,每个品种抑菌效果不同,因此适合各个品种的`微生物限度检查法也不同。
作者曾用常规法、培养基稀释法及薄膜过滤法(用pH7.0氯化钠?蛋白胨缓冲液冲洗)对硝酸咪康唑搽剂进行微生物限度检查,结果均不能达到药典要求。
吐温80是亲水性表面活性剂,具有增溶作用,因此本文选择用薄膜过滤法联用0.1%吐温80?pH7.0氯化钠?蛋白胨缓冲溶液做冲洗剂检查该药品的细菌、真菌、酵母菌数和控制菌,结果满意,可为同类药品的微生物限度检查法提供科学依据。
1材料1.1菌种大肠埃希菌(Escherichia coli)[CMCC(B) 44 102], 金黄色葡萄球菌(Staphylococcus aureus)[CMCC(B) 26 003], 枯草芽孢杆菌(Bacillus subtilis)[CMCC(B)63 501], 金黄色葡萄球菌(Staphylococcus aureus)[CMCC(B) 26 003],铜绿假单胞菌(Pseudomonas aeruginosa)[CMCC(B)10 104]白色念珠菌(Candida albicans)[CMCC(F) 980011], 黑曲霉(Asperg illus niger)[CMCC(F) 98003],由广东生物研究所提供,菌种代数均为第3代。
目的:建立硝酸益康唑软膏的生产工艺规程。
范围:硝酸益康唑软膏的生产。
职责:生产管理部、质量管理部、车间主任、班长、工艺员、操作工、QA。
规程:1.品名、剂型与处方依据1.1通用名称:硝酸益康唑软膏汉语拼音:Xiaosuan Yikangzuo Ruangao英文名: Econazole Nitrate Ointment1.2 剂型:软膏剂1.3 处方与处方依据项的说明1.3.1处方:(制成10000支)硝酸益康唑 1015g 二甲基亚砜6000g 硬酯酸 5000g 十八醇 5000g 白凡士林 8000g 液体石蜡 5000g 单硬脂酸甘油酯 4000g 三乙醇胺 420g甘油 8500g 羟苯乙酯 100g 乙醇 2000ml 玫瑰香精 50ml 纯化水 55.5kg1.3.2 处方依据项说明:药品的生产批文:批准时间:质量标准编号:2.工艺流程示意图:检验→→ ↓← 中间产品检验→↓ ← 成品检验3.生产工艺操作要求、工艺技术参数: 3.1配制:3.1.1 配料操作工按照“软(乳)膏剂、凝胶剂配制岗位标准操作规程” SOP-MN/Z-(R )-001-00规定,在油相缸中加入硬脂酸、单硬脂酸甘油酯、十八醇、白凡士林、液体石蜡,加热至100℃,过滤降温至90℃,并作记录。
3.1.2在水相缸中加入甘油、纯化水、三乙醇胺加热至沸腾,并在搅拌下加入用乙醇溶解的处方量羟苯乙酯,搅拌至均匀。
3.1.3 先后将水相、油相抽入到真空乳化机内,以80—100次/分钟的速度搅拌30分钟后,用水冷却至70℃时,加入处方量的硝酸益康唑(用二甲基亚砜溶解),放去冷却水,保温乳化60分钟,再进行冷却至50℃时加入玫瑰香精,搅拌即得,加主药后共搅拌120分钟。
3.2 中间品检验:检验室按“中间产品取样操作规程”规定,抽取配制好的膏体进行中间产品的检验。
检验合格后,发放“中间产品合格证”。
3.3 灌封:接到“中间产品合格证”后,车间按“软(乳)膏剂灌封岗位标准操作规程”SOP-MN/Z-(R )-002-00的要求,进行灌封工序。
硝酸咪康唑软膏的真伪鉴别
张丽君
【期刊名称】《中国医药导报》
【年(卷),期】2006(000)029
【摘要】@@ 硝酸咪康唑软膏又名达克宁霜,我们在日常调剂、监督工作中发现,标示西安杨森制药有限公司的达克宁存在3种质量问题:①确系杨森公司产品.②冒杨森公司某批产品,含硝酸咪康唑81.7%.③冒充杨森公司产品,不含硝酸咪康唑.本文通过质量分析法、核查对照法鉴别硝酸咪康唑软膏的真伪,现报告如下.
【总页数】1页(P80)
【作者】张丽君
【作者单位】辽宁省友谊医院,辽宁,沈阳,110015
【正文语种】中文
【中图分类】R9
【相关文献】
1.硝酸咪康唑栓联合氟康唑及硝酸咪康唑软膏治疗严重外阴阴道念珠菌病的临床观察 [J], 何甫霞
2.硝酸咪康唑软膏的真伪鉴别 [J], 汤志萍
3.药品快检车近红外系统快速鉴别硝酸咪康唑乳膏的真伪 [J], 李盈;杨小川;汪洋
4.高效液相色谱法测定复方硝酸咪康唑软膏中硝酸咪康唑和丙酸倍氯米松含量 [J], 罗荣;陈标
5.三九皮炎平软膏的真伪鉴别 [J], 鲁安中
因版权原因,仅展示原文概要,查看原文内容请购买。
反相高效液相色谱法测定藓药膏中硝酸咪康唑和丙酸氯倍他索
的含量
林银凤
【期刊名称】《海峡药学》
【年(卷),期】2012(024)002
【摘要】目的建立藓药膏中硝酸咪康唑和丙酸氯倍他索的含量测定方法.方法以十八烷基键合硅胶色谱柱,0.5%醋酸铵溶液-乙腈-甲醇(20∶40∶40)为流动相,检测波长为240nm,流速为1.0mL· min-1.结果丙酸氯倍他索在0.005mg· mL-1~0.05mg·mL-1呈良好的线性关系(r=0.9999),平均回收率为99.8%;硝酸咪康唑在0.2mg· mL-1~2mg·mL-1呈良好的线性关系(r=0.9989),平均回收率为101.5%.结论该方法简便、快速、可靠,可用于该产品的质量控制.
【总页数】2页(P66-67)
【作者】林银凤
【作者单位】福建泉州市药品检验所泉州362000
【正文语种】中文
【中图分类】R969.4
【相关文献】
1.HPLC法测定复方咪康唑软膏中硝酸咪康唑和丙酸氯倍他索的含量 [J], 谢子立;武谷
2.HPLC法测定消炎霜中硝酸咪康唑和丙酸氯倍他索的含量 [J], 利新发;李祥;谭初
宝
3.高效液相色谱法测定硝酸咪康唑擦剂中硝酸咪康唑和丙酸氯倍他索的含量 [J], 刘海燕;崔飙
4.HPLC法测定索咪新尿素乳膏中丙酸氯倍他索和硝酸咪康唑的含量 [J], 王希东
5.反相高效液相色谱法测定咪康唑氯倍他索乳膏中硝酸咪康唑和丙酸氯倍他索的含量 [J], 陈旻;温梅云;李晨辉;陈英;施若靖
因版权原因,仅展示原文概要,查看原文内容请购买。