届江苏省南京三中高三化学二轮复习-物质的组成性质和分类教学 (共53张)PPT课件
- 格式:ppt
- 大小:1.12 MB
- 文档页数:16
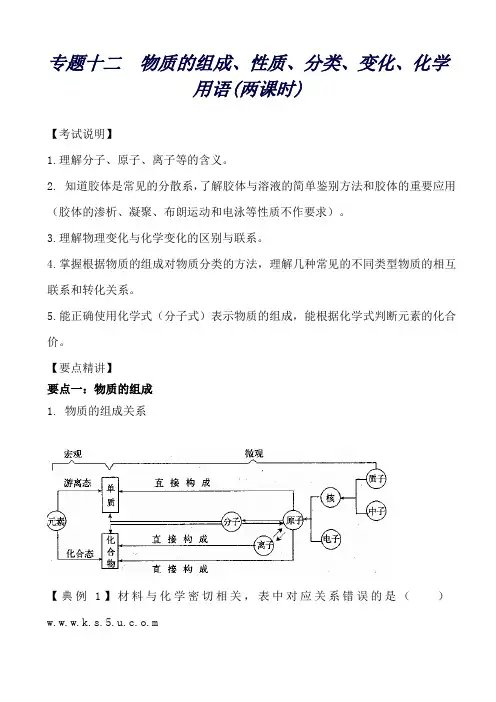
专题十二物质的组成、性质、分类、变化、化学用语(两课时)【考试说明】1.理解分子、原子、离子等的含义。
2. 知道胶体是常见的分散系,了解胶体与溶液的简单鉴别方法和胶体的重要应用(胶体的渗析、凝聚、布朗运动和电泳等性质不作要求)。
3.理解物理变化与化学变化的区别与联系。
4.掌握根据物质的组成对物质分类的方法,理解几种常见的不同类型物质的相互联系和转化关系。
5.能正确使用化学式(分子式)表示物质的组成,能根据化学式判断元素的化合价。
【要点精讲】要点一:物质的组成1. 物质的组成关系【典例1】材料与化学密切相关,表中对应关系错误的是()w.w.w.k.s.5.u.c.o.m2. 分子、原子、离子的比较【典例2】下列化学式既能表示物质的组成,又能表示物质的一个分子的是()A.NaOH B.SiO2C.Fe D.C3H83.离子与基团4.同素异形体与同位素、同系物、同分异构体的区别:【典例3】由两种原子组成的纯净物()A. 一定是化合物B. 可能是化合物或单质C. 一定是单质D. 一定是同素异形体要点二:物质的分类1.分类依据和方法【典例4】某合作学习小组讨论辨析以下说法:①粗盐和酸雨都是混合物;②沼气和水蒸气都是可再生能源;③冰和干冰既是纯净物又是化合物;④不锈钢和目前流通的硬币都是合金;⑤盐酸和食醋既是化合物又是酸;⑥纯碱和熟石灰都是碱;⑦豆浆和雾都是胶体。
上述说法正确的是()A.①②③④B.①②⑤⑥ C.③⑤⑥⑦ D.①③④⑦【典例5】物质分类的依据通常有组成和性质,下列物质分类中,只考虑组成的是()A. Na2SO4是钠盐、硫酸盐、正盐B. HNO3是一元酸、强酸、挥发性酸C. Mg(OH)2是二元碱、难溶性碱、中强碱D. Al2O3是两性氧化物、金属氧化物、最高价氧化物2.胶体1、分类分散剂是液体——液溶胶。
如Al(OH)3胶体,蛋白质胶(1)按分散剂的状态分分散剂是气体——气溶胶。
如雾、云、烟分散剂是固体——固溶胶。

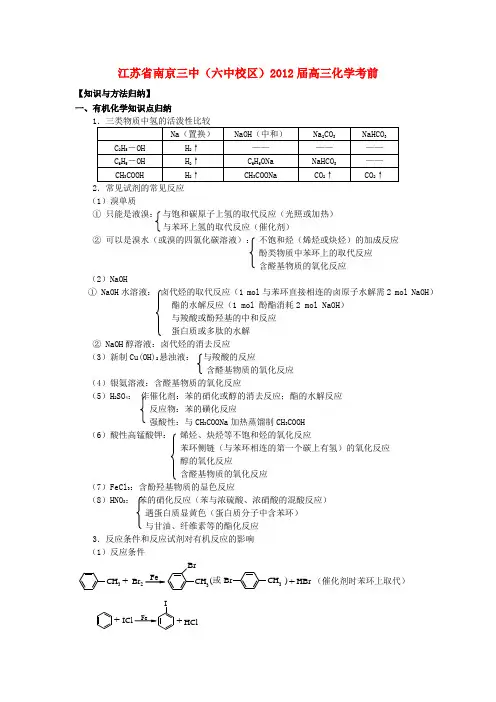
江苏省南京三中(六中校区)2012届高三化学考前【知识与方法归纳】一、有机化学知识点归纳2.常见试剂的常见反应 (1)溴单质①只能是液溴: 与饱和碳原子上氢的取代反应(光照或加热)与苯环上氢的取代反应(催化剂)② 可以是溴水(或溴的四氯化碳溶液): 不饱和烃(烯烃或炔烃)的加成反应酚类物质中苯环上的取代反应 含醛基物质的氧化反应(2)NaOH① NaOH 水溶液: 卤代烃的取代反应(1 mol 与苯环直接相连的卤原子水解需2 mol NaOH )酯的水解反应(1 mol 酚酯消耗2 mol NaOH ) 与羧酸或酚羟基的中和反应 蛋白质或多肽的水解② NaOH 醇溶液:卤代烃的消去反应(3)新制Cu(OH)2悬浊液: 与羧酸的反应含醛基物质的氧化反应(4)银氨溶液:含醛基物质的氧化反应(5)H 2SO 4: 作催化剂:苯的硝化或醇的消去反应;酯的水解反应反应物:苯的磺化反应强酸性:与CH 3COONa 加热蒸馏制CH 3COOH(6)酸性高锰酸钾: 烯烃、炔烃等不饱和烃的氧化反应苯环侧链(与苯环相连的第一个碳上有氢)的氧化反应 醇的氧化反应含醛基物质的氧化反应(7)FeCl 3:含酚羟基物质的显色反应(8)HNO 3: 苯的硝化反应(苯与浓硫酸、浓硝酸的混酸反应)遇蛋白质显黄色(蛋白质分子中含苯环) 与甘油、纤维素等的酯化反应3.反应条件和反应试剂对有机反应的影响 (1)反应条件CH 3CH 3BrCH 3Br +Br 2Fe (或 )+HBr (催化剂时苯环上取代) IFe++IClHCl(2)温度不同2CH 3CH 22SO 43CH 2OCH 2CH 3+H 2OCH 3CH 2OH C H 2CH 224+↑H 2O(2)溶剂影响CH 3-CH 2Br +NaOH CH 3CH 2OH +NaBr CH 3CH 2Br+CH 2=CH 2↑+NaBr +H 2O(3)试剂浓度影响CH 3COOH +CH 3CH 2CH 3COOCH 2CH 3+H 2O CH 3COOCH 2CH 3+H2CH 3COOH +CH 3CH 2OH(3)溶液酸碱性影响R -OH +H R -X +H 2O R -X +H2R -OH +HXCH 3COOCH 2CH 3+H2CH 3COOH +CH 3CH 2OHCH 3COOCH 2CH 3+CH 3COONa +CH 3CH 2OH4.官能团间的演变C22H 2SO 4、稀 H 2SO4、CH 2CH 2Cl3、H 2OCH 2HBr 、H +CH CHO O 2/催化剂32CH CH 32、光、醇2SO 4℃C 2H 5OH 3COOC 2H 5NaOH2 蒸馏2BrCH 32NaOH 、H 2O、H 2OCH 3NaOH 、H 2CH 3CH 2ONa2O5.有机中常见的分离和提纯(1)除杂(括号内为杂质)① C 2H 6(C 2H 4、C 2H 2):溴水,洗气(或依次通过酸性高锰酸钾溶液、NaOH 溶液,洗气) ② C 6H 6(C 6H 5-CH 3):酸性高锰酸钾溶液、NaOH 溶液,分液 ③C 2H 5-OH (H 2O ): 加新制生石灰,蒸馏④C 6H 6(C 6H 5-OH ): NaOH 溶液,分液(或直接蒸馏) ⑤ CH 3COOC 2H 5(CH 3COOH 、C 2H 5OH ):饱和碳酸钠溶液,分液 ⑥C 2H 5OH (CH 3COOH ):NaOH ,蒸馏 (2)分离① C 6H 6、C 6H 5OH :NaOH 溶液,分液,上层液体为苯;然后在下层液体中通过量的CO 2,分液,下层液体为苯酚(或蒸馏收集不同温度下的馏分)② C 2H 5OH 、CH 3COOH :NaOH ,蒸馏收集C 2H 5OH ;然后在残留物中加硫酸,蒸馏得CH 3COOH 。





第一单元 物质的组成、性质及分类[教材基础—自热身]1.元素、物质及微粒间的关系(1)宏观上物质是由元素组成的,微观上物质是由分子、原子或离子构成的。
(2)元素:具有相同核电荷数的同一类原子的总称。
(3)元素与物质的关系元素⎩⎪⎨⎪⎧单质:只由一种元素组成的纯净物。
化合物:由多种元素组成的纯净物。
(4)元素在物质中的存在形态①游离态:元素以单质形式存在的状态。
②化合态:元素以化合物形式存在的状态。
2.同素异形体(1)概念:同种元素形成的不同单质叫同素异形体。
(2)形成方式:①原子个数不同,如O 2和O 3;②原子排列方式不同,如金刚石和石墨。
(3)性质差异:物理性质差别较大,同素异形体之间的转化属于化学变化。
3.混合物和纯净物(1)纯净物:由同种单质或化合物组成的物质。
(2)混合物:由几种不同的单质或化合物组成的物质。
[知能深化—扫盲点]1.常见的气体混合物按要求回答问题。
①冰水混合物②爆鸣气③铝热剂④普通玻璃⑤水玻璃⑥有机玻璃⑦漂白粉⑧TNT ⑨H2SO4⑩含氧40%的氧化镁⑪花生油⑫福尔马林⑬密封保存的NO2气体⑭CuSO4·5H2O ⑮液氯⑯王水⑰KAl(SO4)2·12H2O ⑱分子式为C5H10的烃⑲分子式为C7H8的芳香烃以上物质中一定为纯净物的是______________________,一定为混合物的是________________________________________________________________________,可能是纯净物,也可能是混合物的是__________________________________________。
答案:①⑧⑨⑩⑭⑮⑰⑲②③④⑤⑥⑦⑪⑫⑬⑯⑱[题点全练—过高考]题点一物质组成的基本概念1.下列说法正确的是( )A.化学变化中分子可以再分,离子和原子不可以再分B.同一种元素可能有多种不同原子,同一种原子也可能形成不同的离子C.物质的化学性质一定是由分子保持的D.只由一种元素的阳离子与另一种元素的阴离子组成的物质一定为纯净物解析:选B A项,化学变化中的单原子分子不能再分,如He、Ne等;C项,有些物质是由离子构成的,如NaCl,它们的化学性质不是由分子保持的;D项,可能为混合物,如Na2O、Na2O2。

