晶体结构的计算(历年高考题汇总).pdf
- 格式:pdf
- 大小:1.40 MB
- 文档页数:7
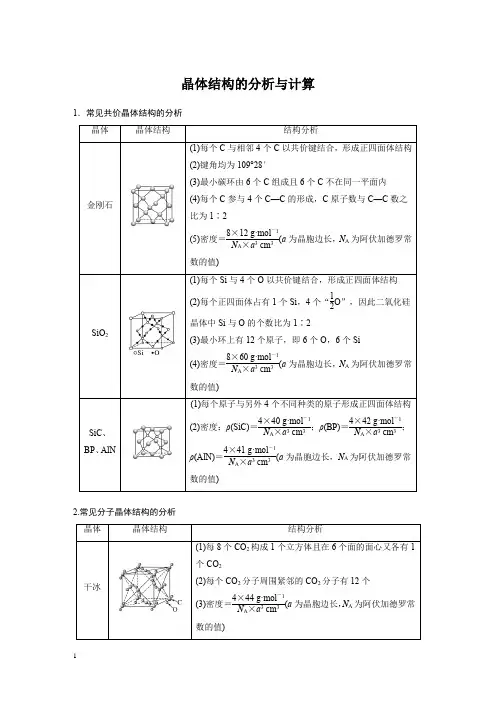
晶体结构的分析与计算1.常见共价晶体结构的分析2.常见分子晶体结构的分析3.常见离子晶体结构的分析684F-:8;Ca2+:41.AB型化合物形成的晶体结构多种多样。
下图所示的几种结构所表示的物质最有可能是分子晶体的是()A.①③B.②⑤C.⑤⑥D.③④⑤⑥2.如图为几种晶体或晶胞的示意图:请回答下列问题:(1)上述晶体中,微粒之间以共价键结合形成的晶体是________。
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为______________________。
(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的离子键________(填“大于”或“小于”)MgO 晶体的离子键,原因是___________________________________________________________。
(4)CaCl2晶体中Ca2+的配位数________。
(5)冰的熔点远高于干冰,除H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是_______________________________________________________________________________。
3.[2017·全国卷Ⅲ,35(5)]MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420 nm,则r(O2-)为________nm。
MnO 也属于NaCl型结构,晶胞参数为a′=0.448 nm,则r(Mn2+)为________nm。
4.Li2O具有反萤石结构,晶胞如图所示。
已知晶胞参数为0.466 5 nm,阿伏加德罗常数的值为N A,则Li2O的密度为________________________________________g·cm-3(列出计算式)。
5.[2018·全国卷Ⅱ,35(5)]FeS2晶体的晶胞如图所示。
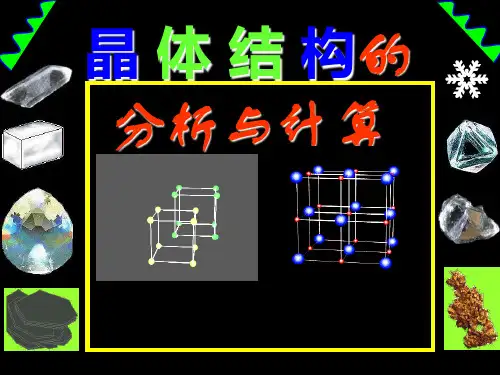

晶体结构的分析与计算1.(2015·全国卷Ⅰ)碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:(1)在石墨烯晶体中,每个C 原子连接________个六元环,每个六元环占有________个C 原子。
(2)在金刚石晶体中,C 原子所连接的最小环也为六元环,每个C 原子连接______个六元环,六元环中最多有______个C 原子在同一平面。
解析:(1)由石墨烯的结构可知,每个C 原子连接3个六元环,每个六元环占有的C 原子数为13×6=2。
(2)由金刚石的结构可知,每个C 可参与形成4条C —C 键,其中任意两条边(共价键)可以构成2个六元环。
根据组合知识可知四条边(共价键)任选其中两条有6组,6×2=12。
因此每个C 原子连接12个六元环。
六元环中C 原子采取sp 3杂化,为空间六边形结构,最多有4个C 原子位于同一平面。
答案:(1)3 2 (2)12 42.(2016·全国卷Ⅱ)某镍白铜合金的立方晶胞结构如图所示。
(1)晶胞中铜原子与镍原子的数量比为________。
(2)若合金的密度为d g·cm -3,晶胞参数a =________nm 。
解析:(1)由晶胞结构图可知,Ni 原子处于立方晶胞的顶点,Cu 原子处于立方晶胞的面心,根据均摊法,每个晶胞中含有Cu 原子的个数为6×12=3,含有Ni 原子的个数为8×18=1,故晶胞中Cu 原子与Ni 原子的数量比为3∶1。
(2)根据m =ρV 可得, 1 mol 晶胞的质量为(64×3+59)g =a 3×d g·cm -3×N A ,则a =⎝⎛⎭⎫2516.02×1023×d 13cm =⎝⎛⎭⎫2516.02×1023×d 13×107 nm 。
答案:(1)3∶1 (2)⎝⎛⎭⎫2516.02×1023×d 13×107 3.(2017·全国卷Ⅰ)(1)KIO 3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立方结构,边长为a =0.446 nm ,晶胞中K 、I 、O分别处于顶角、体心、面心位置,如图所示。

晶体结构是近几年来高考考查的重点和热点,特别是晶体结构的计算更是其 中的重中之重,它体现了高考考试说明中提出的“将化学问题抽象为数学问题, 利用数学工具,通过计算推理解决化学问题的能力”的要求 ,是高考向“ 3+X ”综 合发展的趋势。
在高考的第二轮复习中有必要加以归纳整理。
晶体结构的计算通 常有以下类型:例1:在氯化钠晶体(图1)中,与氯离子距离最近的钠离子有 ____ 个;与氯离子距离最近的氯离子有_________ 个。
解析:我们可以选定中心的氯离子作为基准,设立方体的边长为 a ,则 氯离子与钠离子之间的最近距离为 2,此钠离子位于立方体六个面的面心上, 即有六个钠离子;氯离子间的最近距离为,共有12个。
(如图标号1-12 所示)。
例2: 二氧化碳晶体中,与二氧化碳分子距离最近的二氧化碳分子有 __________ 个。
解析:在图2的二氧化碳分子晶体结构中,8个二 氧化碳分子处于正方体的8个顶点上,还有6个处于正 方体的六个面的面心上。
此时可选定面心的二氧化碳分 子为基准,设正方体的边长为 a,则二氧化碳分子间的最近距离为 子a ,从图中看有8个,它们分别位于该侧面的四个顶点及与之相连的四个面的面心上。
此时 晶体中距离最近的微粒数的计算:• Na + OCl^应注意,图中所给出的结构仅是晶胞。
所谓晶胞,是晶体中最小的重复结构单元, 就是说晶体是以晶胞为核心向空间延伸而得到的,单个的晶胞不能表示整个晶体它能全面正确地表示晶体中各微粒的空间关系。
也的结构。
所以在我们观察晶体结构时应充分发挥空间想象的能力,要将晶胞向各个方向(上,下,左,右,前,后)扩展。
图2向右扩展得图3(为容易观察, 用?表示二氧化碳分子),从中可以看出与二氧化碳分子距离最近的二氧化碳分子有12 个。
从以上的分析可以看出,要正确确定晶体中距离最近的微粒的数目,首先要对晶体结构熟悉,其次要有良好的空间想象能力,要有以晶胞为核心向空间扩展的意识。

【考点概括】1.晶胞化学式的计算晶体中微粒的摆列拥有周期性,晶体中最小的构造重复单元称为晶胞,利用“均派法” 能够计算一个晶胞中的粒子数,进而确立晶体的化学式。
“均派法”的基本思想是晶胞中随意地点上的一个粒子被 n 个晶胞共用,那么每个晶胞对这个原子分得份额就是里波及的晶胞有立方晶胞、六方晶胞、三棱晶胞,以立方晶胞最为常有。
常有考题( 1)立方晶胞:每个极点上的粒子被8 个晶胞共用,每个粒子只有属于该晶胞;每条棱上的粒子被 4 个晶胞共用,每个粒子只有属于该晶胞;每个面心上的粒子被 2 个晶胞共用,每个粒子只有属于该晶胞;晶胞内的粒子完整属于该晶胞。
( 2)六方晶胞:每个极点上的粒子被 6 个晶胞共用;每条横棱上的粒子被 4 个晶胞共用;每条纵棱上的粒子被 3 个晶胞共用;每个面心上的粒子被 2 个晶胞共用;晶胞内的粒子完整属于该晶胞。
( 3)三棱晶胞:每个极点上的粒子被12 个晶胞共用;每条横棱上的粒子被 4 个晶胞共用;每条纵棱上的粒子被 6 个晶胞共用;每个面心上的粒子被 2 个晶胞共用;晶胞内的粒子完整属于该晶胞。
2.晶体密度及微粒间距离的计算(1) 晶体微粒与M、ρ之间的关系:若 1 个晶胞中含有 x 个微粒,则 1mol晶胞中含有 xmol33为晶胞的体积,微粒,其质量为 xM g(M 为微粒的相对“分子”质量 );1 个晶胞的质量为ρag(a33ρ为晶胞的密度 ),则 1mol 晶胞的质量为ρa N A g,所以有xM =ρa N A。
( 2)金属晶体中体心立方聚积、面心立方聚积中的几组公式(设棱长为 a):面对角线长=2 a;体对角线长=3a;体心立方聚积4r= 3a(r 为原子半径 );面心立方聚积4r= 2a(r为原子半径 )。
( 3)空间利用率的计算:空间利用率=晶胞据有的微粒体积晶胞体积。
【过关练习】1.下列图是甲、乙、丙三种晶体的晶胞,则甲晶体中x 与 y 的个数比是 ______,乙中 a 与 b 的个数比是 ______,丙中一个晶胞中有________个 c 离子和 ________个 d 离子。

高中化学晶体结构计算题详解高中化学中,晶体结构计算题是一个重要的考点。
这类题目要求学生根据给定的晶体结构图或者晶体的化学式,计算出晶体中各种离子的个数以及离子的配位数。
这类题目对于学生来说可能有一定的难度,但只要掌握了一些基本的计算方法和技巧,就能够轻松解答。
首先,我们来看一个具体的例子。
假设有一种晶体,化学式为AB2C3,其中A为阳离子,B和C为阴离子。
题目要求计算出晶体中A、B、C离子的个数以及它们的配位数。
首先,我们需要知道晶体中各种离子的个数与它们的化学式有关。
在这个例子中,化学式为AB2C3,意味着每个A离子与2个B离子和3个C离子结合。
因此,我们可以得出以下结论:A离子个数 = B离子个数 / 2 = C离子个数 / 3接下来,我们需要计算出晶体中各种离子的配位数。
配位数是指一个离子周围被其他离子或原子包围的个数。
在晶体中,每个离子都会被周围的离子或原子包围,因此我们可以通过计算每个离子周围的离子或原子个数来得到配位数。
在这个例子中,A离子的配位数等于与之相连的B离子和C离子的个数之和。
同样地,B离子的配位数等于与之相连的A离子和C离子的个数之和,C离子的配位数等于与之相连的A离子和B离子的个数之和。
通过以上的分析,我们可以得出以下结论:A离子配位数 = B离子个数 + C离子个数B离子配位数 = A离子个数 + C离子个数C离子配位数 = A离子个数 + B离子个数通过这个例子,我们可以看出晶体结构计算题的一些考点。
首先,我们需要根据化学式确定各种离子的个数。
其次,我们需要计算出各个离子的配位数。
这些计算都需要基于化学式和晶体结构图进行推导和分析。
在解答这类题目时,我们还可以运用一些技巧来简化计算过程。
例如,如果化学式中的离子有共同的倍数关系,我们可以通过简单的比例计算来得到各个离子的个数。
另外,我们还可以通过观察晶体结构图中的对称性来推断离子的配位数。
总结起来,高中化学晶体结构计算题是一个重要的考点。


高中化学——晶胞的结构与计算专题练习(带答案解析)一、单选题1.快离子导体是一类具有优良导电能力的固体电解质。
图1(Li3SBF4)和图2是潜在的快离子导体材料的结构示意图。
温度升高时,NaCl晶体出现缺陷,晶体的导电性增强。
该晶体导电时,③迁移的途径有两条:途径1:在平面内挤过2、3号氯离子之间的狭缝(距离为x)迁移到空位。
途径2:挤过由1、2、3号氯离子形成的三角形通道(如图3,小圆的半径为y)迁移到空位。
已知:氯化钠晶胞参数a=564pm,r(Na+)=95pm,r(Cl-)=185pm下列说法不正确的是A.第二周期元素中第一电离能介于B和F之间的元素有4种B.图1所示晶体中,每个Li+与4个呈四面体结构的离子相邻C.氯化钠晶体中,Na+填充在氯离子形成的正八面体空隙中D.温度升高时,NaCl晶体出现缺陷,晶体的导电性增强,该晶体导电时,③迁移的途径可能性更大的是途径12.某铜的氯化物常作工业催化剂,其晶胞结构如图所示,晶胞中C、D两原子核间距为298pm。
N,则下列说法正确的是设阿伏加德罗常数的值为AA.Cu的+2价比+1价稳定,是因为最外层电子达到半充满结构CuClB.此氯化物的化学式为2C.晶胞中Cu位于Cl形成的四面体空隙D .Cu 与Cl倍 3.Al x CoO y 的立方晶胞如图所示,已知处在体心处的原子为Co ,晶胞参数anm ,下列说法错误的是A .x=1,y=3B .该晶胞的密度为23-33A1.3410g cm a N ⨯⋅ C .该晶胞的俯视图为D .晶体中一个Al 周围与其最近的O 的个数为64.某立方晶系的锑钾()Sb K -合金可作为钾离子电池的电极材料,下图表示1/8晶胞。
下列说法中错误的是A .该晶胞的体积为33038a 10cm -⨯B .K 和Sb 原子数之比为3:1C .与K 最邻近的Sb 原子数为4D .该晶胞的俯视图为5.2CaC 的晶胞与NaCl 相似,但由于22C -的结构导致晶胞沿一个方向拉长(如图),已知2CaC 的摩尔质量为1M g mol -⋅,若阿伏加德罗常数的值为A N ,下列说法错误..的是A .2Ca +填充在22C -围成的八面体空隙中B .每个2Ca +周围等距紧邻的22C -有6个C .两个最近2Ca +D .2CaC 晶体密度的计算式为3230A 4g cm 10M N a b --⋅⨯ 6.某镁镍合金储氢后所得晶体的立方晶胞如图1(为便于观察,省略了2个图2的结构),晶胞边长为apm 。

高中化学晶体结构的关关算解析一、NaCl型(如图1)1.在晶体中,每个Na+同时吸引6个Cl-,每个Cl-同时吸引着6个Na+,阴、阳离子数目之比是1∶1。
2.在晶体结构中,每个基本结构单元(小立方体)的8个顶点分别由4个Na+、4个Cl-相邻占据,每个小立方体含Na+:(1/8)×4=(1/2)个、含Cl-:(1/8)×4=(1/2)个。
每个晶胞由8个小立方体构成,故每个晶胞有NaCl微粒8×(1/2)=4个。
3.在晶体中,经过立方体的中心Na+的平面有三个,每个平面的四个顶点上的Na+都同晶体中与中心Na+最接近且距离相等。
所以,在晶体中,每个Na+周围与它最接近的距离相等的Na+的个数共有12个。
同理,每个Cl-周围与它最接近且距离相等的Cl-的个数也有12个。
图1 NaCl晶体图2 CsCl晶体1.在晶体中,每个Cl-吸引8个Cs+,每个Cs+吸引8个Cl-,Cs+与Cl-的个数比为1∶1。
2.每个基本结构单元中(小立方体)含Cl-:(1/8)×8=1个,含Cs+1个。
3.在晶体中,若以一个Cs+为原点作三维空间坐标系,以相邻最接近的Cs+间的距离为半径作球面与坐标系共有6个交点。
所以,每个Cs+周围与它最接近且距离相等的Cs+的个数共有6个。
同理,每个Cl-周围与它最接近的且距离相等的Cl-共有6个。
三、干冰型(如图3)以晶型小立方体一个顶点为中心,相邻的三棱两两为边作截面(三个),根据晶体是由多个晶胞累积扩展的原则,可想像出来表示在晶胞图上与一个CO2分子相邻且等距离的CO2分子共有12个。
图3 干冰晶体四、正四面体型(金刚石、硅、二氧化硅)(如图4、图5)1.金刚石晶体中,每个碳原子与4个相邻的碳原子形成4个C—C键。
2.在金刚石晶体中,由于一个碳原子所形成的4个键共有C4^2=6种两两相邻的组合,每个键可形成两个近似垂直的六元环,故每个碳原子最多可形成6×2=12个六元环,一个六元环实际拥有6×(1/12)=(1/2)个碳原子。
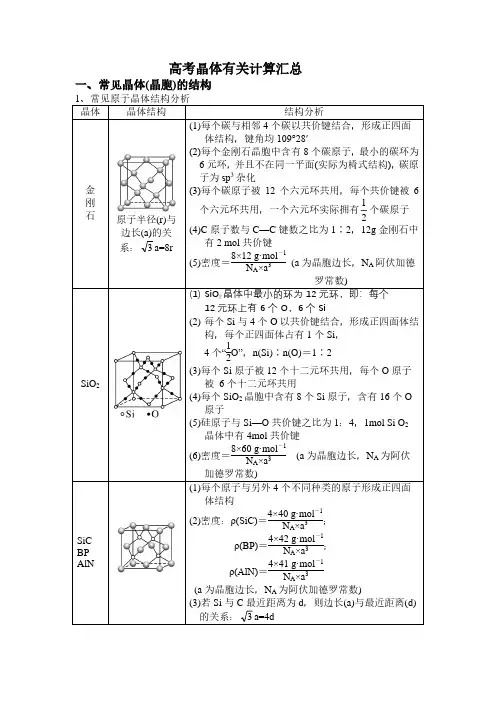

晶体结构高考题汇编20181121相对原子质量:Li-7,B-11,N-14,O-16,Na-23,S-32,K-39,Zn-65,Ge-73,Cu-64,Ni-59,题1 题2 题3 题41、(18国I)Li2O具有反萤石结构,晶胞如上图所示。
已知晶胞参数为0.4665 nm,阿伏加德罗常数的值为N A,则Li2O的密度为_________________________g·cm−3(列出计算式)。
2、(18国II)FeS2晶体的晶胞如上图所示。
晶胞边长为a nm,FeS2相对式量为M,阿伏加德罗常数的值为N A,其晶体密度的计算表达式为____________________________g·cm−3;晶胞中Fe2+位于S22-所形成的正八面体的体心,该正八面体的边长为___________nm。
3、(18国III)金属Zn晶体中的原子堆积方式如上图所示,这种堆积方式称为___________________,六棱柱底边边长为a cm,高为c cm,阿伏加德罗常数的值为N A,Zn的密度为____________________________g·cm−3(列出计算式)。
4、(2017卷I)(1)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立方结构,边长为a=0.446 nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如上图所示。
K与O间的最短距离为___________nm,与K紧邻的O个数为_____________。
(2)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于___________位置,O处于___________位置。
5、(2017国II)晶体R的密度为d g·cm−3,其立方晶胞参数为a nm,晶胞中含有y个[(N5)6(H3O)3(NH4)4Cl]单元,该单元的相对质量为M,则y的计算表达式为______________________________________。
选修3:物质结构与性质晶体结构的计算35.[化学—选修3:物质结构与性质](15分)(2018年全国卷I)Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。
回答下列问题:(5)Li2O具有反萤石结构,晶胞如图(b)所示。
已知晶胞参数为0.4665 nm,阿伏加德罗常数的值为N A,则Li2O的密度为g·cm−3(列出计算式)。
35.[化学——选修3:物质结构与性质](15分)(2018年全国卷II)(5)FeS2晶体的晶胞如图(c)所示。
晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为N A,其晶体密度的计算表达式为___________g·cm−3;晶胞中Fe2+位S 所形成的正八面体的体心,该正八面体的边长为______nm。
于2235.[化学——选修3:物质结构与性质](15分)(2018年全国卷III)锌在工业中有重要作用,也是人体必需的微量元素。
回答下列问题:(1)Zn原子核外电子排布式为________________。
(5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为_______________。
六棱柱底边边长为a cm,高为c cm,阿伏加德罗常数的值为N A,Zn的密度为________________g·cm-3(列出计算式)。
35.[化学——选修3:物质结构与性质](15分)(2017年全国卷III)35.[化学——选修3:物质结构与性质](15分)(2017年全国卷I)37.[化学——选修3:物质结构与性质](15分)(2016年全国卷III)37.[化学——选修3:物质结构与性质](15分)(2016年全国卷II)(4)某镍白铜合金的立方晶胞结构如图所示①晶胞中铜原子与镍原子的数量比为。
②若合金的密度为d g∙cm−3,晶胞参数为nm。
37.[化学——选修3:物质结构与性质](15分)(2016年全国卷I)(6)已知Ge单晶的晶胞参数a=565.76pm,其密度为g∙cm−3(列出计算式即可)(2016年四川高考)(2016年海南高考)37.[化学——选修3:物质结构与性质](15分)(2015年全国卷II)37.[化学——选修3:物质结构与性质](15分)(2015年全国卷I)(5) 碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:石墨烯晶体金刚石晶体①在石墨烯晶体中,C原子所连接个六元环,每个六元环占有个C原子在同一平面。
必刷题晶胞结构分析与计算建议完成时间:60分钟选择题:精选20题实际完成时间:分钟非选择题:精选0题1(2023·广东广州·统考三模)研究者利用冷冻透射电子显微镜,在石墨烯膜上直接观察到了自然环境下生成的二维晶体,其结构如图所示。
下列说法正确的是A.石墨烯属于烯烃,可发生加成反应B.石墨烯中碳原子的杂化轨道类型为sp2C.二维晶体的化学式为CaCl2D.二维晶体中Ca和Cl的配位数均为6【答案】B【详解】A.石墨烯属于碳单质,不含有H元素,不属于烯烃,不能发生加成反应,故A错误;B.石墨烯为平面结构,C的价层电子对数为3,故碳原子的杂化轨道类型为sp2,故B正确;C.每个Ca周围距离最近的Cl有3个,每个Cl周围距离最近的Ca有3个,故二维晶体的化学式为CaCl,故C错误;D.由C分析知,二维晶体中Ca和Cl的配位数均为3,故D错误;故选B。
2(2023·重庆沙坪坝·校考模拟预测)X为一种由汞(Hg)、锗(Ge)、锑(Sb)形成的可作潜在拓扑绝缘体材料的新物质,其晶胞如图所示(底面为正方形)。
下列说法错误的是A.X的化学式为GeHgSb2B.与Hg 距离最近的Sb 的数目为4C.若晶胞中原子1的坐标为(0,0,0),则原子2的坐标为34,34,34D.设X 的最简式的分子量为M r ,则X 晶体的密度为4M r ×1021N A a 2c g ⋅cm -3【答案】C【详解】A .X 中含Hg 个数为4×14+6×12=4,Ge 个数为8×18+4×12+1=4,Sb 个数为8,则X 的化学式为GeHgSb 2,故A 正确;B .以右侧面的Hg 分析,与Hg 距离最近的Sb 的数目为4,故B 正确;C .若晶胞中原子1的坐标为(0,0,0),则原子2在上面那个立方体的体对角线的四分之一处,其z 坐标为12+12×14=58,则其坐标为34,34,58 ,故C 错误;D .设X 的最简式的分子量为M r ,则X 晶体的密度为M r g ⋅mol -1N A mol -1×4(a ×10-7cm )2×c ×10-7cm =4M r ×1021N A a 2c g ⋅cm -3,故D 正确。
选修3:物质结构与性质晶体结构的计算35.[化学—选修3:物质结构与性质](15分)(2018年全国卷I)Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。
回答下列问题:(5)Li2O具有反萤石结构,晶胞如图(b)所示。
已知晶胞参数为0.4665 nm,阿伏加德罗常数的值为N A,则Li2O的密度为g·cm−3(列出计算式)。
35.[化学——选修3:物质结构与性质](15分)(2018年全国卷II)(5)FeS2晶体的晶胞如图(c)所示。
晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为N A,其晶体密度的计算表达式为___________g·cm−3;晶胞中Fe2+位S 所形成的正八面体的体心,该正八面体的边长为______nm。
于2235.[化学——选修3:物质结构与性质](15分)(2018年全国卷III)锌在工业中有重要作用,也是人体必需的微量元素。
回答下列问题:(1)Zn原子核外电子排布式为________________。
(5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为_______________。
六棱柱底边边长为a cm,高为c cm,阿伏加德罗常数的值为N A,Zn的密度为________________g·cm-3(列出计算式)。
35.[化学——选修3:物质结构与性质](15分)(2017年全国卷III)35.[化学——选修3:物质结构与性质](15分)(2017年全国卷I)37.[化学——选修3:物质结构与性质](15分)(2016年全国卷III)37.[化学——选修3:物质结构与性质](15分)(2016年全国卷II)(4)某镍白铜合金的立方晶胞结构如图所示①晶胞中铜原子与镍原子的数量比为。
②若合金的密度为d g∙cm−3,晶胞参数为nm。
37.[化学——选修3:物质结构与性质](15分)(2016年全国卷I)(6)已知Ge单晶的晶胞参数a=565.76pm,其密度为g∙cm−3(列出计算式即可)(2016年四川高考)(2016年海南高考)37.[化学——选修3:物质结构与性质](15分)(2015年全国卷II)37.[化学——选修3:物质结构与性质](15分)(2015年全国卷I)(5) 碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:石墨烯晶体金刚石晶体①在石墨烯晶体中,C原子所连接个六元环,每个六元环占有个C原子在同一平面。
选修3:物质结构与性质
晶体结构的计算
35.[化学—选修3:物质结构与性质](15分)(2018年全国卷I)
Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性
能,得到广泛应用。
回答下列问题:
(5)Li2O具有反萤石结构,晶胞如图(b)所示。
已知晶胞参数为0.4665 nm,阿伏加德罗常数的值为N A,则Li2O的密度为g·cm-3(列出计算式)。
35.[化学——选修3:物质结构与性质](15分)(2018年全国卷II)
(5)FeS2晶体的晶胞如图(c)所示。
晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为N A,其晶体密度的计算表达式为___________g·cm-3;晶胞中Fe2+位于
2
S所形成的正八面体的体心,该正八面体的边长为______nm。
2
35.[化学——选修3:物质结构与性质](15分)(2018年全国卷III)
锌在工业中有重要作用,也是人体必需的微量元素。
回答下列问题:
(1)Zn原子核外电子排布式为________________。
(5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为_______________。
六棱柱底边边长为a cm,高为c cm,阿伏加德罗常数的值为N A,Zn的密度为
-3(列出计算式)。
________________g·cm
35.[化学——选修3:物质结构与性质](15分)(2017年全国卷III)
35.[化学——选修3:物质结构与性质](15分)(2017年全国卷I)
37.[化学——选修3:物质结构与性质](15分)(2016年全国卷III)
37.[化学——选修3:物质结构与性质](15分)(2016年全国卷II)
(4)某镍白铜合金的立方晶胞结构如图所示
①晶胞中铜原子与镍原子的数量比为。
②若合金的密度为d,晶胞参数为nm。
37.[化学——选修3:物质结构与性质](15分)(2016年全国卷I)
(6)已知Ge单晶的晶胞参数a=565.76pm,其密度为(列出计算式即可)
(2016年四川高考)
(2016年海南高考)
37.[化学——选修3:物质结构与性质](15分)(2015年全国卷II)
37.[化学——选修3:物质结构与性质](15分)(2015年全国卷I)
(5) 碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:
石墨烯晶体金刚石晶体
①在石墨烯晶体中,C原子所连接个六元环,每个六元环占有个C原子在同一平面。
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接个六元环,六元环中最多有个C原子在同一平面。
37.[化学——选修3:物质结构与性质](15分)(2014年全国卷II)
37.[化学——选修3:物质结构与性质](15分)(2014年全国卷I)
(4) Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为。
列式表示Al单质的密度(不必计算出结果)
(2013年浙江高考21)
(2013年山东高考32)
37.[化学——选修3:物质结构与性质](15分)(2013年全国卷II)
37.[化学——选修3:物质结构与性质](15分)(2012年全国卷)
(此文档部分内容来源于网络,如有侵权请告知删除,文档可自行编辑修改内容,
供参考,感谢您的配合和支持)。