肺放线菌病24例临床及影像学分析并文献复习
- 格式:pdf
- 大小:300.65 KB
- 文档页数:1



卡氏肺囊虫性肺炎(PCP)影像学诊断卡氏肺囊虫性肺炎(Pneumocystis carinii pneumonia,缩写为PCP)是一种由于卡氏肺囊虫感染引起的肺部疾病。
它主要侵犯免疫功能低下的人群,尤其是艾滋病患者。
PCP的影像学诊断对于早期发现和治疗至关重要。
影像学表现1. X线胸片PCP的X线胸片表现可以分为三个阶段:浸润期、间质期和晚期。
在浸润期,胸片表现为肺纹理增粗和模糊,可见片状、颗粒状和网状浸润阴影,呈双侧对称分布,以肺野外周区域为主。
在间质期,胸片表现为肺纹理清晰,但在结构上仍然有增厚,呈双侧对称性和网状分布。
在晚期,胸片表现为肺纹理恢复正常,间质变薄,但可出现肺囊性病变和肺气肿等并发症。
2. CT扫描CT扫描是PCP影像学诊断的金标准,可以更准确地显示病变部位和范围。
在早期PCP病例中,CT扫描显示为双侧肺泡实变,呈磨玻璃影或类似肺炎的斑点状影像。
随着病情的发展,实变区域逐渐扩大,可见大片磨玻璃影像。
在晚期PCP病例中,CT扫描显示肺部病变范围扩大,出现肺泡壁裂隙和囊泡形成,形成特征性的“蜜蜂窝状”改变。
3. 其他影像学检查除了X线胸片和CT扫描,还可以通过核磁共振(MRI)和正电子发射断层扫描(PET)等影像学检查来辅助诊断PCP。
MRI可以显示肺部病变的微小改变,而PET可以定位肺部感染灶和评估炎症的活动度。
卡氏肺囊虫性肺炎是一种严重的肺部感染疾病,影像学诊断对于早期发现和治疗至关重要。
X线胸片和CT扫描是常用的影像学检查方法,可以显示肺部的病变范围和性质。
MRI和PET等辅助检查也可以提供更多的信息。
及早进行影像学诊断有助于及时治疗和改善患者的预后。


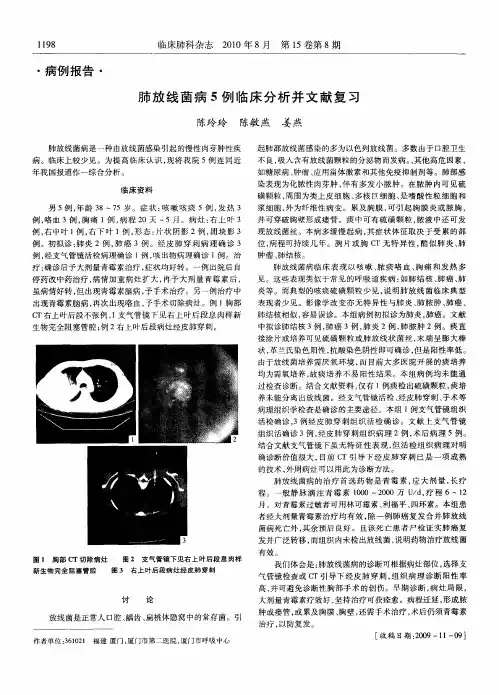


原发性苏黎世放线菌感染1例报告并文献复习摘要】放线菌病是指放线菌引起的人畜共患性疾病,主要表现为慢性、化脓性、肉芽肿性疾病,病程表现为慢性,部分表现为亚急性,由于其为口腔黏膜正常菌群,多通过口腔黏膜突破导致发病,因此多发生在面颊部、颈部,占所有患者中的60%,肺部、腹部、皮下局部均可发病,但相对罕见,其中皮下局部发病报道较少,本例患者表现为腋窝下包块,最终通过抽出分泌物培养、涂片、鉴定为苏黎世放线菌。
【关键词】放线菌;腋窝脓肿;苏黎世放线菌【中图分类号】R519 【文献标识码】A 【文章编号】2095-1752(2019)14-0067-021.资料与方法患者,胡某峰,男,23岁,因“右侧腋窝包块伴红肿疼痛5天”到重庆市某镇医院就诊,给予输注左氧氟沙星治疗5天,症状无减轻,右侧腋窝疼痛加重,右上肢活动受限。
为进一步诊治,于2018年5月21日到我院就诊,以“右侧腋窝脓肿”收入院。
入院查体:T 37.3℃,P 90次/分,R20次/分,BP:137/90mmHg。
急性痛苦表情,步入病房,右侧腋窝皮肤红肿,皮温高,皮下扪及一包块,约5.0x3.0cm,质中,无明显波动感,明显压痛。
体表包块彩超提示:右侧腋窝皮下低至无回声区,考虑脓肿。
胸片示:双肺纹理增多增粗。
血常规:WBC15.44x109/L,N0.79.44L。
在全麻下行了右侧腋窝脓肿切开引流术,术中见:右侧腋窝皮下脓腔,约5.0x3.0x3.0cm,脓腔内有分隔,且切开过程发现包块坚硬,切开困难,切开后有颗粒样物质流出,脓液立即行快速现场评价(raPID on~site evaluation,ROSE)检查,将分泌物送微生物室细菌培养及涂片(电话沟通怀疑放线菌病)。
术后诊断:右侧腋窝脓肿。
因疑诊腋窝下放线菌病,在引流同时,根据《热病~桑福德抗微生物指南》及《ABX指南:感染性疾病的诊断及治疗》予以替卡西林钠3.2g ivdriP q8h抗感染、补液、维持水电解质平衡等对症治疗,术后观察2天,患者手术切口生长良好,无脓液渗出,术后第3天微生物室报告:分泌物培养出放线菌(图1、图2),并送检重庆医科大学附属第一医院行质普分析提示苏黎世放线菌,经静脉抗感染5天后好转出院,并制定了6个月口服阿莫西林克拉维酸钾方案。


肺奴卡菌病1例并文献复习奴卡菌病是由奴卡菌属引起的急性、亚急性或慢性化脓性疾病。
奴卡菌病属机会性感染,其临床表现多变,肺部是主要的受累器官。
近年来,由于免疫抑制剂的使用以及检测方法的改进,本病的发病率呈上升趋势[1]。
但是,由于实验室检查技术的限制,本病极易误诊为其它疾病。
本文通过分析我院就诊的1例肺奴卡菌病患者的临床资料并进行文献复习,以提高对该病的认识。
一、临床资料患者男,17岁。
因“咳嗽、咳痰1周”于2013年1月10日入院。
患者于1周前受凉后出现咳嗽、咳黄痰,量不多,无发热、气促等不适。
门诊查血常规示白细胞23.1×109/L,中性粒细胞比例86.3%,胸片示:右上肺感染,予以“头孢硫脒”治疗4天后症状改善不明显入院。
2月余前因肾病综合征一直口服激素治疗,现治疗剂量为甲泼尼龙12mg/天。
入院后查血常规示白细胞15.9×109/L,中性粒细胞比例81.6%,胸部CT示:右肺上叶尖后段及肺门旁可见多个团片状密度增高影,部分病灶已液化(图1左)。
入院后予头孢哌酮+甲硝唑抗感染,并行纤维支气管镜检查示右肺上叶开口处见较多白色粘性分泌物,2次支气管灌洗液涂片见少量G+杆菌,菌体呈菌丝状,疑似奴卡菌属某种;支气管刷取物16S rRNA 基因测序确诊为奴卡菌感染。
随后2次痰涂片亦见少量G+杆菌,疑似奴卡菌属某种。
考虑为患者本身患肾病综合征及长期使用激素导致奴卡菌感染,在使用头孢哌酮及甲硝唑的基础上加用复方磺胺甲噁唑抗奴卡菌感染,同时予以激素逐渐减量至甲泼尼龙10mg/天维持,期间查头颅CT未见明显异常。
治疗三天后患者咳嗽明显减轻,咳少量黄白色粘痰,两周后复查血常规示白细胞14.9×109/L,中性粒细胞比例78.4%,胸部CT示右肺上叶病变明显吸收,残留多发薄壁空洞影(图1中),予以出院并继续予复方磺胺甲噁唑治疗,出院三月后复查胸部CT示右上肺渗出病变较前进一步吸收,边界较前清楚,原空洞范围较前缩小(图1右)。

肺肺曲霉菌病影像学诊断(一)引言概述:肺肺曲霉菌病是一种由肺曲霉菌感染引起的疾病,在临床上较常见。
准确的影像学诊断对疾病的早期发现和治疗至关重要。
本文将重点介绍肺肺曲霉菌病的影像学诊断,以帮助医生更好地理解该疾病的特点和诊断方法。
正文:一、影像学表现特点1. 广泛散在的结节阴影2. 空洞形成和空气支气管征3. 肺实质病变和纤维化表现4. 支扩大和气胸的出现5. 心脏扩大及胸腔积液的征象二、结节阴影的特征1. 多发性结节阴影2. 结节阴影的大小和形态3. 结节阴影的边缘特征4. 结节阴影的分布情况5. 结节阴影与其他疾病的鉴别诊断三、空洞形成和空气支气管征的诊断1. 空洞的形态和大小2. 空气支气管征的表现3. 空气支气管征与其他疾病的鉴别诊断4. 空洞形成与疾病进展的关系5. 空洞形成和空气支气管征的预后评估四、肺实质病变和纤维化的表现1. 炎症性反应的表现2. 纤维化的程度和范围3. 纤维化的类型和形态4. 纤维化与功能限制的关系5. 肺实质病变和纤维化的治疗方法五、支扩大和气胸的诊断1. 支扩大的特征2. 支扩大与肺功能损害的关系3. 气胸的形态和大小4. 气胸的原因与发展5. 支扩大和气胸的治疗措施总结:肺肺曲霉菌病的影像学诊断是对该疾病进行早期发现和治疗的重要手段。
通过了解该疾病的影像学特点,如广泛散在的结节阴影、空洞形成和空气支气管征、肺实质病变和纤维化表现、支扩大和气胸等,医生可以更准确地诊断该疾病,为患者提供及时有效的治疗措施。
因此,对于临床医生而言,学习和掌握肺肺曲霉菌病的影像学诊断方法具有重要的临床意义。
放线菌病:放线菌病(actinomycosis)主要是以色列氏放线菌(actinomyces israeli)引起的一种慢性化脓性炎症。
根据现代的生物学分类,放线菌不属于真菌而属于一种厌氧细菌。
由于它所引起的病变与霉菌病相似,以及按照过去的习惯,通常仍将放线菌病与真菌病一起叙述。
放线菌有细胞壁,其化学成分与细菌相似,没有核膜。
菌体呈细丝状,与真菌相似,菌丝的粗细与普通杆菌相似,一般直径不超过1μm。
菌丝分支,可断裂为杆状。
放线菌的种类很多。
在自然界分布极广,空气、土壤、水源中都有放线菌存在。
少数菌株对人类有致病性,其中最主要的为以色列氏放线菌。
以色列氏放线菌是人口腔正常菌群中的腐物寄生菌,在拨牙、外伤或其它原因引起口腔粘膜损伤时,放线菌可由伤口侵入。
也可通过吞咽或吸入带菌物质进入胃肠或肺。
因此放线菌病主要发生于颈面部和胸腹器官。
病理变化放线菌病和病变为慢性化脓性炎症。
局部组织水肿,有大量中性粒细胞和单核细胞浸润,其间逐渐出现许多大小不等的坏死区,形成多数小脓肿,周围纤维组织增生。
脓肿大小不等,常相互融合,并向邻近组织蔓延,形成许多窦道和瘘管。
脓肿壁和窦道周围肉芽组织内有大量中性粒细胞、淋巴细胞和单核细胞浸润,有时并有少数多核巨细胞,部分可见大量吞噬脂类的巨噬细胞,因此肉眼观常带黄色。
放线菌在脓肿壁、窦道壁和脓腔内繁殖,形成菌落。
有时肉眼可见脓液内有细小的黄色颗粒,直径约1~2mm,称为“硫黄颗粒”。
取硫黄颗粒直接压片或在组织切片中可见颗粒由分支的菌丝交织而成。
在HE染色的组织切片中,颗粒中央部分染蓝紫色,周围部分菌丝排列成放线状,菌丝末端常有胶样物质组成的鞘包围而膨大呈棒状,染伊红色,所以称为放线菌(图18-36)。
病灶中的“硫黄颗粒”,周围部分菌丝排列成放线状。
菌丝末端膨大呈棒状有时组织切片中菌丝不明显,可作革兰染色,放线菌菌丝体为革兰阳性,胶样鞘为革兰阴性,据此可确诊为放线菌病。
放线菌病常同时合并其他细菌感染。
隐源性机化性肺炎(cryptogenic organizing pneumonia,COP)是指病因不明的机化性肺炎。
由于临床医师对本病缺乏认识,易引起误诊。
现报告我院收治的1 例隐源性机化性肺炎并进行文献复习。
病例资料:患者林清华,男,30岁,因“进行性气促1月余”于2009-5-26入院。
患者于2009年4月10日始,无明显诱因下出现活动后气促,运动耐力明显下降,登3楼即出现明显气促,休息后可缓解,无咳嗽、咳痰,无喘息,无胸闷、胸痛、心悸,夜间可平卧,无夜间阵发性呼吸困难,无发热、畏寒,无关节疼痛,无咯血、盗汗,未予重视,气促呈进行性加重,于2009-5-15到当地医院住院,查肺功能示;重度限制性通气功能障碍,支气管扩张试验阴性。
ENA :S-SB弱阳性,余阴性。
免疫五项、ANCA、抗核抗体阴性。
支气管镜示:气管及1-3级气管内未异常,刷检找抗酸杆菌,找真菌未见异常,灌洗液培养未见异常。
胸部CT:肺内弥漫斑片状及结节状病变,考虑肺内特殊感染,不除外肿瘤。
考虑“肺部感染”予“莫西沙星0.4ivdrip qd”抗感染治疗10天,气促无好转,且进行性加重,平静状态下亦感气促。
遂到我院就诊,拟“双肺弥漫性病变待查”收入我科,起病以来,精神欠佳,睡眠、胃纳可,二便正常,体重近1月来下降约4KG。
既往史:否认肝炎、结核等传染病史,否认高血压病史。
个人史:现从事装饰业半年,偶接触刺激性气味,居住环境可,吸烟10余年,10-20支/天不等,否认吸毒、性病、冶游史。
家族史:家族中无类似症状患者。
入院体查:T37.0℃,P90次/分,R26次/分,BP120/73mmHg,SPO291%(FiO2 21%)。
体型肥胖,全身皮肤未见皮疹。
全身浅表淋巴结无肿大。
无鼻翼扇动,颈静脉无怒张,肝颈静脉回流征(-),气管居中,胸廓无畸形,呼吸稍促,双肺活动度正常,叩诊清音,左肺呼吸音稍弱,右下肺可闻及少量细湿罗音,无干罗音,无胸膜摩擦音,心率90次/分,律齐,未闻及病理性杂音,双下肢无浮肿。
肺放线菌病24例临床及影像学分析并文献复习
发表时间:2013-02-22T11:22:52.793Z 来源:《医药前沿》2012年第34期供稿作者:高万本[导读] 肺放线菌病是一种少见的慢性化脓性肉芽肿性疾病,属肺霉菌感染的一种。
高万本(绵阳市第三人民医院医学影像科四川绵阳 621000)
肺放线菌病是一种少见的慢性化脓性肉芽肿性疾病,属肺霉菌感染的一种。
近年来由于抗生素、激素、细胞毒性药物和免疫抑制剂的大量应用,肺放线菌病的发病率有所增加。
为探讨肺放线菌病的临床及影像学表现特点及诊断方法,结合我院近年诊治的1例肺放线菌病,以及国内近18年(1989~2006年)文献报道的肺放线菌病23例[1-18]进行综合分析并进行文献复习。
1 临床资料
24例肺放线菌病均径病理证实。
其中男15例,女9例,年龄11~87岁,平均年龄49岁。
临床表现:24例均有咳嗽、咳痰等呼吸道症状;其中伴胸痛者10例,伴发热者8例,咳痰带血者3例,痰中带黄色颗粒者2例,盗汗者1例。
发病部位:病变位于左肺上叶8例,左肺下叶3例,位于右肺上叶6例,右肺中叶3例,右肺下叶2例,双肺均有病变2例。
病程1个月~5年不等。
影像学表现:12例表现为肺部实质性肿块或球形病灶,边缘有分叶,周围无卫星病灶;1例病变向上经胸廓入口侵犯至颈根部;5例表现为肺部片状阴影伴胸腔积液;3例表现为支气管扩张改变;2例肺部有空洞改变;1例表现为气管及纵隔向患侧移位。
临床诊断及治疗:15例术前误诊为肺癌,2例误诊为结核球,4例误诊为肺化脓症,2例镜检确诊为本病,1例术中冰冻切片为恶性,术中行扩大切除,术后病检为放线菌病,术后半年复发,再次行手术扩大切除。
20经例手术治疗,4例保守治疗,术后均作病理检查,确诊后给予大剂量青霉素静脉滴注。
术中见患肺与胸壁粘连,尤以肿物处明显,肿物大小各不相同,形态各异,无包膜,质地坚硬,并与健肺粘连,浸润生长。
标本大体所见:肿物部位成灰白色或灰黄色,实性,挤压有少量脓液溢出。
光镜下见病变肺组织类似化脓性肉芽肿样改变,有大量中性粒细胞、单核细胞、淋巴细胞浸润,其间可见大小不等的坏死区,坏死区边缘可见成团粉染的无结构团块,其中大部分成蓝紫色,周围部分排裂成放射状,末端呈球形膨大,PAS染色团块无结构物阳性反应,病变周围的肺组织类似大叶性肺炎肉质性变及纤维化。
其中7例光镜观察到硫磺颗粒,2例观察到放线菌丝,3例痰培养见霉菌生长。
2 讨论
肺放线菌病是由以色列放线菌感染所致,致病菌一般寄生于健康人龋齿及扁桃体小窝内,常因吸入口腔分泌物而得病。
放线菌从支气管蔓延到肺,先引起支气管肺炎,后形成肉芽肿,并侵入胸膜或胸壁软组织,常形成脓胸或胸壁窦道,如并发其他细菌感染,病变常迁延不愈。
肺放线菌病发病部位多变,病程复杂[18]。
临床表现以肺部慢性炎性表现多见,偶有咳黄色颗粒者,症状不典型。
影像学改变与肺炎、肺脓肿、肺结核、肺癌、支气管扩张相似,易误诊。
本组病例除2例诊断正确,其余22例均误诊。
据统计[10],从1971~1988年日本征集到的43例肺放线菌病例中,有30例(占70%)是通过肺病理组织切片检查确诊的。
本组有15例(占63%)初始疑为肺癌、肺结核或支气管扩张,治疗后症状和影像学表现均无改善,最后经纤支镜检查、手术肺叶切除、肺病理组织切片检查确诊。
说明本病早期确诊困难,误诊率高。
误诊原因有[17]:(1)多数临床医生和影像学医生认为放线菌感染较罕见,对其致病性重视不够,对病原菌缺乏认识。
(2)在工作中,分离临床标本中的放线菌比较困难,因为正常菌群的拮抗作用,营养竞争,这需要有标准的培养技术,控制合适的生长条件和针对某些菌采用特殊的培养基。
(3)使用不适当的检验方法导致检出率下降。
由于放线菌培养需要厌氧环境,而目前大多数医院开展的痰培养均是需氧培养,加上培养前用药影响,故痰培养均未能分离出放线菌。
(4)临床实验室仍未广泛应用检验放线菌较可靠的现代分类学方法[11]。
放线菌并非真菌,而类似细菌,菌种的鉴定不能仅靠形态学,必须结合生化反应。
如果标本在使用抗生素治疗前采集,临床上又有高度怀疑放线菌病时,可适当延长厌氧培养时间,以提高阳性培养结果。
肺放线菌病可靠的诊断方法是作纤支镜活组织检查,检出放线菌或对咯出物及窦道流出物的涂片检查,找到硫磺颗粒,后者是一种简单易行的方法,但阳性率不高,本组阳性率为27%[17]。
胸水中培养出放线菌也可确诊。
参考文献
[1]沙宝康,戴法召.肺放线菌病1例报告[J].内蒙古医学杂志.1989,9 (2):63.
[2]张澜,崔忠厚.左下肺放线菌病误诊1例[J].中华胸心血管外科杂志,1995,11(3):118.
[3]刁晓源,冯端兴,乐万祥,等.肺放线菌病2例[J].中华结核和呼吸杂志,1995,18(4):238.
[4]左万里.肺放线菌病误诊为支气管扩张症1例[J].中国实用内科杂志,1997,17(10):595.
[5]王军,王占东,吕建军.肺放线菌病1例[J].河北医科大学学报,1998,19(6):334.
[6]全亚群.肺放线菌病误诊为肺肿瘤1例[J].山西医药杂志,1998,27 (6):502.
[7]牟小芳,张进川.肺癌合并下呼吸道放线菌病1例[J].中华结核和呼吸杂志,1998,21(7):391.
[8]王礼斌,熊健,汤服民.肺放线菌病误诊1例[J].实用医药杂志,1999,12(1):14.
[9]张文,田新平,曾小峰,等.肺放线菌病1例[J].中华传染病杂志,1999,17(2):144.
[10]王红霞,李敬孚.术后并发脓胸的肺放线菌病的治疗[J].国外医学.呼吸系统分册,1995,15(2):11.
[11]阮继生,刘志恒,梁丽糯,等.放线菌研究及应用[M].北京:科学出版社,1990,393.
[12]刘国媚,刘平,崔皖芳,等.原发生肺放线菌病临床分析[J].安徽医药,2001,5(1):41-42.
[13]卑贵光,刘智明,马洁韬,等.肺放线菌病的CT诊断[J].中华综合医学,2002,3(5):447-448.
[14]张光然.肺放线菌病2例误诊分析[J].临床经验荟萃,2002,P(5):25.
[15]崔书安,徐宝亮,仲伟英.肺放线菌病1例[J].医学影像学杂志,2002,12(4):257.
[16]线胤生,弓显凤.肺放线菌病例[J].中国抗感染化疗杂志,2004,4 (5):308—309.
[17]李少文,马琼凤,李庆安.肺放线菌病11例临床分析并文献复习.Journal of postgraduates of Medicine(Medicine Edition),2004;27:32.
[18]陈刚,张林,叶宏飞.肺放线菌病的诊断与治疗11例报告[J].中国医科大学学报,2005,34(2):187.。