第二单元课题2氧气
- 格式:doc
- 大小:108.50 KB
- 文档页数:5

教案课前预习1、生物体所必需的气体是什么?回顾一下生物中所学的知识:什么是呼吸作用?2、通过各种途径了解氧气除了提供给我们呼吸以外,在我们的日常生活中,它还有哪些应用?课上将你了解的知识向大家介绍一下。
3、有什么事实能证明自然界的水中溶有氧气?课内探究一、学习目标1.记住:氧气的存在、自然意义及常见物理性质(不要求记忆具体数据)。
2.了解:常见物质在空气中、氧气中燃烧的现象和产物。
包括:木炭、铁丝、蜡烛、红磷、硫磺等。
领会氧气化学性质的活泼性。
学会检验氧气存在和氧气收集验满。
3.了解:氧化反应、缓慢氧化的基本含义,并能判断常见生活现象是否属于缓慢氧化。
分辨可燃与支持燃烧这两个易混概念。
4.了解:氧气的主要用途。
二、方法指引请同学们看书后回答:1.学习一种具体物质的化学方法是什么?一般包括学习物质的性质、制法、用途、在自然界的存在形式等方面的内容。
在学习氧气时,首先要牢固掌握氧气的性质,再根据性质去了解氧气的用途及制法等。
学习氧气的性质应了解氧气的物理性质,重点掌握氧气的化学性质。
2.如何通过实验获得知识并培养多种能力氧气的性质是学习的重点,对于氧气的性质的感性认识必须通过实验来完成。
可将所做实验内容进行归类整理:3.如何解物质的鉴别习题?分析:鉴别几种物质时应遵循的一般原则:(1)比较物质的性质(物理性质、化学性质),有哪些较明显的差异;(2)实验时可观察到的现象是否有较明显的区别;(3)实验操作(物理方法或化学方法)是否方便、可行;(4)应按“操作——现象——结论”的次序叙述。
例如:怎样用化学方法鉴别分别装有氧气、空气、氮气的三瓶无色气体?答:用燃烧着的木条,分别伸入这三个集气瓶中,能使燃着的木条燃烧更旺的是氧气,能使燃烧的木条熄灭的是氮气,而没有明显变化的则是空气。
4.在描述化学反应时要注意“加热”、“点燃”和“燃烧”,“火焰”与“发光”等述语的区别。
三、实验探究:学生分组实验,教师巡堂指导。

第二单元课题2 氧气教学设计一、教材分析本节课是人教版(2012年版)《义务教育教科书·化学(上册)》第二单元课题2《氧气》。
本课题包括氧气的性质和化合反应、氧化反应两种化学反应类型两部分。
教材以氧气的性质为核心,通过氧气所能发生的一些具体的化学反应,介绍了化合反应的基本概念。
第一部分从介绍氧气的物理性质入手,通过带火星的木条、硫、木炭、铁几种物质在氧气中反应所发生的现象,总结出氧气的化学性质。
第二部分通过实验和讨论归纳,学习化学反应中的一些常见类型:化合反应、氧化反应。
通过本课题的学习,为后面其它物质的学习奠定基础,也激发了学生对学习氧气的制法的迫切愿望,因此本节课起到承前启后的作用。
二、学情分析经过以前的学习,学生对氧气有了初步的了解,但知识不够系统;学生会进行一些简单实验操作,但操作不够规范;对通过实验研究物质及其变化的方法有所了解,但不会运用。
三、素养目标(即教学与评价目标)【教学目标】1.通过硫、碳、铁与氧气反应的实验,知道氧气的性质和用途;认识化学反应,了解化学反应的基本特征,认识化合反应和氧化反应,知道缓慢氧化这一生活中的化学现象。
(知识与技能)2.学习对实验的观察和描述,从实验中获取化学信息;学习从具体到抽象,从个别到一般的归纳方法。
(过程与方法)3.培养实事求是、尊重科学以及事物发展规律的科学态度;逐步树立“性质决定用途,用途体现性质”的辩证规律观点。
(情感态度与价值观)【评价目标】1.通过探究硫、碳、铁与氧气反应,在实验活动的过程中,诊断和发展对实验的观察、分析判断能力及动手实验能力(探究水平)。
2. 通过对实验现象的分析和归纳、对反应的分析,了解生活中的缓慢氧化现象,诊断与发展学生对氧气的性质、化合反应、氧化反应等知识的认知水平(认知水平)。
3. 通过实验现象得出结论,诊断并发展学生实事求是、尊重科学以及事物发展规律的科学态度(价值水平:学科价值、社会价值和育人价值)。
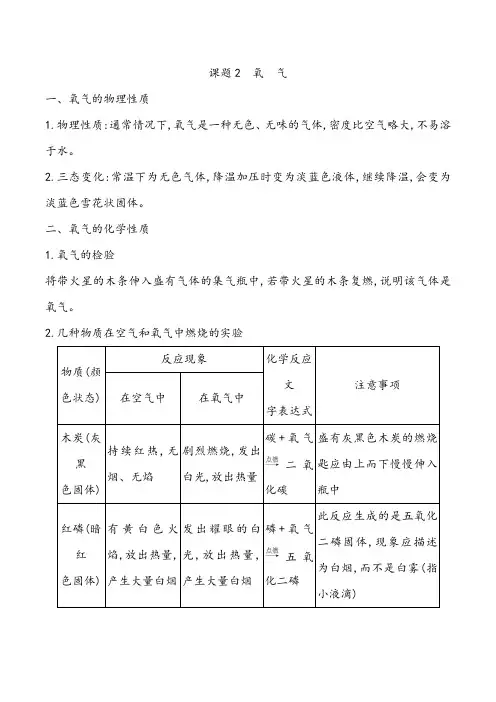
课题2 氧气一、氧气的物理性质1.物理性质:通常情况下,氧气是一种无色、无味的气体,密度比空气略大,不易溶于水。
2.三态变化:常温下为无色气体,降温加压时变为淡蓝色液体,继续降温,会变为淡蓝色雪花状固体。
二、氧气的化学性质1.氧气的检验将带火星的木条伸入盛有气体的集气瓶中,若带火星的木条复燃,说明该气体是氧气。
2.几种物质在空气和氧气中燃烧的实验发出碳+氧气二氧化碳盛有灰黑色木炭的燃烧匙应由上而下慢慢伸入瓶中白,磷+氧气五氧化二磷此反应生成的是五氧化二磷固体为白烟小液滴发出色热生成一种无有刺激性气硫+氧气二氧化硫①硫的用量不能过多防止对空气造成污染②实验前在集气瓶底放少量水的有毒气体火星放出大量生成黑色铁+氧气四氧化三铁①用砂纸打磨过的细铁丝柴②预先放少量水或细沙于瓶底温熔融物使瓶炸裂特别提醒:描述物质在氧气中燃烧的现象时,一般考虑四个方面:(1)物质原来的颜色;(2)对产生的光(火焰或火星)加以描述;(3)放出热量;(4)对生成物的颜色、状态、气味及其他性质加以描述。
三、化合反应与氧化反应1.化合反应化合反应2.氧化反应概念:物质与氧发生的反应叫做氧化反应。
氧气在氧化反应中提供氧,具有氧化性。
注意:氧化反应概念中的“氧”不仅仅是指氧气,也可以是含氧物质中的氧,即氧化反应不一定是物质和氧气的反应,但物质和氧气发生的反应一定属于氧化反应。
3.缓慢氧化有些氧化反应进行得很慢,甚至不容易被察觉,这种氧化叫做缓慢氧化。
如动植物的呼吸、食物的腐烂等。
氧化反应包括剧烈氧化和缓慢氧化两种。




第二单元 课题2氧气初中化学九年级上册 RJ学习目标1.认识氧气能与许多物质发生化学反应,氧气的化学性质比较活泼;2.认识化合反应、氧化反应;3.学会描述化学反应中的一些反应现象。
新知导入水中溶解了氧气让鱼儿能在水中生存,而氧气的这个用途是由它的性质来决定的。
你能说出氧气的一些性质吗?知识点1 氧气的性质新知探究通常状况下,氧气是无色、无味的气体,密度比空气略大,不易溶于水。
无色气体淡蓝色液体101kPa -183℃三态变化:淡蓝色固体(雪花状)物理性质101kPa -218℃加压贮存在蓝色钢瓶中。
氧气的检验方法:将带火星的木条伸入集气瓶内。
现象:木条复燃。
各种物质在空气中和氧气中燃烧的现象一样吗?硫在空气中与氧气中燃烧发出微弱的淡蓝色火焰,放出热量,生成有刺激性气味的气体。
表达式:硫 + 氧气 二氧化硫点燃氧气中发出明亮的蓝紫色火焰,放出热量,生成有刺激性气味的气体。
空气中硫在空气与氧气中燃烧的实验现象实验时集气瓶中为什么要放少量水资料提示:二氧化硫是一种无色、有刺激性气味的有毒气体,易溶于水且与水反应,与水蒸气结合会产生酸雨,是大气污染物之一。
实验时集气瓶中水的作用:吸收二氧化硫,减少空气污染。
木炭在空气中与氧气中燃烧持续红热,放出热量,生成能使澄清石灰水变浑浊的气体。
表达式:碳 + 氧气 二氧化碳点燃氧气中剧烈燃烧,发出白光,放出热量,生成能使澄清石灰水变浑浊的气体。
空气中木炭在空气与氧气中燃烧的实验现象中,确保木炭与氧气充分反应,现象明显。
铁丝在氧气中燃烧红热,不能燃烧。
表达式:铁 + 氧气 四氧化三铁点燃铁丝在氧气中燃烧的实验现象:剧烈燃烧,火星四射,放出热量,生成黑色固体。
铁丝在空气中燃烧的实验现象:回顾实验,思考以下操作的原因①实验前铁丝需打磨:除去铁丝表面的铁锈,有利于铁丝和氧气反应。
②将铁丝绕成螺旋状:增大铁丝的受热面积,有利于铁丝持续燃烧。
③铁丝下端系一根火柴:引燃铁丝。
④待火柴即将燃尽时再将铁丝伸入集气瓶中:防止火柴燃烧消耗集气瓶中过多的氧气而使铁丝燃烧现象不明显。



