工程热力学第2讲-第1章基本概念
- 格式:ppt
- 大小:1000.00 KB
- 文档页数:13


(2)由表B 的读数可知21p p p p p B b C +=+= ⇒ 21p p > 又 C 表为真空表⇒ 21p p p b >>又 )(21b A B B p P p p p p ++=+= 得 表A 的读数为真空度,A 表为真空表∴ 7324971=-=-=C b p p p (KPa )609736731-=--=--=b B A p p p p (KPa ) 即表A 的读数为真空度60KPa(注:表B 的环境压力为容器2的压力) 4、比体积及密度(1)比体积v :单位质量的物质所占有的体积,单位:Kg m /3表达式为:mVv =或 v m V ⋅= 其中:v ——比体积, V ——体积(3m ) m ——质量(Kg )(2)密度:单位体积物质的质量,单位:3/m Kg 表达式为:Vm =ρ v 和ρ互成倒数,因此不是相互独立的参数。
注:工程热力学中通常用v 作为独立参数。
§1-4 平衡状态、状态方程式、坐标图例1:A 、B 两物体的温度分别为A T 、B T ,且B A T T >,当相互接触后,经过一段时间,A 物体的温度逐渐降低,B 物体的温度逐渐升高,最后A 、B 两物体的温度趋于一致。
例2:有一封闭容器,有隔板将其分成A 、B 两部分,A 有气体,B 抽成真空。
当把隔板抽开后,由于A 、B 两边压力不等,A 的气体会向B 转移,过一段时间后,A 、B 两边气体的压力会趋于一致。
2、状态方程对于简单可压缩系统,在处于平衡状态时,两个独立的状态参数确定后,其它的状态参数可通过一定的热力学函数关系来确定,这样系统的平衡状态就完全确定了。
温度、压力和比体积这三个基本状态参数之间的函数关系是最基本的热力学函数关系,称为状态方程,可表示为: 0),,(=T v p f或写成显式形式为: ),(v T p p = ),(v p T T = ),(T p v v =这里只给出表达形式,针对具体情况,状态方程有具体的表述,我们将在以后的章节中进行介绍。




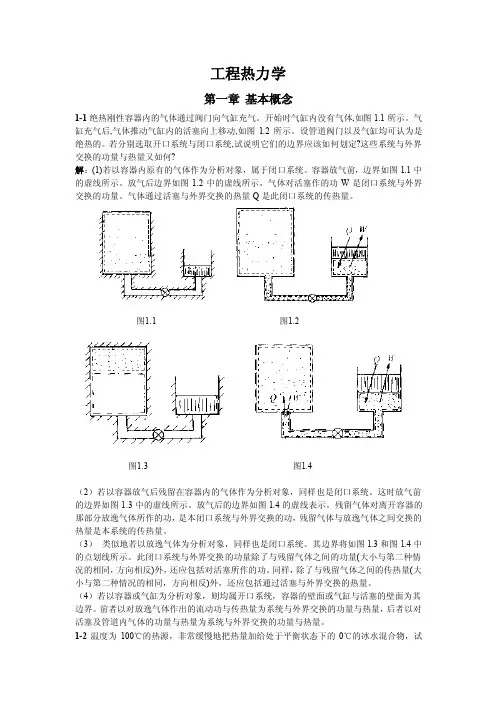
工程热力学第一章基本概念1-1绝热刚性容器内的气体通过阀门向气缸充气。
开始时气缸内没有气体,如图1.1所示。
气缸充气后,气体推动气缸内的活塞向上移动,如图1.2所示。
设管道阀门以及气缸均可认为是绝热的。
若分别选取开口系统与闭口系统,试说明它们的边界应该如何划定?这些系统与外界交换的功量与热量又如何?解:(1)若以容器内原有的气体作为分析对象,属于闭口系统。
容器放气前,边界如图1.1中的虚线所示。
放气后边界如图1.2中的虚线所示。
气体对活塞作的功W是闭口系统与外界交换的功量。
气体通过活塞与外界交换的热量Q是此闭口系统的传热量。
图1.1 图1.2图1.3 图1.4(2)若以容器放气后残留在容器内的气体作为分析对象,同样也是闭口系统。
这时放气前的边界如图1.3中的虚线所示。
放气后的边界如图1.4的虚线表示。
残留气体对离开容器的那部分放逸气体所作的功,是本闭口系统与外界交换的功,残留气体与放逸气体之间交换的热量是本系统的传热量。
(3)类似地若以放逸气体为分析对象,同样也是闭口系统。
其边界将如图1.3和图1.4中的点划线所示。
此闭口系统与外界交换的功量除了与残留气体之间的功量(大小与第二种情况的相同,方向相反)外,还应包括对活塞所作的功。
同样,除了与残留气体之间的传热量(大小与第二种情况的相同,方向相反)外,还应包括通过活塞与外界交换的热量。
(4)若以容器或气缸为分析对象,则均属开口系统,容器的壁面或气缸与活塞的壁面为其边界。
前者以对放逸气体作出的流动功与传热量为系统与外界交换的功量与热量,后者以对活塞及管道内气体的功量与热量为系统与外界交换的功量与热量。
1-2温度为100℃的热源,非常缓慢地把热量加给处于平衡状态下的0℃的冰水混合物,试问:1、冰水混合物经历的是准静态过程吗?2、加热过程是否可逆?解:此热力过程为准静态过程,因为此热力过程的弛豫时间很短,热源非常缓慢地把热量加给冰水混合物,则冰水混合物重建热力平衡的时间远远小于传热过程对冰水混合物平衡状态的破坏,所以可以近似地把此热力过程看作是准静态过程。
1-2 热力系统
1、基本概念
■热力系统(thermodynamic system)
被人为地从周围物体中分割出来,作为热力学
分析对象的有限物质系统。
■外界(surrounding)
与系统发生质能交换的物体。
■边界(boundary)
系统与外界的分界面。
8(a)汽轮机
(a)开口系统
●表压力
(gauge pressure)和真空度(vacuum)
e p v p 压力计处于环境压力下测得的工质压力。
●各压力之间的关系
24
b e
p
p p =+b v
p p p =-当绝对压力高于大气压力时:当绝对压力低于大气压力时:
均匀>平衡>稳定。
pdV
图上,可以用过程
体积变化功的正负与体积的变化相同,
工质膨胀时对外界作功,工质压缩时外界对工质V。
试分别求两过程的
1
初、终状态相同,但中间途径不同,因此膨胀功不同。
41。


第一章基本概念1.基本概念热力系统:用界面将所要研究的对象与周围环境分隔开来,这种人为分隔的研究对象,称为热力系统,简称系统。
边界:分隔系统与外界的分界面,称为边界。
外界:边界以外与系统相互作用的物体,称为外界或环境。
闭口系统:没有物质穿过边界的系统称为闭口系统,也称控制质量。
开口系统:有物质流穿过边界的系统称为开口系统,又称控制体积,简称控制体,其界面称为控制界面。
绝热系统:系统与外界之间没有热量传递,称为绝热系统。
孤立系统:系统与外界之间不发生任何能量传递和物质交换,称为孤立系统。
单相系:系统中工质的物理、化学性质都均匀一致的系统称为单相系。
复相系:由两个相以上组成的系统称为复相系,如固、液、气组成的三相系统。
单元系:由一种化学成分组成的系统称为单元系。
多元系:由两种以上不同化学成分组成的系统称为多元系。
均匀系:成分和相在整个系统空间呈均匀分布的为均匀系。
非均匀系:成分和相在整个系统空间呈非均匀分布,称非均匀系。
热力状态:系统中某瞬间表现的工质热力性质的总状况,称为工质的热力状态,简称为状态。
平衡状态:系统在不受外界影响的条件下,如果宏观热力性质不随时间而变化,系统内外同时建立了热的和力的平衡,这时系统的状态称为热力平衡状态,简称为平衡状态。
状态参数:描述工质状态特性的各种物理量称为工质的状态参数。
如温度(T)、压力(P)、比容(υ)或密度(ρ)、内能(u)、焓(h)、熵(s)、自由能(f)、自由焓(g)等。
基本状态参数:在工质的状态参数中,其中温度、压力、比容或密度可以直接或间接地用仪表测量出来,称为基本状态参数。
温度:是描述系统热力平衡状况时冷热程度的物理量,其物理实质是物质内部大量微观分子热运动的强弱程度的宏观反映。
热力学第零定律:如两个物体分别和第三个物体处于热平衡,则它们彼此之间也必然处于热平衡。
压力:垂直作用于器壁单位面积上的力,称为压力,也称压强。
相对压力:相对于大气环境所测得的压力。
第一章基本概念1.基本概念热力系统:用界面将所要研究的对象与周围环境分隔开来,这种人为分隔的研究对象,称为热力系统,简称系统。
边界:分隔系统与外界的分界面,称为边界。
外界:边界以外与系统相互作用的物体,称为外界或环境。
闭口系统:没有物质穿过边界的系统称为闭口系统,也称控制质量。
开口系统:有物质流穿过边界的系统称为开口系统,又称控制体积,简称控制体,其界面称为控制界面。
绝热系统:系统与外界之间没有热量传递,称为绝热系统。
孤立系统:系统与外界之间不发生任何能量传递和物质交换,称为孤立系统。
单相系:系统中工质的物理、化学性质都均匀一致的系统称为单相系。
复相系:由两个相以上组成的系统称为复相系,如固、液、气组成的三相系统。
单元系:由一种化学成分组成的系统称为单元系。
多元系:由两种以上不同化学成分组成的系统称为多元系。
均匀系:成分和相在整个系统空间呈均匀分布的为均匀系。
非均匀系:成分和相在整个系统空间呈非均匀分布,称非均匀系。
热力状态:系统中某瞬间表现的工质热力性质的总状况,称为工质的热力状态,简称为状态。
平衡状态:系统在不受外界影响的条件下,如果宏观热力性质不随时间而变化,系统内外同时建立了热的和力的平衡,这时系统的状态称为热力平衡状态,简称为平衡状态。
状态参数:描述工质状态特性的各种物理量称为工质的状态参数。
如温度(T)、压力(P)、比容(υ)或密度(ρ)、内能(u)、焓(h)、熵(s)、自由能(f)、自由焓(g)等。
基本状态参数:在工质的状态参数中,其中温度、压力、比容或密度可以直接或间接地用仪表测量出来,称为基本状态参数。
温度:是描述系统热力平衡状况时冷热程度的物理量,其物理实质是物质内部大量微观分子热运动的强弱程度的宏观反映。
热力学第零定律:如两个物体分别和第三个物体处于热平衡,则它们彼此之间也必然处于热平衡。
压力:垂直作用于器壁单位面积上的力,称为压力,也称压强。
相对压力:相对于大气环境所测得的压力。