工程热力学基本概念-精选.pdf
- 格式:pdf
- 大小:35.04 KB
- 文档页数:5
S dEW m ++⎪⎭⎫δδ111.BT w m =22式中22wm —分子平移运动的动能,其中m 是一个分子的质量,w 是分子平移运动的均方根速度; B —比例常数;T —气体的热力学温度。
2.t T +=273压 力 :1.nBT w m n p 322322==式中P —单位面积上的绝对压力;n —分子浓度,即单位容积内含有气体的分子数VNn =,其中N 为容积V 包含的气体分子总数。
2.fFp =F —整个容器壁受到的力,单位为牛(N );f —容器壁的总面积(m 2)。
3.g p B p +=(P >B )H B p -=(P <B )式中 B —当地大气压力P g —高于当地大气压力时的相对压力,称表压力;H —低于当地大气压力时的相对压力,称为真空值。
比容: 1.mV v = m 3/kg式中 V —工质的容积m —工质的质量2.1=v ρ 式中 ρ—工质的密度kg/m3v —工质的比容m 3/kg热力循环:⎰⎰=w q δδ多变过程:凡过程方程为=n pv 常数的过程,称为多变过程。
定容过程:定量工质容积保持不变时的热力过程称为定容过程。
定压过程:定量工质压力保持不变时的热力过程称为定压过程。
定温过程:定量工质温度保持不变时的热力过程称为定温过程。
单级活塞式压气机工作原理:吸气过程、压缩过程、排气过程,活塞每往返一次,完成以上三个过程。
活塞式压气机的容积效率:活塞式压气机的有效容积和活塞排量之比,称为容积效率。
活塞式压气机的余隙:为了安置进、排气阀以及避免活塞与汽缸端盖间的碰撞,在汽缸端盖与活塞行程终点间留有一定的余隙,称为余隙容积,简称余隙。
最佳增压比:使多级压缩中间冷却压气机耗功最小时,各级的增压比称为最佳增压比。
压气机的效率:在相同的初态及增压比条件下,可逆压缩过程中压气机所消耗的功与实际不可逆压缩过程中压气机所消耗的功之比,称为压气机的效率。
热机循环:若循环的结果是工质将外界的热能在一定条件下连续不断地转变为机械能,则此循环称为热机循环。

⼯程热⼒学概念整理⼯程热⼒学与传热学概念整理⼯程热⼒学第⼀章、基本概念1.热⼒系:根据研究问题的需要,⼈为地选取⼀定范围内的物质作为研究对象,称为热⼒系(统),建成系统。
热⼒系以外的物质称为外界;热⼒系与外界的交界⾯称为边界。
2.闭⼝系:热⼒系与外界⽆物质交换的系统。
开⼝系:热⼒系与外界有物质交换的系统。
绝热系:热⼒系与外界⽆热量交换的系统。
孤⽴系:热⼒系与外界⽆任何物质和能量交换的系统3.⼯质:⽤来实现能量像话转换的媒介称为⼯质。
4.状态:热⼒系在某⼀瞬间所呈现的物理状况成为系统的状态,状态可以分为平衡态和⾮平衡态两种。
5.平衡状态:在没有外界作⽤的情况下,系统的宏观性质不随时间变化的状态。
实现平衡态的充要条件:系统内部与外界之间的各种不平衡势差(⼒差、温差、化学势差)的消失。
6.强度参数:与系统所含⼯质的数量⽆关的状态参数。
⼴延参数:与系统所含⼯质的数量有关的状态参数。
⽐参数:单位质量的⼴延参数具有的强度参数的性质。
基本状态参数:可以⽤仪器直接测量的参数。
7.压⼒:单位⾯积上所承受的垂直作⽤⼒。
对于⽓体,实际上是⽓体分⼦运动撞击壁⾯,在单位⾯积上所呈现的平均作⽤⼒。
8.温度T:温度T是确定⼀个系统是否与其它系统处于热平衡的参数。
换⾔之,温度是热⼒平衡的唯⼀判据。
9.热⼒学温标:是建⽴在热⼒学第⼆定律的基础上⽽不完全依赖测温物质性质的温标。
它采⽤开尔⽂作为度量温度的单位,规定⽔的汽、液、固三相平衡共存的状态点(三相点)为基准点,并规定此点的温度为273.16K。
10状态参数坐标图:对于只有两个独⽴参数的坐标系,可以任选两个参数组成⼆维平⾯坐标图来描述被确定的平衡状态,这种坐标图称为状态参数坐标图。
11.热⼒过程:热⼒系从⼀个状态参数向另⼀个状态参数变化时所经历的全部状态的总和。
12.热⼒循环:⼯质由某⼀初态出发,经历⼀系列状态变化后,⼜回到原来初始的封闭热⼒循环过程称为热⼒循环,简称循环。
13.准平衡过程:由⼀系列连续的平衡状态组成的过程称为准平衡过程,也成准静态过程。

工质:实现热能和机械能之间转换的媒介物质。
系统:热设备中分离出来作为热力学研究对象的物体。
状态参数:描述系统宏观特性的物理量。
热力学平衡态:在无外界影响的条件下,如果系统的状态不随时间发生变化,则系统所处的状态称为热力学平衡态。
压力:系统表面单位面积上的垂直作用力.温度:反映物体冷热程度的物理量。
温标:温度的数值表示法。
状态公理:对于一定组元的闭口系统,当其处于平衡状态时,可以用与该系统有关的准静态功形式的数量n加上一个象征传热方式的独立状态参数,即(n+1)个独立状态参数来确定.热力过程:系统从初始平衡态到终了平衡态所经历的全部状态。
准静态过程:如过程进行的足够缓慢,则封闭系统经历的每一中间状态足够接近平衡态,这样的过程称为准静态过程。
可逆过程:系统经历一个过程后如果系统和外界都能恢复到各自的初态,这样的过程称为可逆过程。
无任何不可逆因素的准静态过程是可逆过程.循环:工质从初态出发,经过一系列过程有回到初态,这种闭合的过程称为循环.可逆循环:全由可逆过程粘组成的循环。
不可逆循环:含有不可逆过程的循环.第二章热力学能:物质分子运动具有的平均动能和分子间相互作用而具有的分子势能称为物质的热力学能.体积功:工质体积改变所做的功。
热量:除功以外,通过系统边界和外界之间传递的能量。
焓:引进或排出工质输入或输出系统的总能量。
技术功:工程技术上将可以直接利用的动能差、位能差和轴功三项之和称为技术功。
功:物质间通过宏观运动发生相互作用传递的能量。
轴功:外界通过旋转轴对流动工质所做的功。
流动功:外界对流入系统工质所做的功。
热力学第二定律:克劳修斯说法:不可能使热量从低温物体传到高温物体而不引起其他变化.开尔文说法:不可能从单一热源吸热使之完全转化为有用功而不引起其他变化.卡诺循环:两热源间的可逆循环,由定温吸热、绝热膨胀、定温放热、绝热压缩四个可逆过程组成。
卡诺定理:在温度为T1的高温热源和温度为T2的低温热源之间工作的一切可逆热机,其热效率相等,与工质的性质无关;在温度为T1的高温热源和温度为T2的低温热源之间工作的热机循环,以卡诺循环的热效率为最高.熵:沿可逆过程的克劳修斯积分,与路径无关,由初、终状态决定。


工程热力学基础知识制冷与空调技术理论基础第二部分工程热力学基础知识一、热力学的基本概念( 一)、热力系统与工质1.热力系统1.热力系统在热力学研究中,研究者所指定的具体研究对象称为热力系统,简称系统系统。
和系统发生相互作用( 热力系统,简称系统。
和系统发生相互作用(能量交换或质量交换)的周围环境称为外界质量交换)的周围环境称为外界,或称为环境。
系统与环外界,或称为环境环境。
系统与环境的分界面称为边界境的分界面称为边界。
边界。
闭口系:与外界没有质量交换的系统,称为闭口系统。
闭口系:开口系:开口系:与外界有质量交换的系统,称为开口系统。
绝热系:绝热系:与外界没有热量交换的系统,称为绝热系统。
完全绝热的系统实际上是不存在的,工程上将与外界换热量相对很小的系统近似为绝热系统。
2.工质 2.工质在制冷与空调工程及其他热力设备中,热能与机械能的转换或热能的转移,都要借助于某种携带热能的工作物转换或热能的转移,都要借助于某种携带热能的工作物质的状态变化来实现,这类工作物质称为工质。
质的状态变化来实现,这类工作物质称为工质。
制冷系统中使用的工质称为制冷剂制冷系统中使用的工质称为制冷剂,也叫冷媒制冷剂,也叫冷媒(二)系统的热力状态及其基本参数1.热力状态1.热力状态某时刻,系统中工质表现在热力现象方面某时刻,系统中工质表现在热力现象方面的总的状况称为系统的热力状态的总的状况称为系统的热力状态,简称状热力状态,简称状态。
描述系统状态的物理量称为状态参数描述系统状态的物理量称为状态参数状态参数的取值完全由状态确定。
如果工质的状态参数可以在一段时间内保持稳定的数值,不随时间变化而变化,则称为热力平衡态称为热力平衡态,简称平衡态。
热力平衡态,简称平衡态平衡态。
2.基本状态参数2.基本状态参数如果系统的状态发生了变化,那么将表现为状态参数的变化,换而言之,我们可以通过观测系统状态参数的变化来了解系统的变化。
表示系统状态变化的参数有六个,分别为: 表示系统状态变化的参数有六个,分别为: 压力、温度、比体积(或密度)、内能、)、内能压力、温度、比体积(或密度)、内能、焓、熵,其中温度、压力、比体积可以直接或者间接的用一起测出,称为基本状态接或者间接的用一起测出,称为基本状态参数。





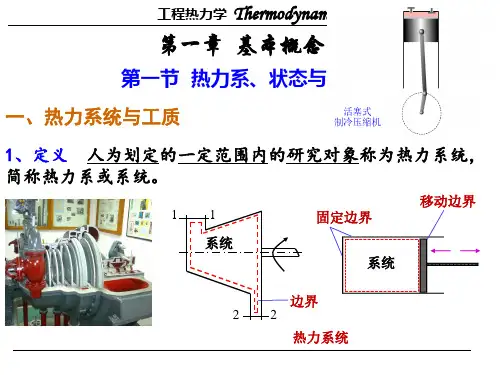
第一章基本概念1.基本概念热力系统:用界面将所要研究的对象与周围环境分隔开来,这种人为分隔的研究对象,称为热力系统,简称系统。
边界:分隔系统与外界的分界面,称为边界。
外界:边界以外与系统相互作用的物体,称为外界或环境。
闭口系统:没有物质穿过边界的系统称为闭口系统,也称控制质量。
开口系统:有物质流穿过边界的系统称为开口系统,又称控制体积,简称控制体,其界面称为控制界面。
绝热系统:系统与外界之间没有热量传递,称为绝热系统。
孤立系统:系统与外界之间不发生任何能量传递和物质交换,称为孤立系统。
单相系:系统中工质的物理、化学性质都均匀一致的系统称为单相系。
复相系:由两个相以上组成的系统称为复相系,如固、液、气组成的三相系统。
单元系:由一种化学成分组成的系统称为单元系。
多元系:由两种以上不同化学成分组成的系统称为多元系。
均匀系:成分和相在整个系统空间呈均匀分布的为均匀系。
非均匀系:成分和相在整个系统空间呈非均匀分布,称非均匀系。
热力状态:系统中某瞬间表现的工质热力性质的总状况,称为工质的热力状态,简称为状态。
平衡状态:系统在不受外界影响的条件下,如果宏观热力性质不随时间而变化,系统内外同时建立了热的和力的平衡,这时系统的状态称为热力平衡状态,简称为平衡状态。
状态参数:描述工质状态特性的各种物理量称为工质的状态参数。
如温度(T)、压力(P)、比容(υ)或密度(ρ)、内能(u)、焓(h)、熵(s)、自由能(f)、自由焓(g)等。
基本状态参数:在工质的状态参数中,其中温度、压力、比容或密度可以直接或间接地用仪表测量出来,称为基本状态参数。
温度:是描述系统热力平衡状况时冷热程度的物理量,其物理实质是物质内部大量微观分子热运动的强弱程度的宏观反映。
热力学第零定律:如两个物体分别和第三个物体处于热平衡,则它们彼此之间也必然处于热平衡。
压力:垂直作用于器壁单位面积上的力,称为压力,也称压强。
相对压力:相对于大气环境所测得的压力。
第一章基本概念1.基本概念热力系统:用界面将所要研究的对象与周围环境分隔开来,这种人为分隔的研究对象,称为热力系统,简称系统。
边界:分隔系统与外界的分界面,称为边界。
外界:边界以外与系统相互作用的物体,称为外界或环境。
闭口系统:没有物质穿过边界的系统称为闭口系统,也称控制质量。
开口系统:有物质流穿过边界的系统称为开口系统,又称控制体积,简称控制体,其界面称为控制界面。
绝热系统:系统与外界之间没有热量传递,称为绝热系统。
孤立系统:系统与外界之间不发生任何能量传递和物质交换,称为孤立系统。
单相系:系统中工质的物理、化学性质都均匀一致的系统称为单相系。
复相系:由两个相以上组成的系统称为复相系,如固、液、气组成的三相系统。
单元系:由一种化学成分组成的系统称为单元系。
多元系:由两种以上不同化学成分组成的系统称为多元系。
均匀系:成分和相在整个系统空间呈均匀分布的为均匀系。
非均匀系:成分和相在整个系统空间呈非均匀分布,称非均匀系。
热力状态:系统中某瞬间表现的工质热力性质的总状况,称为工质的热力状态,简称为状态。
平衡状态:系统在不受外界影响的条件下,如果宏观热力性质不随时间而变化,系统内外同时建立了热的和力的平衡,这时系统的状态称为热力平衡状态,简称为平衡状态。
状态参数:描述工质状态特性的各种物理量称为工质的状态参数。
如温度(T)、压力(P)、比容(υ)或密度(ρ)、内能(u)、焓(h)、熵(s)、自由能(f)、自由焓(g)等。
基本状态参数:在工质的状态参数中,其中温度、压力、比容或密度可以直接或间接地用仪表测量出来,称为基本状态参数。
温度:是描述系统热力平衡状况时冷热程度的物理量,其物理实质是物质内部大量微观分子热运动的强弱程度的宏观反映。
热力学第零定律:如两个物体分别和第三个物体处于热平衡,则它们彼此之间也必然处于热平衡。
压力:垂直作用于器壁单位面积上的力,称为压力,也称压强。
相对压力:相对于大气环境所测得的压力。
第一章基本概念1.基本概念热力系统:用界面将所要研究的对象与周围环境分隔开来,这种人为分隔的研究对象,称为热力系统,简称系统。
边界:分隔系统与外界的分界面,称为边界。
外界:边界以外与系统相互作用的物体,称为外界或环境。
闭口系统:没有物质穿过边界的系统称为闭口系统,也称控制质量。
开口系统:有物质流穿过边界的系统称为开口系统,又称控制体积,简称控制体,其界面称为控制界面。
绝热系统:系统与外界之间没有热量传递,称为绝热系统。
孤立系统:系统与外界之间不发生任何能量传递和物质交换,称为孤立系统。
单相系:系统中工质的物理、化学性质都均匀一致的系统称为单相系。
复相系:由两个相以上组成的系统称为复相系,如固、液、气组成的三相系统。
单元系:由一种化学成分组成的系统称为单元系。
多元系:由两种以上不同化学成分组成的系统称为多元系。
均匀系:成分和相在整个系统空间呈均匀分布的为均匀系。
非均匀系:成分和相在整个系统空间呈非均匀分布,称非均匀系。
热力状态:系统中某瞬间表现的工质热力性质的总状况,称为工质的热力状态,简称为状态。
平衡状态:系统在不受外界影响的条件下,如果宏观热力性质不随时间而变化,系统内外同时建立了热的和力的平衡,这时系统的状态称为热力平衡状态,简称为平衡状态。
状态参数:描述工质状态特性的各种物理量称为工质的状态参数。
如温度(T)、压力(P)、比容(υ)或密度(ρ)、内能(u)、焓(h)、熵(s)、自由能(f)、自由焓(g)等。
基本状态参数:在工质的状态参数中,其中温度、压力、比容或密度可以直接或间接地用仪表测量出来,称为基本状态参数。
温度:是描述系统热力平衡状况时冷热程度的物理量,其物理实质是物质内部大量微观分子热运动的强弱程度的宏观反映。
热力学第零定律:如两个物体分别和第三个物体处于热平衡,则它们彼此之间也必然处于热平衡。
压力:垂直作用于器壁单位面积上的力,称为压力,也称压强。
相对压力:相对于大气环境所测得的压力。
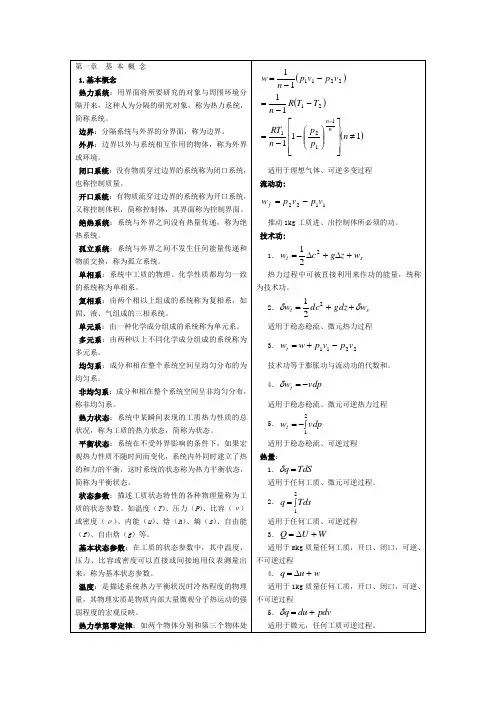
工程热力学基本概念及重要公式(总24页)-本页仅作为预览文档封面,使用时请删除本页-第一章基本概念1.基本概念热力系统:用界面将所要研究的对象与周围环境分隔开来,这种人为分隔的研究对象,称为热力系统,简称系统。
边界:分隔系统与外界的分界面,称为边界。
外界:边界以外与系统相互作用的物体,称为外界或环境。
闭口系统:没有物质穿过边界的系统称为闭口系统,也称控制质量。
开口系统:有物质流穿过边界的系统称为开口系统,又称控制体积,简称控制体,其界面称为控制界面。
绝热系统:系统与外界之间没有热量传递,称为绝热系统。
孤立系统:系统与外界之间不发生任何能量传递和物质交换,称为孤立系统。
单相系:系统中工质的物理、化学性质都均匀一致的系统称为单相系。
复相系:由两个相以上组成的系统称为复相系,如固、液、气组成的三相系统。
单元系:由一种化学成分组成的系统称为单元系。
多元系:由两种以上不同化学成分组成的系统称为多元系。
均匀系:成分和相在整个系统空间呈均匀分布的为均匀系。
非均匀系:成分和相在整个系统空间呈非均匀分布,称非均匀系。
热力状态:系统中某瞬间表现的工质热力性质的总状况,称为工质的热力状态,简称为状态。
平衡状态:系统在不受外界影响的条件下,如果宏观热力性质不随时间而变化,系统内外同时建立了热的和力的平衡,这时系统的状态称为热力平衡状态,简称为平衡状态。
状态参数:描述工质状态特性的各种物理量称为工质的状态参数。
如温度(T)、压力(P)、比容(υ)或密度(ρ)、内能(u)、焓(h)、熵(s)、自由能(f)、自由焓(g)等。
基本状态参数:在工质的状态参数中,其中温度、压力、比容或密度可以直接或间接地用仪表测量出来,称为基本状态参数。
温度:是描述系统热力平衡状况时冷热程度的物理量,其物理实质是物质内部大量微观分子热运动的强弱程度的宏观反映。
热力学第零定律:如两个物体分别和第三个物体处于热平衡,则它们彼此之间也必然处于热平衡。
压力:垂直作用于器壁单位面积上的力,称为压力,也称压强。