有机化学第二版高占先课后习题第13章答案
- 格式:ppt
- 大小:685.00 KB
- 文档页数:12


有机化学(第二版)课后习题参考答案第一章绪论1-1 扼要解释下列术语.(1)有机化合物(2) 键能、键的离解能(3) 键长(4) 极性键(5) σ键(6)π键(7) 活性中间体(8) 亲电试剂(9) 亲核试剂(10)Lewis碱(11)溶剂化作用(12) 诱导效应(13)动力学控制反应(14) 热力学控制反应答:(1)有机化合物-碳氢化合物及其衍生物(2) 键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所吸收的能量称为键能。
键的离解能:共价键断裂成两个原子所吸收的能量称为键能。
以双原子分子AB为例,将1mol气态的AB 拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。
应注意的是,对于多原子分子,键能与键的离解能是不同的。
分子中多个同类型的键的离解能之平均值为键能E(kJ.mol-1)。
(3) 键长:形成共价键的两个原子核之间距离称为键长。
(4) 极性键: 两个不同原子组成的共价键,由于两原子的电负性不同, 成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有部分负电荷性质,另一端电子云密度较小具有部分正电荷性质,这种键具有极性,称为极性共价键。
(5) σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道, 所形成的键叫σ键。
(6) π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键。
(7) 活性中间体:通常是指高活泼性的物质,在反应中只以一种”短寿命”的中间物种存在,很难分离出来,,如碳正离子, 碳负离子等。
(8) 亲电试剂:在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。
(9) 亲核试剂:在反应过程中,如果试剂把电子对给予有机化合物与它反应的那个原子并与之共有形成化学键,这种试剂叫亲核试剂。
(10) Lewis碱:能提供电子对的物种称为Lewis碱。
(11)溶剂化作用:在溶液中,溶质被溶剂分子所包围的现象称为溶剂化作用。
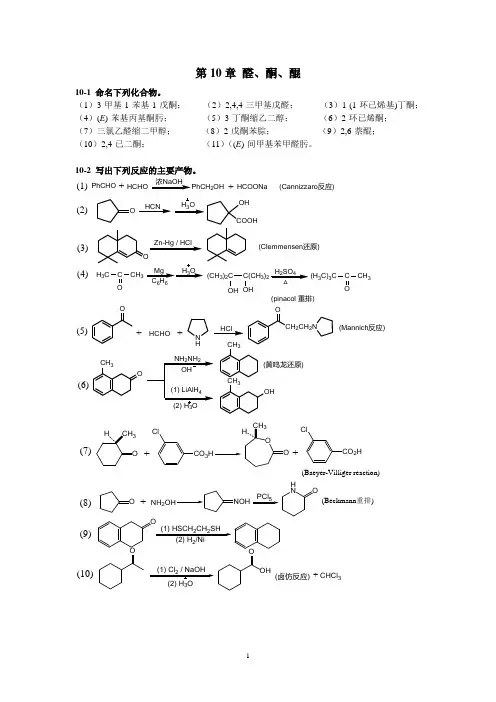
第10章 醛、酮、醌10-1 命名下列化合物。
(1)3-甲基-1-苯基-1-戊酮; (2)2,4,4-三甲基戊醛; (3)1-(1-环已烯基)丁酮; (4)(E )-苯基丙基酮肟; (5)3-丁酮缩乙二醇; (6)2-环已烯酮; (7)三氯乙醛缩二甲醇; (8)2-戊酮苯腙; (9)2,6-萘醌; (10)2,4-已二酮; (11)((E )-间甲基苯甲醛肟。
10-2 写出下列反应的主要产物。
PhCHOHCOONa +浓NaOHHCHO2OH+(Cannizzaro 反应)OZn-Hg / HClHCNH 3OOH COOHO(Clemmensen 还原)H 3CC CH 3OMg 66H 3OH 2SO 4△(CH 3)2C C(CH 3)2OH OH(H 3C)3CC CH 3O(pinacol 重排)(1)(2)(3)(4)+HCHO(Mannich 反应)+HCl(5)(6)O N HCH 2CH 2NOCH 3OCH3CH 3OH(黄鸣龙还原)CO 3Cl+CO 2HCl+(Baeyer-Villiger reaction)ONH 2+PCl 5H NO(Beckmann 重排)O(1) HSCH 2CH 2SH2O(1) Cl 2 / NaOH 3OHO(卤仿反应)(7)(8)(9)(10)CHCl 3+(Wittig reaction)CH 3MgBr +Ph 3(1) CuCl 3(13)(12)(11)O+O(1,4-加成产物)OCHCH 2CH 3O OOHHONCO(双烯合成反应)10-3 比较下列化合物的亲核加成反应活性。
(2)(1)C OCH 3H 3C C CH 3OH 3CC HOCOCH 3H 3C(3)(4)(3)>(1)>(2)>(4)10-4 将下列化合物按烯醇式的含量多少排列成序。
CH 3COCHCOCH 3CH 3COCH 2CH 3(2)(1)PhC H 2C O(3)(4)3CH 3COCH 2COCH 3C CH 3O(1)>(4)>(3)>(2)10-5 指出下列化合物中,哪些能发生碘仿反应?哪些能与饱和NaHSO 3反应?(2)(1)O(3)(4)(5)ICH 2CHOCH 3CH 2CHOC 6H 5COCH 3CH 3CHOCH 3CH 2CH 2OHCH 3CH 22CH 3CH 3CH 23OH(7)(6)(8)O能与饱和NaHSO 3反应的有(1)、(2)、(5)、(8)[脂肪族甲基酮、大多数醛和8个碳以下的脂肪酮能进行此反应]。

---------------------------------------------------------------最新资料推荐------------------------------------------------------ 有机化学答案(高占先版)—第13章杂环化合物第 13 章杂环化合物 13-1 命名下列化合物或写出结构式。
(1) 4-甲基-2-乙基噻唑(2) 2-呋喃甲酸(3) N-甲基吡咯(4) 2,3-吡啶二甲酸(5) 3-乙基喹啉(6) 5-异喹啉磺酸(7) 3-吲哚乙酸(8) 6-氨基嘌呤(9) 4-甲基-2-乙基咪唑知识点:杂环化合物的命名。
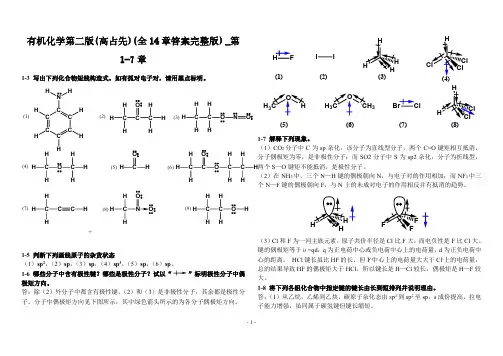
13-2 下列化合物是否是极性分子?若是,请标出分子偶极矩的方向。
它们都是极性分子,偶极矩方向如下:NHONHONH2N芳香结构知识点:偶极矩的判断。
13-3 下列化合物有无芳香性?(1)、(2)、(4)、(5)和(6)有芳香性;(3)无芳香性。
知识点:杂环化合物的芳香性判据。
13-4 指出下列各组化合物的碱性中心,按碱性由强到弱排列成序。
(1)氮原子为碱性中心, C>B>D>A。
(2) A 的两性氮均为碱性中心; B 氮原子为碱性中心; C 中双键氮为碱性中心。
1 / 7A>C>B, B 由于孤对电子参与芳香性大键,故碱性极弱。
知识点:含氮化合物碱性比较。
13-5 判断下列化合物中每个氮原子的杂化状态并比较氮原子的碱性强弱。
NClNHCH2CH2CH2CH2N(CH3)2NNCH2CH2NH2HNNCH3CH3CH3OCOH3CHNABCABCABC (1)(2)(3) (1) A. sp3杂化 B. sp2 杂化 C.sp3杂化;碱性:C>B>A。
(2) A. sp2杂化 B. sp2 杂化 C.sp3杂化;碱性: C>A>B。
(3) A. sp2杂化 B. sp3 杂化 C.sp3杂化;碱性: C>B>A。
知识点:杂化类型判断,碱性判断。

徐寿昌主编《有机化学》(第二版)-课后1-13章习题答案work Information Technology Company.2020YEAR第一章 有机化合物的结构和性质无课后习题第二章 烷烃1.用系统命名法命名下列化合物:1.(CH 3)2CHC(CH 3)2CHCH 3CH 32.CH 3CH 2CH CHCH 2CH 2CH 3CH 3CH(CH 3)22,3,3,4-四甲基戊烷 3-甲基-4-异丙基庚烷3.CH 3CH 2C(CH 3)2CH 2CH 34.CH 3CH 3CH 22CH 2CCH 2CH3CHCH 3CH 3CH 2CH 3123456783,3-二甲基戊烷 2,6-二甲基-3,6-二乙基辛烷5.12345676.2,5-二甲基庚烷 2-甲基-3-乙基己烷7.8.12345672,4,4-三甲基戊烷 2-甲基-3-乙基庚烷2.写出下列各化合物的结构式:1.2,2,3,3-四甲基戊烷 2,2,3-二甲基庚烷CH 3CCCH 2CH 3CH 3CH 3CH 3CH 3CH 3CH 3CHCHCH 2CH 2CH 2CH 3CH 33、 2,2,4-三甲基戊烷4、2,4-二甲基-4-乙基庚烷CH 3C CHCH 3CH 3CH 3CH 3CH 3CHCH 2CCH 2CH 2CH 33CH 3CH 35、 2-甲基-3-乙基己烷6、三乙基甲烷CH 3CH 3CHCHCH 2CH 2CH 32CH 3CH 3CH 2CHCH 2CH 32CH 37、甲基乙基异丙基甲烷 8、乙基异丁基叔丁基甲烷CH 3CHCH(CH 3)2CH 2CH 3CH 3CH 2CHC(CH 3)3CH 2CHCH 3CH 33.用不同符号表示下列化合物中伯、仲、叔、季碳原子3CH 2CCH 32CH 3CCH 3CH31.1111112CH 3402.431323)334.2.3.4.5.6.1.5.不要查表试将下列烃类化合物按沸点降低的次序排列: (1) 2,3-二甲基戊烷 (2) 正庚烷 (3) 2-甲基庚烷 (4) 正戊烷 (5) 2-甲基己烷解:2-甲基庚烷>正庚烷> 2-甲基己烷>2,3-二甲基戊烷> 正戊烷(注:随着烷烃相对分子量的增加,分子间的作用力亦增加,其沸点也相应增加;同数碳原子的构造异构体中,分子的支链愈多,则沸点愈低。
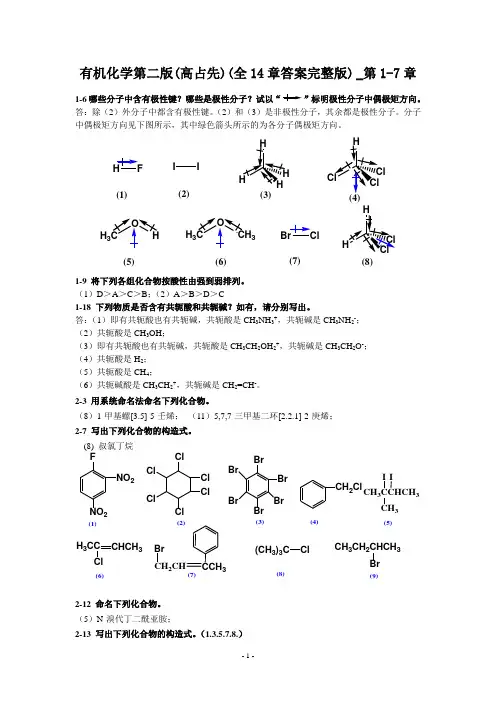
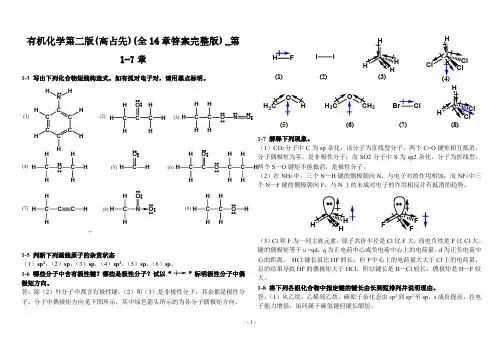
有机化学第二版(高占先)(全14章答案完整版) _第1-7章1-6哪些分子中含有极性键?哪些是极性分子?试以“”标明极性分子中偶极矩方向。
答:除(2)外分子中都含有极性键。
(2)和(3)是非极性分子,其余都是极性分子。
分子中偶极矩方向见下图所示,其中绿色箭头所示的为各分子偶极矩方向。
HH 33H 3I I(1)(2)(3)(5)(6)(7)(8)1-9 将下列各组化合物按酸性由强到弱排列。
(1)D >A >C >B ;(2)A >B >D >C1-18 下列物质是否含有共轭酸和共轭碱?如有,请分别写出。
答:(1)即有共轭酸也有共轭碱,共轭酸是CH 3NH 3+,共轭碱是CH 3NH 2-; (2)共轭酸是CH 3OH ;(3)即有共轭酸也有共轭碱,共轭酸是CH 3CH 2OH 2+,共轭碱是CH 3CH 2O -; (4)共轭酸是H 2; (5)共轭酸是CH 4;(6)共轭碱酸是CH 3CH 2+,共轭碱是CH 2=CH -。
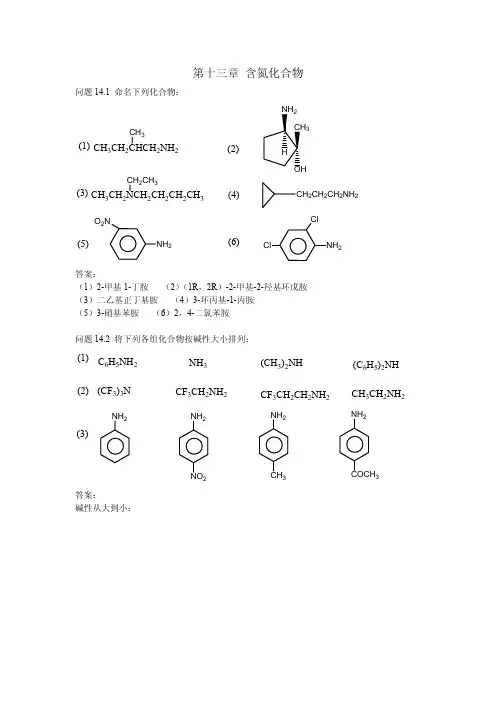
2-3 用系统命名法命名下列化合物。
(8)1-甲基螺[3.5]-5-壬烯; (11)5,7,7-三甲基二环[2.2.1]-2-庚烯; 2-7 写出下列化合物的构造式。
(8) 叔氯丁烷(1)(2)(3)(4)(5)(6)(7)(8)(9)FNO 22ClCl ClClClCl Br BrBrBrBr CH 2Cl CH 3CCHCH3I 3IH 3CCCHCH 3ClCH 2CHCCH 3Br (CH 3)3CClCH 3CH 2CHCH 3Br2-12 命名下列化合物。
(5)N-溴代丁二酰亚胺;2-13 写出下列化合物的构造式。
(1.3.5.7.8.)(1)(2)(3)(4)(6)(7)(8)C CH 2COCH 2CH 2CHCH 3ClO3CH 322H 5OOO OCO Cl C OCH 2CH 2CH 2CH 2CH 3CH 3C O NCH 3CH 3O C O C O OO OH 3CSO 2NH 22-15 写出下列化合物的构造式。

第一章绪论1-1 扼要解释下列术语.(1)有机化合物(2) 键能、键的离解能(3) 键长(4) 极性键(5) σ键(6)π键(7) 活性中间体(8) 亲电试剂(9) 亲核试剂(10)Lewis碱(11)溶剂化作用(12) 诱导效应(13)动力学控制反应(14) 热力学控制反应答:(1)有机化合物-碳氢化合物及其衍生物(2) 键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所吸收的能量称为键能。
键的离解能:共价键断裂成两个原子所吸收的能量称为键能。
以双原子分子AB为例,将1mol气态的AB拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。
应注意的是,对于多原子分子,键能与键的离解能是不同的。
分子中多个同类型的键的离解能之平均值为键能E(kJ.mol-1)。
(3) 键长:形成共价键的两个原子核之间距离称为键长。
(4) 极性键: 两个不同原子组成的共价键,由于两原子的电负性不同, 成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有部分负电荷性质,另一端电子云密度较小具有部分正电荷性质,这种键具有极性,称为极性共价键。
(5) σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道, 所形成的键叫σ键。
(6) π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键。
(7) 活性中间体:通常是指高活泼性的物质,在反应中只以一种”短寿命”的中间物种存在,很难分离出来,,如碳正离子, 碳负离子等。
(8) 亲电试剂:在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。
(9) 亲核试剂:在反应过程中,如果试剂把电子对给予有机化合物与它反应的那个原子并与之共有形成化学键,这种试剂叫亲核试剂。
(10) Lewis碱:能提供电子对的物种称为Lewis碱。
(11)溶剂化作用:在溶液中,溶质被溶剂分子所包围的现象称为溶剂化作用。

有机化学课后习题答案第13章第十三章羧酸及其衍生物一、用系统命名法命名下列化合物:1 . CH3 (CH 2) 4COOH 2.CH 3 CH(CH 3)C(CH 3) 2COOH 3 .CH 3CHClCOOH己酸2,2,3-三甲基丁酸2-氯丙酸4 . COOH 5. CH2 =CHCH2COOH 6. COOH 2-萘甲酸3-丁烯酸环己烷甲酸7 .CH3 COOCH38.HOOCCOOH 9 .CH2COOH对甲基甲酸甲酯对苯二甲酸1-萘乙酸10 . (CH 3CO) 2 O 11. COCH .HCON(CH3) 2OCO乙酸酐2-甲基顺丁烯二酸酐N,N-2 -甲基甲酰胺O2N13. COOH 14. CONHO2N CO3,5-二硝基苯甲酸邻苯二甲酰亚胺CH315. CH3CHCHCOOH 16. OHCOOH2-甲基-3-羟基丁酸1-羟基-环己基甲酸二、写出下列化合物的构造式:1.草酸2,马来酸3,肉桂酸4,硬脂酸HHOOCCOOHC C OOHC H=CHCOOH CH3(CH 2) 16 COOHCHCOOH5.α -甲基丙烯酸甲酯 6,邻苯二甲酸酐 7,乙酰苯胺 8,过氧化苯甲酰胺OOCH 3 CH 2=CCOOCH 3C OOC OONHCOCH 3CCO9.ε-己内酰胺 10,氨基甲酸乙酯 11,丙二酰脲 12,胍OH NCOOC H 2 2 5CNHH 2 N C NH 2NHO CNHC NHO 13,聚马来酸酐14,聚乙酸乙烯酯[ ] CH 2CHnCO OC OnO C OCH 3三、写出分子式为 C 5H 6O 4 的不饱和二元酸的所有异构体(包括顺反异构)的结构式,并指出那些容易生成酸酐:解:有三种异构体: 2-戊烯-1,5-二酸;2-甲基-顺丁烯二酸;2 -甲基-反丁烯二酸。
其中2-甲基-顺丁烯二酸易于生成酸酐。
HOOC CH=CHCH 2 COOHC H 3HOOCCH 3COOHCCH C COOHCCOOH 2-戊烯-1,5-二酸;2-甲基-顺丁烯二酸;2-甲基-反丁烯二酸四、比较下列各组化合物的酸性强度:1,醋酸,丙二酸,草酸,苯酚,甲酸, , OH ,HCOOH CH3COOH, HOOCCH HOOCCOOH2 COOH酸性强度顺序:OH> > > >HOOCCOOH HOOCCH2COOH HCOOH CH3COOH2. C6H5OH , CH3COOH, F3CCOOH , ClCH 2COOH , C2 H5 OH酸性强度顺序为:F3CCOOH > ClCH 2COOH > CH3COOH > C6H5OH > C2 H5 OH3. COOH COOH COOH OH OHNO2 NO2酸性强度顺序为:COOH COOH COOH OH OH> > > >NO2NO2五、用化学方法区别下列化合物:1.乙醇,乙醛,乙酸乙醇乙醛乙酸I2, NaOH HCI3 CHI3 不变Tollens试剂不变银镜2.甲酸,乙酸,丙二酸甲酸乙酸丙二酸T ollens试剂银镜不变不变加热不变CO23.草酸,马来酸,丁二酸草酸马来酸丁二酸溴水不变褪色不变高锰酸钾褪色——不变4,COOH COOH CH2OHOH2-羟基苯甲酸苯甲酸苯甲醇2-羟基苯甲酸苯甲酸苯甲醇三氯化铁水溶液显色不变不变氢氧化钠水溶液——溶解不溶5.乙酰氯,乙酸酐,氯乙烷乙酰氯乙酸酐氯乙烷硝酸银水溶液立即生成氯化银沉淀不反应加热才有氯化银沉淀六、写出异丁酸和下列试剂作用的主要产物:1. Br 2/PCH3CH3CHCOOHBr 2/PCH3CH3CCOOHBr CH3LiAlH 4/H 2 O2 . LiAlH 4/H 2O CH3 CHCOOHCH3CH3CHCH2OH3. SOCl 2CH 3CH3CHCOOHSOCl 2CH3CH3CHCOClCH3(CH3C O)2O/CH34.(CH3C O)2O/CH3CHCOOH(O+CH3COOHCH3CHCO)25.PBr3CH3CH3CHCOOHPBr3(CH3)2CHCOBr6.CH3CH2OH/H2SO4CH3CH3CHCOOHC H3CH2OH/H2SO4(CH3)2CHCOOC2H57.NH3/CH3CH3C HCOOHN H3/(CH3)2CHCONH2七、分离下列混合物:用氢氧化钠水溶液处理,再酸化分出丁酸CH3CH2C OCH2CH3,CH3C H2CH2CHO,CH3CH2C H2CH2OH ,CH3CH2CH2COOHCH3CH2C H2COOHCH3CH2C H2CH2OH CH3CH2CH2CHOCH3CH2COCH2CH3N aOHaq加饱和NaHSO3CH3C H2CH2COONaHClCH3CH2CH2C OOHCH3CH2C H2CH2OH CH3CH2C H2CHOOHCH3CH2CH2C HSO3Na+,H2OHCH3CH2C H2CHOCH3CH2C OCH2CH3CH3CH2CH2C H2O H N H23N HOHCH3C H2CCH2C H3H ClCH3C H2COCH2CH3CH3CH2COCH2CH3NNHOH 八、写出下列化合物加热后生成的主要产物:(CH3)2CCOOH 1,1,2-甲基-2-羟基丙酸OH CH3CH3COOCO CCCH3CHO2,2,β-羟基丁酸C H3CHC H2COOHOHCH3CH=CHCOOH3,3,β-甲基-γ-羟基戊酸CH3CH3C HCHCH2COOHC H3C OO OH4,4,δ-羟基戊酸C O5,5,乙二酸HOCH2CH2CH2C H2COOH O HOOCCOOH HCOOH+CO2九、完成下列各反应式(写出主要产物或主要试剂)(A)H2O,H+CH3CH2COOH1.CH3C H2CNNH3(D)P2O5(B)SOCl2(E) CH3C H2CONH2(F)NaOBr,NaOH NH3(C)CH3C H2COCl(G)H2,Pd/BaSO4 CH3C H2NH2C H3C H2CHOC=O 1.C2H5MgBr2,H3O+OHC2H5PBr31.Mg,(C2H5)2O+2.CO2,H3OC2H5COOH3.Cl C ClO 2NH3H2N C NH2OH2N C NH2O H2N CONH C NH2O4.C=O NaCN,H2S O4OH+ H3OO HCNCOOH OOCO CO十、完成下列转变:1.CH3CH2COOH CH3CH2C H2C OOHCH3CH2COOH [H]CH3C H2CH2OHP Br3CH3C H2CH2BrNaCNCH3CH2C H2CN+H3O CH3C H2CH2COOH2.CH3CH2C H2COH CH3CH2COOHCH3C H2CH2COOH C l2/PCH3C H2C HCOOH-OH C H3CH2C HCOOHCl OH+KMnO4,H C H3CH2C OOH3.C=CH2CH2C OOHC=CH2+HBr R OORCH2BrMg,(C2H5)OCH2MgBr1,CO2C H2COOH2,H3O4.CH3COCH2CH2CBr(CH3)2CH3COCH2CH2C(CH3)2C OOH+HOCH2CH2OH/HO OCH3C OCH2CH2C Br(CH3)2CH3C CH2CH2CBr(CH3)2Mg,(C2H5)O OO CH 3CH3C CH2C H2CMgBrCH31.CO2+2.H3OCH3COCH2CH2C(CH3)2COOH十一、试写出下列反应的主要产物:6.(R )-2-溴丙酸 + (S)-2-丁醇H+/⊿ OHBrCH 3COOHCH 3CH 2+C H 3HH+HBr CH 3C OH OC 2H 5CH 3 H7.CH 3 CH 2 COONa+CH 3 CH 2 CH 2COClCH 3CH 2CH 2CO O CCH 2CHCH 3 OO8. CH2CH 2CCO+ 2C 2H 5OHC 2H 5 OCCH 2CH 2 COC 2H 5OOO9.C H 3+NaOBr-OHCH 3 CONH 2NH 210 .CONH 2+ P 2 O 5CN十二、预测下列化合物在碱性条件下水解反应的速度顺序。
糖类课后习题参考答案习题1,各糖构型如下:OHOH OH O OH OH OH OOH OH OH O OHOH OH OH O OH OH习题2,各糖哈沃斯式如下:O OH OH OH OOH OHOH OH O O H O H OHOH OHH H习题3,有半缩醛(酮)羟基存在的物质就有变旋现象,故(1)、(2)和(6)有变旋现象。
习题4,有半缩醛(酮)羟基存在的物质,或单糖都有还原性,可以还原本尼迪克试剂。
故(1)不能,为糖苷;(2)可以,为单糖;(3)不能,为糖酸内酯;(4)不能,为多元醇。
习题5,D-己醛糖的2、3、4、5号碳原子上羟基对称分布的,可以氧化成内消旋的糖二酸。
OH OH OH O OH OHOH OHO H O OHOHOH OH OHO OH OHO H O OHOH OH OH 习题5的结构式 习题6 的结构式习题6,同种剎由不同糖生成,这些糖只在1、2号碳原子上有差别,即一种酮糖,两种醛糖。
习题7,提示:葡萄糖和蔗糖,用斐林试剂、托勒试剂、2,4-二硝基苯肼均可鉴别。
纤维素和淀粉用单酯碘鉴别;麦芽糖和淀粉用单质碘、用斐林试剂、托勒试剂、2,4-二硝基苯肼均可鉴别。
葡萄糖和果仁糖用间苯二酚/浓盐酸可鉴别,用溴水亦可鉴别;(5)是鉴别糖和糖苷,用斐林试剂、托勒试剂、2,4-二硝基苯肼均可鉴别。
习题8,各反应产物如下:(1)OHOH OHOOHOHO OH OH OH + (2)OHOH OHO OH OH (3)O OCH 3O H OH O H O H (4)OH O OH OOH OH OH O H O OH OH(5)OH OHOH O H OH O OH OH OH O H OO(此处题目表述不准确,麦芽糖本来就是α-1,4-苷,纤维二糖本来就是β-1,4苷。
)(6)OHOH OH O HNO OHOH OH O O H OH H习题9,下列各反应产物如下:(1)OH O H OH OOHO H OH (2)OH O H OH OOH O H OHO(3)OOH OH O H O H CH 3O OH OH O H O H OCH 3+(4)OO OOOOCH 3CH 3CH 3CH 3C H 3O O O OOOCH 3H 3CH 3CH 3CH 3+(5)OO O O O OCH 3CH 3C H 3CH 3CH 3O O OOO(结构式中的波浪线代表基团的伸展方向不确定。
第一章绪论1-1 扼要解释下列术语.(1)有机化合物(2) 键能、键的离解能(3) 键长(4) 极性键(5) σ键(6)π键(7) 活性中间体(8) 亲电试剂(9) 亲核试剂(10)Lewis碱(11)溶剂化作用(12) 诱导效应(13)动力学控制反应(14) 热力学控制反应答:(1)有机化合物-碳氢化合物及其衍生物(2) 键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所吸收的能量称为键能。
键的离解能:共价键断裂成两个原子所吸收的能量称为键能。
以双原子分子AB为例,将1mol气态的AB拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。
应注意的是,对于多原子分子,键能与键的离解能是不同的。
分子中多个同类型的键的离解能之平均值为键能E(kJ.mol-1)。
(3) 键长:形成共价键的两个原子核之间距离称为键长。
(4) 极性键: 两个不同原子组成的共价键,由于两原子的电负性不同, 成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有部分负电荷性质,另一端电子云密度较小具有部分正电荷性质,这种键具有极性,称为极性共价键。
(5) σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道, 所形成的键叫σ键。
(6) π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键。
(7) 活性中间体:通常是指高活泼性的物质,在反应中只以一种”短寿命”的中间物种存在,很难分离出来,,如碳正离子, 碳负离子等。
(8) 亲电试剂:在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。
(9) 亲核试剂:在反应过程中,如果试剂把电子对给予有机化合物与它反应的那个原子并与之共有形成化学键,这种试剂叫亲核试剂。
(10) Lewis碱:能提供电子对的物种称为Lewis碱。
(11)溶剂化作用:在溶液中,溶质被溶剂分子所包围的现象称为溶剂化作用。
有机化学(第二版)课后习题参考答案第一章绪论1-1扼要解释下列术语.(1)有机化合物(2) 键能、键的离解能(3) 键长(4) 极性键(5) σ键(6)π键(7) 活性中间体(8) 亲电试剂(9) 亲核试剂(10)Lewis碱(11)溶剂化作用(12) 诱导效应(13)动力学控制反应(14) 热力学控制反应答:(1)有机化合物-碳氢化合物及其衍生物(2) 键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所吸收的能量称为键能。
键的离解能:共价键断裂成两个原子所吸收的能量称为键能。
以双原子分子AB为例,将1mol气态的AB 拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。
应注意的是,对于多原子分子,键能与键的离解能是不同的。
分子中多个同类型的键的离解能之平均值为键能E(kJ.mol-1)。
(3) 键长:形成共价键的两个原子核之间距离称为键长。
(4)极性键: 两个不同原子组成的共价键,由于两原子的电负性不同, 成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有部分负电荷性质,另一端电子云密度较小具有部分正电荷性质,这种键具有极性,称为极性共价键。
(5) σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道, 所形成的键叫σ键。
(6) π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键。
(7) 活性中间体:通常是指高活泼性的物质,在反应中只以一种”短寿命”的中间物种存在,很难分离出来,,如碳正离子, 碳负离子等。
(8) 亲电试剂:在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。
(9)亲核试剂:在反应过程中,如果试剂把电子对给予有机化合物与它反应的那个原子并与之共有形成化学键,这种试剂叫亲核试剂。
(10) Lewis碱:能提供电子对的物种称为Lewis碱。
(11)溶剂化作用:在溶液中,溶质被溶剂分子所包围的现象称为溶剂化作用。