CHO细胞的稳定转染与基因表达
- 格式:doc
- 大小:26.50 KB
- 文档页数:1

cho细胞重组蛋白原理
CHO细胞重组蛋白的原理涉及到CHO细胞的特性以及重组蛋白的生产过程。
首先,CHO细胞是一种哺乳动物细胞,常用于生物制药中。
它具有许多优点,如对重组蛋白的翻译后修饰能力强、生长快速等。
重组蛋白的原理是利用这些CHO细胞来表达外源基因,从而生产所需的蛋白质。
具体来说,CHO细胞重组蛋白的原理包括以下几个步骤:
1. 基因克隆,首先需要将所需的外源基因(编码目标蛋白的基因)克隆到适当的表达载体中,通常是质粒。
这个质粒中还包含一些调控元件,如启动子、终止子和增强子,以确保基因在CHO细胞中得到高效表达。
2. 细胞转染,将经过构建的表达载体导入CHO细胞中。
这可以通过化学方法、电穿孔法或者病毒载体等方式实现。
3. 选择和培养,转染后的CHO细胞需要进行筛选,以确保只有含有外源基因的细胞得以生长和繁殖。
通常会加入抗生素或者其他筛选标记物来实现这一步骤。
筛选后的细胞需要进行培养,以扩大
细胞数量。
4. 蛋白表达和纯化,经过培养的CHO细胞会表达外源基因编码的蛋白质。
这些蛋白质可以分泌到培养液中或者留存在细胞内。
随后,需要对培养液或者细胞进行相应的分离和纯化步骤,以获取纯
净的重组蛋白。
总的来说,CHO细胞重组蛋白的原理是利用CHO细胞表达外源
基因,并通过细胞培养和蛋白纯化等步骤最终获取纯净的重组蛋白。
这一技术在生物制药领域得到广泛应用,为生产重组蛋白药物提供
了重要的手段。

CHO (Chinese Hamster Ovary) 细胞是常用的哺乳动物细胞系统,用于表达重组蛋白的研究和生产。
以下是一般性的CHO 细胞表达重组蛋白的方案:
1. 购买表达载体:选择适合的表达载体,可以是质粒或病毒载体。
载体应包含适当的启动子、选择标记等。
2. 转染CHO 细胞:将表达载体导入CHO 细胞中。
转染方法可以选择经典的化学或电穿孔法,也可以选择使用特定的转染试剂或转染仪器。
3. 选择稳定转染株:在转染后,使用适当的选择剂(如抗生素) 处理细胞,以选择稳定表达重组蛋白的细胞株。
可通过单克隆分离等方法筛选和扩增单一细胞克隆。
4. 细胞培养条件优化:优化培养基配方和细胞培养条件,包括温度、pH 值、培养基组分等,以提高重组蛋白的产量和纯度。
5. 表达蛋白的诱导:使用适当的诱导剂或方法,例如添加诱导剂(如甲酪酸) 到培养基中,以启动重组蛋白的表达。
6. 重组蛋白的纯化和分析:通过细胞破碎和不同的纯化步骤(如亲和层析、离子交换层析、凝胶过滤等)从培养基或细胞提取物中纯化目标重组蛋白,并使用适当的分析方法验证表达的蛋白的纯度和功能。
在每个步骤中,需要根据具体的重组蛋白和研究目的进行优化和调整。
此外,合理的培养细胞和操作操作也至关重要,以确保产量和纯度的理想达到。
这些方案的细节将根据具体的实验目的和需要进行个体化定制。



EndoFectin™-CHO 转染试剂■ 产品概述:EndoFectin™ CHO 转染试剂是一种具有专利的阳离子聚合物试剂,它能与核酸形成复合物,并使该复合物进入哺乳动物细胞。
EndoFectin™ CHO 转染试剂专为转染CHO 细胞,并构建稳定的细胞系而设计。
即使在有血清存在的情况下,它仍然能高效的将核酸导入细胞。
GeneCopoeia 公司提供的 EndoFectin™ CHO 转染试剂有如下优点:• 优越的转染效率• 重组蛋白的高表达水平• 与含血清的培养基相兼容• 低细胞毒性• 易于操作■ 成分及储存条件:• 每管含有经过滤除菌的EndoFectin™ CHO 转染试剂• EndoFectin™ CHO 转染试剂 可于常温下运输。
4-8℃密闭保存。
该试剂在4-8℃的条件下,可保持稳定至少12个月。
■ 质量控制:每批EndoFectin™ CHO 均经过转染测试。
我们将eGFP 表达质粒(GeneCopoeia Catalog No. EX-EGFP-Lv01)用EndoFectin™ CHO 转染试剂转入subconfluent HEK-293 细胞。
转染16小时后,超过95%的细胞表达eGFP 。
■ 实验开始前的注意事项:质粒的质量:请务必使用高质量转染级无内毒素的质粒。
通过260nm 光吸收测定DNA 浓度,260nm/280nm 比值确定DNA 纯度(比值应该在1.8~2.0的范围之内)。
如有可能,请通过琼脂糖凝胶电泳检测质粒的完整性。
细胞的条件:使用适当保存和经常传代的健康细胞。
确保培养基没有被细菌,真菌或支原体污染。
如果细胞是近期复苏的液氮冻存细胞,请在转染前至少传代两次。
■ 瞬时转染方法:1. 接种细胞1转染前一天,用胰酶消化细胞并计数。
调整细胞浓度,将细胞铺入细胞培养的器皿,总体积如表1所示。
每个孔置入的细胞量应能使转染时细胞汇合度达到70~80%。
2. 准备DNA/EndoFectin™复合物GeneCopoeia Inc.19520 Amaranth DriveGermantown, Maryland 20874USATel: 301-515-6982; 1-866-360-9531Fax: 301-515-6983Web: GeneCopoeiaTMExpressway to Discovery用于转染核酸到哺乳动物细胞产品套装编号: Z0103储存条件:4℃-8℃保存 产品编号Z01030A Z01030BZ01030C (A*5)包装规格1mL 0.5mL 5 mL地址:广州高新技术产业开发区广州科学城掬泉路3号广州国际企业孵化器D 区8楼,510663客服电话*************电子信箱:********************网址:该产品仅限于实验科学研究用,若有任何单位或个人将该产品用于临床诊断、治疗等其他国家专门规定的特殊用途,本公司概不承担任何责任。

cho细胞的瞬时电转染方法
CHO细胞的瞬时电转染方法如下:
1. 以细胞密度、转染试剂的添加量、含目的基因的质粒的添加量为因素,以目的基因的表达量和转染效率为响应变量,进行三因子九水平的均匀设计,获得瞬时转染工艺参数。
2. 根据瞬时转染工艺参数,以质粒的添加量和转染试剂的添加量为因素,以目的基因的表达量和转染效率为响应变量,进行二因子的正交设计,获得包含CHO胞悬液的细胞密度、转染试剂的添加量以及质粒的添加量的瞬时转染条件。
3. 根据瞬时转染条件,向CHO细胞悬液中加入转染试剂和质粒进行瞬时转染,培养,得到重组CHO细胞。
以上方法仅供参考,具体步骤可能因实验条件和目的的不同而有所差异。
如需更多信息,建议阅读专业文献或请教专业人士。

cho细胞表达系统及筛选原理Cho细胞表达系统及筛选原理一、引言Cho细胞表达系统是一种常用的哺乳动物细胞表达系统,被广泛应用于重组蛋白的生产。
本文将介绍Cho细胞表达系统的原理以及其在蛋白质筛选中的应用。
二、Cho细胞表达系统的原理Cho细胞是一种中国仓鼠卵巢细胞系,具有较高的生长速度和蛋白质表达能力。
Cho细胞表达系统主要包括以下几个关键步骤。
1. 转染将目标基因导入Cho细胞中,通常使用质粒转染法或病毒载体转染法。
质粒转染法通过将目标基因插入质粒DNA中,然后利用转染试剂将质粒DNA导入细胞内。
病毒载体转染法则通过构建携带目标基因的病毒载体,将其感染到Cho细胞中。
2. 选择性筛选为了确保只有转染成功的细胞能够表达目标蛋白,通常在培养基中添加适当的选择性抗生素,如G418或葡萄糖酸钾。
只有转染成功的细胞才能抵抗抗生素的作用,存活下来。
3. 扩增和表达经过筛选的细胞将被扩增培养,以获得足够数量的细胞进行大规模蛋白质表达。
通常选择合适的培养基和培养条件,以提高细胞的生长速度和蛋白质表达水平。
4. 蛋白质纯化经过表达的目标蛋白质需要进行纯化,以去除其他杂质。
常用的纯化方法包括亲和层析、离子交换层析、凝胶过滤层析等。
通过这些方法,可以获得高纯度的目标蛋白质。
三、Cho细胞表达系统在蛋白质筛选中的应用Cho细胞表达系统在蛋白质筛选中具有以下优势。
1. 高表达水平Cho细胞具有较高的蛋白质表达能力,能够快速产生大量目标蛋白。
这对于需要大量蛋白质的研究和工业应用非常有利。
2. 真核细胞表达与原核细胞表达系统相比,Cho细胞表达系统能够实现真核细胞蛋白质表达。
这使得Cho细胞表达系统适用于需要进行正确的蛋白质翻译修饰、蛋白质折叠和组装的蛋白质研究。
3. 可选择性筛选通过添加适当的选择性抗生素,可以筛选出成功表达目标蛋白的细胞。
这样可以确保筛选后的细胞具有较高的表达水平和纯度。
4. 灵活性Cho细胞表达系统可以应用于多种类型的蛋白质,包括单链抗体、重组蛋白、酶等。

生物技术进展2016年㊀第6卷㊀第4期㊀239~243CurrentBiotechnology㊀ISSN2095 ̄2341进展评述Reviews㊀收稿日期:2016 ̄02 ̄22ꎻ接受日期:2016 ̄04 ̄04㊀作者简介:郑惠惠ꎬ技术员ꎬ主要从事真核重组抗原研发研究ꎮE ̄mail:shanjvqiuming@163.comꎮ∗通信作者:江洪ꎬ工程师ꎬ主要从事重组抗原研发研究ꎮE ̄mail:jiang@wondergen.comCHO细胞表达系统研究进展郑惠惠ꎬ㊀江㊀洪∗北京万达因生物医学技术有限责任公司ꎬ北京141017摘㊀要:CHO细胞表达系统是目前重组糖蛋白生产的首选系统ꎮ随着无血清悬浮培养技术㊁基因工程技术和大规模培养技术的应用和不断发展ꎬCHO细胞表达系统已经成为生物技术药物最重要的表达或生产系统ꎬ并被广泛应用于抗体㊁重组蛋白药物和疫苗等产品的研发和生产中ꎮ近年来ꎬ针对CHO细胞表达系统在某些重组蛋白的表达和大规模生产中存在的不足ꎬ研究者们通过利用基因工程技术手段ꎬ结合重组蛋白表达机制的研究成果ꎬ为优化和应用CHO细胞表达系统做出了不懈努力ꎮ从培养基的优化㊁高产重组CHO细胞株的构建㊁大规模培养三个方面综述了CHO细胞表达系统的最近研究进展ꎬ以期为CHO细胞表达系统的研究与应用提供参考ꎮ关键词:CHO细胞培养ꎻ细胞改造ꎻ重组抗原表达DOI:10.3969/j.issn.2095 ̄2341.2016.04.03ProgressofCHOExpressionSystemZHENGHui ̄huiꎬJIANGHong∗BeijingWondergenBio ̄medicineTechnologyCo.Ltd.ꎬBeijing141017ꎬChinaAbstract:CHOcellexpressionsystemisthepreferredsystemforrecombinantglycoproteinproduction.Withtheevolvingdevelopmentandapplicationsofserum ̄freesuspensionculturetechnologyꎬgeneticengineeringandthelarge ̄scaleculturetechnologiesꎬCHOcellexpressionsystemhasbecomethemostimportantexpressionorproductionsystemofbiotechnologyproducts.Thissystemiswidelyusedintheresearchandproductionofantibodiesꎬrecombinantproteinsandvaccines.Inrecentyearsꎬresearchershavemadegreateffortstoimprovetheexpressionandlarge ̄scaleproductionofrecombinantproteinsbyusinglatestbioengineeringtechnologyandthedevelopmentoftherecombinantproteinexpressionmechanism.ThisarticlebrieflyreviewedtherecentdevelopmentoftheCHOcellexpressionsysteminthreeaspects:theoptimizationoftheculturemediumꎬconstructionofengineeredCHOstrainsforhigh ̄levelproductionandlarge ̄scalecultureresearchꎬwhichwasexpectedtoprovidereferenceforresearchandapplicationofCHOcellexpressionsystem.Keywords:CHOcellcultureꎻcellengineeringꎻrecombinantantigenexpression㊀㊀CHO细胞是由Puck于1957年建成的中国仓鼠卵巢成纤维细胞系ꎮ发展至今ꎬCHO细胞已成为生物技术药物最重要的表达或生产系统ꎮ随着无血清悬浮培养技术㊁基因工程技术㊁生物反应器设计放大与强化技术㊁大规模高密度流加和连续灌注培养技术等的发展ꎬCHO细胞系统被广泛应用于抗体㊁基因重组蛋白质药物㊁病毒疫苗等生物技术产品的研究开发和工业化生产中ꎮCHO细胞是目前重组糖基蛋白生产的首选体系ꎮ因为它具有准确的转录后修饰功能ꎬ表达的蛋白在分子结构㊁理化特性和生物学功能方面更接近于天然蛋白分子ꎮ但CHO细胞在无血清培养基中会出现活力差㊁分泌外源蛋白能力弱等问题ꎮ所以建立稳定㊁高产的重组CHO细胞成为很多研究者的目标ꎮ近年来ꎬ研究者从细胞营养㊁代谢㊁凋亡㊁信号传导等角度ꎬ结合蛋白表达机制等研究成果ꎬ对这一目标的实现做出了很多努力ꎮ本文从培养基优化㊁高产重组CHO细胞株的构. All Rights Reserved.建㊁大规模培养三个方面综述了CHO细胞表达系统的最新研究进展ꎬ以期为CHO细胞表达系统的应用提供参考ꎮ1㊀培养基的优化研究发现ꎬ不同的细胞株甚至克隆对营养成分的需求都有差别ꎮ通过筛选比较不同培养基成分对重组抗原生产的影响ꎬ并开发适用于不同重组CHO细胞株的培养基ꎬ成为很多研究者提高CHO细胞表达系统产量的重要方式ꎮ为了维持细胞在无血清培养基中的正常生长ꎬ需要在基础培养基中添加很多其他因子ꎬ如激素㊁生长因子㊁蛋白水解物等ꎮ蛋白质水解物含有丰富的营养成分ꎬ可有效缩短细胞对无血清培养基的适应过程ꎮDavami等[1]通过组合比较不同来源的蛋白水解物对细胞密度及表达产量的影响ꎬ优化得到更适于DG44的培养基ꎮ酵母水解物作为一种成本较低的非动物源蛋白水解物ꎬ可以使细胞密度增加的同时ꎬ使重组表达抗体的表达量大幅提高[2]ꎮ大豆水解物等都可以被添加到基础培养基中[1ꎬ3ꎬ4]ꎮ由于蛋白水解物的构成复杂ꎬ且批间差异大ꎬ因此蛋白水解物的添加会影响细胞培养基批次间的稳定性ꎮ如果去除培养基中的蛋白质水解物ꎬ需要添加氨基酸或微量元素等ꎬ通过优化调整其比例ꎬ仍能支持高密度的CHO细胞培养[5]ꎮ刘兴茂等[6]采用Plackett ̄Burman实验对影响细胞生长的培养添加成分进行了考察ꎬ确定了腐胺㊁胰岛素及转铁蛋白对11G ̄S细胞的悬浮培养有明显的生长促进作用ꎮ设计的培养基可以使细胞最大生长密度达到4.12ˑ106cells/mLꎮXu等[7]采用Plackett ̄Burman设计与支持向量机(SVM)预测并实验确定了硫酸锌㊁转铁蛋白及BSA对CHO ̄K1细胞的生长有促进作用ꎮ另有研究表明ꎬ使用柠檬酸铁作为转铁蛋白的替代物ꎬ可以使细胞的密度达到7.0ˑ106cells/mLꎬ但是会降低转染效率[8]ꎮMiki等[9]研究发现ꎬ添加生长因子IGF ̄1和脂类信号分子溶血磷脂酸(LPA)也可以有效加速CHO细胞生长ꎮ优化培养基能有效提高重组CHO细胞的培养密度ꎮ高密度的CHO细胞培养是CHO细胞表达系统实现工业化生产应用的必要条件之一ꎮ与大肠杆菌和酵母表达系统相比ꎬCHO细胞有生长较慢㊁培养周期较长㊁产量较低等缺点ꎮ为了提高重组蛋白产量㊁扩大CHO细胞表达系统的生产应用范围ꎬ研究者们在优化培养基的实验基础上ꎬ构建高产的重组CHO细胞系ꎬ为大规模的重组蛋白生产提供基础ꎮ2㊀高产重组CHO细胞株的构建研究者们利用发展迅速的基因编辑技术对CHO细胞进行筛选和改造ꎬ得到高产的重组细胞株ꎮ研究者们通过过量表达或敲除某个基因ꎬ调整代谢途径㊁延缓细胞凋亡㊁增强转录表达效率ꎬ有效的增加了重组蛋白产量ꎮ通过结合全基因组测序和基因敲除技术的研究成果ꎬ研究者们为得到反应性更好的糖基化重组蛋白做出了不懈努力ꎮ2.1㊀调整代谢途径乳酸作为糖酵解产生的代谢产物会影响细胞生长ꎮZhou等[10]使用siRNA技术降低乳酸脱氢酶A(LDHa)和丙铜酸脱氢酶激酶(PDHKs)基因的表达ꎬ使乳酸的产生降低了90%ꎬ并增加了单抗的产量ꎮToussaint等[11]通过在rCHO中表达酵母丙酮酸羧化酶(PYC2)ꎬ改变了流加培养方式中葡萄糖的代谢速率ꎬ增长了细胞的对数生长期ꎬ从而增加了细胞密度及产量ꎮ2.2㊀延缓细胞凋亡为了延长细胞培养的时间从而增加产量ꎬ有研究者建立了能表达抗凋亡基因的CHO细胞系ꎮMajos等[12]通过在CHO中表达1个Asp29Asn突变的抑制凋亡基因ꎬ有效延缓了细胞凋亡ꎮ也有研究者通过敲除细胞中的促凋亡基因来延缓细胞凋亡ꎬ如Cost等[13]敲除了BCL2相关蛋白X(BAX)和BAK的基因ꎬ使单克隆抗体产量增加了5倍ꎮRitter等[14]发现8号染色体端粒区的缺失也可以使产物产量成倍增加ꎮ2.3㊀增强转录表达效率有研究者在细胞信号通路研究成果的基础上ꎬ通过表达转录及翻译过程中的相关蛋白ꎬ增强转录和表达效率ꎬ以增加目的重组蛋白的产量ꎮLeFourn等[15]通过在CHO中表达人信号受体蛋白SRP14ꎬ成功增加了分泌表达的重组蛋白的产042生物技术进展CurrentBiotechnology. All Rights Reserved.量ꎮPeng等[16]通过表达转录翻译相关蛋白SLY1㊁MUNC18C和XBP1ꎬ使IgG的产量提高了20倍ꎻRahimpour等[17]在CHO细胞中表达神经酰胺转移蛋白(CERT)的突变基因使t ̄PA的产量增加了35%ꎮ2.4㊀表达糖基化酶能产生糖基化的重组蛋白是CHO细胞表达系统重要的优势ꎬ研究者们通过建立能表达N ̄糖基化途径中不同酶类的细胞系以增加糖基化重组蛋白的反应性ꎮ如Goh[18]建立的一个含有N ̄乙酰氨基葡萄糖转移酶I基因的突变体CHO ̄gmt4细胞系ꎬ其表达的重组葡萄糖脑苷脂酶将不需要多糖重构可直接用于治疗戈谢病患者ꎮZhang等[19]通过CHO ̄gmt5细胞株表达的重组抗体ꎬ其Fc的N ̄多糖缺少岩藻糖和唾液酸能增强ADCC的作用ꎮ根据CHO ̄K1的基因组信息ꎬYang等[20]通过锌指核酸酶(ZFNs)基因敲除的方法ꎬ研究了19种包括作用于N ̄糖基链分支㊁半乳糖基㊁聚LacNAc延伸㊁唾液酸化加盖的N ̄糖基转移酶对N ̄糖基化作用的影响ꎬ为更准确的表达特定糖基化方式的重组蛋白提供了重要参考ꎮ重组CHO细胞表达重组蛋白能力的高低ꎬ不能简单的归结为某些关键基因的作用ꎮ为了得到高产的重组细胞株ꎬ需要研究者们综合考虑细胞的代谢情况㊁培养条件㊁蛋白表达效率和蛋白加工修饰能力等诸多因素ꎮ3㊀大规模培养研究基因工程技术㊁细胞融合技术及抗体类药物的迅速发展ꎬ推进了生物反应器培养技术在生物制药中的应用ꎮ由于CHO细胞能以悬浮培养的方式高密度培养ꎬ培养体积可达1000L以上ꎬ所以在大规模培养和重组蛋白的高产量生产中ꎬCHO细胞表达系统拥有广阔的发展前景ꎮ在大规模生产中ꎬ通常采用流加培养方式ꎬ通过添加营养物质来延长培养时间ꎬ增加细胞密度和目的产品的浓度ꎮ为了更大程度的提高重组蛋白的生产效率ꎬ研究者们需要根据不同细胞株的生长代谢特点ꎬ选择和优化起始培养基㊁补料培养基及补料策略ꎮ现代计算机技术㊁数学算法及理论的应用ꎬ也为研究者对细胞流加培养的优化提供了很大帮助ꎮ3.1㊀优化培养参数选择合适的培养基㊁优化细胞培养的参数(如温度㊁pH㊁溶氧㊁CO2浓度㊁渗透压等)对生产至关重要ꎮ同时ꎬ流加工艺参数(如流加培养基成分㊁流加时间等)均需根据不同的细胞株及反应器的特点来设计优化ꎮFan等[21]采用分批补料方式培养CHO细胞ꎬ实验显示培养基中的氨基酸和葡萄糖浓度对细胞的生长㊁IgG浓度和N ̄糖基化生成都很重要ꎮKim等[22]使用分批补料培养使IgG的产量达到2.3g/Lꎮ通过用小麦蛋白水解物(WGH)代替补料中的谷氨酰胺可以使t ̄PA的产量达到422mg/L[23]ꎮ3.2㊀应用新的培养技术微载体培养是一种动物细胞大规模培养技术ꎮ培养液中大量的微载体为细胞提供了极大的附着表面ꎬ从而可实现细胞的高密度培养ꎮ胡显文等[24]在搅拌式反应器中无血清培养分泌u ̄PA的DNA重组CHO细胞ꎬ通过部分更换Cytopore多孔微载体ꎬ解决了大规模细胞培养中细胞凋亡的问题ꎮ并使用周期变压刺激技术使u ̄PA的产量提高了10倍ꎬ且可以降低葡萄糖厌氧代谢产生乳酸的转化率ꎮVentini等[25]通过Cytodex微载体培养CHO ̄hTSH细胞的实验表明ꎬ培养基中微载体的数量及在rhTSH合成期开始时的细胞浓度是提高目的蛋白产量的重要参数ꎮ李智等[26]利用CHO细胞能在培养过程中自然结团的特性ꎬ采用超声沉降柱二合一灌流系统促进细胞结团和加强截留的特性ꎬ用无血清培养基连续灌流培养基因重组CHO细胞MK3 ̄A2株ꎬ分泌表达的rhTNK ̄tPA生产率平均为89mg/L dꎮ3.3㊀添加保护剂聚醚F68可以有效减少生物反应器中搅拌对细胞产生的机械损伤ꎮ针对F68对某些细胞株的生长及产量降低的情况ꎬ研究者发现0.05%或0.075%的500kDa的γPGA可以替代F68应用于CHODG44细胞的培养中[27]ꎮ在细胞培养工艺逐级放大的过程中ꎬ每一步都需要研究者们监控细胞在生长和表达方面的相关指标ꎮ生物反应器在线监控pH㊁溶氧等参数的功能㊁色谱和在线蛋白分解监测等技术为大规模培养的过程控制提供了帮助ꎮ142郑惠惠ꎬ等:CHO细胞表达系统研究进展. All Rights Reserved.4 展望CHO细胞是表达外源蛋白最多也是最成功的一类细胞ꎬ有其不可比拟的优点ꎬ同时也存在现行技术手段不能弥补的不足之处ꎮ结合生物信息学㊁细胞生物学㊁基因工程技术和生物反应器技术的研究成果ꎬ研究者们可以通过综合考虑细胞代谢特性㊁蛋白表达特性等影响因素ꎬ通过研发个性化培养条件及培养工艺ꎬ构建高表达载体ꎬ筛选稳定高产的重组细胞株ꎬ改造宿主细胞等角度继续优化CHO细胞表达系统ꎬ为产业化生产重组蛋白提供基础ꎮ用于产业化生产的重组CHO细胞ꎬ需要具备生长特性良好㊁能在无血清培养基中高密度培养㊁表达重组蛋白能力强㊁能正确的进行翻译后修饰等特点ꎮ糖基化是蛋白翻译后最重要的修饰之一ꎬ直接影响重组蛋白的空间结构㊁生物活性㊁稳定性㊁免疫原性和生物反应性等ꎮ对重组蛋白的糖基化研究一直是研发和生产真核重组蛋白的热点课题ꎮ随着基因编辑技术的发展ꎬ研究者们通过表达特定糖基化相关酶从而得到完整㊁准确的特定形式的糖链结构ꎬ为糖基化蛋白在免疫诊断㊁临床治疗等领域的持续发展奠定了基础ꎮ随着基因技术的不断发展ꎬ对细胞代谢㊁信号传导等方面研究的持续深入ꎬ构建能表达准确修饰的糖基化重组蛋白的高产重组CHO细胞株仍将成为研究热点ꎮ参㊀考㊀文㊀献[1]㊀DavamiFꎬEghbalpourFꎬNematollahiLꎬetal..EffectsofpeptonesupplementationindifferentculturemediaongrowthꎬmetabolicpathwayandproductivityofCHODG44cells:anewinsightintoaminoacidprofiles[J].Iran.Biomed.J.ꎬ2015ꎬ19(4):194-205.[2]㊀SungYHꎬLimSWꎬChungJYꎬetal..Yeasthydrolysateasalow ̄costadditivetoserum ̄freemediumfortheproductionofhumanthrombopoietininsuspensionculturesofChinesehamsterovarycells[J].Appl.Microbiol.Biotechnol.ꎬ2004ꎬ63(5):527-536.[3]㊀DavamiFꎬBaldiLꎬRajendraYꎬetal..PeptonesupplementationofculturemediumhasvariableeffectsontheproductivityofCHOcells[J].Int.J.Mol.CellMed.ꎬ2014ꎬ3(3):146-156.[4]㊀ChunBHꎬKimJHꎬLeeHJꎬetal..Usabilityofsize ̄excludedfractionsofsoyproteinhydrolysatesforgrowthandviabilityofChinesehamsterovarycellsinprotein ̄freesuspensionculture[J].Bioresour.Technol.ꎬ2007ꎬ98(5):1000-1005.[5]㊀张大鹤ꎬ易小萍ꎬ张元兴ꎬ等ꎬ适于重组CHO细胞培养的无血清培养基的制备[J].中国生物制品学杂志ꎬ2011(10):1152-1156.[6]㊀刘兴茂ꎬ刘红ꎬ叶玲玲ꎬ等ꎬCHO工程细胞无血清悬浮分批培养的生长代谢特征及动力学模型[J].生物工程学报ꎬ2010ꎬ(1):85-92.[7]㊀XuJꎬYanFRꎬLiZHꎬetal..Serum ̄freemediumoptimizationbasedontrialdesignandsupportvectorregression[J].Biomed.Res.Int.ꎬ2014ꎬdoi:10.1155/2014/269305. [8]㊀EberhardySRꎬRadzniakLꎬLiuZ.Iron(III)citrateinhibitspolyethylenimine ̄mediatedtransienttransfectionofChinesehamsterovarycellsinserum ̄freemedium[J].Cytotechnologyꎬ2009ꎬ60:1-9.[9]㊀MikiHꎬTakagiM.Designofserum ̄freemediumforsuspensioncultureofCHOcellsonthebasisofgeneralcommercialmedia[J].Cytotechnologyꎬ2015ꎬ67(4):689-697.[10]㊀ZhouMꎬCrawfordYꎬNgDꎬetal..DecreasinglactatelevelandincreasingantibodyproductioninChineseHamsterOvarycells(CHO)byreducingtheexpressionoflactatedehydrogenaseandpyruvatedehydrogenasekinases[J].J.Biotechnol.ꎬ2011ꎬ153(1-2):27-34.[11]㊀ToussaintCꎬHenryOꎬDurocherY.MetabolicengineeringofCHOcellstoalterlactatemetabolismduringfed ̄batchcultures[J].J.Biotechnol.ꎬ2015ꎬ217:122-131.[12]㊀MajorsBSꎬChiangGGꎬPedersonNEꎬetal..Directedevolutionofmammaliananti ̄apoptosisproteinsbysomatichypermutation[J].ProteinEng.Des.Sel.ꎬ2012ꎬ25(1):27-38.[13]㊀CostGJꎬFreyvertYꎬVafiadisAꎬetal..BAKandBAXdeletionusingzinc ̄fingernucleasesyieldsapoptosis ̄resistantCHOcells[J].Biotechnol.Bioeng.ꎬ2010ꎬ105(2):330-40. [14]㊀RitterAꎬVoedischBꎬWienbergJꎬetal..Deletionofatelomericregiononchromosome8correlateswithhigherproductivityandstabilityofCHOcelllines[J].Biotechnol.Bioeng.ꎬ2016ꎬ113(5):1084-1093.[15]㊀LeFournVꎬGirodPAꎬBucetaMꎬetal..CHOcellengineeringtopreventpolypeptideaggregationandimprovetherapeuticproteinsecretion[J].Metab.Eng.ꎬ2014ꎬ21:91-102.[16]㊀PengRWꎬFusseneggerM.MolecularengineeringofexocyticvesicletrafficenhancestheproductivityofChinesehamsterovarycells[J].Biotechnol.Bioeng.ꎬ2009ꎬ102(4):1170-1181.[17]㊀RahimpourAꎬVaziriBꎬMoazzamiRꎬetal..EngineeringthecellularproteinsecretorypathwayforenhancementofrecombinanttissueplasminogenactivatorexpressioninChinesehamsterovarycells:effectsofCERTandXBP1sgenes[J].J.Microbiol.Biotechnol.ꎬ2013ꎬ23(8):1116-1122. [18]㊀GohJSꎬLiuYꎬChanKFꎬetal..ProducingrecombinanttherapeuticglycoproteinswithenhancedsialylationusingCHO ̄gmt4glycosylationmutantcells[J].Bioengineeredꎬ2014ꎬ5242生物技术进展CurrentBiotechnology. All Rights Reserved.(4):269-273.[19]㊀ZhangPꎬHaryadiRꎬChanKFꎬetal..IdentificationoffunctionalelementsoftheGDP ̄fucosetransporterSLC35C1usinganovelChinesehamsterovarymutant[J].Glycobiologyꎬ2012ꎬ22(7):897-911.[20]㊀YangZꎬWangSꎬHalimAꎬetal..EngineeredCHOcellsforproductionofdiverseꎬhomogeneousglycoproteins[J].Nat.Biotechnol.ꎬ2015ꎬ33(8):842-844.[21]㊀FanYꎬJimenezDelValIꎬMullerCꎬetal..Aminoacidandglucosemetabolisminfed ̄batchCHOcellcultureaffectsantibodyproductionandglycosylation[J].Biotechnol.Bioeng.ꎬ2015ꎬ112(3):521-535.[22]㊀KimBJꎬZhaoTꎬYoungLꎬetal..Batchꎬfed ̄batchꎬandmicrocarriercultureswithCHOcelllinesinapressure ̄cycledrivenminiaturizedbioreactor[J].Biotechnol.Bioeng.ꎬ2012ꎬ109(1):137-145.[23]㊀KimdoYꎬChaudhryMAꎬKennardMLꎬetal..Fed ̄batchCHOcellt ̄PAproductionandfeedglutaminereplacementtoreduceammoniaproduction[J].Biotechnol.Prog.ꎬ2013ꎬ29(1):165-175.[24]㊀胡显文ꎬ肖成祖ꎬ高丽华ꎬ等.用多孔微载体大规模长期培养动物细胞的方法[J].生物技术通报ꎬ2001ꎬ(1):45-48. [25]㊀VentiniDCꎬDamianiRꎬSousaAPꎬetal..ImprovedbioprocesswithCHO ̄hTSHcellsonhighermicrocarrierconcentrationprovideshigheroverallbiomassandproductivityforrhTSH[J].Appl.Biochem.Biotechnol.ꎬ2011ꎬ164(4):401-409.[26]㊀李智ꎬ肖成祖ꎬ杨琴ꎬ等.CHO细胞无血清结团灌流培养:超声-沉降柱二合一灌流系统[J].中国生物工程杂志ꎬ2008ꎬ(4):53-58.[27]㊀ChunBHꎬLeeYKꎬChungN.Poly ̄gamma ̄glutamicacidenhancesthegrowthandviabilityofChinesehamsterovarycellsinserum ̄freemedium[J].Biotechnol.Lett.ꎬ2012ꎬ34(10):1807-1810.342郑惠惠ꎬ等:CHO细胞表达系统研究进展. All Rights Reserved.。

CHO细胞表达体系特点及CHO细胞表达疫苗来源:易生物实验浏览次数:533 网友评论0 条CHO细胞表达体系特点及CHO细胞表达疫苗关键词:细胞疫苗CHO细胞表达体系CHO细胞表达分子生物学、分子免疫学等学科的发展使基因工程疫苗具有越来越重要的地位。
在基因工程疫苗研究的动物细胞表达系统中,最具代表性的就是中国仓鼠卵巢细胞(Chinese Hamster Ovary,CHO)。
它是用来表达外源蛋白最多也最成功的一类细胞。
本文就CHO细胞表达系统在疫苗研制中的应用做一综述。
1、CHO细胞表达体系及其特点CHO细胞属于成纤维细胞,既可以贴壁生长。
也可以悬浮生长。
目前常用的CHO细胞包括原始CHO和二氢叶酸还原酶双倍体基因缺失型(DHFR-) 突变株CHO。
近年来,为降低生产成本和减少血制品带来的潜在危害性,动物细胞生产开始使用无血清培养基(SFM),但SFM往往导致细胞活力差,贴壁性差,分泌外源蛋白的能力差等缺点。
另有研究者尝试将类胰岛素生长因子IGF基因和转铁蛋白基因转入CHO细胞获得能自身分泌必需蛋白的“超级CHO”,无需在培养基中转铁蛋白和胰岛素,细胞可在sFM 中生长良好。
与其他表达系统相比,CHO表达系统具有以下的优点:(1)具有准确的转录后修饰功能,表达的蛋白在分子结构、理化特性和生物学功能方面最接近于天然蛋白分子;(2)既可贴壁生长,又可以悬浮培养,且有较高的耐受剪切力和渗透压能力;(3)具有重组基因的高效扩增和表达能力,外源蛋白的整合稳定;(4)具有产物胞外分泌功能,并且很少分泌自身的内源蛋白,便于下游产物分离纯化;(5)能以悬浮培养方式或在无血清培养基中达到高密度培养。
且培养体积能达到1000L以上,可以大规模生产。
2、CHO细胞表达疫苗(1)乙肝疫苗CHO细胞表达疫苗的种类不多,多数处于研究阶段。
目前只有CHO表达乙肝疫苗已投入生产,这是除酵母表达乙肝疫苗以外,唯一已用于人类使用的基因工程亚单位疫苗。

cho细胞优化蛋白表达的方式Cho细胞是一种常用的宿主细胞,被广泛应用于蛋白表达领域。
Cho细胞优化蛋白表达的方式主要包括以下几个方面:选择适当的表达载体、优化启动子和信号序列、调节培养条件、选择合适的转染方法以及利用辅助蛋白等。
在Cho细胞中进行蛋白表达,需要选择适当的表达载体。
常见的表达载体包括质粒和病毒载体。
质粒载体通常用于转染Cho细胞,而病毒载体则可以通过感染Cho细胞来实现蛋白表达。
根据实验的需要,可以选择不同类型的载体,如pCDNA3.1、pLVX等。
优化启动子和信号序列也是提高蛋白表达效率的重要策略。
启动子是控制基因转录的序列,在Cho细胞中常用的启动子有CMV、EF1α等。
信号序列则是控制蛋白质转运和分泌的序列,可以选择合适的信号序列来提高蛋白表达的效率。
调节培养条件也是优化蛋白表达的重要手段之一。
Cho细胞的培养条件包括培养基的选择、培养温度、CO2浓度、培养时间等。
合理调节这些条件可以促进细胞的生长和蛋白表达。
此外,添加适当的营养物质和辅助因子,如氨基酸、维生素和抗生素等,也能提高蛋白表达的效率。
选择合适的转染方法也是Cho细胞优化蛋白表达的重要环节。
常用的转染方法包括瞬时转染和稳定转染。
瞬时转染通过将表达载体导入Cho细胞,使细胞在一段时间内表达目标蛋白。
稳定转染则是将表达载体导入Cho细胞,并筛选出稳定表达目标蛋白的细胞株。
选择适当的转染方法可以提高蛋白表达的稳定性和效率。
利用辅助蛋白也是优化蛋白表达的一种策略。
辅助蛋白可以提高蛋白质的折叠和稳定性,从而增加蛋白表达的效率。
常见的辅助蛋白包括分泌辅助蛋白、折叠辅助蛋白等。
在表达目标蛋白时,可以选择适当的辅助蛋白来提高表达效果。
Cho细胞优化蛋白表达的方式主要包括选择适当的表达载体、优化启动子和信号序列、调节培养条件、选择合适的转染方法以及利用辅助蛋白等。
通过这些方式的综合应用,可以提高Cho细胞中蛋白表达的效率和稳定性,为后续的蛋白研究和应用奠定基础。
cho高效瞬时表达方法
CHO细胞高效瞬时表达方法是一种用于瞬时转染真核细胞的方法,该方法使用一种重组的腺病毒或质粒载体将外源基因瞬时转染入CHO细胞。
这种方法的优点是转染效率高,能够实现大规模的基因表达和生产,并且可以在短时间内完成实验。
CHO细胞高效瞬时表达方法的具体步骤包括:
1.准备重组质粒或腺病毒载体:将目的基因克隆到质粒或腺病毒载体中,并进行测序验证。
2.转染CHO细胞:将重组质粒或腺病毒载体与CHO细胞混合,通过特定的转染试剂将其导入细胞中。
3.筛选阳性克隆:在转染后的一段时间内,通过特定的筛选方法,如抗生素筛选或荧光激活细胞分选(FACS),从众多的细胞中筛选出阳性克隆。
4.扩大培养:将筛选出的阳性克隆进行扩大培养,以获得更多的目的基因产物。
5.收集产物:在目的基因产物积累到一定量后,收集产物并进行纯化和质量检测。
CHO细胞高效瞬时表达方法的应用范围广泛,可以用于抗体、重组蛋白、siRNA等生物制品的生产和研究。
cho细胞表达Cho细胞表达是指在生物学中,利用Cho细胞(Chinese Hamster Ovary cells)作为表达系统来表达外源蛋白质的过程。
Cho细胞是一种常用的哺乳动物细胞系,具有较高的蛋白质表达能力和稳定的遗传特性,因此被广泛应用于生物医学研究和制药工业中。
Cho细胞表达系统的优势在于其能够高效地表达外源蛋白质,并能够正确地折叠和修饰蛋白质。
Cho细胞具有相对简单的遗传背景和较低的背景蛋白质表达,可以避免其他细胞系统中常见的问题,如蛋白质聚集、不稳定、部分折叠等。
此外,Cho细胞的培养和维持相对容易,生长速度快,适应不同的培养条件,对不同的基因表达系统都具有较高的兼容性。
Cho细胞表达系统的应用范围广泛,包括生物医学研究、药物发现与研发、生物制药等领域。
在生物医学研究中,Cho细胞表达系统常被用于产生重组蛋白,如抗体、细胞因子、酶等,用于研究蛋白质功能、结构与机制。
在药物发现与研发中,Cho细胞表达系统被用于产生药物靶标蛋白、药物载体、药物代谢酶等,用于筛选和评价药物候选化合物。
在生物制药中,Cho细胞表达系统常被用于大规模生产重组蛋白药物,如单克隆抗体、重组蛋白等。
Cho细胞表达系统的建立和优化需要考虑多个因素。
首先,选择合适的载体和表达系统是关键。
常用的载体包括质粒、病毒载体等,表达系统可以是稳定转染系统或转染后选择稳定表达细胞的系统。
其次,选择合适的表达宿主细胞株和培养条件也十分重要。
Cho细胞的培养基和培养条件需要根据表达蛋白的特性和需求进行优化,包括培养基成分、温度、pH值、培养密度等。
此外,还需考虑到蛋白质折叠、修饰和纯化等后续步骤。
Cho细胞表达系统的优势也存在一些限制和挑战。
首先,Cho细胞是一种非人类细胞,因此相较于人类细胞,其表达的蛋白质可能存在差异。
其次,Cho细胞在遗传稳定性和蛋白质表达水平上存在一定的变异性,需要进行筛选和优化。
此外,Cho细胞的培养和维持相对费时费力,对于大规模的生产需求可能不太适用。
CHO细胞转染CM=MEM+HT+FBS SM=MEM+FBS TM =MEM+HTHT 是次黄嘌呤和胸腺嘧啶核苷混合剂,由于CHO-dhfr-细胞自身缺失二氢叶酸还原酶(dhfr),无法自身合成四氢叶酸,所以必须在添加了次黄嘌呤(hypoxanthine)、胸腺嘧啶(Thymidine)和甘氨酸的培养液中才能得以存活。
FBS 胎牛血清含有维持细胞生长的激素,基础培养基中没有的少量营养物;提供结合蛋白;解毒;贴壁细胞生长所需因子来源;缓冲系统;提供蛋白酶抑制剂。
1 初筛先用TM培养到6H(不含血清,因为转染所用是脂质体转染,其中阳离子脂质体其主要作用,将DNA包裹其中,血清中存在缓冲液系统,破坏转染),换用CM,因为是贴壁细胞,要用还有血清培养液;另外还有有HT才能正常生存。
24H换CM到48H(6-48h,一方面,转染主要有瞬时转染和稳定转染,在这个时间,瞬时转染基本消失,只剩下稳定转染;另一方面,转染成功细胞蛋白的表达时间),胰酶消化,用10倍胰酶的SM 中止——此时若DHFR基因已经成功转染,则可以在不含有HT的培养液中生存,即起一个筛选作用。
同时可以认为与其连锁的目的基因也成功转染到宿主细胞。
接下来再用G418进行筛选,NEO也是一个与目的基因连锁的基因,但是与DHFR结合在不同质粒上。
如果成功转染,则可以在含有G418的培养液中生存。
2 复筛用MTX筛选。
而通过目的基因与dhfr基因共转染,不仅得到在不含上述添加剂的培养基上也能生长的细胞克隆,更为重要的是由于dhfr可被叶酸类似物MTX所抑制,在MTX浓度选择压力下,dhfr基因必须扩增到很多的拷贝数才能生存,从而得到抗MTX细胞系;又由于与dhfr基因共转染的目的基因倾向于同它一起整合到细胞染色体上的同一区域,所以编码外源重组蛋白的序列片段也随着dhfr基因的扩增而扩增,我们就得到了能大量表达外源蛋白的细胞克隆,这在基因工程抗体及各种基因工程蛋白的表达中是可行度很高的一种措施。
CHO细胞(中国仓鼠卵巢细胞)表达系统CHO细胞表达系统原理分子生物学、分子免疫学等学科的发展使基因工程疫苗具有越来越重要的地位。
在基因工程疫苗研究的动物细胞表达系统中,最具代表性的就是中国仓鼠卵巢细胞(Chinese Hamster Ovary,CHO)。
它是用来表达外源蛋白最多也最成功的一类细胞。
本文就CHO细胞表达系统在疫苗研制中的应用做一综述。
CHO细胞表达体系及其特点诞生于70年代末的基因工程药物因其具有其他药物无法比拟的优点,已迅速成为制药工业中一个引人瞩目的领域。
1995年美国基因工程药物销售额约为48亿美元,1997年超过60亿美元,年增长率达20%以上。
各国政府将其视为新的经济增长热点而给予了大力支持。
基因工程药物研究与开发的主要环节包括:①基因的克隆和基因工程菌的构造;②重组细胞的培养;③目的产物的分离纯化等。
针对这些主要环节,研究人员正致力于高效表达、培养工艺及下游分离纯化等方面的研究。
随着基因工程技术的不断发展,目前已有多种表达系统可用于生产具有医疗价值的人或动物来源的蛋白质(表1)。
大肠杆菌(E.coli)是使用最早的表达系统,其显著优点是易于操作,产量高,成本低,但由于用E.coli生产的蛋白质药物因缺乏糖基化而在人体内易被降解,因此它的药放大大降低。
此外,它还存在易产生内毒素和包涵体的问题。
真核细胞中CHO细胞是目前重组糖基蛋白生产的首选体系;因为与其他表达系统相比,它具有许多优点:①具有准确的转录后修饰功能,表达的糖基化药物蛋白在分子结构、理化特性和生物学功能方面最接近于天然蛋白分子;②具有产物胞外分越功能,便于下游产物分离纯化;③具有重组基因的高效扩增和表达能力;④具有贴壁生长特性,且有较高的耐受剪切力和渗透压能力,可以进行悬浮培养,表达水平较高;⑤CHO细胞属于成纤维细胞(fibroblast),很少分泌自身的内源蛋白,利于外源蛋白的启分离。
但CHO细胞培养成本高,条件难掌握,易污染,在一定程度上影响了它的广泛应用。
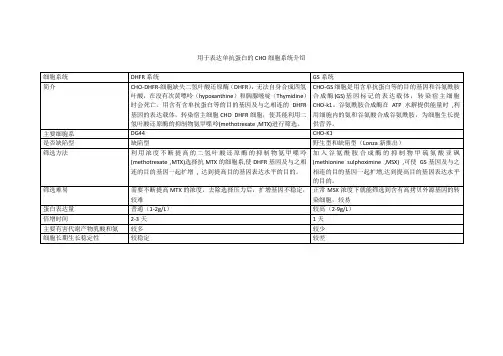
CHO细胞的稳定转染与基因表达
1、pcDNA3.1+-gD的线性化:pcDNA3.1+使用说明书推荐了以下几个酶作为线性化酶(BglⅡMfeⅡBst 1107ⅠEam1105ⅠPvuⅠScaⅠSspⅠ),通过DNAMAN分析gD序列发现其带有MfeⅡ酶切位点。
2、转染前一天,在60mm的dish中接种8×105个细胞,加入5ml培养基(含血清,不含抗生素),37℃,5%CO2培养,至转染时要求细胞40%-80%汇合。
3、通过分光光度计测定pcDNA3.1+-gD的浓度,用不含血清、抗生素、蛋白质的培养基稀释2.5ug的pc DNA3.1+-gD至总体积150ul,其最小浓度不低于0.1ug/ul,稀释后应颠倒几次EP管以混匀混合物。
4、向混匀的混合物中加入15ul转染试剂(PolyFect Transfection Reagent QIAGEN),用加样器吹打5次。
6、在室温下(20-25℃)孵育混合物5-10分钟。
7、在孵育的同时,吸出dish中的培养基,用PBS液洗涤一次,加入3ml的培养基(含血清,不含抗生素)。
8、孵育完成后加入1ml培养基(含血清),用加样器吹打2次,将产物全部加入60mm的dish中,轻轻摇动dish以混匀。
9、37℃,5%CO2培养,在细胞汇合度不超过50%时加入G418进行筛选。
转染时转染两组细胞,组一在转染后细胞汇合度不超过50%时(一般是24小时)加入G418进行筛选;组二在转染后待细胞汇合度达到80%时1/4000、1/1000、1/300分别接种于dish中,48小时后加G418筛选。
10、加入G418后,每3天更换一次含有筛选浓度的G418。
当有大量细胞死亡(5-7天)时,可以把G4 18的浓度减半维持筛选(此时可以加入适应性培养基1:4来改善细胞对培养基的同化作用)。
11、筛选10-14天后,可见有抗性的克隆出现,停药培养,待其逐渐增大后,制备细胞悬液,记数,用培养基稀释细胞到1个/10ul。
在96孔板中加入培养基150ul/孔,再加入细胞悬液10ul/孔。
待其逐渐增大后转入48孔板中增殖(为了减少实验失误带来的风险建议冻存部分增殖细胞)。
12、细胞大量扩增后,提取总DNA,做PCR检测目的基因是否存在。