硫及其化合物性质
- 格式:doc
- 大小:484.31 KB
- 文档页数:6

硫及其化合物讲义第一部分、知识梳理一、硫【物理性质】硫为固体、溶于水、溶于酒精、溶于CS2【化学性质】硫原子最外层个电子,较易电子,硫元素的常见化合价有,通常表现。
①与金属反应(与变价金属反应,金属均被氧化成低价态)Na + SHg + SFe + SCu + S②与非金属反应S + O2③与化合物的反应S + HNO3(浓)S + H2SO4(浓)S + NaOH④黑火药的反应【用途】大量用于制造硫酸、硫化天然橡胶,也用于制药和黑火药。
二、硫的氧化物1、二氧化硫【物理性质】色、有气味的气体,密度比空气,容易液化,溶于水。
【化学性质】①和水反应:SO2 +H2O此反应属于。
②与碱和碱性氧化物反应:SO2 +NaOHSO2 +Na2O SO2 +CaO③ 既有氧化性又有还原性: SO 2 + O 2 此反应属于SO 2 + H 2SSO 2 + Cl 2+ H 2OSO 2 + KMnO 4 + H 2OSO 2 + H 2O 2④ 漂白性:SO 2通入品红溶液,现象品红 ,然后稍稍加热,恢复到原来的红色。
SO 2漂白性的特点:有选择的暂时的化合漂白。
【实验室制法】Na 2SO 3 + H 2SO 4(浓) === Na 2SO 3 + H 2O +SO 2↑或Cu + 2H 2SO 4(浓) === CuSO 4 + 2H 2O + SO 2↑2、三氧化硫【物理性质】标况下为无色 、常温下为无色 、熔点 、沸点【化学性质】具有酸性氧化物的通性。
☆ 性质对比三、硫的氢化物【物理性质】 色、有 气味的有毒气体; 溶于水,密度比空气 。
【化学性质】① 强还原性:常见氧化剂Cl 2、Br 2、Fe 3+、HNO 3、KMnO 4等,甚至SO 2均可将H 2S 氧化。
△②不稳定性:300℃以上易受热分解③H2S的水溶液叫氢硫酸,是二元弱酸。
④可燃性四、硫酸1、稀硫酸无色水状液体,密度大于水具有酸的通性2、浓硫酸无色、难挥发的油状液体,密度大于水,熔沸点。


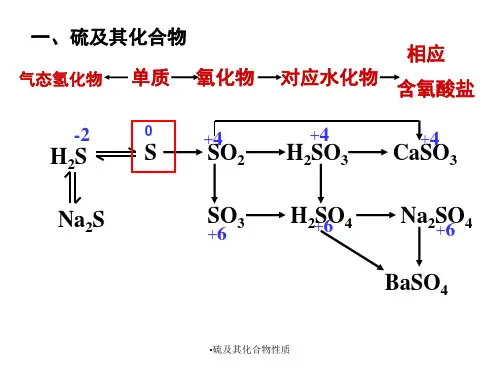
硫及其重要化合物一、硫1、S 的原子结构 ,相对原子质量:32,化合价:-2、0、+4、+4、+6.2、S3、S 的物理性质:俗称硫黄,颜色状态:淡黄色固体,溶解性:不溶于水,微溶于酒精,易溶于CS 2中。
4、S的化学性质:(1)与金属反应Fe +S=====△FeS 2Cu +S=====△Cu 2SHg +S=HgS (用以除去有毒的汞)2Ag +S=Ag 2S (黑色)(2)与非金属的反应S +O 2=====点燃SO 2(现象:空气中淡蓝色火焰;纯氧中蓝紫色火焰)。
S +H 2=====△H 2S (3)与碱反应:3S +6NaOH=====△2Na 2S +Na 2SO 3+3H 2O 。
二、硫的氧化物 (一)二氧化硫 1、物理性质:无色、有刺激性气味的有毒气体,密度比空气大,容易液化,易溶于水。
2、化学性质: (1)SO 2是酸性氧化物:A. 与H 2O 反应:SO 2+H 2O===H 2SO 3B. 与碱性氧化物反应与CaO 的反应为:CaO +SO 2===CaSO 3 与Na 2O 的反应为:Na 2O +SO 2===Na 2SO 3 C. 与碱反应SO 2少量:2NaOH +SO 2===Na 2SO 3+H 2O SO 2过量:NaOH +SO 2===NaHSO 3 D. 与某些弱酸盐溶液反应与NaHCO 3溶液反应(SO 2少量):2NaHCO 3+SO 2===Na 2SO 3+CO 2+H 2O 与NaHCO 3溶液反应(SO 2足量):NaHCO 3+SO 2===NaHSO 3+CO 2(2)SO 2的氧化性与还原性A. 氧化性:与H2S反应:2H2S+SO2===3S↓+2H2O(SO2通入氢硫酸中,溶液变浑浊)B. 还原性(能被O2、X2(Cl2、Br2、I2)、KM nO4(H+)溶液等强氧化剂氧化。
)①被O2氧化:2SO2 + O2 =====2SO3 (催化剂V2O5)②被Fe3+氧化:SO2+2Fe3++2H2O==2Fe2++SO42-+4H+③SO2能使酸性高锰酸钾溶液褪色。

硫及其化合物知识点加加加点加加硫及其化合物一、硫及其重要化合物的主要性质及用途: 1.硫:(1)物理性质:硫为淡黄色固体;不溶于水,微溶于酒精,易溶于CS 2(用于洗去试管壁上的硫);硫有多种同素异形体:如单斜硫、斜方硫、弹性硫等。
(2)化学性质:硫原子最外层6个电子,较易得电子,表现较强的氧化性。
①与金属反应(与变价金属反应,均是金属氧化成低价态)2Na+S===Na 2S (剧烈反应并发生爆炸)2Al+3S Al 2S 3(制取Al 2S 3的唯一途径)Fe+SFeS (黑色)2Cu + S Cu 2S (黑色) ②与非金属反应S+O 2 SO 2S+H 2H 2S (说明硫化氢不稳定)③与化合物的反应S+6HNO 3(浓)点H 2SO 4+6NO 2↑+2H 2O S+2H 2SO 4(浓) 2SO 2↑+2H 2O3S+6NaOH2Na 2S+Na 2SO 3+3H 2O (用热碱溶液清洗硫)(3)用途:大量用于制造硫酸、硫化天然橡胶,也用于制药和黑火药。
三药一柴:医药、火药、农药、和火柴的原料。
2.硫的氢化物: ①硫化氢的物理性质:H 2S 是无色、有臭鸡蛋气味的有毒气体;能溶于水,密度比空气略大。
②硫化氢的化学性质 A .可燃性:当2/O S H n n ≥2/1时,2H 2S+O22S+2H 2O (H 2S 过量) 当22/O S H n n ≤2/3时,2H 2S+3O 2点燃2SO 2+2H 2O (O 2过量)当23222<<O S H n n 时,两种反应物全部反应完,而产物既有硫又有SO 2B .强还原性:常见氧化剂Cl 2、Br 2、I 2、Fe 3+、HNO 3、浓H 2SO 4、KMnO 4等,甚至SO 2均可将H 2S 氧化。
加③H2S的水溶液叫氢硫酸,是二元弱酸。
除杂:用CuSO4溶液除去H2S:CuSO4+H2S===CuS↓+H2SO43.硫的氧化物:(1)二氧化硫:①SO2是无色而有刺激性气味的有毒气体,密度比空气大,容易液化,易溶于水。


高三一轮复习——硫及其化合物一.硫1.结构硫原子的原子结构示意图;硫位于周期表中第周期族;硫元素在自然界中的存在形态。
硫单质通常可以形成两种结构不同的晶体:单斜硫和正交硫,它们互为;硫可以形成多种分子,如S2、S4、S8等。
2.性质⑴物理性质:硫为淡黄色固体,有特殊气味;不溶于水,微溶于酒精,易溶于二硫化碳⑵硫化学性质①与非金属(H2、O2)反应:②与金属(Na、Al、Fe、Cu)反应:③与强碱反应S + NaOH →+ Na2SO3 + H2O3.用途:工业、农业、医疗二.硫化氢1.结构H2S的电子式,结构式,是由键构成的性分子,其形成的晶体属于晶体。
2.性质⑴物理性质:无色,具有气味的有毒气体,微溶于水,密度比空气大⑵化学性质①不稳定性:②可燃性:,③较强还原性(SO2、H2SO3、Fe3+、卤素、HNO3、浓H2SO4等)④其它:H2S + Cu2+→CuS↓+ 2H+(弱酸制强酸);Na2S + H2S →⑤氢硫酸:二元弱酸,具有酸的通性3.实验室制法⑴原理:。
能否用HNO3或浓H2SO4来制取?⑵装置:⑶除杂:⑷收集:⑸尾气处理:4.S2-及H2S的检验方法:气体使湿润的醋酸铅试纸变黑【巩固练习】1.欲除去H2S气体中少量的HCl,应使气体通过A.饱和NaHCO3溶液B.饱和Na2S溶液C.饱和NaHS溶液D.NaOH溶液2.在标况下,将50mL H2S和60mL O2混合引燃,待反应完全后,恢复至标况下,此时生成SO2的体积为A.40mL B.35mL C.45mL D.110mL 3.常温常压下,将a L SO2和b L H2S混合,当反应后气体体积是反应前气体体积的1/4时,则a和b之比可能是A.1∶1 B.1∶2 C.1∶3 D.2∶14.有关H2S的叙述正确的是A.H2S因含有-2价的硫,所以只有还原性B.H2S能与Na2S溶液反应C.H2S与FeSO4溶液反应有黑色沉淀FeS生成D.实验室制取H2S 时,只能用稀盐酸或稀硫酸,而不能用浓硫酸或硝酸5.下列物质中,不能与硫化氢反应的是A.K2S溶液B.SO2C.双氧水D.FeSO4溶液6.下列物质中既可以利用化合反应制取,又可以利用溶液中的复分解反应制取的是A.NaOH B.FeS2C.FeCl3D.CuS7.在标准状况下,将a mol H2S和b mol O2混合充分燃烧后,两反应物都没有剩余,得到三种产物(S、SO2和H2O),则下列判断不正确的是A.产生的SO2是(b-0.5a)mol B.反应后生成水的质量为18a gC.3a>2b>a D.反应后氧化产物的质量为(16a-32b)8.右图中每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点代表的是A.H2S B.HCl C.PH3D.SiH49.将一定量铁粉和硫粉的混合物共热,充分反应后冷却,再加入足量稀硫酸,得到标准状况下的气体11.2L,则原混合物的组成可能是A.n(Fe)<n(S),总质量等于44g B.n(Fe)>n(S),总质量等于44gC.n(Fe)=n(S),总质量大于44g D.n(Fe)>n(S),总质量小于44g10.向300mL KOH溶液中缓慢通入2.24L(标准状况下)CO2气体,充分反应后,在减压低温下蒸发溶液,得到11.9g不含结晶水的白色固体。
东方教育学科教师辅导讲义讲义编号学员编号: 年 级: 课时数:学员姓名: 辅导科目: 学科教师:课 题硫及其重要化合物的性质 授课时间:备课时间:教学目标重点、难点教学内容[知识点归纳]1、硫的物理性质:黄色或淡黄色固体,很脆,俗称硫磺。
硫不溶于水,微溶于酒精,易溶于CS 2硫的化学性质:从化合价分析,硫元素有-2、0、+4、+6四种常见化合价,单质硫是0价,既有氧化性又有还原性。
从原子结构分析,硫原子最外层有6个电子,为了达到稳定结构,在化学变化中一般容易获得2个 电子,也可以偏离6个电子,所以单质硫既有氧化性又有还原性。
A:硫的氧化性(1)与金属反应: Fe+S FeS2Cu+S Cu 2S2Na+S Na 2S2Al+3S Al 2S 3Hg+S HgS(2)硫与氢气反应: H 2+S H 2S 点燃B:硫的还原性(3)硫与氧气反应: S+O 2 SO 2点燃2、硫元素和氯元素非金属性的差异的比较与金属反应时,氯可将铁和铜分别氧化成高价的+3和+2价,而硫只能将它们分别氧化成低价的+2和+1价。
所以非金属性:氯强于铝3、硫化氢的物理性质:无色有臭鸡蛋气味气体,密度比空气大,有剧毒,是一种大气污染物。
能溶于水。
硫化氢的化学性质:H 2S 中S 显-2价,是硫元素的最低价,因此发生氧化还原反应时,S 的化合价只能升高,表 现还原性。
A :H 2S 在空气中的燃烧(可燃性)(1)2H 2S+O 2(不足) 2S+2H 2O 点燃 发出淡蓝色火焰,小烧杯内壁有水珠,且出现黄色固体。
(2)2H 2S+3O 2(充足) 2SO 2+2H 2O 点燃发出淡蓝色火焰,并产生有刺激性气味的气体。
B :还原性(1) SO 2+ 2H 2S —→3S+2H 2O(2) H 2S+ H 2SO 4(浓)—→SO 2 + S + 2H 2O(3) H 2S+ X 2—→2HX+ S (X 为氯、溴、碘)C :不稳定性H 2S —→H 2+S4、二氧化硫的物理性质:无色具有刺激性气味的有毒气体。

硫及其化合物第一部分基础知识一、硫(一)结构和存在1、结构(1)硫位于第三周期第ⅥA族电子排布式为 [Ar]3s23p4(2)结构式 S8 (斜方硫和单斜硫的化学式均为S8,除此之外还有其他分子种类,如S2、S3、S4、S5、S6、S7……S20和其他硫链等。
)2、存在形式(1)游离态:存在火山喷口附近或地壳岩层里。
原因:气体中还有的SO2与H2S气体相遇生成硫单质沉积在火山口附近。
(2H2S+SO2=3S↓+2H2O)(2)化合态:硫化物:硫铁矿(FeS2)、黄铜矿(CuFeS2)硫酸盐:芒硝(Na2SO4·10H2O)、石膏(CaSO4·2H2O)其他:蛋白质、化石燃料(煤、石油、天然气)(二)物理性质1、颜色状态:黄色晶体、质脆、易研成粉末。
俗称:硫磺2、溶解性:不溶于水,微溶于酒精,易溶于二硫化碳(CS2)。
可以用二硫化碳洗涤内壁附着硫单质的试管。
(三)化学性质1、氧化性(1)与Na反应 2Na + S Na2S将硫粉和金属钠混合在研钵中研磨,可以听到轻微的爆炸声。
(2)与比价金属反应时生成低价金属硫化物Fe + S FeS , 2Cu + S CuS研磨(3)硫蒸气与H2反应 H2+ S H2S2、还原性(1)与O2反应S + O2 SO2硫在空气中燃烧产生微弱的淡蓝色火焰,在纯氧中燃烧产生蓝紫色火焰,都产生刺激性气味的气体。
(2)与浓硫酸反应S + 2H2SO4(浓) 3SO2↑ + 2H2O 归中反应3、既表现氧化性,又表现还原性——与NaOH反应3S + 6NaOH 2Na2S + Na2SO3+ 3H2O(四)用途1、制农药:如硫合剂(石灰、硫磺),可用于杀死果树的害虫。
2、制黑火药:“一硫二硝三木炭”S + 2KNO3 + 3C K2S + N2↑ +3CO2↑3、消除汞蒸气:实验室里不慎洒落一些汞,可以撒上硫粉处理。
二、硫的化合物(一)二氧化硫 SO21、物理性质无色、具有刺激性气味的气体,密度大于空气,易溶于水(1:40),沸点较低,易液化,有毒2、化学性质(1)酸性氧化物与H2O反应 H2O + SO2= H2SO3与碱反应SO2 + NaOH = NaHSO3SO2过量SO2 + 2NaOH = Na2SO3+ H2O SO2少量SO2 + Ca(OH)2= CaSO3↓ + H2OSO2 + Ba(OH)2= BaSO3↓ + H2O与碱性氧化物反应 SO2 + CaO = CaSO3与某些盐反应 SO2(少) + 2NaHCO3= Na2SO3 + H2O +2CO2点燃点燃SO2(过) + NaHCO3= NaHSO3 + CO2 (2)氧化性与H2S反应 2H2S+SO2=3S↓+2H2O(3)还原性①使卤族单质水溶液褪色Cl2 + SO2+ 2H2O = H2SO4+ 2HClBr2 + SO2+ 2H2O = H2SO4+ 2HBrI 2 + SO2+ 2H2O = H2SO4+ 2HI②使KMnO4(H+)褪色2KMnO4 + 5O2+2H2O = K2SO4+ 2MnSO4+ 2H2SO4③使FeCl3由黄色变为浅绿色2FeCl3 + SO2+ 2H2O = FeCl2+ FeSO4+ 4HCl④催化氧化2SO2 + O22SO3(4)漂白性SO2与某些有色物质化合成不稳定的无色物质,这种无色物质受热易分解,而使有色物质恢复原来的颜色。

硫及其化合物一、硫及其重要化合物的主要性质及用途: 1.硫:(1)物理性质:硫为淡黄色固体;不溶于水,微溶于酒精,易溶于CS 2(用于洗去试管壁上的硫);硫有多种同素异形体:如单斜硫、斜方硫、弹性硫等。
(2)化学性质:硫原子最外层6个电子,较易得电子,表现较强的氧化性。
①与金属反应(与变价金属反应,均是金属氧化成低价态)Al 2S 3的唯一途径) 2S (黑色) ②与非金属反应2 (说明硫化氢不稳定)③与化合物的反应 S+6HNO 34+6NO 2↑+2H 2O S+2H 2SO 4+2H 2O 2S+Na 2SO 3+3H 2O (用热碱溶液清洗硫)(3)用途:大量用于制造硫酸、硫化天然橡胶,也用于制药和黑火药。
三药一柴:医药、火药、农药、和火柴的原料。
2.硫的氢化物:①硫化氢的物理性质:H 2S 是无色、有臭鸡蛋气味的有毒气体;能溶于水,密度比空气略大。
②硫化氢的化学性质A .可燃性:当22/O S H n n ≥2/1时,2H 2S+O 22O (H 2S 过量)当22/O S H n n ≤2/3时,2H 2S+3O 2 点燃2SO 2+2H 2O (O 2过量)当23222<<O S H n n 时,两种反应物全部反应完,而产物既有硫又有SO 2 B .强还原性:常见氧化剂Cl 2、Br 2、I 2、Fe 3+、HNO 3、浓H 2SO 4、KMnO 4等,甚至SO 2均可将H 2S 氧化。
③H 2S 的水溶液叫氢硫酸,是二元弱酸。
除杂:用CuSO 4溶液除去H 2S : CuSO 4+H 2S===CuS ↓+H 2SO 4 3.硫的氧化物:(1)二氧化硫:①SO 2是无色而有刺激性气味的有毒气体,密度比空气大,容易液化,易溶于水。
②SO 2是酸性氧化物,能跟水反应生成亚硫酸,亚硫酸是中强酸。
③SO 2有强还原性 常见氧化剂(见上)均可与SO 2发生氧化一还原反应 如:SO 2 + Cl 2 +2H 2O == H 2SO 4 + 2HCl④SO 2也有一定的氧化性 2H 2S + SO 2 == 3S ↓ +2H 2O⑤SO 2具有漂白性,能跟有色有机化合物生成无色物质(可逆、非氧化还原反应)⑥实验室制法:Na 2SO 3 + H 2SO 4(浓) == Na 2SO 3 + H 2O +SO 2↑或Cu + 2H2SO4(浓) === CuSO4 + 2H2O + SO2↑(2)三氧化硫:是一种没有颜色易挥发的晶体;具有酸性氧化物的通性,遇水剧烈反应生成硫酸并放出大量的热。

硫及其重要化合物的性质和应用一、知识梳理1.硫(1)游离态:硫单质俗名硫黄,主要存在于火山口附近或地壳的岩层里。
(2)化合态:主要以金属硫化物和硫酸盐的形式存在,如硫铁矿(FeS 2)、黄铜矿(CuFeS 2)、石膏(CaSO 4·2H 2O)和芒硝(Na 2SO 4·10H 2O)等。
(3)物理性质:硫为淡黄色固体;不溶于水,微溶于酒精,易溶于CS 2(用于洗去试管壁上的硫);硫有多种同素异形体:如单斜硫、斜方硫、弹性硫等。
(4)化学性质:硫原子最外层6个电子,较易得电子,表现较强的氧化性。
①与金属反应(与变价金属反应,均是金属被氧化成低价态)2Na+SNa 2S (剧烈反应并发生爆炸) 2Al+3S Al 2S 3(制取Al 2S 3的唯一途径)Fe+S FeS (黑色) 2Cu + S Cu 2S (黑色) ②与非金属反应S+O 2 点燃SO 2 S+H 2 H 2S (说明硫化氢不稳定)③与化合物的反应S+6HNO 3(浓)H 2SO 4+6NO 2↑+2H 2O S+2H 2SO 4(浓)2SO 2↑+2H 2O 3S+6NaOH2Na 2S+Na 2SO 3+3H 2O (用热碱溶液清洗硫)(5)用途:大量用于制造硫酸、硫化天然橡胶,也用于制药和黑火药。
2、硫的氢化物 (1)硫化氢的制取Fe+H 2SO 4(稀)FeSO 4+H 2S↑(不能用浓H 2SO 4或硝酸,因为H 2S 具有强还原性)——H 2S 是无色、有臭鸡蛋气味的有毒气体;能溶于水,密度比空气略大。
(2)硫化氢的化学性质A .可燃性:当22(H S)(O )21n n 时,2H 2S+O 2 点燃2S+2H 2O (H 2S 过量)当22(H S)(O )23n n ≤时,2H 2S+3O 2 点燃2SO 2+2H 2O (O 2过量) 当22(H S)(O )223n n 〈〈时,两种反应物全部反应完,而产物既有S 又有SO 2 B .强还原性:常见氧化剂Cl 2、Br 2、Fe 3+、HNO 3、KMnO 4等,甚至SO 2均可将H 2S 氧化。
硫与其化合物的性质与应用硫(S)是一种常见的非金属元素,存在于自然界中的许多矿石和有机物中。
它具有多种化合物,拥有独特的性质和广泛的应用。
本文将探讨硫及其化合物的性质和应用。
一、硫的性质硫是一种黄色的固体,无味,无毒。
它具有较低的熔点和沸点,能在常温下蒸发。
硫在空气中加热后会燃烧,产生剧烈的蓝色火焰和刺激性气味。
1. 物理性质硫具有单斜晶系结构,晶体呈现六角形的螺旋结构。
它的密度约为2 g/cm³,硬度较低。
在常温下,硫为柔软的固体,可以被切割成薄片或压成粉末。
2. 化学性质硫具有较强的化学活性。
它可以与许多元素反应,形成各种化合物。
例如,硫与氧气反应会生成二氧化硫(SO₂),该化合物是大气污染的主要来源之一。
硫还能与金属反应形成金属硫化物,如铁与硫反应生成硫化铁(FeS)。
此外,硫还与氢反应生成硫化氢(H₂S),具有强烈的恶臭味道。
二、硫化物的性质与应用1. 金属硫化物金属硫化物是硫与金属元素形成的化合物,具有重要的性质和应用。
例如,硫化铁是一种黑色的固体,可以用于制备磁性材料和矿石的磁选。
硫化铜是一种红色的固体,广泛应用于电镀、颜料和催化剂等领域。
此外,硫化锌也是一种重要的无机材料,广泛用于制备橡胶增塑剂、涂料和橡胶产品。
2. 有机硫化物有机硫化物是含有硫原子的有机化合物,具有独特的性质和广泛的应用。
其中,二硫化物是一类重要的有机硫化合物,具有良好的润滑性能和耐热性。
二硫化钼(MoS₂)常用于制备润滑油和减摩剂。
含有硫的有机化合物还常用作药物和农药的中间体。
硫醇是含有硫原子和氢原子的有机化合物,常用于金属表面防锈和抗氧化剂。
3. 硫酸及其盐类硫酸(H₂SO₄)是一种强酸,广泛应用于化工、冶金、制药和环保等领域。
硫酸可用于制备肥料、染料和塑料等工业产品。
此外,一些硫酸盐如硫酸铜、硫酸锌等也具有重要的应用,如用于制备电池、电镀和农药等。
4. 硫化氢硫化氢(H₂S)是一种无色有毒气体,具有刺激性气味。
硫及其化合物的性质【知识精要】1.二氧化硫化学性质(1)酸性氧化物通性二氧化硫与水的反应:SO2澄清石灰水反应:(2)还原性①二氧化硫与氧气的反应:SO3物理性质:无色固体,熔点:16.8℃,沸点:44.8℃都较低。
SO3是硫酸的酸酐,SO3与水化合生成硫酸,同时放出大量的热。
方程式为:SO3 + H2O = H2SO4 + Q②SO2的水溶液可被O2、H2O2、X2、Fe3 +、KMnO4、Ca(ClO)2等强氧化剂氧化:SO2通入氯水(3)氧化性(4)二氧化硫的漂白作用①品红通二氧化硫后颜色变化;②褪色后的溶液加热后的颜色变化。
2.酸雨的形成3.硫酸的制备4.硫酸的吸水性、脱水性、强氧化性例1.根据下图回答问题:(1)上述装置中,在反应前用手掌紧贴烧瓶外壁检查装置的气密性,如观察不到明显的现象,还可以用什么简单的方法证明该装置不漏气。
答:。
(2)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:(3)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入的试剂的名称及其作用:A中加入的试剂是,作用是。
B中加入的试剂是,作用是。
C中加入的试剂是,作用是。
D中加入的试剂是,作用是。
(4)实验时,C中应观察到的现象是。
例2.一定物质的量的SO2与NaOH溶液反应,所得产物中含Na2SO3和NaHSO3物质的量之比为3∶5,则参加反应的SO2与NaOH物质的量之比为—————()A.1∶2 B.3∶5 C.8∶11 D.18∶8例3.我国农业因遭受酸雨而造成的损失每年高达15亿多元,为了有效控制酸雨,目前国务院已批准了《酸雨控制区和二氧化硫污染控制区划分方案》等法规。
分析数据,回答下列问题:①雨水样品的pH变化的原因是(用化学方程式表示)_____________________;②如果将刚取样的上述雨水与自来水相混合,pH将变_____________,原因是(用化学方程式表示)_______________________。
(2)为防治酸雨,降低煤燃烧时向大气排放的SO2,工业上将生石灰和含硫煤混合后使用,请写出燃烧时,有关“固硫”(不使硫化合物进入大气)反应的化学方程式______________________________,_________________________________。
例4.根据下列化学反应和事实,说明反应利用了硫酸的什么性质,将表示性质的选项的字母填在各小题的横线上。
A.难挥发性B.酸性C.吸水性D.脱水性E.强氧化性F.强酸性(1)浓硫酸可作气体干燥剂_______________;(2)CuSO4·5H2O 浓硫酸CuSO4+5H2O ;(3)2NaCl+H2SO4(浓)Na2SO4+2HCl↑_______________;(4)FeS+H2SO4=FeSO4+H2S↑_______________;(5)Zn+H2SO4=ZnSO4+H2↑_______________;(6)Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O _______________;(7)Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O_______________;(8)S+2H2SO4(浓)3SO2↑+2H2O_______________;【硫酸根离子的检验方法】已知稀硝酸具有强氧化性滤液气体沉淀【思考】三个学生设计了下述三个实验方案,并都认为,如果观察到的现象和自己设计的方案一致,即可确证试液中含有SO42-。
方案甲:试液−−−→−溶液2BaCl白色沉淀−−−→−足量稀盐酸沉淀不溶解方案乙:试液−−−→−足量稀盐酸无沉淀−−−→−溶液2BaCl白色沉淀方案丙:试液−−−→−足量稀硝酸无沉淀−−−→−硝酸钡溶液白色沉淀试评价上述三种方案是否严格,并分别说明理由。
例1.写出可除去下列气体中杂质(括号内为杂质)的试剂:(1)Cl2(HCl、H2O)(2)CO2(HCl)(3)CO2(SO2)(4)SO2(SO3)(5)CO2(CO)(6)CO(CO2)(7)SO2(HCl)(8)N2(O2 、Cl2、H2O)例2.下列反应中,一定有沉淀生成的是A.CO2通入CaCl2溶液B.足量CO2通入饱和Na2CO3溶液C.SO2通入BaCl2溶液D.过量SO2通入澄清石灰水E.向久置的Na2SO3溶液中加入BaCl2溶液,再加入稀盐酸F.向Na2SO3溶液中通入Cl2,再滴加BaCl2和稀盐酸例3.某课外活动小组的同学,在实验室做锌与浓硫酸反应的实验时,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫外,还可能产生氢气。
为了验证甲、乙两位同学的判断是否正确,丙同学设计了如下图所示实验装置。
(锌与浓硫酸共热时产生的气体为X,且该装置略去)试回答:(1)上述反应中生成二氧化硫的化学方程式_____________。
(2)乙同学认为还可能产生氢气的理由_________________。
(3)丙同学在安装好装置后,必不可少的一步操作是____________。
(4)A中加入的试剂可能是______,作用是_____________B中加入的试剂可能是________,作用是_____________E中加入的试剂可能是________,作用是_____________(5)可以证明气体X中含有氢气的实验现象是:C中:______________,D中:______________。
如果去掉装置B,还能否根据D中的现象判断气体X中有氢气?____(填能或不能),原因是_________________________。
【练习】1. Cl2和SO2都有漂白作用,能使品红溶液褪色.若将等物质的量的Cl2和SO2混合后,再通入品红与BaCl2的混合溶液,能观察到的现象是: ①溶液很快褪色;②溶液不褪色; ③出现沉淀; ④不出现沉淀A.①②B.①③C.②③D.②④2. 浓H2SO4在下列反应中,既表现氧化性,又表现酸性的是A. Cu + 2H2SO4(浓) = CuSO4 + SO2 + 2H2OB. C + 2H2SO4(浓) = CO2 + 2SO2 +2H2OC. 2FeO + 4H2SO4(浓) = Fe2(SO4)3 + SO2 + 4H2OD. Fe2O3 + 3H2SO4(浓) = Fe2(SO4)3 + 3H2O3. 关于SO2的叙述中正确的是A.它可使石蕊试液褪色B.与水作用生成硫酸C.能使溴水褪色D.等物质的量的氯气和二氧化硫通入品红溶液中,品红溶液褪色.4. 将二氧化硫通到显红色的酚酞试液中,发现红色消失,主要原因是SO2有A.漂白性B.还原性C.氧化性D.溶于水显酸性5.下列说法正确的是A.二氧化硫能使高锰酸钾酸性溶液迅速褪色B用澄清石灰水鉴别二氧化硫和二氧化碳C.硫粉在过量的纯氧中燃烧可以生成三氧化硫D.少量二氧化硫通入浓的氯化钙溶液中能生成白色沉淀6. 你认为减少酸雨产生的途径可采用的措施是①少用煤作燃料②把工厂烟囱造搞③燃料脱硫④在已酸化的土壤中加石灰;⑤开发新能源A.①②③B.②③④⑤C.①③⑤D.①③④⑤7.能证明SO2有漂白性的是A.酸性KMnO4溶液通入SO2后紫色消失B.显红色的酚酞溶液通入SO2后红色消失C.品红溶液通入SO2气体后红色消失D.溴水通入SO2气体后橙色消失8.下列实验中:①使澄清石灰水变浑浊②使湿润的蓝色石蕊试纸变红③使品红褪色④通入足量的NaOH溶液中,再滴加BaCl2溶液有白色沉淀生成,该沉淀溶于稀盐酸⑤通入溴水中能使溴水褪色,且滴加Ba(NO3)2溶液有白色沉淀产生其中能证明有SO2存在的是A.都能证明B.都不能证明C. ③④⑤能证明D.只有⑤能证明9.向FeCl3和BaCl2的酸性混合溶液中通入SO2气体,有白色沉淀生成,此沉淀是A.BaSO4B.FeSC.BaSO3D.S10.在氢硫酸溶液中加入(或通入)少量下列物质,能使溶液pH减小的是①O2 .②Cl2. ③SO2. ④CuCl2A. ①②B.②③④C.②④ D. ②11. 下列溶液中,不能区别SO2和CO2气体的是①石灰水②H2S溶液③KMnO4溶液④溴水⑤酸化的Ba(NO3)2溶液⑥品红溶液A.①②③⑤B.②③④⑤C.只有①D.①③12.下列说法不正确的是————————————————()A.硫是一种淡黄色的能溶于水的晶体B.硫与氧属于同一主族C.硫的化合物常存在于火山喷出的气体中和矿泉水里D.硫在空气中的燃烧产物是二氧化硫,在纯氧中的燃烧产物是三氧化硫13.高温下硫酸亚铁发生如下反应:2FeSO4高温Fe2O3+SO2↑+SO3↑,若将生成的气体通入氯化钡溶液中,得到的沉淀物是————————————————()A.BaSO3和BaSO4 B.BaS C.BaSO3 D.BaSO414.下列微粒中,只具有还原性的是——————————————————()A.S2–B.SO32–C.SO42–D.SO215.SO2是重要的大气污染物,大量SO2的来源是。
SO2不仅本身污染大气,而且它在大气中经尘粒催化能与水、氧气作用形成危害更大的酸雨,反应的化学方程式是、。
抽取某地酸雨水样进行检验,测得各离子的浓度分别是:c(Na+)= 2.3×10-5mol/L,c(Cl-)= 2.3×10-5mol /L,c(NH4+)= 2.3×10-5mol/L,c(SO42-)= 2.3×10-5mol/L,则该酸雨中的c(H+) = 。
16.Na2SO3在空气中极易被氧化,现有a g样品,将其溶解后,加入足量BaCl2溶液,可得干燥的沉淀b g。
(Na 23 Ba 137 S 32)(1)若Na2SO3未被氧化,b=a。
(2)若Na2SO3全部被氧化,b=a。
(3)若Na2SO3部分被氧化,b与a的关系式为。
17.含有下列离子的水溶液中,长期露置在空气中会变质,但不是被氧化的是()A.OH—B.Fe2+C.SO32--D.ClO--18.关于浓硫酸的叙述错误的是———————————————————()A.具有脱水性,故能做干燥剂B.常温下可使某些金属钝化C.是难挥发的粘稠状液体D.溶于水放出大量的热19.将SO2通入显红色的酚酞试剂中,发现红色消失,主要是因为SO2———()A.有漂白性B.有还原性C.溶于水后显酸性D.有氧化性20.煤是一种重要的能源,含有硫元素,下列说法正确的是————————()A.煤是含碳化合物B.煤是一种可再生能源C.在水吸收SO2的过程中只发生物理变化D.SO2是酸性氧化物,被云雾吸收后转化成酸雨21、.向50ml 18 mol·L-1硫酸中加入足量铜片,充分反应后,被还原的硫酸物质的量为()A、等于0.9molB、大于0.45mol小于0.9molC、等于0.45molD、小于0.45mol22.既能使石蕊试液变红,又能使品红试液变为无色,还能使溴水褪色的是( )A. Cl2B. H2SC. SO2D. CO223.下列物质均具有漂白作用,其中一种与另外三种的漂白原理不同的是()A.HClO B.H2O2 C.SO2 D.O324.下列物质中硫元素只显示还原性的是()A.H2SB.SO2C.SD.H2SO425.除去SO2中混有的HC1气体,可选用的试剂是()A.石灰水B.浓硫酸C.饱和NaHSO3溶液D.饱和Na2SO3溶液26.将PH试纸蘸取浓H2SO4后,试纸的颜色将变为()A.蓝B.黑C.红D.27、取三张蓝色石蕊试纸湿润后贴在玻璃片上,然后按顺序分别滴加65%硝酸溶液、98%的硫酸溶液、新制氯水,三张试纸最终变成()。