苯乙酮肟的合成
- 格式:doc
- 大小:26.50 KB
- 文档页数:2



酮肟的合成方法-概述说明以及解释1.引言1.1 概述酮肟是一类有机化合物,其分子中含有酮和肟基团。
酮肟分子的结构具有独特的特点,使其在有机合成和药物研究领域得到广泛应用。
酮肟化合物广泛存在于天然产物、药物和农药中,具有抗菌、抗病毒、抗肿瘤等生物活性,因此受到了研究人员的极大关注。
酮肟化合物的合成方法研究成为有机化学领域的重要课题。
在酮肟的合成方法方面,研究人员通过不同的反应策略实现了高效和高选择性的合成。
常用的合成方法包括氧化肟、羰基化合物与氨或胺进行反应、肟化合物的氢化等。
这些方法不仅具有较高的合成效率,还能提供多样化的结构类型,满足不同需求。
酮肟的合成方法研究还涉及到了反应机理的探索。
研究人员通过实验和计算化学方法,揭示了不同反应条件下,酮肟形成的机制和关键步骤。
这对于进一步改进合成方法、提高产率和选择性具有重要意义。
本文将系统地介绍酮肟的定义、应用、合成方法和反应机理。
通过综述已有的研究成果,总结不同的合成策略,并展望酮肟合成的发展方向。
同时,对酮肟在相关领域的应用前景进行展望,为进一步研究和应用酮肟化合物提供参考和启示。
1.2文章结构1.2 文章结构本文将分为引言、正文和结论三个部分进行讨论。
下面对每个部分的内容进行详细介绍:(1)引言部分(Introduction):本部分将对酮肟合成方法的研究背景和意义进行概述,介绍酮肟在化学和医药领域的广泛应用,并阐明酮肟合成方法的重要性。
同时,将简单介绍本文的研究目的和结构安排。
(2)正文部分(Main Body):本部分将分为三个小节,分别是酮肟的定义和应用、酮肟的合成方法以及酮肟的反应机理。
- 酮肟的定义和应用:首先,将介绍酮肟的化学结构和常见的物理性质。
然后,探讨酮肟在有机合成、药物合成和材料科学领域的重要应用,以及其在生物学和医学领域中的潜在应用价值。
- 酮肟的合成方法:本节将详细介绍目前已知的各种酮肟合成方法,包括传统的化学合成方法和新近发展的绿色合成方法。

肟基苯乙酮合成工艺优化研究作者:朱平华陈文宾来源:《湖北农业科学》2011年第22期摘要:以亚硝酸钠、甲醇、浓硫酸和苯乙酮为原料,氢氧化钠为催化剂通过两步反应合成了肟基苯乙酮。
通过正交试验确定最佳合成的工艺条件是亚硝酸钠∶甲醇∶浓硫酸∶苯乙酮=0.8∶1.0∶0.5∶1.0(摩尔比),催化剂的用量10mL(1.2mol/L),反应温度5℃。
产品的总收率83.1%,纯度99.0%。
试验的分析结果表明,反应温度是反应的主要影响因素。
关键词:肟基苯乙酮;合成;优化工艺;正交试验中图分类号:TQ244.2文献标识码:A文章编号:0439-8114(2011)22-4612-02Optimization of Synthesis Technology of Oximido-acetophenoneZHUPing-hua,CHENWen-bin(SchoolofChemicalEngineering,HuaihaiInstituteofTechnology,Lianyungang222005,Jiangsu,China)Abstract:Oximido-acetophenone wassynthesizedfromsodiumnitrite,methanol,concentratedsulphuricacidandacetophenonewithsodiumhydroxideasthecatalystbytwostepsreaction.Bestreactionconditionsarefoundbyorthogonaltest.Theoptimumconditions were asfollows the amount ratioofsodiumnitrite,methano,sulfuricacid and acetophenone was 0.8∶1.0∶0.5∶1.0;theamountofcatalystsodiumhydroxide was10mL(1.2mol/L),reactiontemperature was5℃.Thetotalyield ratio ofproducts was83.1%,andthecontent was99.0%.Resultsshowthattemperature wasthemainaffectingfactor.Keywords:oximido-acetophenone;synthesis;optimumoperations; orthogonaltest肟基苯乙酮是一种重要的农药中间体,可以用来合成肟酯类化合物[1,2]。

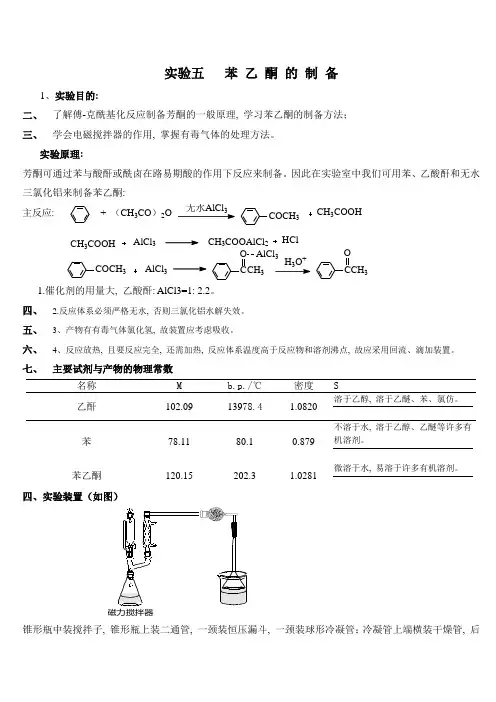
实验五 苯 乙 酮 的 制 备1、实验目的:二、 了解傅-克酰基化反应制备芳酮的一般原理, 学习苯乙酮的制备方法; 三、 学会电磁搅拌器的作用, 掌握有毒气体的处理方法。
实验原理:芳酮可通过苯与酸酐或酰卤在路易期酸的作用下反应来制备。
因此在实验室中我们可用苯、乙酸酐和无水三氯化铝来制备苯乙酮:主反应: + (CH 3CO )2O3COCH 3CH 3COOHCOCH 3AlCl 3CH 3COOAlCl 2HClAlCl 3CH 3COOHCCH 3O AlCl 3H O +CCH 3O1.催化剂的用量大, 乙酸酐: AlCl3=1:2.2。
四、 2.反应体系必须严格无水, 否则三氯化铝水解失效。
五、 3、产物有有毒气体氯化氢, 故装置应考虑吸收。
六、 4、反应放热, 且要反应完全, 还需加热, 反应体系温度高于反应物和溶剂沸点, 故应采用回流、滴加装置。
七、 主要试剂与产物的物理常数名称 M b.p./℃ 密度 S乙酐 102.09 13978.4 1.0820 溶于乙醇, 溶于乙醚、苯、氯仿。
苯 78.11 80.1 0.879 不溶于水, 溶于乙醇、乙醚等许多有机溶剂。
苯乙酮120.15202.31.0281微溶于水, 易溶于许多有机溶剂。
四、实验装置(如图)锥形瓶中装搅拌子, 锥形瓶上装二通管, 一颈装恒压漏斗, 一颈装球形冷凝管;冷凝管上端横装干燥管, 后装长颈漏斗, 用碱液吸收。
五、操作步骤向装有恒压滴液漏斗、电磁加热搅拌器和回流冷凝管(上端通过一氯化钙干燥管与氯化氢气体吸收装置相连)的50 mL三颈(或二颈)烧瓶中迅速加入研细的6.0g无水三氯化铝和8.0mL无水苯。
在电磁搅拌下自滴液漏斗慢慢滴加2 mL乙酐(加2 mL苯稀释), 开始少加几滴, 待反应发生后再继续滴加, 切勿使反应过于激烈, 滴加速度以烧瓶稍热为宜。
加完后(约需10~15min), 待反应速度稍缓和后, 水浴加热回流, 直到不再有氯化氢气体逸出为止。

苯乙酮生产原材料
苯乙酮是一种重要的化工原料,被广泛用于制造染料、香料、农药等精细化学品。
生产苯乙酮需要使用多种原材料,其中包括:
苯胺:苯胺是生产苯乙酮的主要原料之一,它可以通过化学合成或生物转化等方法获得。
乙醛:乙醛是生产苯乙酮的中间体之一,它可以由石油裂解气或其他来源获得。
硫酸:硫酸是生产苯乙酮过程中必不可少的催化剂和氧化剂,可以由硫磺制酸或间接法合成得到。
其他辅助材料:在生产苯乙酮的过程中,还需要使用一些其他辅助材料,如甲苯、丙酮等有机溶剂,以及三氯化铝、四氯化锡等催化剂。
这些原材料都是经过严格筛选和处理的,以确保其质量和纯度符合生产要求。
同时,在生产过程中也需要严格控制工艺条件和操作规程,确保产品的质量和安全性。
总之,苯乙酮的生产过程涉及到多个环节和复杂的化学反应,需要使用多种原材料和催化剂。
只有掌握了正确的原材料选择和使用方法,才能保证生产的稳定性和可靠性,从而满足市场需求并提高企业的竞争力。

苯乙酮的制备一、工作目标1.学习实验室中利用Friedel-Crafts酰基化法制备苯乙酮的原理与方法。
2.掌握带有机械搅拌和气体吸收的加热回流装置的操作方法。
3.掌握带干燥管和吸收有害气体的回流装置使用4.掌握终点监控的方法原理5.掌握有机液体的干燥及高沸点化合物的蒸馏6.掌握使用分液漏斗洗涤和分离液体有机物的操作技术二、工作内容1.解读方案,并确定初步方案2.列出准备单(仪器、试剂以及相关溶液的配制)3.进行试验1)带干燥管和吸收有害气体回流装置的搭建2)物料的投放3)水浴回流装置的搭建4)反应一段时间,进行反应终点的监控5)粗产物的干燥(有机液体的分离与干燥)6)粗产物的蒸馏提纯7)空气冷凝的装置的搭建4.对馏出物进行称重5.结束工作(装置的拆除、清洗、归还)6.数据的处理与总结7.计算产率并撰写报告三、工作进程与安排四、苯乙酮合成准备单1.试剂:2.仪器:五、 苯乙酮的合成原理芳酮一般通过辅克反应来制备,该反应在无水三氯化铝存在下由酰氯或酸酐与芳烃反应得到高产率的芳酮。
本实验以乙酸酐为酰化试剂,与苯发生乙酰化反应制备苯乙酮,其中苯既是反应物,又作为反应溶剂,可用下列反应式表示:+CH 3COCCH 3O O无水 AlCl 3CCH 3O+ CH 3COOH具体反应过程:CH 3C O O CCH 3O+ AlCl 3CH 3C O O CCH 3O AlCl 3AlCl 3(红色溶液)CCH 3O AlCl 3+ H 2O CCH 3O+ Al(OH)Cl 2 + HCl白(放热)CH 3COO AlCl 2 + H 2O Al(OH)Cl 2 + CH 3COOH (放热)Al(OH)Cl 2 + HCl AlCl 3 + H 2O 六、苯乙酮合成工作步骤1. 在250mL 三口烧瓶中,分别安装搅拌器,滴液漏斗及球形冷凝管。
在冷凝管上端装上氯化钙[1]干燥管,并连接气体吸收装置[2],用水做吸收液。

3,4-二甲基苯乙酮肟的合成思考题
3,4-二甲基苯乙酮肟可以通过以下合成路径得到:
1. 首先,合成3,4-二甲基苯乙酮。
这可以通过乙基苯与2-丁烯酸经碱催化酯化反应得到。
乙基苯 + 2-丁烯酸→ 3,4 -二甲基苯乙酮
2. 然后,将3,4-二甲基苯乙酮与羟胺反应,生成3,4-二甲基苯
乙酮肟。
3,4-二甲基苯乙酮 + 羟胺→ 3,4-二甲基苯乙酮肟
请注意,这只是一个合成路径的示例,实际的合成可根据实验条件和反应物的可用性进行调整和优化。
如果我从前一个回答的第二步继续,我可以提供以下合成路线:
3. 将3,4-二甲基苯乙酮肟与邻硝基苯甲酰氯反应,生成3,4-二
甲基-N-(2-硝基苯基)苯乙酮肼。
3,4-二甲基苯乙酮肟 + 邻硝基苯甲酰氯→ 3,4-二甲基-N-(2-硝
基苯基)苯乙酮肼
4. 最后,将3,4-二甲基-N-(2-硝基苯基)苯乙酮肼还原,得到最
终的产物3,4-二甲基苯乙酮肟。
3,4-二甲基-N-(2-硝基苯基)苯乙酮肼 + 还原剂→ 3,4-二甲基苯
乙酮肟
相同地,这只是一个合成路径的示例。
在实际合成中,可能需要考虑选择不同的反应条件和试剂,并进行优化和调整。

苯乙酮肟结构
苯乙酮肟(氧苯乙酮),又称卡尔马克思肟,因20世纪30年代的瑞士气体设备制造
商卡尔·马克思而获得其命名,是一种芳香族单元。
它可以用来调节汽车燃料混合分析,
硝基溴苯醇,脲醛橙,甲苯,二甲苯等的指session应用,也可以作为一种溶剂使用。
苯乙酮肟的化学结构是C5H5NO,它是一种芳香烃的二甲基开环醛,具有强烈的鼠李味,熔点约为-80℃,耐热性和耐气候性很好。
苯乙酮肟通常制备方法有N-氧化酰胺法,氨氧化法和卤素加成法。
该物质的制备通常需要氯乙烯和氨(可直接从氯化钠中提取),最后由多组分反应所形成,最终形成苯乙酮肟。
苯乙酮肟在实际使用中被人们称为“硝基汽油”,被用作燃料,以延长汽油燃烧时间
并防止积碳的产生。
它也可以用于除脱柴油机的积碳,以及用于合成芳香族产品,如芳香酮,砜烯,丙醇和羟基本烷化合物。
苯乙酮肟也涉及药物开发,该物质可用于治疗肝性脑病,耐多药性抗生素耐药菌,肺癌,DC未特异性结节病,sjogren综合征和艾滋病抗体病病毒感染等疾病。
苯乙酮肟还可以用于化妆品和个人护理用品中,з作为抗菌剂,也可以用来清洁水处理系统中的微生物。
此外,它还可用于消毒药物和农药中,用于防止腐败,抵抗病菌,虫
害和真菌等。
苯乙酮肟作为乙醇混合物的组分,在风险评估过程中显示出中等毒性,但它被认为是
不可接受的污染物。
它也可以用在医用和工业产品中,但如果用量超过规定的上限,则可
能对人体有害。
因此,在使用苯乙酮肟时应当十分小心,以确保不超出其规定的上限。

【精品】苯乙酮的制备
苯乙酮是一种重要的化学品,广泛应用于香精、药品、农药等行业中。
本文将介绍几
种制备苯乙酮的方法。
1. 酮化反应法
酮化反应法是苯乙酮制备的重要方法之一,反应条件简单,易于控制,适用于大规模
工业生产。
酮化反应一般用苯和乙酸为原料,催化剂为硫酸或磷酸。
反应物质比例要求苯
和乙酸之间的摩尔比为1:1.5-2。
反应温度为150℃左右,反应时间为4-5小时。
反应产物经过蒸馏分离,得到纯苯乙酮。
不同生产厂家的分离方法略有不同,但大多
采用水蒸汽蒸馏法进行分离。
将反应物加入至反应釜,升温至160℃-175℃,经过蒸馏分离,得到苯乙酮和副产物乙酸酯。
经过多级分离、净化,最终得到纯苯乙酮。
总之,以上几种方法都适用于苯乙酮的制备。
其中,酮化反应法应用最为广泛,适用
于大规模工业制备;氧化反应法适用于小规模实验室制备;而醇解反应法则原料价格低廉,能够实现大规模工业生产,成本低。
一、实验目的1. 学习肟的制备方法。
2. 掌握实验室基本操作技能。
3. 熟悉有机合成实验的步骤和注意事项。
二、实验原理肟(Hydrazine)是一种重要的有机化合物,具有多种用途,如用作还原剂、合成中间体等。
本实验采用苯肼与醛或酮在酸性条件下反应制备肟。
反应方程式如下:R-CHO + NH2-C6H4-NH2 → R-CH=N-NH-C6H4-NH2 + H2O三、实验仪器与试剂1. 仪器:锥形瓶、烧杯、玻璃棒、滴管、酒精灯、冷凝管、干燥管、温度计等。
2. 试剂:苯肼、无水乙醇、醛或酮、浓硫酸、氢氧化钠、蒸馏水等。
四、实验步骤1. 准备工作(1)将苯肼溶解于无水乙醇中,配制成苯肼溶液。
(2)将醛或酮溶解于无水乙醇中,配制成醛或酮溶液。
(3)将浓硫酸溶解于蒸馏水中,配制成浓硫酸溶液。
2. 实验操作(1)将苯肼溶液倒入锥形瓶中。
(2)加入适量的醛或酮溶液,搅拌均匀。
(3)缓慢滴加浓硫酸溶液,边加边搅拌,控制反应温度在40-50℃。
(4)反应一段时间后,观察反应液的颜色变化,待颜色变为深棕色时,停止加热。
(5)将反应液倒入烧杯中,用冰水冷却。
(6)向冷却后的反应液中加入氢氧化钠溶液,调节pH值至中性。
(7)过滤,收集滤液。
(8)将滤液倒入锥形瓶中,加入适量的氢氧化钠溶液,加热回流。
(9)冷却后,用稀盐酸调节pH值至中性。
(10)过滤,收集滤液。
(11)将滤液倒入烧杯中,加入适量的无水乙醇,加热蒸发至浓缩。
(12)冷却结晶,收集固体产物。
五、实验结果与分析1. 通过实验,成功制备了肟。
2. 实验过程中,注意控制反应温度和pH值,以确保反应顺利进行。
3. 反应液颜色变化可作为反应进行的参考。
六、实验总结1. 本实验成功制备了肟,掌握了实验室基本操作技能。
2. 在实验过程中,注意安全操作,防止意外事故发生。
3. 实验结果符合预期,达到了实验目的。
七、实验注意事项1. 实验过程中,注意保持实验环境整洁,防止交叉污染。
对羟基苯乙酮氨肟化制备对羟基苯乙酮肟王洪波;李皓凌;程时标;傅送保;任欣【期刊名称】《精细化工》【年(卷),期】2006(23)3【摘要】考察了在HTS-1分子筛催化剂上对羟基苯乙酮(简写为4-HAP)在固定床反应器中与氨和过氧化氢发生氨肟化反应合成对羟基苯乙酮肟(简写为4-HAPO)的反应规律,4-HAP氨肟化反应的适宜条件为:以乙醇为溶剂、温度高于60℃、反应时间大于5 h、4-HAP宜一次性加入、氨和过氧化氢连续加入、催化剂的质量分数为w(HTS-1)=1.4%、n(NH3)∶n(H2O2)∶n(4-HAP)=4.2∶1.1∶1、n(溶剂)∶n(4-HAP)=6∶1,4-HAP转化率达到73.9%,4-HAPO选择性达到98.9%,该结果优于类似条件下US 5 466 869报道的结果。
通过色质联用分析鉴定了4-HAP 氨肟化反应的产物,与现有的文献报道相比,HTS-1分子筛具有较高的活性和选择性,副产物的种类和数量均较少。
4-HAP氨肟化反应过程中产生的副产物主要为1,8,9-蒽三酚(THA)和对苯二酚(HQ)。
适当提高反应温度和催化剂浓度、提高氨与4-HAP的比例、控制过氧化氢与4-HAP在适当的摩尔比(如1.1∶1),可抑制这两种副产物的生成。
HQ和1,8,9-蒽三酚在氨存在下发生氧化反应是反应产物颜色变深的原因。
【总页数】5页(P302-306)【关键词】对羟基苯乙酮;对羟基苯乙酮肟;氨肟化;对乙酰氨基酚【作者】王洪波;李皓凌;程时标;傅送保;任欣【作者单位】中石化股份有限公司巴陵分公司;中石化股份有限公司石油化工科学研究院【正文语种】中文【中图分类】TQ612.9【相关文献】1.2-羟基-5-特辛基苯乙酮肟的合成及表征 [J], 肖友军;贺燕华;陈建钗2.2-羟基-5-特辛基苯乙酮肟的合成及表征 [J], 肖友军;贺燕华;陈建钗;3.MCM-41负载对羟基苯乙酮肟环钯催化剂的制备及催化Suzuki反应的研究 [J], 张井峰;白雪峰4.2-乙基己酸在2-羟基-5-壬基苯乙酮肟化过程中的相转移催化作用 [J], 王慧;许磊;李效军5.4-羟基-3-甲氧基苯乙酮肟环钯配合物催化Suzuki偶联反应的研究 [J], 张井峰;白雪峰因版权原因,仅展示原文概要,查看原文内容请购买。
苯乙酮肟化学结构其化学结构式为:
苯乙酮肟是一种化学物质,分子式是:C8H9NO。
【分子结构】
1、摩尔折射率:40.58
2、摩尔体积(m3/mol):133.7
3、等张比容(90.2K):326.3
4、表面张力(dyne/cm):35.4
5、极化率(10 -24cm 3):16.08
【物性数据】
1. 性状:无色针状结晶。
能随水蒸气挥发。
2. 密度(g/mL,25/4℃):1.11g/ml
3. 相对蒸汽密度(g/mL,空气=1):未确定
4. 熔点(ºC):60
5. 沸点(ºC):245
6. 沸点(ºC,5.2kPa):未确定
7. 折射率:1.539
8. 闪点(ºC):118
9. 比旋光度(º):未确定
10. 自燃点或引燃温度(ºC):未确定
11. 蒸气压(kPa,25ºC):未确定
12. 饱和蒸气压(kPa,60ºC):未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC):未确定
15. 临界压力(KPa):未确定
16. 油水(辛醇/水)分配系数的对数值:未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V):未确定
19. 溶解性:溶于乙醇、丙酮、乙醚、氯仿和石油英混溶,微溶于水。
对羟基苯乙酮肟的制备对乙酰氨基酚实验
报告
一、目的要求:
1、了解对氨基酚的氨基的选择性乙酰化而保留酚羟基的方法。
2、掌握易被氧化产品的重结晶精制方法。
3、进一步认识和掌握显微熔点测定仪的工作原理和操作方法,并利用其测定产品熔点。
二、基本原理:
用计算量的醋酐与对氨基酚在水中反应,可迅速完成N-乙酰化而保留酚羟基。
反应式:副反应:
七、思考题:试比较冰醋酸、醋酐、乙酰氯三种乙酰化剂的优缺点。
答:醋酸:优点是冰醋酸易得,不与被提纯物质发生化学反应,易与结晶分离除去,能给出较好的结晶。
缺点是活性没有醋酐乙酰氯强,与反应物生成的水分子抑.制了反应的进行程度,所表现出的活性太低。
醋酐:醋酸酐容易断键,反应较快,醋上的碳基被酯健活化有强亲电性,可以和氨基形成酰氨键,一定程度上避免了对氨基苯磺酰胺副产物的产生。
缺点是气味强价格贵,反应速率和转化率任不及乙酰氯,产物有乙酸单体,比起乙酰氯产物氯化氢来说分离提纯相对困难。