第9章烷基化反应
- 格式:ppt
- 大小:1.26 MB
- 文档页数:98


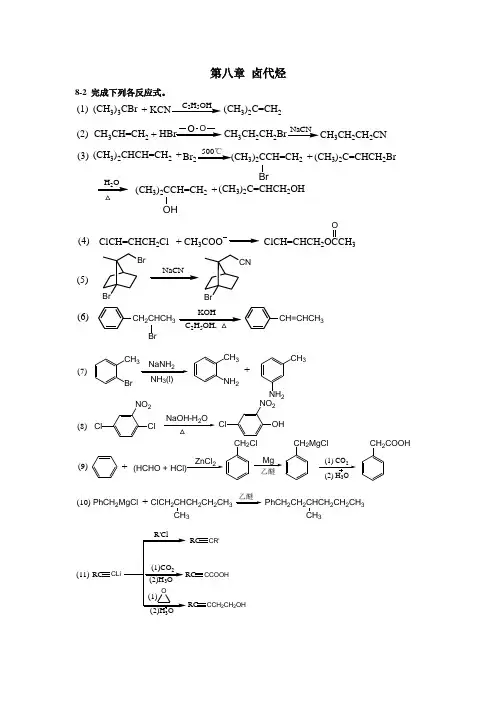
第八章 卤代烃8-2 完成下列各反应式。
(CH 3)3CBr C 2H 5OH(CH 3)2C=CH 2+CH 3CH=CH 2HBr+O OCH 3CH 2CH 2CH 3CH 2CH 2CNNaCN(1)(2)(CH 3)2CHCH=CH 2Br +500℃(CH 3)2CCH=CH 2BrH 2O (CH 3)2C=CHCH 2Br+(CH 3)2CCH=CH 2OH(CH 3)2C=CHCH 2OH+(3)NaCNKOH 25(4)(5)(6)ClCH=CHCH 2Cl CH 3+ClCH=CHCH 2OCCH 3OBrBrBrCNCH 2CHCH 3Br CH=CHCH 3CH 3Br2NH 3(l)CH 3NH 2CH 32+ClClNO 22OHClNO 2ZnCl 2(HCHO + HCl)+CH 2ClMgCH 2MgClCH 2COOHClCH 2CHCH 2CH 2CH 3PhCH 2MgCl 3+PhCH 2CH 2CHCH 2CH 2CH 33(7)(8)(9)(10)3RC CLi(11)RCCR'RC CCOOHRC CCH 2CH 2OHCHBr3BrBr(12)8-3 写出下列反应主要产物的构型式。
C2H5CH3NaI+C2H5CH3NaINaSCH3+(S N2)(S N2)(S N2)CH3ICH2(CH2)4CH3HH2OCH3H2(CH2)4CH3HOCBrBrCH2CH2CH3CCH2CH32Lindar催化剂CHCCH2CH2CH3H(1)(2)(3)(4)3KOH253H3t-BuOKt-BuOH, △H3Ph PhC6H5H3C HC6H5H BrC6H5H C6H5CH32525Br(H3C)2HCCH3(H3C)2HCCH3CH3H Br2CH3H BrC2H5CH325Znt-BuOKt-BuOH, △(E2反式消除)(E2反式消除)(E2反式消除)(顺式消除)(E2反式消除,但很慢)(5)(6)(7)(8)(9)8-6 把下列各组化合物按发生S N1反应的活性排列成序。




第九章 卤代烃教学要点:1.介绍了卤代烃的分类及同分异构现象、卤代烃的命名、卤代烷的结构和物理性 质、化学性质、制备方法。
2.介绍了一卤代烷的取代反应、消去反应(查依采夫规则)、还原反应。
几种常见 的有机金属化合物。
3.介绍了S N 1和S N 2反应历程、碳正离子的生成、结构、不同结构碳正离子的相对稳定性。
4.一卤代烯烃和一卤代芳烃的分类、物理性质、化学性质、有机氟化合物的特性、有机氟化合物的应用。
本章重点:卤代烷的结构,卤代烷的化学反应,亲核取代反应的机理,一卤代烯烃和一卤代芳烃,卤代烃的制备方法,几种常见的有机金属化合物。
本章难点:卤代烷的化学反应,亲核取代反应的机理。
考核要求:识记:卤代烷的命名,一卤代烷的结构。
领会:亲核取代反应的机理。
综合分析:SN1和SN2反应立体化学及影响因素。
熟练应用:一卤代烷的化学反应,卤代烃的制备方法,几种常见的有机金属化合物。
教学时数:6学时 教学内容:第一节 卤代烃的分类、命名及同分异构现象;第二节 卤代烃;第三节 亲核取代反应历程;第四节 一卤代烯烃和一卤代芳烃;第五节 卤代烃的制法; 第六节 重要的卤代烃;第七节 有机氟化合物;第二十四次课 (第47~48学时)卤代烃可以看作是烃分子中一个或多个氢原子被卤原子取代后所生成的化合物。
卤原子是卤代烃的官能团。
常所说的卤代烃是指氯代烃、溴代烃和碘代烃。
而氟代烃的性质和制法都较为特殊。
一卤代烃的性质比较活泼,能发生多种化学反应转化成各种其他类型的化合物。
所以卤代烃是重要的合成中间产物。
第一节 卤代烃的分类、同分异构和命名一、分类 二、命名 三、同分异构现象一、分类卤代烃氟代烃碘代烃溴代烃氯代烃一卤代烃多卤代烃根据卤代烃分子中所含卤原子的数目:根据卤代烃分子中所含卤原子的种类:根据卤代烃分子中烃基的类型:饱和卤代烃不饱和卤代烃芳香族卤代烃根据和卤原子直接相连的碳原子类型:一级卤代烃(伯卤代烃) R -CH 2-X 10-X 二级卤代烃(仲卤代烃) R 2CH-X 20-X 三级卤代烃(叔卤代烃) R 3C-X 30-X二、命名 1.简单的卤代烃,按卤原子相连的烃基的名称来命名,称为卤代某烃或某基卤。
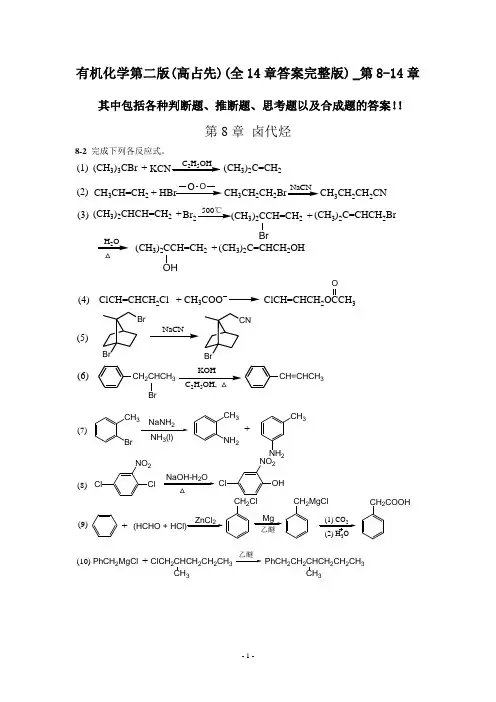
有机化学第二版(高占先)(全14章答案完整版) _第8-14章其中包括各种判断题、推断题、思考题以及合成题的答案!!第8章 卤代烃8-2 完成下列各反应式。
(CH 3)3CBr C 2H 5OH(CH 3)2C=CH 2+CH 3CH=CH 2HBr+O OCH 3CH 2CH 2CH 3CH 2CH 2CNNaCN(1)(2)(CH 3)2CHCH=CH 2Br +500℃(CH 3)2CCH=CH 2BrH 2O (CH 3)2C=CHCH 2Br+(CH 3)2CCH=CH 2OH(CH 3)2C=CHCH 2OH+(3)NaCNKOH 25(4)(5)(6)ClCH=CHCH 2Cl CH 3+ClCH=CHCH 23OBrBrBrCNCH 2CHCH 3Br CH=CHCH 3CH 3Br2NH 3(l)CH 3NH 2CH 3NH 2+ClClNO 2NaOH-H 2OOHClNO 2ZnCl 2(HCHO + HCl)+CH 2ClMgCH 2MgClCH 2COOHClCH 2CHCH 2CH 2CH 3PhCH 2MgCl CH 3+PhCH 2CH 2CHCH 2CH 2CH 3CH3(7)(8)(9)(10)3RC CLi (11)RC CR'RC CCOOHRC CCH2CH2OH CHBr350%NaOH(aq)BrBr(12)8-3写出下列反应主要产物的构型式。
C2H5CH3NaI+C2H5CH3NaSCH3+(S N2)(S N2)(S N2)CH3ICH2(CH2)4CH3HH2OCH3HCH2(CH2)4CH3HOCBrBrCH2CH2CH3CCH2CH3H2Lindar催化剂C CCH2CH2CH3H(1)(2)(3)(4)3KOH253H3t-BuOKt-BuOH, △H3CPh PhHC6H5H3C H6H5H BrC6H5H C6H5CH32525Br(H3C)2HCCH3(H3C)2HCCH3CH3H BrCH2CH3H BrC2H5CH325Znt-BuOK(E2反式消除)(E2反式消除)(E2反式消除)(顺式消除)(E2反式消除,但很慢)(5)(6)(7)(8)(9)8-4比较下列每对亲核取代反应,哪一个更快,为什么?(1)B>A (亲核性C2H5O->C2H5OH)(2)A>B (烯丙型卤代烃活泼)(3)B>A (极性非质子溶剂有利于S N2反应)(4)A>B (亲核性-SH>-OH)(5)A>B (亲核性硫比氮强)(6)B>A (离去能力I->Cl-)8-5卤代烷与NaOH在H2O-C2H5OH溶液中进行反应,指出哪些是S N2机理的特点,哪些是S N1机理的特点?(1)产物发生Walden转化;S N2(2)增加溶剂的含水量反应明显加快;S N1(3)有重排反应产物;S N1(4)反应速率明显地与试剂的亲核性有关;S N2(5)反应速率与离去基的性质有关;S N2和S N1(6)叔卤代烷反应速度大于仲卤代烷。

----------------------- Page 1-----------------------文件编码:CHRP-104-PE-OI-0001-2011烷基化装置操作规程版本/状态:B/1分发号:中海石油炼化有限责任公司惠州炼油分公司----------------------- Page 2-----------------------2011年01月01日发布2011月01日实施编写签字表名称签字时间编写人审校人审核人----------------------- Page 3-----------------------专业会审表单位专业名称签字时间技术中技术专业心质量专业指挥中心调度专业动设备专业设备中静设备专业心仪表专业电气专业安全专业HSE中环保专业心消防专业职业卫生专业--------------------- Page 4-----------------------审核签字表中心领导签字时间技术中心经理设备中心经理HSE中心经理批准签字表公司领导签字时间总工程师目录第一章工艺技术规程3第一节设计依据第二节装置概况、特点及工艺原理第三节工艺流程说明第四节工艺指标第五节原材料指标第六节半成品、成品主要性质指标第七节公用工程(水、电、汽、风等)指标第八节主要操作条件及质量指标详见第十二节第九节原材料、公用工程消耗、能耗计算指标和节能措施.第十节物料平衡第十一节主要设备选择及工艺计算汇总第十二节生产控制化验分析第十三节装置内外关系第二章岗位操作法54第一节烷基化装置操作原则第二节预加氢系统操作法第三节烷基化反应系统操作法第四节致冷系统操作法第五节分馏系统操作法第三章岗位开停工规程86第一节开工规程第二节停工规程第四章设备操作规程164第一节大型专用设备操作规程第二节基础设备操作规程第五章事故处理191第一节事故处理原则第二节紧急停工方法第三节事故处理预案第四节事故处理预案演练规定第六章仪表控制系统操作法231第一节仪表控制系统概况及操作第二节工艺操作仪表控制回路说明第四节仪表投用、停用及注意事项第七章操作规定325第一节定期工作规定第二节操作规定第八章安全生产及环境保护330第一节安全知识第二节安全规定第三节烷基化装置防风防台措施第四节同类装置典型事故分析、处理方法及经验教训.第五节烷基化装置易燃易爆物质的安全性质第六节本装置主要有害物质的性质第七节装置污染物主要排放部位和排放的主要污染物.第八节消防器材、设施使用方法及消防规定第九节职业卫生九章附录366 附表一主要设备明细表附表二主要设备结构图附表三装置平面分布图附表四可燃气体报警仪布置图附表五装置消防设施布置图附表六控制参数报警值附表七安全阀定压值附录八工艺流程简图附表九开工统筹图附录十停工统筹图----------------------- Page 7-----------------------惠炼16万吨/年烷基化装置操作规程第3 页共397 页第一章工艺技术规程第一节设计依据1中国海洋石油总公司惠州炼油项目管理项目组关于“惠州炼油项目基础设计工作”的委托书(2005年6月16日);2中国石化工程建设公司与中国海洋石油总公司签订的关于开展“中国海洋石油总公司惠州炼油项目基础设计”的合同和合同附件;3 DUPONT公司提供的硫酸烷基化工艺包;4中国海洋石油总公司惠州炼油项目设计统一规定;5上游MTBE、加氢裂化装置提供的原料液化气量及组成;6中国石化工程建设公司与中国海洋石油总公司召开的PFD、PID等审查会会议纪要。

第九章 烷基化第一节 概述一、烷基化反应及其重要性1.定义:烷基化反应是指向有机化合物分子中的碳、氮,氧等原子上引入烃基增长碳链(包括烷基、烯基、炔基、芳基等)的反应,其中以引入烷基最为重要。
2.可发生烷基化反应的有机物:芳烃、活泼亚甲基化合物、胺类等。
3.烷基化试剂种类:卤烷、烯烃、醇及醚类、硫酸酯、醛和酮,环氧化物等。
4.催化剂种类 ⎩⎨⎧等、质子酸等、、路易斯酸42323SO H HF BF ZnCl FeCl5.研究作用:可以合成塑料、医药、溶剂、合成洗涤剂、药物、染料、香料、催化剂、表面活性剂等功能产品。
如通过O -烷基化可制得聚乙二醇型非离子表面活性剂。
通过N -烷基化合成的季铵盐是重要的阳离子表面活性剂、相转移催化剂、杀菌剂等。
二、烷基化反应的类型⎪⎩⎪⎨⎧---生成醚类化合中的氧原子上引入烷烷基化反应:向醇、酚生成伯、仲、中的氮原子上引入烷烷基化反应:向氨或胺烷基生成烷基作用下向芳环碳上引烷基化反应:在催化剂O N C 1.C -烷基化反应如烷基苯的制备反应:+R C l3R +H C l2.N -烷基化反应如N,N -二甲基苯胺的制备反应:N H 2+C H 3O H 2H 2S O 4N (C H 3)2+2O H 23.O -烷基化反应如壬基酚聚氧乙烯醚的制备反应:O H C 9H 19+OC H 2C H 2O C H 2C H 2O H C 9H 19OC H 2C H 2n O (C H 2C H 2)C 9H 19nC H 2C H 2O H第二节 烷基化反应的基本原理一、芳环上的C -烷基化反应芳环上的C -烷基化是在催化剂作用下直接向芳环碳原子上引入烷基的反应,也称为Friedel -Cartfts 反应。
利用这类烷基化反应可以合成一系列烷基取代芳烃。
1.烷化剂主要有卤烷、烯烃和醇类,以及醛、酮类。
(1) 卤烷卤烷(R -X )是常用的活性较强的烷化剂。

一.羰基化合物的α-烷基化(芳基化)反应1.1 手性底物或辅助基团诱导的不对称烷基化反应(1) 金属配位型手性辅基传递---螯合的手性诱导从Evans试剂出发可以合成各种烷基酸和相应的化合物试剂)缺点是:制备困难,价格较高。
手性辅基切除困难∙以手性肼为为辅助基,生成腙手性腙体系∙与手性胺辅基不同,没有生成金属-烯胺,而是直接金属化(d) 手性磺内酰胺体系亲电试剂从氮原子的孤对电子方向相反的Re MLn R”X(3)“手性记忆”又称:“手性中心的自我再生”手性季碳原子的构建是有机合成化学中的难点之一∙利用不对称烷基化反应构筑手性季碳中心Seebach, Angew , 1996,35,2708∙“手性记忆”策略的应用base: LiHMDSJACS ,2013,13294Up to 99%ee♣不对称α-芳基化反应(芳基重排)构筑手性季碳中心手性配体(L*)1.2. 试剂控制的不对称α-烷基化反应∙手性锂试剂及手性胺配体的应用添加剂无手性配体:产率:<1%, 86%回收原料20 mol% L*: 产率:1%,(52%ee )20 mol% L* + 乙二胺:产率:83%,92% eeF idi 会使催化剂中毒∙Ni 催化的吡啶鎓离子的芳基化反应Doyle Angew ,2013,9153∙Free pyridine 会使催化剂中毒。
∙选择4-methoxypyridine 是因为在低温下,可以与氯甲酸酯成盐。
∙在Nigishi 反应中,第一次以Ni 活化亚胺离子,并高对映选择性地生成C-C 键。
Proposed mechanismMX n2.2 手性辅基的Michael 加成反应举例:格氏试剂为亲核试剂(2) 有机硼试剂的共轭加成反应COOEt COOEtPh+PhB(OH)2Rh(acac)(C 2H 4)2(S)-BINAP100o C, 1,4-dioxane/H 2O>99%, 90% eeOORh(acac)(C 2H 4)2(S)-BINAP BINAP-Rh 催化剂(S)BINAP+∙手性sulfuro-olefin 配体-Rh 催化剂Du, OL ,2011, 3300Sulfer 和olefin 与Rh 的配位被1HNMR 和络合物单晶分析证明。
化学工艺学课后答案【篇一:化学工艺学复习题及答案】、氧化还原、加氢-醇、酸、脂和芳烃等:①经转化先制成合成气,或含氢很高的合成氨原料气,然后进分氧化制乙炔;③直接制造化工产品,如制造炭黑、氢氰酸、各。
c3、c4和中等大小的分子居多②异构化、芳构化、环烷化,使裂解产物中异,使催化汽油中容易聚合的二烯烃类大为减少④聚合、缩合反应.-气化-液化;热解-气化-发电;气化-合成-燃料;液化-燃料-气化;液化-加氢气化、丁二烯和r-ch2-ch3←→r-ch=ch2+h2;断链反应:r-ch2-ch2-r’→ r-ch2=ch2+r’hc-h键能大于c-c键能,固断链比脱氢容易②烷烃的相对稳定性随碳c-h键或c-c键,较直链的键能小⑤低分子烷烃的c-c键在c4以上烯烃、单环芳烃h缩合反应。
芳烃的一次反应中,芳烃经脱氢缩合转化为稠环芳成单烯烃的反应;芳烃:无烷基的芳烃基本上不易裂解为烯烃,有烷基的芳烃,主要是烷基发生断和脱氢反应,芳环不开裂,可脱氢缩合为多环芳烃,芳烃直至转化为焦。
烯烃加氢转化为烷烃,脱氢变为二烯烃或炔烃;芳烃经脱氢缩合转化为稠环芳烃进一步转化为焦;烷烃会进一步裂解成低级烷烃,——pona值;适于表征石脑油、轻柴油等轻质馏分油;烷烃(paraffin)烯烃(olefin)环烷烃(naphthene);芳烃(aromatics) ;72.3、16.3、11,大庆石脑油则为53、43、425左右,:750-900℃,原料分子量越小,所需裂解温度越高,乙烷生成,所得裂解汽油的收率相对较低,使炔烃收率明显增加.③压力对裂解反应的影响,从化学平衡角度分析(压力只对脱氢反应有影响)对一次反应:,结论:低压有利于乙烯的生产.18题。
-101℃(高压法),使乙炔以上烷烃和烯烃冷凝为液体,与甲烷和氢气分开,c4馏分分开,从而得到聚合级高纯乙烯和聚合级高纯丙烯。
(lummus)按c1、c3加氢→丙烯塔→脱丁烷。
②前脱乙烷流程(linde法);压缩→脱乙烷→加氢→脱甲烷→乙烯塔→脱丙烷→丙烯塔→脱丁烷③前脱丙烷流程(三菱油化法),压缩→脱丙烷→脱丁烷→压缩→加氢→脱甲c4烃较多的裂解:急冷锅炉废热锅炉,用换热器h2s、co2)、少量水分、炔烃、酸性气体:不仅会腐蚀设备和管路,而且还会是脱炔催化剂中毒;水分和co2在低温下结冰,堵塞管路;乙炔和丙乙炔的存在不仅使高纯乙醇和丙烯聚合时采用的催化剂中毒,而且还会在系统里自聚,生成液体产物绿油。
环氧乙烷烷基化反应
烷基化反应的机理通常涉及环氧乙烷分子中的亲电环开反应。
在碱性条件下,碱性催化剂(如氢氧化钠或氢氧化钾)可以促进环氧乙烷分子的开环,生成烷基离子。
这些烷基离子随后可以攻击其他环氧乙烷分子,形成烷基环氧乙烷产物。
这种反应通常需要适当的温度和压力条件来促进反应的进行。
从应用角度来看,环氧乙烷烷基化反应在化工行业中具有广泛的应用。
例如,烷基环氧乙烷可以用作溶剂,用于涂料、油墨和粘合剂的生产。
此外,它们还可以用作表面活性剂,用于制备洗涤剂和乳化剂。
在化工生产中,烷基化反应的选择催化剂、反应条件和生产工艺对产物的纯度和产率都有重要影响。
总的来说,环氧乙烷烷基化反应是一种重要的有机合成反应,具有广泛的应用前景和研究价值。
通过深入研究反应机理和优化反应条件,可以进一步提高产物的质量和产率,促进其在工业生产中的应用。