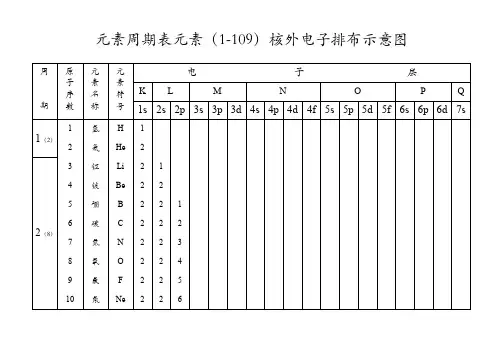
核外电子排布-元素周期表
- 格式:ppt
- 大小:2.11 MB
- 文档页数:22


原子核外电子排布与元素周期律一、原子结构(Z 个)原子核注意:(N 个) 质量数(A)=质子数(Z)+中子数(N)1.X 原子序数= = =核外电子(Z 个)2.原子核外电子的排布规律:①电子总是尽先排布在能量 的电子层里;②各电子层最多容纳的电子数是 ;③最外层电子数不超过 个(K 层为最外层不超过 个),次外层不超过 个,倒数第三层电子数不超过 个。
电子层: 一(能量最低) 二 三 四 五 六 七 对应表示符号: 3.元素、核素、同位素元素: 。
核素: 。
同位素: 。
(对于原子来说) 二、元素周期表 1.编排原则:①按 递增的顺序从左到右排列 ②将 相同..的各元素从左到右排成一横行..。
(周期序数=原子的电子层数) ③把 相同..的元素按电子层数递增的顺序从上到下排成一纵行..。
=原子最外层电子数 2.结构特点:核外电子层数 元素种类第一周期 种元素短周期 第二周期 种元素周期 第三周期 种元素元 (7个横行) 第四周期 种元素 素 (7个周期) 第五周期 种元素 周 长周期 第六周期 种元素 期 第七周期 未填满(已有 种元素) 表 主族:ⅠA ~ⅦA 共7个主族族 副族:ⅢB ~ⅦB 、ⅠB ~ⅡB ,共7个副族 (18个纵行) 第Ⅷ族: 纵行,位于 之间 (16个族) 零族: ① 主族(A ):由 和 元素共同组成的族(除第18纵列)列序与主族序数的关系② 副族(B ):完全由 元素组成的族(第8、9、10纵列除外)③ Ⅷ族:包括 三个纵列。
④ 0族:第 纵列,该族元素又称为 元素。
三、元素周期律1.元素周期律: 。
元素性质的周期性变化实质是... 。
族碱金属元素: ( 是金属性最强的元素,位于周期表 ) 第ⅦA 族卤族元素: ( 是非金属性最强的元素,位于周期表 ) ★判断元素金属性和非金属性强弱的方法:(1)金属性强(弱)——① ;② ;③ 。
(2)非金属性强(弱)——① ;② ;③ 。

促敦市安顿阳光实验学校第2课时核外电子排布与元素周期表、原子半径1.认识核外电子排布与元素周期表的关系,了解元素周期表中各区、周期、族的划分依据。
2.了解原子结构与原子半径周期性变化的联系。
核外电子排布与元素周期表1.核外电子排布与周期划分的本质联系(1)周期与能级组、原子轨道的对关系(2)规律①7个能级组对7个周期。
②周期序数=□1________________。
③本周期所包含元素种数=对能级组所含原子轨道数的2倍=对能级组最多容纳的电子数。
2.核外电子排布与族的划分(1)划分依据:取决于原子的□2________和价电子排布。
(2)规律①主族元素②过渡元素③稀有气体→价电子排布:□9______(□10________除外)3.元素周期表的分区(1)根据核外电子排布根据核外电子排布,可把周期表里的元素划分成5个区:s区、p区、d区、ds区和f区。
除ds区外,区的名称来自最后填入电子的能级的符号。
(2)根据元素金属性与非金属性4.金属元素与非金属元素在元素周期表中的位置(1)金属元素和非金属元素的线为沿B、Si、As、Te、At与Al、Ge、Sb、Po之间所画的一条连线,非金属性较强的元素处于元素周期表的右上角位置,金属性较强的元素处于元素周期表的左下角位置。
(2)处于d区、ds区和f区的元素是金属元素。
s区的元素除氢、氦外,也是金属元素。
自我校对:□1最外层电子所在轨道的主量子数□2价电子数目□3n s1~2□4n s2n p1~6周期序数对能级组原子轨道数最多容纳电子数价电子排布式元素种数ⅠA族0族1 1s 12 1s11s2 22 2s2p 4 8 2s12s22p683 3s3p4 8 3s13s23p684 4s3d4p 9 18 4s14s24p6185 5s4d5p 9 18 5s15s25p6186 6s4f5d6p 16 32 6s16s26p6327 7s5f6d7p 16 32 7s1-不完全□5价电子数□6(n-1)d1~10n s0~2□7价电子数□8n s电子数□9n s2n p6□10He 1.判断正误(1)元素周期表中每一周期主族元素最外层电子都是由1个逐渐增加到8个。


原子核外电子排布和元素周期律原子是由原子核和围绕核运动的电子组成的。
原子核由质子和中子组成,而质子的数量决定了原子的元素。
原子核外的电子以不同的方式排布,这种排布决定了元素的化学性质。
元素周期律描述了元素的周期性变化规律,是化学中最重要的概念之一原子核外电子排布是描述电子在原子中的位置和能量分布的方式。
根据量子力学理论,电子存在于不同的能级上,每个能级可以容纳一定数量的电子。
根据波尔模型,原子的外层电子称为价电子,也是化学反应中参与原子间相互作用的电子。
原子核外电子排布可以通过倒易电子构型的方式来表示。
倒易电子构型表示了一个元素最外层电子的分布情况。
在倒易电子构型中,外层电子被表示为和最接近核心的壳层相同的能级。
例如,石墨的原子核是由6个质子和6个中子组成的,其倒易电子构型为1s²2s²2p²。
这意味着石墨的最外层电子是在2p轨道上的。
在倒易电子构型中,电子的分布遵循普遍原则、泡利不相容原理和阜居规则。
普遍原则指出,电子首先填充能量最低的轨道。
泡利不相容原理指出,一个轨道上最多只能容纳两个电子,并且这两个电子的自旋方向必须相反。
阜居规则指出,当填充轨道时,电子会尽量选择不同的轨道来填充,以最小化库伦排斥力。
元素周期律是根据元素的原子核中质子的数量和原子核外电子的排布,将元素按照一定规律排列的表格。
最早的元素周期表是由门捷列夫于1869年提出的。
现代元素周期表按照亨利·莫西里夫在1913年提出的核电荷排列。
元素周期表按照原子序数的增加顺序列出了所有已知元素。
原子序数是指原子核中质子的数量,也是元素周期表中元素的核电荷。
元素周期表的每一行称为一个周期,原子序数在周期内逐渐增加。
元素周期表的每一列称为一个组,元素周期表中的元素按照相似的性质分布在同一组中。
元素周期表按照一定的规律排列,这些规律反映了元素的原子结构和化学性质的周期性变化。
最著名的周期性性质是元素的物理性质和化学性质的周期性变化。

原子核外电子排布和元素周期律首先,我们来了解一下原子的结构。
原子是由质子、中子和电子组成的。
质子和中子位于原子核中心,质子的电荷为正,中子的电荷为中性。
电子则围绕原子核的轨道上运动,电子的电荷为负。
原子核外电子排布描述了电子如何分布在原子的不同能级(轨道)上。
根据能级理论,电子可以处于不同的能级和亚能级上。
其中,第一能级最靠近原子核,能级数越高,离原子核越远。
每个能级最多容纳2n^2个电子,其中n为能级数。
例如,第一能级最多容纳2个电子,第二能级最多容纳8个电子。
根据电子能级的规律,我们可以了解到元素周期表的排布方式。
元素周期表是将化学元素按照原子序数的增序排列的表格。
元素周期表可以分为周期和族两个方向。
元素周期表的周期是指元素周期性质的变化规律。
周期表中的每一个周期代表着一个能级。
在同一个周期中,元素的最外层电子壳的能级相同,受到的核吸引力相近,因此具有类似的化学性质。
元素周期表的周期依次为K、L、M、N、O等,对应着原子的能级。
元素周期表的族是指元素的主族和次族。
主族元素是指位于周期表左边的元素,它们具有相似的化学性质。
主族元素的最外层电子壳填满的电子数都相同。
例如,第一族(碱金属)的元素最外层电子壳只填满了一个电子,第二族(碱土金属)的元素最外层电子壳填满了两个电子。
次族元素是指位于周期表右边的元素,它们具有相似的化学性质。
次族元素的最外层电子壳填满的电子数也相同。
例如,第十六族(卤族)的元素最外层电子壳填满了六个电子。
元素周期表的排列方式和周期性质的变化规律可以总结为以下几点:1.周期性:在元素周期表中,各周期的化学性质有规律地变化。
例如,金属元素通常位于周期表左侧,具有良好的导电性和热导性,而非金属元素通常位于周期表右侧,具有较差的导电性。
2.原子半径:随着周期数的增加,原子半径逐渐增大。
这是因为随着电子层数的增加,电子对原子核的屏蔽作用增强,电子云的尺寸增大。
3.电离能:随着周期数的增加,元素的电离能逐渐增大。


2021-2022学年高二化学重难点专题突破模块一原子结构与性质专题02 核外电子排布与元素周期表一、选择题1. 已知某元素+3价离子的电子排布式为1s22s22p63s23p63d5,该元素在周期表中的位置是()A.第3周期Ⅷ族,p区B.第3周期ⅤB族,ds区C.第4周期Ⅷ族,d区D.第4周期Ⅴ族,f区【答案】C【解析】+3价离子的核外有23个电子,则对应的原子核外有26个电子,26号元素是铁,位于元素周期表中第4周期Ⅷ族,位于d区。
2. 元素周期表中有如图所示的元素,下列叙述正确的是()A.钛元素原子的M层上共有10个电子B.钛元素是ds区的过渡元素C.钛元素原子最外层上有4个电子D.47.87是钛原子的近似相对原子质量【答案】A【解析】钛元素原子的M层为第三层,M层电子排布式为3s23p63d2,共有10个电子,A正确;钛元素是d区元素,B错误;钛元素原子最外层电子排布式为4s2,有2个电子,C错误;47.87是钛元素的相对原子质量,D错误。
3. 某基态原子的价电子排布式为4d15s2,则下列说法正确的是()A.该元素原子最外层共有3个电子B.该元素位于第5周期ⅡA族,处于ds区C.该元素原子的M层上共有18个运动状态不同的电子D.该元素原子的N层上有5个空轨道【答案】C【解析】由价电子排布式为4d15s2可知,该元素应位于第5周期ⅢB族,该元素原子中共有39个电子,分5个电子层,其中M层上有18个电子,最外层上有2个电子,故A错误;该元素位于第5周期ⅢB族,处于d区,故B 错误;该元素基态原子的电子排布式为1s22s22p63s23p63d104s24p64d15s2,M能层上有18个电子,故C正确;该元素原子的N层的电子排布为4s24p64d1,4d轨道有4个空轨道,故D错误。
4.主族元素A和B可形成组成为AB2的离子化合物,则A、B两原子的最外层电子排布分别为()A.n s2n p2和n s2n p4B.n s2和n s2n p4C.n s2和n s2n p5D.n s2和n s【答案】选C。


《基态原子的核外电子排布原则》知识清单在化学的微观世界里,原子是构成物质的基本单元。
而基态原子的核外电子排布遵循着一系列特定的原则,这些原则对于理解原子的结构、性质以及元素周期表的规律都具有至关重要的意义。
一、能量最低原理能量最低原理是核外电子排布的首要原则。
简单来说,就是电子在排布时会优先占据能量较低的轨道,以使整个原子的能量处于最低状态。
就像一个人在选择座位时,总是倾向于先坐空着的、更舒适的位置。
为什么要遵循这个原理呢?这是因为处于能量最低状态的原子更加稳定。
想象一下,一个不稳定的原子就像一个摇摇欲坠的建筑,随时可能发生变化,而处于能量最低状态的原子则像是坚固的大厦,结构稳定。
在多电子原子中,轨道的能量是不同的。
一般来说,离原子核越近的轨道能量越低。
比如,1s 轨道的能量低于 2s 轨道,2s 轨道的能量又低于 2p 轨道。
二、泡利不相容原理泡利不相容原理指出,在同一个原子中,不可能有两个电子具有完全相同的四个量子数。
量子数是描述电子状态的一组参数,包括主量子数、角量子数、磁量子数和自旋量子数。
这就好比在一个教室里,每个座位都有其独特的坐标(行、列、楼层等),不可能有两个同学占据完全相同的座位。
由于泡利不相容原理的存在,每个轨道最多只能容纳两个电子,而且这两个电子的自旋方向必须相反。
自旋可以简单理解为电子的一种内禀属性,就像人的左右手一样,要么是“左手”,要么是“右手”。
三、洪特规则洪特规则进一步补充了电子在等价轨道(能量相同的轨道)上的排布方式。
当电子排布在等价轨道上时,会优先以相同的自旋状态分别占据不同的轨道,而且全充满、半充满和全空的状态相对更加稳定。
例如,对于氮原子(N),其电子排布式为 1s² 2s² 2p³。
2p 轨道有三个等价轨道,按照洪特规则,三个电子会分别占据三个 2p 轨道,并且自旋相同。
再比如,铬原子(Cr)的电子排布式为 1s² 2s² 2p⁶ 3s² 3p⁶ 3d⁵ 4s¹,而不是 1s² 2s² 2p⁶ 3s² 3p⁶ 3d⁴ 4s²。