2020高考化学一轮综合复习 第二章 化学物质及其变化 第8讲 氧化还原反应的概念练习
- 格式:doc
- 大小:166.50 KB
- 文档页数:20


第二章化学物质及其变化知识清单一、物质的分类1. 元素的存在形式有两种,分别是什么?游离态(单质)、化合态(化合物)2.从熔沸点角度看,纯净物和混合物有何差别?纯净物有固定的熔沸点,混合物没有3.只含一种元素的物质一定是纯净物吗?不一定;如氧气与臭氧、石墨与金刚石组成的都是混合物4.从与酸或碱反应的情况看,氧化物是如何分类的。
酸性氧化物:与碱反应生成盐和水的氧化物(如CO2、SO2、SO3、P2O5)碱性氧化物:与酸反应生成盐和水的氧化物(如Na2O、CaO)不成盐氧化物:既不与酸反应,也不与碱反应的氧化物(如CO、NO)5.酸性氧化物一定是非金属氧化物吗?不一定,如Mn2O7非金属氧化物一定是酸性氧化物吗?不一定,如CO、NO碱性氧化物一定是金属氧化物吗?是金属氧化物一定是碱性氧化物吗?不一定,如Al2O3、Mn2O76.酸碱盐是如何定义和再分类的?酸的定义:在水溶液中电离出的阳离子都是H+的化合物。
酸可以分为强酸与弱酸;或含氧酸与无氧酸;或一元酸与多元酸;或氧化性酸与非氧化性酸等;碱的定义:在水溶液中电离出的阴离子全是OH-的化合物。
碱可以分为强碱与弱碱;或一元碱与多元碱等。
盐的定义:由金属阳离子(或铵根离子)与酸根离子组成的化合物盐可以分为正盐与酸式盐;或可溶性盐与难容性盐等盐的溶解性:钾钠硝铵全都溶,盐酸不溶银亚汞;硫酸难容钡和铅,碳酸只溶钾钠铵;钙银硫酸盐微溶;亚硫酸盐似碳酸。
7. 常见物质俗名和化学式生石灰:CaO 熟石灰:Ca(OH)2 石灰石:CaCO3碱石灰:CaO+NaOH烧碱(苛性钠):NaOH 纯碱(苏打):Na2CO3小苏打:NaHCO38.分散系如何分类的?分类的标准是什么?分散系分为溶液、胶体和浊液;分类的标准是分散质粒子的直径大小:其中小于1-100nm属于溶液,1-100nm之间的属于胶体,大于100nm的属于浊液。
9.常见的胶体有哪些?云、烟、雾、牛奶、豆浆、河水、血液、有色玻璃等10.胶体有哪些性质?丁达尔效应、聚沉、电泳、渗析使胶体聚沉的方法有哪些?加热、搅拌、加入电解质溶液、加入胶粒带相反电荷的胶体。

教学资料参考范本【2019-2020】高考化学一轮综合复习第2章化学物质及其变化课时4 氧化还原反应的综合应用——配平、计算及滴定题型冲关练习撰写人:__________________部门:__________________时间:__________________1.已知aM2++bO2+4H+===cM3++dH2O,则化学计量数c的值为( )A.1 B.2C.3 D.4解析根据质量守恒可得a=c;根据电荷守恒可得2a+4=3c,解得c=4,选项D正确。
答案D2.含有a mol FeBr2的溶液中,通入x mol Cl2。
下列各项为通入Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是( ) A.x=0.4a,2Fe2++Cl2===2Fe3++2Cl-B.x=0.6a,2Br-+Cl2===Br2+2Cl-C.x=a,2Fe2++2Br-+2Cl2===Br2+2Fe3++4Cl-D.x=1.5a,2Fe2++4Br-+3Cl2===2Br2+2Fe3++6Cl-解析根据氧化还原反应的先后顺序知,Cl2先氧化Fe2+,然后再氧化Br-。
x=0.4a时,Cl2不能完全氧化Fe2+,只能发生反应2Fe2++Cl2===2Fe3++2Cl-,A项正确;当x=0.6a时,Cl2能将Fe2+完全氧化后,又能氧化的Br-,故B错误;x=a时,Cl2氧化Fe2+后又能氧化a mol的Br-,C正确;x=1.5a时,Cl2能将Fe2+、Br-完全氧化,D正确。
答案B3.FeS与一定浓度的HNO3反应,生成Fe(NO3)3、Fe2(SO4)3、NO2、N2O4、NO和H2O,当NO2、N2O4、NO的物质的量之比为1∶1∶1时,实际参加反应的FeS与HNO3的物质的量之比为( )A.1∶6B.1∶7C.2∶11D.16∶25解析设参加反应的FeS的物质的量为a mol,被还原的HNO3的物质的量为b mol,根据得失电子守恒有:a×(1+8)=×1+×2+×3,b=6a,又因为起酸性作用的HNO3的物质的量为3n[Fe(NO3)3]=3×(a-×2)mol=a mol,故实际参加反应的FeS与HNO3的物质的量之比为a∶(a+b)=1∶7。






专题讲座相互竞争的离子反应和氧化还原反应反应物间一对多的化学反应常有“平行反应”和“竞争反应”两类,平行反应主要指多个反应相互间没有影响可同时进行;而竞争反应是指由于反应能力不同,多个反应按一定的先后顺序逐次进行。
竞争反应主要包括两种基本题型:一是一种氧化剂(还原剂)与多种还原剂(氧化剂)反应,如把Cl2通入含I-、Br-、Fe2+的溶液中,按照还原能力由强到弱的顺序,I-优先反应,其次是Fe2+,最后是Br-;二是一种酸(碱)与多种碱性(酸性)物质反应,如把盐酸逐滴加入到含有NaOH、Na2CO3的混合溶液中,按照碱性由强到弱的顺序,NaOH优先反应,然后是Na2CO3,此类竞争反应的先后顺序即是其有效顺序。
在实际问题中有部分看似平行的反应,由于物质的性质而出现了“有效”和“无效”两种可能性,准确地确定有效反应就成了解题的关键。
1.复分解反应之间的竞争。
若某一溶液中同时存在几个可能的复分解反应,则生成更难溶解或更难电离的物质的反应将优先进行。
2.氧化还原反应之间的竞争。
若某一溶液中同时含有多种还原性(氧化性)物质,则加入一种氧化剂(还原剂)时,优先氧化(还原)还原性(氧化性)强的物质。
3.氧化还原反应与非氧化还原反应之间的竞争。
一般情况下,氧化还原反应优先于非氧化还原反应发生。
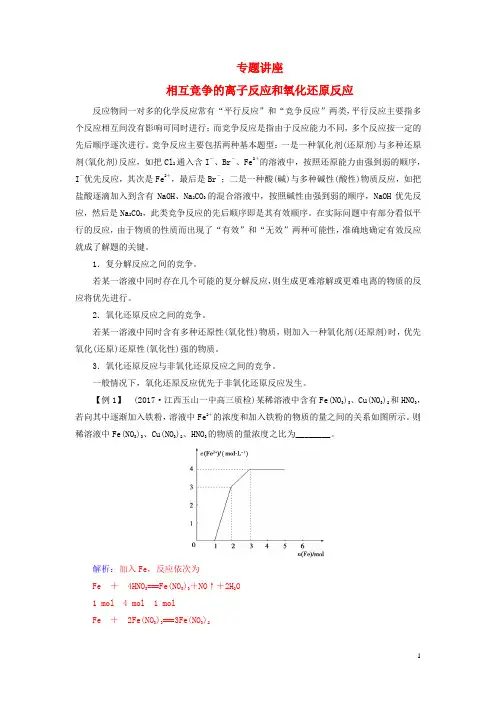
【例1】(2017·江西玉山一中高三质检)某稀溶液中含有Fe(NO3)3、Cu(NO3)2和HNO3,若向其中逐渐加入铁粉,溶液中Fe2+的浓度和加入铁粉的物质的量之间的关系如图所示。
则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3的物质的量浓度之比为________。
解析:加入Fe,反应依次为Fe +4HNO3===Fe(NO3)3+NO↑+2H2O1 mol 4 mol 1 molFe +2Fe(NO3)3===3Fe(NO3)21 mol2 mol3 molFe +Cu(NO3)2===Fe(NO3)2+Cu1 mol 1 mol 1 mol由上可知c[Fe(NO3)3]∶c[Cu(NO3)2]∶c(HNO3)=1∶1∶4。

第三节 氧化还原反应考点(一)氧化还原反应的基本概念【精讲精练快冲关】[知能学通]1. 本质和特征氧化还原反应的本质是电子转移 (得失或偏移),特征是反应过程中元素的化合价发生变化。
2. 相关概念及其关系巻电壬化合价升禹,被也牝还』剂 烂長临性 蔭勻礙反哑 匸巴|械化》物洱廡物] [生成物?其化剂洁习粗化性単長庄反应単勺还原产物__L~~f~~得到电子,化合价降低,被述厢△例如,反应MnO 2+ 4HCI (浓) ------ M nCl 2+ Cl 2T + 2H 2O 中,氧化剂是 MnO 2,还原剂 是HCl ,氧化产物是 Cl ?。
生成1 mol CI 2时转移电子数目为 2N A ,被氧化的HCI 的物质 的量是2_mol , HCI 显示的性质是还原性和酸性。
3. 氧化还原反应与四种基本反应类型间的关系4. 元素化合价的判断正确分析氧化还原反应中电子转移的数目,判断氧化剂和还原剂,其前提是确定物质 中各元素(特别是变价元素)的化合价。
先标出熟悉元素的化合价, 再根据化合物中元素化合 价代数和为零的规则,求解其他元素的化合价。
(1)常见元素的化合价可以借助化合价口诀来记忆:一价氢、氯、钾、钠、银;二价氧、钙、钡、镁、锌; 三铝、四硅、五价磷;说变价也不难,二三铁、二四碳、二四六硫都齐全;铜汞二价最常 见。
(2)近几年高考中一些特殊物质中元素的化合价+ 2+ 4+ 3+ 2菲削牝谨原反应分解化合反应粗优还煉反咸5.(1) 常见的氧化剂6.氧化还原反应中电子转移的表示方法(1)双线桥法蒔到*輒化和+还原剤一还貧产物一輸化产物失击mT请写出Cu与稀硝酸反应的化学方程式并用双线桥标出电子转移的方向和数目:r 丫3Cu-HSHNO a( #)-—3CuCN()s)f-H2XOt +4H2<)I •*得到2 X 3e-____________________________________ -(2)单线桥法>ie*氧化刑一还原剂一还原产物+氧化产物请写出Cu与稀硝酸反应的化学方程式并用单线桥标出电子转移的方向和数目:騒一T兀u+呂(称〕眈十十[题点练通]1 •判断下列说法的正误(正确的打V,错误的打“x”)。
高考化学一轮复习目录第一章化学计量在实验中的应用第1 讲物质的量、气体摩尔体积第2 讲物质的量浓度第二章化学物质及其变化第1 讲物质的组成、性质及分类第2 讲离子反响离子方程式第3 讲氧化复原反响的根本概念第4 讲氧化复原反响的规律和应用第三章金属及其化合物第1 讲碱金属元素——钠第2 讲铁及其化合物第3 讲镁及其化合物第4 讲铝及其化合物第四章常见的非金属及其化合物第1 讲无机非金属材料的主角——硅第2 讲富集在海水中的元素——氯第3 讲硫及其化合物第4 讲氮的氧化物和硝酸第5 讲氨和铵盐第五章物质结构与元素周期律第1 讲元素周期表第2 讲元素周期律第3 讲化学键第六章化学反响中的能量变化电化学第1 讲化学反响中的能量变化实验探究:中和热的测定第2 讲原电池化学电源第3 讲电解池金属的电化学腐蚀与防护第七章化学反响速率和化学平衡第1 讲化学反响速率第2 讲化学反响的方向和限度第3 讲化学平衡移动第八章水溶液中的离子平衡第1 讲弱电解质的电离平衡第2 讲水的电离和溶液的酸碱性第3 讲盐类的水解第4 讲难溶电解质的溶解平衡第九章认识有机化合物第1 讲有机物的结构特点和分类第2 讲研究有机化合物的方法第十章烃第1 讲脂肪烃第2 讲芳香烃第十一章烃的衍生物第1 讲卤代烃第2 讲醇酚第3 讲醛羧酸酯第十二章根本营养物质、高分子化合物第1 讲根本营养物质第2 讲进入合成有机高分子化合物的时代第十三章化学实验根底第1 讲化学实验根底知识实验探究:“仪器改造〞与“一器多用〞第2 讲物质的检验、别离和提纯第3 讲实验方案的设计与评价第4 讲探究性化学实验。
【2019最新】精选高考化学一轮综合复习第二章化学物质及其变化第8讲氧化还原反应的概念练习考纲要求 1.了解氧化还原反应的本质。
2.了解常见的氧化还原反应。
考点一用“双线桥”理解氧化还原反应的概念1.氧化还原反应与四种基本反应类型的关系(1)氧化还原反应的本质与特征本质:反应过程中有电子的转移(得失或偏移)。
特征:反应过程中有元素的化合价发生改变。
(2)四种基本反应类型和氧化还原反应的关系可用下图表示。
[示例]下列反应属于氧化还原反应的是___________________________________________,属于化合反应的是____________,属于分解反应的是________________________,属于置换反应的是______________,属于复分解反应的是______________。
①Cu2S+O22Cu+SO2②3O22O3③Fe2O3+3CO2Fe+3CO2④2Na+2H2O===2NaOH+H2↑⑤CaCO3CaO+CO2↑⑥2H2O22H2O+O2↑⑦SO3+H2O===H2SO4⑧2Fe+3Cl22FeCl3⑨H2SO4+2NaOH===Na2SO4+2H2O⑩NaH+H2O===NaOH+H2↑⑪IBr+H2O===HIO+HBr答案①③④⑥⑧⑩⑦⑧⑤⑥①④⑨⑪2.氧化还原反应的概念之间的关系概括为“升失氧、降得还,剂性一致、其他相反”。
实例:在Fe2O3+3CO2Fe+3CO2的反应中Fe2O3是氧化剂,CO是还原剂;C元素被氧化,Fe元素被还原;Fe2O3具有氧化性,CO具有还原性;CO2是氧化产物,Fe是还原产物。
3.氧化还原反应电子转移的表示方法(1)双线桥法:①标变价,②画箭头,③算数目,④说变化。
用双线桥法标出铜和浓硝酸反应电子转移的方向和数目:_____________________________。
(2)单线桥法:箭头由失电子原子指向得电子原子,线桥上只标电子转移的数目,不标“得”“失”字样。
用单线桥法标出铜和稀硝酸反应电子转移的方向和数目:_____________________________。
答案(1)(2)4.常见的氧化剂和还原剂(1)常见氧化剂常见氧化剂包括某些非金属单质、含有高价态元素的化合物、过氧化物等。
如:(2)常见还原剂常见还原剂包括活泼的金属单质、非金属阴离子及含低价态元素的化合物、低价金属阳离子、某些非金属单质及其氢化物等。
如:(3)元素化合价处于中间价态的物质既有氧化性,又有还原性其中Fe2+、理解氧化还原反应的基本概念(1)有单质参加或有单质生成的化学反应一定是氧化还原反应(×)(2)金属阳离子一定只具有氧化性(×)(3)NO2溶于水发生氧化还原反应(√)(4)氧化还原反应中有一种元素被氧化时,一定有另一种元素被还原(×)(5)氧化还原反应中的反应物,不是氧化剂就是还原剂(×)(6)某元素从游离态变为化合态,该元素可能被氧化也可能被还原(√)(7)浓硫酸具有强氧化性,不能干燥SO2、CO等还原性气体(×)(8)置换反应一定是氧化还原反应,化合反应、分解反应不一定是氧化还原反应(√)(9)NaHCO3+H2===HCOONa+H2O的反应中,NaHCO3被氧化(×)(10)Na2O2与水的反应中,水是还原剂(×)反应MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O中,氧化剂是__________,还原剂是__________,氧化产物是________,还原产物是________,MnO2发生________反应,HCl发生________反应;生成1molCl2时转移电子数目为________,被氧化的HCl的物质的量是________mol,盐酸显示的性质是________性和________性。
答案MnO2 HCl Cl2 MnCl2 还原氧化2NA2 还原酸1.(2016·上海,13)O2F2可以发生反应:H2S+4O2F2―→SF6+2HF+4O2,下列说法正确的是( )A.氧气是氧化产物B.O2F2既是氧化剂又是还原剂C.若生成4.48LHF,则转移0.8mol电子D.还原剂与氧化剂的物质的量之比为1∶4答案D解析A项,O元素的化合价由反应前的+1价变为反应后的0价,化合价降低,获得电子,所以氧气是还原产物,错误;B项,在反应中O2F2中的O元素的化合价降低,获得电子,所以该物质是氧化剂,而H2S中的S元素的化合价是-2价,反应后变为SF6中的+6价,所以H2S是还原剂,错误;C项,外界条件不明确,不能确定HF的物质的量,所以不能确定转移电子的数目,错误;D项,根据反应化学方程式可知还原剂H2S与氧化剂O2F2的物质的量的比是1∶4,正确。
2.(2018·烟台模拟)某种飞船以N2H4和N2O4为动力源,发生反应:2N2H4+N2O4===3N2+4H2O,反应温度可高达2700℃,对于该反应,下列说法中正确的是( )A.该反应属于置换反应B.N2H4是氧化剂C.N2O4是还原剂D.N2既是氧化产物又是还原产物答案D解析该反应的反应物中无单质,不属于置换反应;该反应实际上是不同价态的氮元素之间发生的归中反应,N2H4是还原剂,N2O4是氧化剂,N2既是氧化产物又是还原产物。
3.偏二甲肼[(CH3)2NNH2]与N2O4是常用的火箭推进剂,二者发生如下化学反应:(CH3)2NNH2(l)+2N2O4(l)===2CO2(g)+3N2(g)+4H2O(g),反应中氧化剂是___________________________。
答案N2O4解析反应中N2O4中N由+4价变为0价,作为氧化剂。
1.解决氧化还原反应概念的一般思路找变价、判类型、分升降、定其他。
其中“找变价”是非常关键的一步,特别是不同反应物中含有同种元素的氧化还原反应,必须弄清元素化合价的变化情况。
2.代数和法确定化合物中变价元素的化合价先标出熟悉元素的化合价,再根据化合物中正、负化合价的代数和为零的原则求解其他元素的化合价。
如有机物中碳元素化合价(设为x)的确定方法:有机物中氧元素的化合价为-2,氢元素的化合价为+1。
利用元素化合价代数和为零的规则确定碳元素的化合价。
乙酸(C2H4O2)中满足2x+(+1)×4+(-2)×2=0,则x=0。
考点二氧化性、还原性强弱的判断1.氧化性、还原性的判断(1)氧化性是指得电子的性质(或能力);还原性是指失电子的性质(或能力)。
(2)氧化性、还原性的强弱取决于得、失电子的难易程度,与得、失电子数目的多少无关。
如:Na-e-===Na+,Al-3e-===Al3+,但根据金属活动性顺序表,Na比Al活泼,更易失去电子,所以Na比Al的还原性强。
从元素的价态考虑:最高价态——只有氧化性,如:Fe3+、H2SO4、KMnO4等;最低价态——只有还原性,如:金属单质、Cl-、S2-等;中间价态——既有氧化性又有还原性,如:Fe2+、S、Cl2等。
2.氧化性、还原性强弱的比较方法(1)根据化学方程式判断氧化剂(氧化性)+还原剂(还原性)===还原产物+氧化产物氧化性:氧化剂>氧化产物;还原性:还原剂>还原产物。
(2)根据反应条件和产物价态高低进行判断①与同一物质反应,一般越易进行,则其氧化性或还原性就越强。
如Na与冷水剧烈反应,Mg与热水反应,Al与水加热反应也不明显,所以还原性:Na>Mg>Al;非金属单质F2、Cl2、Br2、I2与H2反应,F2与H2暗处剧烈反应并爆炸,Cl2与H2光照剧烈反应并爆炸,Br2与H2加热到500℃才能发生反应,I2与H2在不断加热的条件下才缓慢发生反应,且为可逆反应,故氧化性:F2>Cl2>Br2>I2。
②当不同的氧化剂作用于同一还原剂时,如果氧化产物价态相同,可根据反应条件的高低进行判断:一般条件越低,氧化剂的氧化性越强,如:MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O,2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O,由上述反应条件的不同,可判断氧化性:KMnO4>MnO2。
当不同氧化剂作用于同一还原剂时,如果氧化产物价态不相同,可根据氧化产物的价态高低进行判断:氧化产物的价态越高,则氧化剂的氧化性越强,如:2Fe+3Cl22FeCl3,Fe+SFeS,则氧化性:Cl2>S。
(1)强氧化剂与强还原剂混合不一定能发生氧化还原反应(√)(2)阳离子只有氧化性,阴离子只有还原性(×)(3)元素的非金属性越强,其氧化性越强,相应单质越活泼(×)(4)难失电子的物质一定易得电子(×)(5)NO2和NH3之间可能发生反应产生N2(√)(6)含硫化合物X、Y的转化关系S+Na OH―→X+Y+H2O中,硫单质的化合价最低(×)(7)锌粉加入硝酸铁、硝酸铜的混合溶液中,锌首先与硝酸铁反应置换出铁(×)(8)硝酸铜分解的产物可能是CuO、NO2、NO(×)外因对氧化性、还原性的影响物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度等有关。
下列各组物质:①Cu与HNO3溶液②Cu与FeCl3溶液③Zn与H2SO4溶液④Fe与FeCl3溶液⑤Cl2和NaOH溶液⑥Fe和HNO3溶液⑦Fe和H2SO4溶液⑧Na和O2(1)由于浓度不同而发生不同氧化还原反应的是_________________________________(填序号,下同)。
(2)由于温度不同而发生不同氧化还原反应的是_____________________________________。
(3)氧化还原反应不受浓度、温度影响的是__________。
答案(1)①③⑥⑦(2)⑤⑥⑦⑧(3)②④解析⑥Fe和浓HNO3常温下钝化,加热继续反应,Fe和稀HNO3反应,HNO3被还原成NO。
⑦Fe和浓H2SO4常温下钝化,加热继续反应,Fe和稀H2SO4反应生成FeSO4和H2。
根据影响因素判断氧化性、还原性强弱的方法(1)浓度:同一种物质浓度越大,氧化性(或还原性)越强。
如氧化性:浓H2SO4>稀H2SO4,浓HNO3>稀HNO3,还原性:浓HCl>稀HCl。
(2)温度:同一种物质,温度越高其氧化性越强。
如:热的浓硫酸的氧化性比冷的浓硫酸的氧化性强。
(3)酸碱性:同一种物质,所处环境酸(碱)性越强其氧化性(还原性)越强。
1.(氧化性、还原性强弱判断)铊(Tl)盐与氰化钾(KCN)被列为A级危险品。