2021年高考化学:化学物质及其变化2-2-2
- 格式:ppt
- 大小:2.60 MB
- 文档页数:41


第二章化学物质及其变化知识清单一、物质的分类1. 元素的存在形式有两种,分别是什么?游离态(单质)、化合态(化合物)2.从熔沸点角度看,纯净物和混合物有何差别?纯净物有固定的熔沸点,混合物没有3.只含一种元素的物质一定是纯净物吗?不一定;如氧气与臭氧、石墨与金刚石组成的都是混合物4.从与酸或碱反应的情况看,氧化物是如何分类的。
酸性氧化物:与碱反应生成盐和水的氧化物(如CO2、SO2、SO3、P2O5)碱性氧化物:与酸反应生成盐和水的氧化物(如Na2O、CaO)不成盐氧化物:既不与酸反应,也不与碱反应的氧化物(如CO、NO)5.酸性氧化物一定是非金属氧化物吗?不一定,如Mn2O7非金属氧化物一定是酸性氧化物吗?不一定,如CO、NO碱性氧化物一定是金属氧化物吗?是金属氧化物一定是碱性氧化物吗?不一定,如Al2O3、Mn2O76.酸碱盐是如何定义和再分类的?酸的定义:在水溶液中电离出的阳离子都是H+的化合物。
酸可以分为强酸与弱酸;或含氧酸与无氧酸;或一元酸与多元酸;或氧化性酸与非氧化性酸等;碱的定义:在水溶液中电离出的阴离子全是OH-的化合物。
碱可以分为强碱与弱碱;或一元碱与多元碱等。
盐的定义:由金属阳离子(或铵根离子)与酸根离子组成的化合物盐可以分为正盐与酸式盐;或可溶性盐与难容性盐等盐的溶解性:钾钠硝铵全都溶,盐酸不溶银亚汞;硫酸难容钡和铅,碳酸只溶钾钠铵;钙银硫酸盐微溶;亚硫酸盐似碳酸。
7. 常见物质俗名和化学式生石灰:CaO 熟石灰:Ca(OH)2 石灰石:CaCO3碱石灰:CaO+NaOH烧碱(苛性钠):NaOH 纯碱(苏打):Na2CO3小苏打:NaHCO38.分散系如何分类的?分类的标准是什么?分散系分为溶液、胶体和浊液;分类的标准是分散质粒子的直径大小:其中小于1-100nm属于溶液,1-100nm之间的属于胶体,大于100nm的属于浊液。
9.常见的胶体有哪些?云、烟、雾、牛奶、豆浆、河水、血液、有色玻璃等10.胶体有哪些性质?丁达尔效应、聚沉、电泳、渗析使胶体聚沉的方法有哪些?加热、搅拌、加入电解质溶液、加入胶粒带相反电荷的胶体。

冠夺市安全阳光实验学校考点二离子反应和离子方程式李仕才1.离子反应(1)概念:离子反应通常是指在溶液中有离子参加或有离子生成的反应。
(2)本质:使溶液中某些离子的浓度减小。
(3)离子反应发生的条件①复分解反应类型a.生成难溶性的物质,如Al(OH)3、BaSO4等。
b.生成难电离的物质,如弱酸、弱碱、水等。
c.生成易挥发性的物质,如CO2、SO2、NH3等。
②氧化还原反应类型强氧化性物质+强还原性物质―→弱氧化性物质+弱还原性物质。
如FeCl3溶液与Cu反应的离子方程式为2Fe3++Cu===2Fe2++Cu2+。
③络合反应:生成稳定的络合物或络合离子。
如向FeCl3溶液中滴入KSCN溶液时反应的离子方程式为Fe3++3SCN-===Fe(SCN)3。
④盐类的水解反应:在溶液中盐电离出的离子与水电离出的H+或OH-结合生成弱电解质。
如NH4Cl水解离子方程式为NH+4+H2O NH3·H2O+H+。
⑤电化学反应:实质为氧化还原反应,但需要添加电解或通电条件。
2.离子方程式(1)概念:用实际参加反应的离子符号来表示离子反应的式子。
(2)意义:离子方程式不仅可以表示某一个具体的化学反应,还可以表示同一类型的离子反应,如H++OH-===H2O可以表示可溶于水的强酸与可溶于水的强碱反应生成可溶性的盐和水的反应。
(3)书写步骤(以CaCO3与盐酸的反应为例)判断下列离子方程式的正误(正确的打“√”,错误的打“×”)1.Na2O2固体与水反应:2O2-2+2H2O===4OH-+O2↑。
( ×)2.醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+===Ca2++H2O+CO2↑。
( ×)3.Fe(OH)3和稀硫酸的反应:OH-+H+===H2O。
( ×)4.硫酸铜溶液跟氢氧化钡溶液反应:Ba2++SO2-4===BaSO4↓。
( ×)5.澄清石灰水与稀盐酸反应:H++OH-===H2O。

新课标化学必修1第二章《化学物质及其变化》知识点1.分类是学习和研究化学物质及其变化的一种常用的方法。
运用分类的方法不仅能使有关的化学物质及其变化的知识系统化,还可以通过分门别类的研究,发现物质及其变化的规律。
2.简单分类法就是把大量事物按照事先设定的标准进行分类的方法,它是人们最熟悉、也是最方便的一种工作方法。
意义:当分类的标准确定过后,同类中的事物在某些方面的相似性可以帮助我们做到举一反三;对于不同类事物的了解使我们做到由此及彼。
3.交叉分类法:为了弥补一种分类方法的局限性,人们在认识事物时从不同的角度设定不同的标准对同一事物进行认识,这种方法叫交叉分类法。
例1:对班级学生采用交叉分类法,有利于全面了解学生,便于班级的管理,其分类标准和意义如下:(1)按性别分:男生、女生。
意义:①男女生体能不同,劳动分工不同,运动会报名分男子组和女子组。
②男女生生理特征不同,剧烈活动要考虑女生的特殊例假。
③男女生的思维特点和个性心理不同,分班时尽量考虑男生女生的均衡性,以形成优势互补。
④男女生身材特点不同,审美情趣不同,夏季校服的设计要考虑男生女生的区别。
(2)按学习成绩、平时表现分:学优生、学困生。
意义:抓学优生保升学率,抓学困生保稳定,控制学生流失率,抓两头带中间,保整体进步。
(3)按高考发展方向分:文史类、理工类、艺体特长类、保送类、意义:不同类别的学生,在学习时侧重点不同,老师要求也不同,将来发展方向也不同。
(4)按是否承担社会工作分:干部、群众意义:干部与群众在责、权、利三方面都不会相同,干部的锻炼机会更多些、责任更大些、有机会参与优秀干部的评选,群众则没有。
(5)按政治面貌分:团员、群众意义:团员的政治觉悟要更高些,学校活动参与得更主动些,表现更优秀些,活动效果老师更放心些。
(6)按家长工作单位分:城市的(管局的、油公司的、炼化的、石化的、市政的)、农村的、招商的意义:根据家长的工作单位和收入情况对学生进行理财教育,避免奢侈浪费,养成节约的好习惯,对城市低保护、农村低收入家庭进行政策性照顾,实现胡锦涛主席“学有所教”的十七大目标。

高三化学一轮复习专题二 化学物质及其变化第一节 物质的分类考点2分散系 胶体 (1)概念:把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系。
其中,被分散的物质称为分散质,容纳分散质的物质是分散剂。
根据分散质粒子直径的大小的不同可将分散系分为溶液、胶体和浊液。
(2)理清三种分散系的差异2胶体—分散质粒径在1nm~100nm之间(1)Fe(OH)3胶体的制备(2)胶体的性质及应用③聚沉④电泳⑤渗析①丁达尔效应②布朗运动(2)原理总结(1)方法点拨1.(RJ必修1·P29改编题)下列不能产生丁达尔效应的分散系是 ( )A.氯化钠溶液 B.淀粉溶液C.蒸馏水D.氢氧化铁胶体练习1【解析】 A中,NaCl溶液属于分散系,但不能产生丁达尔效应;B中,淀粉溶液属于胶体,可产生丁达尔效应 ;C中,蒸馏水为纯净物,不能构成分散系;D中,氢氧化铁胶体属于胶体,可产生丁达尔效应 。
A2.下列说法中不正确的是( )A.明矾[KAl(SO4)2·12H 2O]在水中能形成Al(OH)3胶体,可用作净水剂B.江河入海口三角洲的形成通常与胶体的性质有关C.向沸水中逐滴加入少量饱和FeCl 3溶液,可制得Fe(OH)3胶体D.依据丁达尔效应可将分散系分为溶液、胶体与浊液练习2D 【解析】 A中,明矾水解Al3++3H 2O Al(OH)3(胶体)+3H +,生成的Al(OH)3胶体有吸附性,可以净水; B中,因河水中由泥沙形成的胶体颗粒带有电荷,与海水中的电解质溶液所带的电荷发生中和而聚沉; C中,制Fe(OH)3胶体就是向沸水中逐滴加入少量饱和FeCl 3溶液;D中,三种分散系的分类依据是分散质微粒的大小,不能根据是否具有丁达尔效应。
3.下列说法不正确的是( )A.用激光笔照射鸡蛋清溶液,侧面可观察到明显的光路B.氢氧化铁胶体带正电荷是氢氧化铁胶体稳定存在的主要原因C.根据分散质微粒的直径的大小,将分散系分为溶液、胶体、浊液D.江河入海口三角洲的形成通常与胶体的性质有关练习3B 【解析】A中,鸡蛋清溶液是胶体,激光笔照射可产生丁达尔效应;B中,氢氧化铁胶体粒子带电,氢氧化铁胶体是电中性的分散系;C中,分散系分类的根本依据就是分散质微粒的直径的大小;D中,江河入海口三角洲的形成与胶体的聚沉有关。
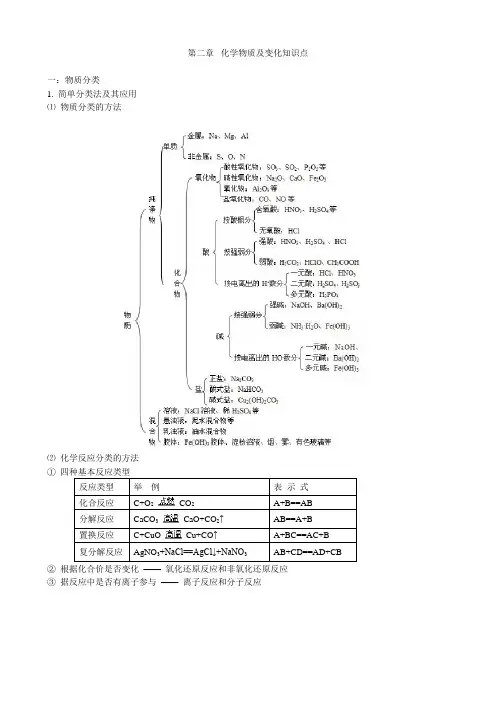
第二章化学物质及变化知识点一:物质分类1. 简单分类法及其应用⑴物质分类的方法⑵化学反应分类的方法①四种基本反应类型反应类型举例表示式化合反应C+O2CO2A+B==AB分解反应CaCO3CaO+CO2↑AB==A+B置换反应C+CuO Cu+CO↑A+BC==AC+B复分解反应AgNO3+NaCl==AgCl↓+NaNO3AB+CD==AD+CB②根据化合价是否变化——氧化还原反应和非氧化还原反应③据反应中是否有离子参与——离子反应和分子反应二、分散系及其分类分散系分散系粒子大小主要特征举例溶液分散质<1nm 透明、稳定、均一NaCl溶液、H2O浊液分散质>100nm 不透明、不稳定、不均一泥水、石灰水胶体1n m<分散质<100nm 较透明、较稳定、均一豆浆、牛奶、墨水(一)、胶体的性质1、丁达尔效应:当光束照射胶体时出现一个光亮的“通路”。
而溶液没有这样的一个现象,所以可以利用此效应区分溶液和胶体。
2、电泳现象①、胶体稳定的原因:a、主要原因:胶体粒子带电,同种胶体粒子的电性相同,它们之间相互排斥阻碍了胶体粒子变大,使它们不易聚沉。
注:胶体本身不带电,胶粒带电。
b、次要原因:胶体粒子作布朗运动。
②、电泳现象:在外加电场的作用下,胶体粒子在分散剂里面作定向移动。
③胶体粒子所带电荷分类:a、正电荷:金属氧化物、金属氢氧化物;例Fe(OH) 3、Fe2O3、卤化银(AgCl、AgBr、AgI)胶体等。
b、负电荷:非金属氧化物、金属硫化物;例SiO2、Ag2S、H2SiO3等。
(二)、胶体的聚沉————中和胶体粒子的电荷1、加电解质溶液2、加相反电荷的胶体二、离子反应(一)、电解质1、电解质:(酸、碱、盐、水)在水溶液里或熔融状态下能够导电的化合物。
非电解质:(包括CO2、SO2)在水溶液里或熔融状态下不能够导电的化合物。
注:电解质实际上是指不与水反应通过自身电离出自由移动的离子而导电的化合物。
例:①、NaCl=Na++Cl-KOH=K++OH-H2SO4=2H++SO42-②、CO2溶于H2O的溶液能导电,那么CO2是电解质吗?回答:CO2+H2O=H2CO3H2CO3=2H++CO32-CO2本身不能电离故CO2不是电解质。

第二节离子反应离子方程式考纲定位要点网络1。
了解电解质的概念;了解强电解质和弱电解质的概念。
2.理解电解质在水溶液中的电离以及电解质溶液的导电性。
3.了解离子反应的概念、离子反应发生的条件.4.能正确书写离子方程式,并能进行相关计算.电解质的分类和电离知识梳理1.电解质和非电解质(1)分类依据(2)电解质的强弱与物质类别的关系(3)熟记常见酸、碱的强弱ⅠA除LiOH外其余都是强碱ⅡA除Mg(OH)2、Be(OH)2外其余都是强碱ⅢA H3BO3为弱酸、Al(OH)3是两性氢氧化物ⅣA H2CO3、H2SiO3均为弱酸ⅤA强酸:HNO3;中强(或弱)酸:HNO2、H3PO4ⅥA强酸:H2SO4;弱酸:H2SO3、H2SⅦA强酸:HCl、HBr、HI、HClO4等弱酸:HF、HClO等过渡元素中常见的弱碱Fe(OH)3、Fe(OH)2、Cu(OH)2等羧酸CH3COOH、HCOOH、HOOCCOOH等[辨易错](1)NH3、SO2溶于水形成的溶液均导电,故NH3、SO2均为电解质。
()(2)液态AlCl3和液态HCl均不导电,则AlCl3和HCl为非电解质。
()(3)BaCO3的水溶液的导电性很弱,故它是弱电解质。
()(4)Cu和NaCl熔化均导电,二者均为电解质。
()(5)25 ℃时,0.1 mol·L-1的HA溶液的pH=1,说明HA为强电解质. ()[答案](1)×(2)×(3)×(4)×(5)√2.电解质的电离(1)电离是指电解质在水溶液里或熔融状态下,产生能够自由移动离子的过程.(2)电离方程式的书写①强电解质的电离方程式中,用“===”连接,弱电解质(包括弱酸的酸式酸根)的电离方程式中,用“”连接.如Na2SO4:Na2SO4===2Na++SO错误!;HClO:HClO H++ClO-.②多元弱酸的电离分步书写,多元弱碱的电离一步写出.如H2CO3:H2CO3H++HCO错误!,HCO-3H++CO错误!;Fe(OH)3:Fe(OH)3Fe3++3OH-.③酸式盐的电离如NaHSO4溶液中:NaHSO4===Na++H++SO错误!;NaHCO3溶液中:NaHCO3===Na++HCO错误!,HCO错误!H++CO错误!;NaHSO4熔化:NaHSO4===Na++HSO错误!.④两性氢氧化物[Al(OH)3]的电离Al3++3OH-Al(OH)3H++AlO-2+H2O。



2021山东高考化学双向细目表一、物质的结构与性质1.1 原子结构1.1.1 原子的组成及结构1.1.2 原子的尺寸与质量1.1.3 元素周期表的基本规律1.1.4 原子的结构与性质关系1.2 化学键及其性质1.2.1 价键理论及其原则1.2.2 共价键、离子键和金属键的特点1.2.3 键的极性及其影响1.2.4 键的性质与物质性质的关系1.3 物质的结构与性质1.3.1 晶体的结构及其性质1.3.2 分子的结构及其性质1.3.3 聚合物的结构及其性质1.3.4 点择性吸附与分离技术二、化学反应与能量2.1 化学反应及其类型2.1.1 化学反应的基本概念2.1.2 氧化还原反应及其类型2.1.3 酸碱中和反应及其类型2.1.4 水解与水合反应2.2 反应速率与化学平衡2.2.1 反应速率的测定及影响因素2.2.2 化学平衡的条件和平衡常数2.2.3 平衡常数与反应的热力学关系2.2.4 平衡常数与反应进行方向的关系2.3 化学能量变化2.3.1 化学反应的热力学基础2.3.2 燃烧和爆炸的热效应2.3.3 化学反应的热效应计算2.3.4 化学反应的能量变化与反应进行方向的关系三、物质的量与浓度3.1 物质的量及其计算3.1.1 质量、物质的量及摩尔的概念3.1.2 原子量、分子量及摩尔质量计算3.1.3 溶质的量浓度计算3.1.4 离子在溶液中的浓度计算3.2 溶液与离子平衡3.2.1 溶液的分类及其表达方式3.2.2 溶解度、溶解度积与离子平衡3.2.3 溶液的酸碱性及其浓度3.2.4 氧化还原反应与化学平衡3.3 溶液的反应性3.3.1 溶液的电导率与电解质3.3.2 溶液的中和与沉淀生成3.3.3 溶液的挥发性与溶解度规律3.3.4 离子的选择性吸附分离技术四、电化学与化学动力学4.1 电解质溶液4.1.1 电解质溶液的电导率及其测定4.1.2 离子迁移与电泳现象4.1.3 离子迁移速率与电解质溶液浓度关系4.1.4 电解质溶液的极化现象4.2 电解与电沉积4.2.1 电解的基本概念及电解池的组成4.2.2 电解的电压与电解的施行4.2.3 电沉积与析氢析氧以及析金析银反应4.2.4 电沉积与电化学腐蚀的关系4.3 化学动力学4.3.1 化学反应速率的概念及测定方法4.3.2 影响化学反应速率的因素4.3.3 化学反应机理及速率定律4.3.4 化学反应的速率与热力学关系五、化学反应中的能量变化5.1 化学反应的热效应5.1.1 化学反应的热效应概念及测定方法5.1.2 燃烧与爆炸的热效应计算5.1.3 化学反应的热效应对反应进行方向的影响5.1.4 化学反应的热效应与热化学方程的关系5.2 化学反应中的能量转化5.2.1 化学反应热与能量转化的基本规律5.2.2 化学反应热效应计算应用5.2.3 标准生成焓与生成焓变的计算5.2.4 化学反应热性质与热力学关系5.3 化学反应的热力学基础5.3.1 系统与外界的热力学基本概念及关系5.3.2 热力学第一定律与能量守恒定律的适用性5.3.3 热力学第二定律与熵增加原理的应用5.3.4 化学反应热力学基础与热化学方程的关系六、化学元素及其化合物6.1 元素的发现及应用6.1.1 元素的发现及命名6.1.2 元素的性质及其规律6.1.3 元素的应用及其环境影响6.1.4 新型元素的发现及其应用前景6.2 元素及其化合物的制备6.2.1 元素及其化合物的实验制备6.2.2 元素及其化合物的工业制备6.2.3 元素及其化合物的纯化6.2.4 元素及其化合物的再利用与资源的可持续利用6.3 元素周期律及离子理论6.3.1 原子的结构与性质周期律6.3.2 元素化合价与价态规律6.3.3 阱离子稳定性规律及其应用6.3.4 离子组成及其性质与周期律的关系以上便是2021年山东高考化学的双向细目表,通过系统的学习与复习这些内容,相信学生们定能在高考中取得优异的成绩。

离子反应李仕才考点一电解质及其电离1.电解质和非电解质(1)电解质:在水溶液中或熔融状态下,能导电的化合物,如NaOH、H2SO4、NaCl。
(2)非电解质:在水溶液中和熔融状态下,都不导电的化合物,如蔗糖、酒精。
2.强电解质和弱电解质(1)(2)强电解质和弱电解质的比较3.电离(1)概念:电解质在水溶液中或熔融状态下,离解成自由移动的离子的过程。
(2)电离条件:共价化合物的电离条件是溶于水,离子化合物的电离条件是溶于水或熔融。
4.电离方程式的书写(1)强电解质:完全电离,用===表示。
如H2SO4、NaOH、(NH4)2SO4的电离方程式分别为H2SO4===2H++SO2-4、NaOH===Na ++OH-、(NH4)2SO4===2NH+4+SO2-4。
(2)弱电解质:部分电离,用表示。
①多元弱酸分步电离,且电离程度逐步减弱,酸性主要由第一步电离决定。
如H2S的电离方程式为H2S H++HS-,HS-H++S2-。
②多元弱碱分步电离,但一步写出。
如Cu(OH)2Cu2++2OH-。
③两性氢氧化物双向电离。
如Al(OH)3的电离方程式:H++AlO-2+H2O Al(OH)3Al3++3OH-。
(3)酸式盐①强酸酸式盐完全电离,一步到底。
如NaHSO4在水溶液中的电离方程式为NaHSO4===Na++H++SO2-4,在熔融状态下的电离方程式为NaHSO4===Na++HSO-4。
②多元弱酸酸式盐,第一步完全电离,其余部分电离。
如NaHCO3===Na++HCO-3、HCO-3H++CO2-3。
判断正误(正确的打“√”,错误的打“×”)1.液氯不导电,氯水导电是因为氯气与水反应生成电解质电离而导电,故氯气是非电解质。
( ×)2.NaCl固体不导电,熔融的KCl能导电,所以前者是非电解质,而后者是电解质。
( ×) 3.H2SO4是强电解质,故浓硫酸具有强的导电性。
回夺市安然阳光实验学校"【走向高考】高考化学一轮复习第二章化学物质及其变化第2课时配套课后强化作业 "一、选择题1.(2013·西安模拟)用如图所示的装置分别进行如下实验:各组物质反应后,溶液的导电性比反应前明显增强的是( )A.向亚硫酸溶液中通入氯气:H2SO3+Cl2+H2O===H2SO4+2HClB.向硝酸银溶液中通入少量氯化氢:AgNO3+HCl===AgCl↓+HNO3C.向硫化氢饱和溶液中通入少量氧气:2H2S+O2===2H2O+2S↓D.向NaOH溶液中通入少量氯气:2NaOH+Cl2===NaCl+NaClO+H2O解析:溶液导电性的强弱与离子浓度及离子所带的电荷数有关。
A项中反应生成了强电解质,明显增加了离子浓度;B、D项离子浓度几乎不变,导电性几乎没有变化,C项反应生成更弱的电解质,因此离子浓度减小,导电能力明显减弱。
答案:A2.(2013·顺义十中高三化学模拟)下列说法正确的是( )A.强电解质溶液的导电性一定比弱电解质溶液的导电性强B.食盐溶液能导电,所以它是电解质C.SO3的水溶液可以导电,但它不是电解质D.NaHSO4无论在水溶液里还是在熔融状态下都可以电离出Na+、H+和SO2-4解析:判断电解质的强弱是根据其溶于水的部分是否全部电离,溶液导电性的强弱与溶液中离子的浓度大小有关,电解质强弱与其溶液导电性强弱并无直接联系,A项错误;食盐溶液不是电解质,NaCl是电解质,B项错误;SO3是非金属氧化物,属于非电解质,C项正确;NaHSO4在熔融状态下电离出Na+、HSO-4,D项错误。
答案:C3.(2013·内蒙古师大附中高三化学模拟)下列说法正确的一组是( )①不溶于水的盐(CaCO3、BaSO4等)都是弱电解质②盐都是强电解质③0.5mol/L的所有一元酸中氢离子浓度都是0.5mol/L ④强酸溶液中氢离子浓度一定大于弱酸溶液中氢离子浓度⑤电解质溶液导电的原因是溶液中有自由移动的阴、阳离子⑥熔融的电解质都能导电A.①③⑤⑥ B.②④⑤⑥C.只有⑤ D.只有⑥解析:CaCO3、BaSO4虽不溶于水,但它们是强电解质,故①错;绝大多数盐是强电解质,故②错;0.5mol/L一元强酸中氢离子浓度为0.5mol/L,一元弱酸中氢离子浓度小于0.5mol/L,故③错;0.000 1mol/L盐酸中氢离子浓度小于1mol/L CH3COOH中氢离子浓度,故④错;熔融的纯硫酸不导电,故⑥错误;⑤正确。
高考化学复习化学物质及其变化知识点化学对我们认识和利用物质具有重要的作用。
小编准备了化学物质及其变化知识点,具体请看以下内容。
一、重点聚集1.物质及其变化的分类2.离子反应3.氧化还原反应4.分散系胶体二、知识网络1.物质及其变化的分类(1)物质的分类分类是学习和研究物质及其变化的一种基本方法,它可以是有关物质及其变化的知识系统化,有助于我们了解物质及其变化的规律。
分类要有一定的标准,根据不同的标准可以对化学物质及其变化进行不同的分类。
分类常用的方法是交叉分类法和树状分类法。
(2)化学变化的分类根据不同标准可以将化学变化进行分类:①根据反应前后物质种类的多少以及反应物和生成物的类别可以将化学反应分为:化合反应、分解反应、置换反应、复分解反应。
②根据反应中是否有离子参加将化学反应分为离子反应和非离子反应。
③根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应。
2.电解质和离子反应(1)电解质的相关概念①电解质和非电解质:电解质是在水溶液里或熔融状态下能够导电的化合物;非电解质是在水溶液里和熔融状态下都不能够导电的化合物。
②电离:电离是指电解质在水溶液中产生自由移动的离子的过程。
③酸、碱、盐是常见的电解质酸是指在水溶液中电离时产生的阳离子全部为H+的电解质;碱是指在水溶液中电离时产生的阴离子全部为OH-的电解质;盐电离时产生的离子为金属离子和酸根离子或铵根离子。
(2)离子反应①有离子参加的一类反应称为离子反应。
②复分解反应实质上是两种电解质在溶液中相互交换离子的反应。
发生复分解反应的条件是有沉淀生成、有气体生成和有水生成。
只要具备这三个条件中的一个,复分解反应就可以发生。
③在溶液中参加反应的离子间发生电子转移的离子反应又属于氧化还原反应。
(3)离子方程式离子方程式是用实际参加反应的离子符号来表示反应的式子。
离子方程式更能显示反应的实质。
通常一个离子方程式不仅能表示某一个具体的化学反应,而且能表示同一类型的离子反应。
学习资料陌生氧化还原反应和离子反应方程式的书写命题分析:两大反应是中学化学的重点知识内容,也是历届高考的必考点,分析近几年高考题可知,以化工流程为载体,结合题给条件书写有离子参加的氧化还原反应方程式并配平,然后结合配平后的离子方程式进行计算是高考的常考题型。
1.要注意溶液的酸碱性不同对产物的影响:如高锰酸钾在酸性条件下一般被还原为Mn2+,而在碱性条件下则得到MnO错误!。
2.要考虑溶液的酸碱性条件:在酸性条件下,离子方程式中不能出现OH-;在碱性条件下,离子方程式中不能出现H+。
酸性条件下多氧配H+另一侧补水;碱性条件下多氧配水另一侧补OH-。
3.要注意反应物的量不同(或溶液浓度的不同)产物不同.如过量的铁与稀硝酸反应,生成硝酸亚铁;浓硝酸和稀硝酸分别和铜反应的还原产物不同。
(2019·全国卷Ⅱ)立德粉ZnS·BaSO4(也称锌钡白),是一种常用白色颜料。
回答下列问题:(1)利用焰色反应的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐.灼烧立德粉样品时,钡的焰色为________(填标号)。
A.黄色B.红色C.紫色D.绿色(2)以重晶石(BaSO4)为原料,可按如下工艺生产立德粉:[解析](1)根据常见元素的焰色反应,可知钡元素的焰色为绿色。
(2)①重晶石和过量焦炭粉经回转炉、浸出槽后得到净化的BaS溶液,可判断重晶石(BaSO4)被还原为BaS,焦炭则被氧化为有毒气体CO,根据得失电子守恒法可配平氧化还原反应方程式BaSO4+4C错误!BaS+4CO↑;CO与水蒸气反应得到的清洁能源气体为H2,另一种产物为CO2,则CO与水蒸气反应的化学方程式为CO+H2O===CO2+H2。
②潮湿空气中的CO2和水蒸气跟“还原料”中的硫化钡反应生成的臭鸡蛋气味的气体为H2S,水溶性变差是因为发生了反应BaS+CO2+H2O===H2S+BaCO3↓,由此可知难溶于水的物质为BaCO3。
学案二氧化还原反应规律在配平及在定量测定中的应用【教学目标】1.进一步巩固氧化还原反应各概念,掌握其内在联系。
2.了解氧化还原反应规律,理解氧化还原反应中的得失电子守恒。
3.通过对氧化还原反应规律应用的学习,增强科学的态度、探索精神,提高归纳推理能力。
【教学重、难点】氧化还原反应的配平;氧化还原反应在Ⅱ卷计算及定量测定中的应用。
【考情分析】命题点五年考情分析解读氧化还原反应规律2017·课标全国Ⅱ,T82016·课标全国Ⅰ,T8氧化还原反应规律及应用是课标卷每年的必考内容,但一般不单独命题,而是分散在选择题的某个选项或非选择题的某些设问中,选择题往往与阿伏加德罗常数或化学计算相结合,非选择题则可能与基本理论、元素化合物、化学实验及工艺流程题相结合,分值一般占4~6分;从考查的内容上看。
侧重氧化还原反应的规律及氧化还原反应方程式的书写、配平及相关计算的考查,尤其是陌生反应方程式的书写,近几年来更是常考不衰,随着新课标对考生能力要求的提高,这种趋势将会有增无减。
氧化还原反应方程式的书写(配平) 2017·课标全国Ⅰ,T27(6) 2017·课标全国Ⅲ,T28(2) 2016·课标全国Ⅱ,T28(2)氧化还原反应定量计算2017·课标全国Ⅱ,T26(4) 2015·课标全国Ⅱ,T28(3)1.氧化还原反应规律(1)价态规律升降规律:氧化还原反应中,化合价有升必有降,升降总值相等。
价态归中规律含不同价态的同种元素的物质间发生氧化还原反应时,该元素价态的变化一定遵循“高价+低价―→中间价”。
而不会出现交叉现象。
简记为“两相靠,不相交”。
例如,不同价态硫之间可以发生的氧化还原反应是注:⑤中不会出现H 2S 转化为SO 2而H 2SO 4转化为S 的情况。
歧化反应规律“中间价―→高价+低价”。
具有多种价态的元素(如氯、硫、氮和磷元素等)均可发生歧化反应,如:Cl 2+2NaOH===NaCl +NaClO +H 2O 。