2019高考化学一轮复习化学物质及其变化教案(1)
- 格式:doc
- 大小:2.25 MB
- 文档页数:4



第一节物质的组成与分类; 物质的变化与性质一、基本概念辨析:㈠元素和微粒的区别元素——宏观概念,相同,不同的总称。
1.概念的范畴不同微粒——微观概念, 包括等。
元素——由 (质子)数决定。
只要原子的数确定,则元素种类就确定。
2.决定因素不同原子——由数和数两者来决定。
同位素之间属于元素,原子。
分子——由原子的、及 (考虑同分异构体)决定。
离子——由组成原子、质子数及电子数决定。
同种元素可形成不同离子,如Fe2+、Fe3+。
㈡比较“四同”概念名称同位素同素异形体同系物同分异构体相同点结构相似(官能团相同)不同点分子构成或晶体结构分子组成相差 CH2描述对象无机物、有机物物理性质化学性质相似实例H、D、T O2、O3;红磷,白磷;金刚石,石墨乙烯,丙烯;甲苯,乙苯乙醇和甲醚;甘氨酸和硝基乙烷氰酸铵和尿素从组成上判断(经验方法),化学式中含有的化合物为离子化合物,其余为共价化合物。
从性质上判断,是离子化合物,否则为共价化合物。
㈣判别混合物和纯净物:比较内容纯净物混合物是否有固定组成、结构是否有固定熔点、沸点是否有固定化学性质保持原有物质各自的化学性质【解题注意】一定得到混合物,如常温..下NO2就会自动可逆转化为N2O4,属于混合物。
1.回答下列各题并举例说明。
(1)质子数相同的微粒一定是同一种元素吗?。
(2)是否可理解为分子是保持物质性质的微粒?。
(3)为什么说原子是化学变化中的最小微粒?。
(4)氢元素有种,氢原子有种,氕(H)、氘(D)、氚(T), H、D、T相互形成的氢气分子有种。
(5)若由三种氢原子(H、D、T)和两种氧原子(16O、18O)形成的水分子有种。
(6)H2、D2、T2是否属于同位素?属于什么关系?。
(7)无机物存在同分异构现象吗?。
(8)同种元素组成的物质一定是纯净物吗?。
2.下列各组物质均由真实的分子构成的是( )A. CH4、H2O、SiO2B. CS2、O2、Cl2C. P、C、SiH4D. C2H4、H3PO4、NaCl3.下列所指物质属于纯净物的是( )A.分子式为C2H4Cl2的物质B. CuSO4·5H2OC.常温下的二氧化氮D. 同条件下按体积比为2:1混合H2和O2㈤物理变化与化学变化的特征、本质1.特征:是否有新物质生成。
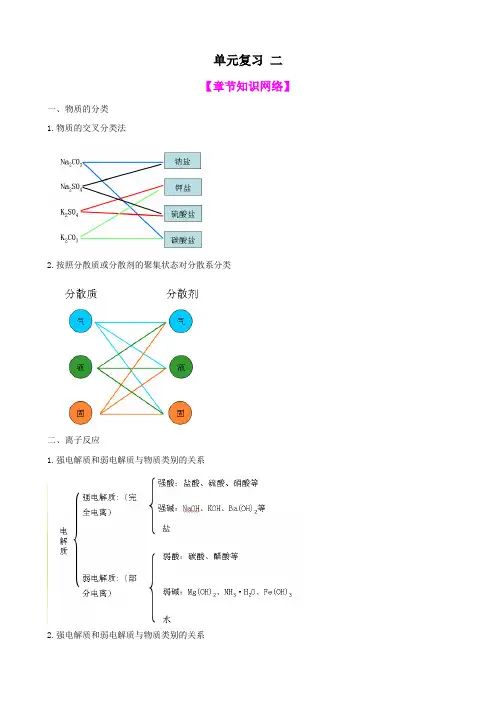
单元复习二【章节知识网络】一、物质的分类1.物质的交叉分类法2.按照分散质或分散剂的聚集状态对分散系分类二、离子反应1.强电解质和弱电解质与物质类别的关系2.强电解质和弱电解质与物质类别的关系三、氧化还原反应1.氧化还原反应的四对概念2.氧化还原反应与四种基本反应类型的关系【章节巩固与提高】一、选择题1.(2012·辽宁省重点中学协作体模拟考试)下列各组物质的分类正确的是( )A.胶体:雾、银氨溶液、蛋白质溶液B.非电解质:己烷、乙酸乙酯、淀粉C.糖类:葡萄糖、麦芽糖、纤维素D.同系物:正戊烷、异戊烷、新戊烷2.某溶液中含有大量的Cl-、CO2-3、SO2-4三种阴离子,如果只取一次溶液,分别将三种离子检验出来,下列加入试剂及其顺序(从左至右)正确的是( ) A .氯化钡溶液、硝酸、硝酸银溶液 B .硝酸、硝酸银溶液、氯化钡溶液 C .硝酸、硝酸钡溶液、硝酸银溶液 D .稀硫酸、硝酸钡溶液、硝酸银溶液3.(2012·潍坊模拟)溶液和胶体具备的共同性质是( ) A.分散质微粒都能透过半透膜B.用石墨电极做导电性实验时,分散质微粒都定向且朝一个方向移动C.都有丁达尔效应D.都比较稳定4.(2012·黄冈模拟)下列离子方程式书写正确的是( )A .向Ba(OH)2溶液中滴加NaHSO 4溶液至恰好为中性:22442Ba OH H SO ====BaSO H O ↓+-+-++++ B .NH 4HCO 3溶液与过量KOH 浓溶液共热:432NH OH NH H O ====↑+-++C .稀硝酸和过量的铁屑反应:3323Fe 8H 2NO ====3Fe 2NO 4H O ↑+-+++++ D .KI 溶液与H 2SO 4酸化的H 2O 2溶液混合:22222I H O 2H ====2H O I -++++5.(2012·枣庄模拟)下列变化中起氧化作用和还原作用的元素不是同一种元素的是( ) A .在400 ℃左右且有催化剂存在的条件下,用氨气把一氧化氮还原为氮气 B .工业上用稀硫酸和氧气与单质铜反应制取硫酸铜 C .工业上用石灰乳和氯气制备漂白粉 D .实验室用氯酸钾和浓盐酸制取氯气6.水热法制备Fe 3O 4纳米颗粒的反应为3Fe 2++2S 2O 2-3+O 2+x OH -===Fe 3O 4+S 4O 2-6+2H 2O ,下列说法中,不正..确.的是( ) A .每生成1 mol Fe 3O 4,反应转移的电子总数为4 mol B .Fe 2+和S 2O 2-3都是还原剂C .1 mol Fe 2+被氧化时,被Fe 2+还原的O 2的物质的量为1/3 mol D .x =47.某溶液中含有较大量的四种离子,在其中加入稀硫酸后它们的物质的量几乎不发生变化。


化学高考第一轮复习教案(经典版)编制人:__________________审核人:__________________审批人:__________________编制单位:__________________编制时间:____年____月____日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的经典范文,如工作总结、述职报告、策划方案、演讲致辞、合同协议、条据文书、教案资料、好词好句、作文大全、其他范文等等,想了解不同范文格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!Moreover, our store provides various types of classic sample essays for everyone, such as work summaries, job reports, planning plans, speeches, contract agreements, doctrinal documents, lesson plans, good words and sentences, complete essays, and other sample essays. If you want to learn about different sample formats and writing methods, please pay attention!化学高考第一轮复习教案化学高考第一轮复习教案七篇化学高考第一轮复习教案都有哪些?化学是在原子和分子水平上研究物质的组成、结构、性质、转化和应用的基础自然科学。
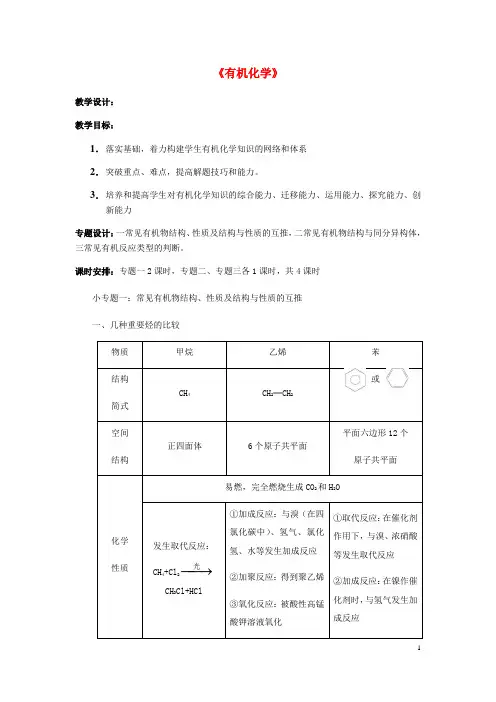
《有机化学》教学设计:教学目标:1.落实基础,着力构建学生有机化学知识的网络和体系2.突破重点、难点,提高解题技巧和能力。
3.培养和提高学生对有机化学知识的综合能力、迁移能力、运用能力、探究能力、创新能力专题设计:一常见有机物结构、性质及结构与性质的互推,二常见有机物结构与同分异构体,三常见有机反应类型的判断。
课时安排:专题一2课时,专题二、专题三各1课时,共4课时小专题一:常见有机物结构、性质及结构与性质的互推一、几种重要烃的比较二、几种重要烃的衍生物的比较2CH)或K2Cr2O小专题拓展结构(官能团)决定性质,性质反映结构(官能团)重要反应的断键机理共线、共面的母体有机物小专题二:常见有机物的结构与同分异构体一、同分异构体的书写方法与规律书写有机物的同分异构体时要按一定的顺序,避免遗漏和重复,一般的思路为:类别异构→碳链异构→位置异构。
1.判类别:根据有机物的分子组成判定其可能的类别异构。
2.写碳链:根据有机物的类别异构写出各类别异构的可能的碳链结构(先写最长的碳链,依次写出少一个碳原子的碳链,把余下的碳原子挂到相应的碳链上去。
)3.移官位:一般是先写出不带官能团的烃的同分异构体,然后在各条碳链上依次移动官能团的位置,有两个或两个以上的官能团时,先上一个官能团,再上第二个官能团,依此类推。
4.氢饱和:按“碳四键”的原理,碳原子剩余的价键用氢原子去饱和,就可得所有同分异构体的结构简式。
二、同分异构体数目的判断1.等效氢法有机物分子中,位置等同的氢原子叫等效氢,有多少种等效氢,其一元取代物就有多少种。
等效氢的判断方法是:(1)同一个碳原子上的氢原子是等效的。
如分子中—CH3上的3个氢原子等效。
(2)同一分子中处于轴对称位置或镜面对称位置上的氢原子是等效的。
如分子中,在苯环所在的平面内有两条互相垂直的对称轴,故有两类等效氢。
2.换元法对多元取代产物的种类判断,要把多元换为一元或二元再判断,它是从不同视角去想问题,思维灵活,答题简便,如二氯苯和四氯苯的同分异构体都为3种。

2019-2020年高三化学第一轮复习教案新课标人教版[课程标准]1.能根据物质的性质和组成对物质进行分类。
(尝试用不同的方法进行分类)2.知道胶体是一种常见的分散系。
(实验:氢氧化铁胶体的制备)3.知道酸、碱、盐在溶液中能发生电离,通过实验事实认识离子反应及其发生的条件,了解常见离子的检验方法(实验:溶液中Ag+ CO32-Cl- SO42-等离子的检验)4.根据实验事实了解氧化还原反应的本质是电子的转移,举例说明生产、生活中常见的氧化还原反应5.根据生产、生活中的实例或通过实验探究,了解金属铁极其化合物的主要性质(实验:铁盐的净水作用)[内容覆盖]化学必修1模块化学反应原理模块第三章第四节离子反应[时间安排] 一周(5+2课时)[复习思路][实施建议]第一学时 元素与物质的分类 (一课时)[情况分析]根据新课程标准,新高考将重视分类法在化学学习中的应用,并加强对不同类别物质、反应间的联系与考察的力度。
这部分难度不大,对我们的学生掌握不会造成问题。
[考点剖析]考点一:物质的组成和分类 例1 拓展1 智能训练12考点二:单质、氧化物、酸、碱、盐之间的相互关系考点三:胶体(性质、制备、提纯、聚沉方法、应用) 例3 拓展5 6 智能训练10[补充建议]第二学时 电解质 离子反应(二课时)[情况分析]离子方程式的书写及正误判断和离子共存问题,是高考的热点。
常以中等难度的选择题、填空题的形式出现。
另外离子反应在混合物的分离、物质的提纯等也可能是新高考的方向。
这部分知识学生较熟悉,可离子反应含盖的知识面广,将对学生的掌握造成一定的难度。
应多练习特别是化学用语的书写,xx高考的分析中我省的考生对化学用语的掌握很不乐观,因此这部分内容更加不容忽视。
[考点剖析]考点1 关于电解质的概念夯基固本1 例1 拓展1、3 智能训练1、2、3考点2 离子反应的条件及离子共存问题(注意常见不能共存的离子组,小心附加条件)例3、4 拓展4、6 智能训练4-7考点3 离子方程式的书写(用量问题是很大的难点)例5 6 拓展9 7考点4 离子方程式的正误判断例7 拓展11 10 智能训练8-12考点5 离子推断和检验例8 9 拓展13 智能训练13-15[补充建议]第三学时氧化还原反应铁极其化合物(2课时)[情况分析]氧化还原反应在生产实践中应用极为广泛,他贯穿于中学化学的全过程,是历年高考命题的热点之一。


第一讲物质的量⒈掌握物质的量、物质的量的单位——摩尔(mol)、阿伏加德罗常数、摩尔质量的概念。
⒉理解物质的量、阿伏加德罗常数与粒子(原子、分子、离子等)数目之间的相互关系一、摩尔1、物质的量:表示的物理量。
符号:,单位:。
物质的量是国际单位制中规定的七个基本物理量之一。
物质的量是以阿佛加德罗常数为计数单位,表示物质的基本单元数多少的物理量。
2、摩尔:物质的量这一物理量的单位,每摩尔物质含有个微粒。
符号:。
※使用时摩尔这个概念时应注意的事项:①物质的量与摩尔的关系,是基本物理量与其单位的关系②摩尔的量度对象是构成物质的基本微粒,这里的“基本微粒”可以是分子、原子、离子、电子、质子、中子等单一微粒,也可以是这些粒子的特定组合,如1molCaCl2可以说含1molCa2+、2molCl-或3mol阴、阳离子,或54mol电子,因此通常要指明具体微粒。
③摩尔概念只适用于微观,不适用于宏观。
3、阿伏加德罗常数:1mol任何粒子的粒子数叫阿伏加德罗常数,用表示;单位:;NA的准确值:kg12C所含有的碳原子数。
NA的近似值:。
4、NA的测定:(1)电解法(2)油膜法(3)晶体结构法【例1】下列说法正确的是()A. 物质的量是把物质的质量和微观粒子数联系起来的一个基本物理量B. 摩尔是国际单位制中七个基本物理量之一C. 1mol任何物质的质量就是该物质的相对分子质量D. 6.02×1023个H2所含分子的物质的量为1mol【例2】若将阿伏加德罗常数规定为0.024kg 12C所含有的碳原子数,其他规定(概念)不变,下列各项值不会发生变化的是()A. 物质的量B. 相对原子质量C. 1mol物质的质量D. 12g 12C所含有的碳原子数[变形训练]假如把12C的相对原子质量定为24,以0.024kg所含的碳原子数为阿伏加德罗常数,下列说法正确的是A、32O2在标准状况下所占的体积约为22.4LB、2.4g镁作还原剂时可失去0.2NA个电子C、2molNaOH与NA个H2SO4分子恰好中和D、1molZn与足量的稀硫酸反应时共生成2gH2【例3】设NA代表阿伏加德罗常数,下列说法正确的是()A. 8.4gNaHCO3晶体中含有阳离子和阴离子总数为0.2NAB.1.5g CH3+所含电子数为NAC.在常温、常压下,46g二氧化氮气体所含分子数为NAD.1L1mol/LNa 2CO3溶液中所含阴离子总数为NA【例4】、用电解法根据电极上析出物质的质量来验证阿伏加德罗常数值,其实验方案的要点为:①用直流电电解氯化铜溶液,所用仪器如图所示。

第二章化学物质及其变化一、本章内容概述本章是从化学学科内容方面展开化学科学。
作为从学科内容方面使学生认识化学科学的起始章,是连接义务教育阶段《化学》《科学》与高中化学的纽带和桥梁,对于发展学生的科学素养,引导学生有效地进行高中阶段的化学学习,具有非常重要的承前启后的作用。
“承前”意味着要复习义务教育阶段化学的重要内容,“启后”意味着要在复习的基础上进一步提高和发展,从而为化学必修课程的学习,乃至整个高中阶段的化学学习奠定重要的基础。
因此,本章在全书中占有特殊的地位,具有重要的功能,是整个高中化学的教学重点之一。
从化学物质的分类来看,纯净物的分类在初中已初步介绍过,这里主要是通过复习使学生进一步系统化。
溶液和浊液这两种混合物虽然初中也涉及过,但是,还没有从分散系的角度对混合物进行分类。
因此,分散系和液态分散系的分类、胶体及其主要性质是高中化学的新知识。
胶体的性质表现在很多方面,这里只是从胶体与溶液区分的角度,涉及到胶体的丁达尔效应。
从化学反应的分类来看,本章涉及到化学反应分类的3个标准:(1)反应物和生成物的类别以及反应前后物质种类的多少,按此标准划分,可将化学反应分为化合反应、分解反应、置换反应和复分解反应,这4种反应学生在初中已经学习过,这里主要是通过复习使学生进一步系统化;(2)反应中是否有离子参加;(3)反应中是否有电子转移。
后两种分类初中没有涉及过,因而是高中化学的新知识。
离子反应和氧化还原反应在高中化学学习中将大量涉及,因此,这两种反应是重要的基础知识,是本章的重点内容。
二、学习方法指导1、理解掌握一种化学研究方法—分类法,并使之贯穿于化学学习。
2、通过实验了解分散系的概念和胶体的性质,强化由实验学化学的学习方法。
3、学习两种新的化学反应分类法,是化学知识进一步系统化。
4、利用氧化反应和离子反应回顾总结所学知识,并且为以后学习打下良好基础。
三、高考命题趋势1、分类法的应用、分散系的概念及胶体的性质2、对于离子反应的考查主要有以下几个方面:⑴离子反应,此类试题考查的主要内容有:①理解离子反应的概念,②掌握离子反应发生的条件,③会判断离子在溶液中能否大量共存。
回夺市安然阳光实验学校第一讲物质的组成、性质和分类[课后达标训练]一、选择题1.(2018·新余联考)分类是科学研究的重要方法,下列物质分类不正确的是( )A.化合物:干冰、冰水共存物、烧碱、小苏打B.同素异形体:活性炭、C60、C80、石C.非电解质:乙醇、四氯化碳、氯气、葡萄糖D.混合物:漂白粉、纯净矿泉水、盐酸、大理石解析:选C。
干冰、冰水共存物、烧碱、小苏打都是由两种或两种以上元素组成的化合物,故A正确;活性炭、C60、C80、石都是由碳元素组成的不同单质,互为同素异形体,故B正确;氯气是单质,不是非电解质,故C错误;漂白粉、纯净矿泉水、盐酸、大理石都含有两种以上物质,属于混合物,故D正确。
2.胶体与溶液最简单的鉴别方法和本质区别分别是( )A.能否透过滤纸,是否有丁达尔效应B.是否无色透明,是否稳定C.是否有丁达尔效应,分散质粒子直径大小D.是否稳定,能否电泳解析:选C。
胶体分散系与其他分散系的本质区别是分散质粒子直径大小,鉴别溶液和胶体最简单的方法是丁达尔效应。
3.(2015·高考重庆卷)中华民族有着光辉灿烂的发明史,下列发明创造不涉及化学反应的是( )A.用胆矾炼铜B.用铁矿石炼铁C.烧结黏土制陶瓷D.打磨磁石制指南针解析:选D。
A.胆矾炼铜就是“湿法炼铜”,其原理是将胆矾溶于水,再将铁放入胆矾溶液中把铜置换出来,是化学反应。
B.铁矿石炼铁是将原料(铁矿石、焦炭、石灰石和空气)加入高炉中,在高炉中发生一系列化学反应,生成铁单质,是化学反应。
C.黏土烧结制成陶瓷的过程中有新物质生成,是化学反应。
D.四氧化三铁常称作“磁性氧化铁”,是磁石的主要成分,打磨磁石制指南针,只是磁石的形状发生变化,是物理变化。
4.下列生活中的做法没有利用物质化学性质的是( )A.葡萄酒中添加二氧化硫B.鲜花店的老板用浸泡了高锰酸钾的硅土延长鲜花的保存期C.用双氧水漂洗衣服上的污渍D.夏天超市用干冰给物质降温解析:选D。
化学物质及其变化
目录
一、高考要求和命题趋向
二、学生基本情况分析
三、复习思路
一、考纲要求
第一节物质的分类
1、了解分子、原子、离子等概念的含义。
了解原子团的定义。
2、物理变化与化学变化的区别与联系。
3、理解混合物和纯净物、单质和化合物、金属和非金属的概念。
4、理解酸、碱、盐、氧化物的概念及其相互联系。
5、了解胶体是一种常见的分散系。
第二节离子反应
1、了解电解质的概念。
了解强电解质和弱电解质的概念。
2、了解电解质在水溶液中的电离,以及电解质溶液的导电性。
3、能正确书写离子方程式。
第三节氧化还原反应
1、了解氧化还原反应的本质是电子的转移。
2、了解常见的氧化还原反应。
3、掌握常见氧化还原反应的配平和相关计算。
高考纵览
高考命题探究
第一节 物质的分类
内容探究:物质的分类主要判断各选项的正误,考查角度是对概念的辨析;单质、氧化物、酸、碱、盐之
间的转化会结合与社会热点相关的物质、材料、工业流程等进行考查;分散系的相关知识主要侧重胶体性
质与应用的考查。
形式探究:(1)物质的分类、物质的性质与变化常与其他知识综合考查,一般以选择题形式出现。
(2)分
散系的知识考查频率不高,难度不大,一般出现在选择题的个别选项中。
第二节 离子反应
内容探究:离子反应是高中化学的重点内容,是考查元素化合物知识的一种重要形式,主要以离子方程式的书写和正误的判断、离子是否能在溶液中大量共存的判断两种题型考查。
综合分析每年的高考题,离子方程式正误的判断主要涉及反应物或生成物的拆分问题、是否遵循守恒问题、是否注意用量等三个方面知识;离子方程式的书写主要出现在第Ⅱ卷中,根据题目要求填空;离子在溶液中是否能大量共存的判断主要涉及是否能发生复分解反应、是否能发生氧化还原反应、是否能发生水解反应、是否能发生络合反应等四个方面的知识;离子检验与推断与离子共存有密切联系,往往结合元素化合物知识,综合性较强。
形式探究:(1)离子共存以选择题的形式出现,是高考的热点。
(2)离子方程式的书写一般根据信息写出相应离子方程式,是必考点。
(3)离子的推断与检验多以选择题的形式出现,也可能以实验题形式出现,甚
至有实验设计。
第三节 氧化还原反应
内容探究:本节考查点有四个方面:一是氧化还原反应概念的辨析,二是氧化还原反应规律及应用,三是
氧化还原反应方程式的书写和配平,四是氧化还原反应的定量计算。
形式探究:通过分析近几年各省的高考题,在理综的考试中一般很少以完整的题目单独出现,往往与其他知识点融合,分散到不同题目中进行考查。
氧化还原反应基本概念的考查多在选择题的某一选项中出现。
以氧化还原反应方程式配平和得失电子守恒思想为基础的“新情境下方程式”的书写是高考的热点,在填
空题中多有出现,考查了考生运用知识解决问题的能力,是高考命题的方向和重点。
高考常将离子反应与氧化还原反应融合在一起考查,即书写离子方程式时往往用到氧化还原反应理论,这
类题能很好的考查学生全面思考和解决问题的能力。
二、学生基本情况分析
氧化还原反应 江苏13(选择)18(填空);上海2(选择)13(选择);全国1卷8(选择)36(填空);四川9(填空);浙江27(填空) 江苏12 (选择)19(填空);
海南4(选择);全国1卷27(填空);天津3(选择)
10(填空);浙江4 月4(选择)
全国1卷7(选择);北京9(选择)28(填空);浙江4月7(选择)
暴露出来的问题:(1)基础知识和基本技能不够扎实;(2)解题不够规范;(3)知识不够系统;(4)思维不够灵活;(5)平时学习的主观能动性不强;(6)课时少,内容多,导致学好化学的信心不足。
三、复习思路
1、立足课本,落实细节。