2018年创新设计必修一高中化学第四章 章末核心素养整合
- 格式:ppt
- 大小:3.78 MB
- 文档页数:31

高中化学必修一第四章知识点总结(详细)(word版可编辑修改)编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(高中化学必修一第四章知识点总结(详细)(word版可编辑修改))的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为高中化学必修一第四章知识点总结(详细)(word版可编辑修改)的全部内容。
教学重点:常见非金属元素(H、C、N、O、Si、S、Cl等)单质及其重要化合物的主要性质及应用。
教学难点:了解硅、氯、氮、硫及其重要化合物的主要性质。
教学过程:一.硅1.相关反应Si物理性质无色气体、有刺激性气味、密度小于空气、1:700溶于水化学性质与H2O NH3 + H2O NH3·H2O NH4++ OH—与酸NH3 + HCl = NH4Cl氨的催化氧化4NH3 + 5O2错误! 4NO + 6H2O实验室制取原理NH4+ + OH-错误! NH3↑+ H2O2NH4Cl +Ca(OH )2错误! 2NH3↑+ CaCl2 + 2H2O5.实验室制取干燥NH3的方法:制取原理: 2NH4Cl +Ca(OH )2错误! 2NH3↑+ CaCl2 + 2H2O气体成分: NH3( H2O )除水用试剂:碱石灰(不用浓H2SO4 、CaCl2原因是:2NH3+ H2SO4= (NH4)2SO4 ; CaCl2 + 8NH3 =CaCl2·8NH3)6.受热易分解 NH3·H2O 错误! NH3↑+ H2O NH4HCO3 错误! NH3↑+ CO2↑+ H2O7.氨水中的微粒分子:H2O NH3·H2O NH3 离子:NH4+ H+ OH-四.硫1.SO2的性质物理性质无色气体、有刺激性气味、有毒、1:40溶于水、密度大于空气化学性质与H2O SO2 + H2O = H2SO3与碱溶液先:SO2 +2NaOH = Na2SO3+H2O后:SO2 + Na2SO3 + H2O = 2NaHSO3 SO2过量时总反应:SO2 + NaOH = NaHSO3 与盐溶液SO2 + Na2CO3 = CO2+ Na2SO3 ( SO2不过量时 )与氯水SO2 + Cl2 + 2H2O = H2SO4 + 2HClH2SO3 + Cl2 + H2O = H2SO4 + 2HCl漂白性SO2能使品红溶液 (有机色质)褪色(生成了不稳定的无色物质),但加热褪色后的无色溶液,又恢复为原来的红色(不稳定的无色物质分解复原)实验室制法Na2SO3 +H2SO4(浓) = Na2SO4 + SO2↑+ H2O2.H2S物理性质无色气体、剧毒、有臭鸡蛋气味、1:2.6溶于水、密度大于空气化学性质与浓H2SO4H2S + H2SO4(浓)= S↓+ SO2 + 2H2O与碱溶液先H2S + NaOH= NaHS + H2O; 后NaHS + NaOH = Na2S + H2O。

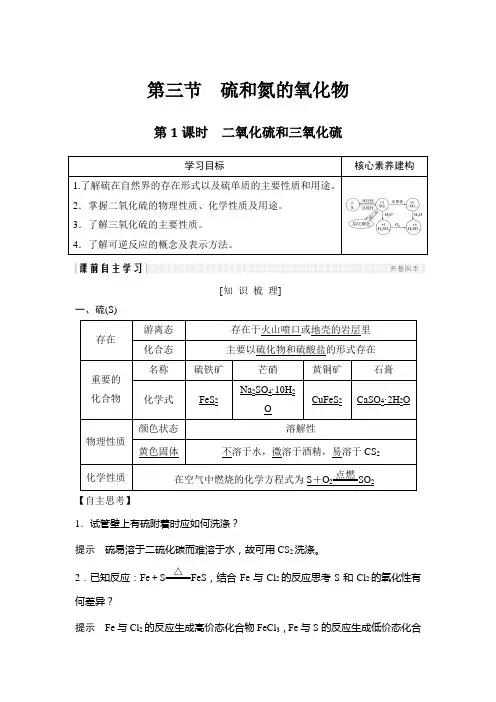
第三节 硫和氮的氧化物第1课时 二氧化硫和三氧化硫[知 识 梳 理]一、硫(S)【自主思考】1.试管壁上有硫附着时应如何洗涤?提示 硫易溶于二硫化碳而难溶于水,故可用CS 2洗涤。
2.已知反应:Fe +S=====△FeS ,结合Fe 与Cl 2的反应思考S 和Cl 2的氧化性有何差异?提示 Fe 与Cl 2的反应生成高价态化合物FeCl 3,Fe 与S 的反应生成低价态化合物FeS ,说明氯气的氧化性强于硫。
二、二氧化硫和三氧化硫 1.二氧化硫(SO 2) (1)物理性质(2)化学性质SO 2⎩⎪⎨⎪⎧与H 2O 反应:SO 2+H 2O H 2SO 3漂白性:SO 2能与某些有色物质生成不稳定的无色物质与O 2反应:2SO 2+O 2催化剂△2SO 3(3)SO 2的用途①漂白纸浆、毛、丝、草帽辫等; ②用于杀菌消毒。
2.三氧化硫三氧化硫具有酸性氧化物的通性,主要反应如下:SO 3⎩⎨⎧与H 2O :SO 3+H 2O===H 2SO 4与碱性氧化物(CaO ):SO 3+CaO===CaSO 4与碱[Ca (OH )2]:SO 3+Ca (OH )2===CaSO 4+H 2O【自主思考】3.书写SO 2与H 2O ,SO 2与O 2反应的化学方程式时需要注意什么问题? 提示 上述两反应都是可逆反应,在书写化学方程式时必须注意用“”表示。
4.将SO 2通入BaCl 2溶液中,会有沉淀生成吗?若是Ba(OH)2溶液有没有沉淀呢?提示 没有;有。
[效 果 自 测]1.判断正误,正确的打“√”,错误的打“×”。
(1)自然界中不存在游离态的硫单质。
()(2)S能氧化Fe,使Fe生成+3价铁的化合物。
()(3)S在空气中燃烧生成SO2,在过量的纯O2中燃烧生成SO3。
()(4)SO2和CO2可用澄清石灰水鉴别。
()(5)SO2使品红溶液褪色是因为SO2具有强氧化性。
()(6)SO2的水溶液存在SO2、H2SO3的原因是SO2与H2O反应为可逆反应。
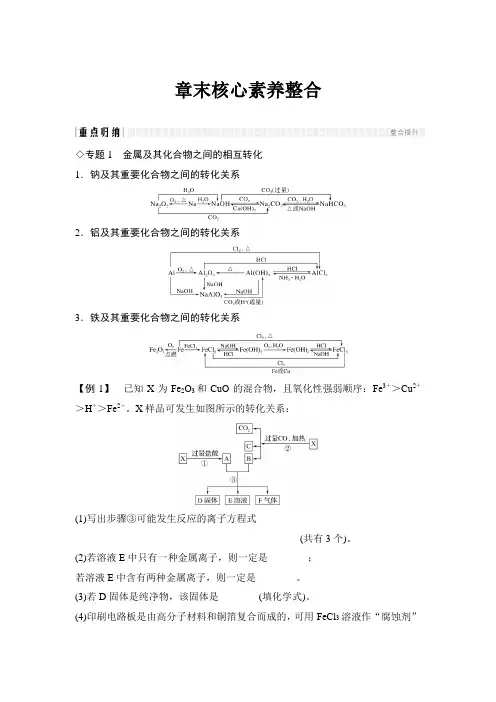
章末核心素养整合◇专题1金属及其化合物之间的相互转化1.钠及其重要化合物之间的转化关系2.铝及其重要化合物之间的转化关系3.铁及其重要化合物之间的转化关系【例1】已知X为Fe2O3和CuO的混合物,且氧化性强弱顺序:Fe3+>Cu2+>H+>Fe2+。
X样品可发生如图所示的转化关系:(1)写出步骤③可能发生反应的离子方程式_______________________________________________________________________(共有3个)。
(2)若溶液E中只有一种金属离子,则一定是________;若溶液E中含有两种金属离子,则一定是________。
(3)若D固体是纯净物,该固体是________(填化学式)。
(4)印刷电路板是由高分子材料和铜箔复合而成的,可用FeCl3溶液作“腐蚀剂”刻制印刷电路板,该过程发生反应的离子方程式为____________________ _____________________________________________________________。
解析 (1)①步中的反应为CuO +2HCl===CuCl 2+H 2O 、Fe 2O 3+6HCl===2FeCl 3+3H 2O ,所得溶液为FeCl 3、CuCl 2及过量的HCl 的混合溶液;步骤②得到的固体有铜、铁两种,若B 是铜,根据题给的氧化性顺序可知,只有一个反应,不符合3个反应的要求,故B 应是铁。
(2)若溶液E 中只有一种金属离子,则必然是氧化性最弱的Fe 2+;若溶液E 中含有两种金属离子,则为Fe 2+、Cu 2+。
(4)根据氧化性Fe 3+>Cu 2+可知,腐蚀电路板的反应为2Fe 3++Cu===2Fe 2++Cu 2+。
答案 (1)2Fe 3++Fe===3Fe 2+、Cu 2++Fe===Fe 2++Cu 、2H ++Fe===Fe 2++H 2↑ (2)Fe 2+ Fe 2+、Cu 2+ (3)Cu (4)2Fe 3++Cu===2Fe 2++Cu 2+◇专题2 常见金属及其化合物推断的“突破口” 1.物质颜色 (1)有色固体:红色:Cu ;砖红色:Cu 2O ;红棕色:Fe 2O 3;红褐色:Fe(OH)3;淡黄色:S 或Na 2O 2;蓝色:Cu(OH)2;紫黑色:KMnO 4、I 2;黑色:炭粉、CuO 、FeO ;白色沉淀:Fe(OH)2、Mg(OH)2、CaCO 3、BaSO 4、AgCl 、BaSO 3;(2)有色溶液:Fe 2+(浅绿色)、Fe 3+(棕黄色)、Cu 2+(蓝色)、MnO -4(紫红色)、Fe(SCN)3(红色)。





专题4 化学科学与人类文明本专题知识体系构建与核心素养解读1.科学探究与创新意识化学是一门以实验为基础的科学,科学探究是认识物质及其变化的重要活动。
科学探究与创新意识核心素养的具体表现有:能发现和提出有探究价值的问题。
能从问题和假设出发,确定探究目的,设计探究方案,进行探究实验。
能对观察记录的实验信息进行加工并获得结论。
能提出进一步探究或改进实验的设想。
例析二氧化硫是一种危害严重的大气污染物,烟气脱硫是控制二氧化硫污染的主要技术手段。
利用海水脱硫是一种有效的方法,其工艺流程如图所示:某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水吸收含硫烟气的模拟实验,实验结果如图所示。
(1)根据图示实验结果,为了提高一定浓度含硫烟气中SO2的吸收效率,下列措施正确的是________(填字母)。
A.降低通入含硫烟气的温度B.减小通入含硫烟气的流速C.减少天然海水的进入量D.在天然海水中加入生石灰(2)天然海水吸收了含硫烟气后会溶有H2SO3,使用空气中的氧气将其氧化,写出该反应的离子方程式______________________________________________________________________________________________________________________________________。
(3)该小组采用如图装置在实验室测定烟气中SO2的体积分数(假设烟气中其余组分不能与水反应且不溶于水,实验在标准状况下进行):①上述装置连接的正确顺序是:原料气→_______→_______→_______→_______→_______。
(填a、b、c、d、e)②下列试剂中(浓度、体积一定),可以用来代替试管中的I2淀粉溶液的是________(填字母)。
A.酸性KMnO4溶液B.NaOH溶液C.溴水D.氨水答案(1)ABD (2)2H2SO3+O2===4H++2SO2-4(3)①c d b a e ②AC解析(1)总体看,SO2的吸收效率随温度的升高而降低;当温度和SO2的浓度一定时,SO2的吸收效率随烟气流速的增大而降低;当温度和烟气流速一定时,SO2的吸收效率随SO2浓度的增大而降低,所以,要提高一定浓度含硫烟气中SO2的吸收效率,应降低含硫烟气的温度、减小烟气流速。
4.1.1原子结构元素周期表核素本课时是教材第四章第一节第一课时的内容,该课时包括两部分内容:原子结构和元素周期表。
首先是在初中学习原子结构的基础上,继续学习原子结构,尤其是深入理解原子的核外电子排布,了解质量数和同位素的基本概念。
其次是在学习原子核外电子排布的基础上,了解元素周期表的绘制原则,了解族和周期的概念。
在之前的学习中,学生已经知道了原子是由核外电子、质子和中子构成的,但是还没有质量数的概念,对于原子的核外电子排布也没有非常清晰的印象。
同时,学生在初中也了解了元素周期表的简单概念,但是不清楚元素周期表的编写原则,对于族和周期的分类也不是非常清晰。
通过本课时的学习,学生可以建立原子结构的简单模型,理解元素周期表尤其是短周期元素的编写方式,为今后元素周期律的学习打下坚实的基础。
宏观辨识与微观探析:从微观上理解原子核外电子排布的基本规律,明确宏观上的元素周期表与微观上的原子核外电子排布之间的关系,理解元素的排列规律。
证据推理与模型认知:建立原子结构的微观模型,理解门捷列夫利用已知元素的性质推理出元素周表的科学思想。
科学精神与社会责任:通过对元素周期表的学习,认识化学知识的规律性,理解化学知识从实验到理论,再由理论推测出实验结果的科学精神。
元素周期表的结构,元素周期表中元素的排列与原子核外电子排布的关系。
学生复习初中有关原子结构、元素周期表的知识,预习本课内容;教师准备多媒体课件。
【引入】在序言的学习中,我们知道门捷列夫绘制出第一张元素周期表是化学科学发展中一个重要的里程碑。
【投影】门捷列夫绘制元素周期表的视频。
【过渡】门捷列夫是根据什么对元素进行排列的呢?这就是我们今天这节课要学习的内容。
【板书】原子结构与元素周期表一、原子结构【投影】原子结构与元素周期表一、原子结构【学生活动】根据初中学习的关于原子结构的知识,请同学们描述一下原子的结构。
【讲解】初中化学中,我们学习了,原子是由原子核以及核外电子组成的,而原子核又由质子和中子构成。